Spektroskopi erbjuder ett snabbt och exakt sätt att övervaka tillväxtmedier i odlad köttproduktion. Genom att spåra näringsämnen som glukos och glutamin i realtid hjälper det till att optimera celltillväxt och bibehålla kvalitet. Två viktiga metoder utmärker sig:
- NIR-spektroskopi: Verkar i intervallet 780–2 500 nm, idealiskt för att spåra näringsämnen och metaboliter som glukos och laktat. Det är kostnadseffektivt och integreras enkelt med bioreaktorer men kan stöta på störningar från vattensignaler.
- Raman-spektroskopi: Använder oelastisk ljusspridning för att ge mycket specifik molekylär data. Det fungerar bra i vatten-dominerade miljöer och erbjuder precision för metaboliter som laktat och glukos men medför högre kostnader.
Båda metoderna stöder automatiserade system för näringstillförsel och kontaminationsdetektion, vilket förbättrar effektiviteten och minskar riskerna med manuell provtagning.Plattformar som
NIR-spektroskopi för analys av tillväxtmedia
Hur NIR-spektroskopi fungerar
När-infraröd (NIR) spektroskopi fungerar inom våglängdsområdet 780 nm till 2 500 nm, och fokuserar på att upptäcka övertoner och kombinationsband av grundläggande molekylära vibrationer [7]. Detta gör den särskilt effektiv för att identifiera bindningar som C-H, O-H och N-H, som vanligtvis finns i molekyler som glukos, aminosyror och proteiner.
Processen innebär att NIR-ljus skiner genom tillväxtmediet och mäter hur mycket ljus som absorberas vid olika våglängder. Varje molekyl producerar ett unikt spektralt mönster, eller "fingeravtryck", som ger insikter i mediets sammansättning.Erca för de spektrala förtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollningsförtollnings
NIR-applikationer i övervakning av tillväxtmedier
NIR-spektroskopi används i stor utsträckning för att spåra kritiska näringsämnen och metaboliter, såsom glukos, glutamin, aminosyror, laktat, ammoniak och totalt cellantal (TCC) [6][8]. Genom att tillhandahålla realtidsdata hjälper det producenter att upptäcka näringsbrist tidigt, förhindra påverkan på cellviabilitet eller identifiera giftiga biprodukter innan de ackumuleras.
Studier har visat de praktiska fördelarna med NIR. Till exempel använde en undersökning NIR för online-övervakning i en omrörd tankbioreaktor och uppnådde prediktionsfel på 1,54 mM för glukos och 0,83 mM för laktat [8]. För odlingsprocesser av kött, där celler växer på mikrobärare, är system-specifik kalibrering avgörande på grund av ljusspridningseffekter orsakade av mikrobärarkulorna.Forskning vid Sanofi Pasteur tillämpade framgångsrikt NIR för att övervaka Vero-celler odlade på Cytodex 1 mikrobärare, och uppnådde prediktionsnoggrannheter på 0,36 g/l för glukos och 0,29 g/l för laktat [9] . Dessa resultat understryker vikten av skräddarsydd kalibrering för olika system.
"NIR-spektroskopi (NIRS) är ett lovande alternativt in situ PAT-verktyg... som tillhandahåller ett spektrum representativt för 'signaturen' av alla komponenter som finns i den analyserade lösningen."
- Annie Marc, Process Biochemistry [9]
En annan växande användning av NIR är att skapa "gyllene batch"-profiler - riktmärken som representerar optimal processprestanda. Operatörer kan jämföra aktuella körningar mot dessa profiler i realtid. Till exempel använde forskare vid Leibniz Universität Hannover NIR för att övervaka CHO-K01-cellodlingar i en 7,5-liters bioreaktor.Deras system upptäckte bakteriell kontaminering i "Batch 3" bara 30 timmar in i processen, eftersom NIR-avläsningarna överskred definierade processgränser [4].
Grunderna i NIR-spektroskopi – Hur fungerar NIR-spektroskopi?
Raman-spektroskopi för analys av tillväxtmedia
Medan NIR-spektroskopi är utmärkt för att avkoda överlappande absorptionsband, tar Raman-spektroskopi en annan väg. Den använder oelastisk ljusspridning för att fördjupa sig i den molekylära strukturen, vilket erbjuder en kompletterande analysmetod.
Hur Raman-spektroskopi fungerar
Raman-spektroskopi fungerar genom att lysa en 785 nm laser på ett prov och fånga de fotoner som sprids oelastiskt. När dessa fotoner interagerar med molekyler sker energiförskjutningar på grund av vibrationella rörelser.Dessa skiftningar skapar ett unikt spektralt "fingeravtryck" som avslöjar den molekylära strukturen hos komponenter som proteiner, lipider, nukleinsyror och socker [12][5].
Den huvudsakliga skillnaden från NIR-spektroskopi ligger i vad Raman mäter. Istället för att detektera förändringar i dipolmoment fokuserar Raman på förändringar i polariserbarhet hos molekylära bindningar under vibration [5]. Denna skillnad gör det särskilt användbart för odlat kött-applikationer. Varför? Eftersom vatten, som dominerar tillväxtmedier, är nästan osynligt för Ramans detektion. Detta innebär att Raman kan "se igenom" vattnet för att upptäcka små mängder näringsämnen och metaboliter, och undvika den störning som ofta komplicerar infraröda metoder [11][12][5] .
Raman-spektroskopi genererar analytspecifika signaler som inte överlappar med vattensignaler... vilket gör det särskilt fördelaktigt för applikationer i cellkulturer, där matrisen är övervägande vattenbaserad.
- Morandise Rubini, Forskare, University of Tours [12]
Men eftersom spektralband kan överlappa, används ofta avancerade matematiska modeller som Partial Least Squares eller Principal Component Analysis för att extrahera exakt kvantitativ data från de skarpa, specifika spektra [12][13] [14].
Raman-applikationer i övervakning av tillväxtmedia
Tack vare dess förmåga att producera detaljerade molekylära fingeravtryck har Raman-spektroskopi blivit ett kraftfullt verktyg för in-line övervakning i produktionsmiljöer.Fungerar som en optisk sensor för bänktoppsbioreaktorer, den spårar näringsämneskonsumtion - som glukos och glutamin - och produktionen av metaboliska biprodukter, såsom laktat och ammoniak [14]. Denna realtidsåterkoppling möjliggör automatiserade justeringar, såsom optimering av näringsmatningsscheman för att förbättra effektiviteten.
Till exempel, i april 2025, använde forskare en Viserion Raman-spektrometer i fem 10-liters CHO-cellkulturer, och uppnådde mycket exakta förutsägelser (e.g. , RMSEP på 0,51 g/l för glukos) [12]. På liknande sätt, i mars 2018, använde ett team vid Cell and Gene Therapy Catapult i London ett in-line Raman-system (Kaiser Optical Systems RamanRxn2™-analysator) för att övervaka autologa T-cellproduktion. De spårade glukos (R = 0,987) och laktat (R = 0.986) nivåer med precision, identifiera donatorspecifika metaboliska förändringar och proliferationshastigheter utan behov av manuell provtagning [14].
Utöver näringsämnen och biprodukter övervakar Raman-spektroskopi också cellkoncentration, utvärderar cellviabilitet och upptäcker potentiella faror som Salmonella eller E. coli. Detta säkerställer konsistens mellan batcher och ger ett tillförlitligt sätt att karakterisera mediekomponenter [11][1][14] [15].
NIR vs Raman: Vilken metod ska användas
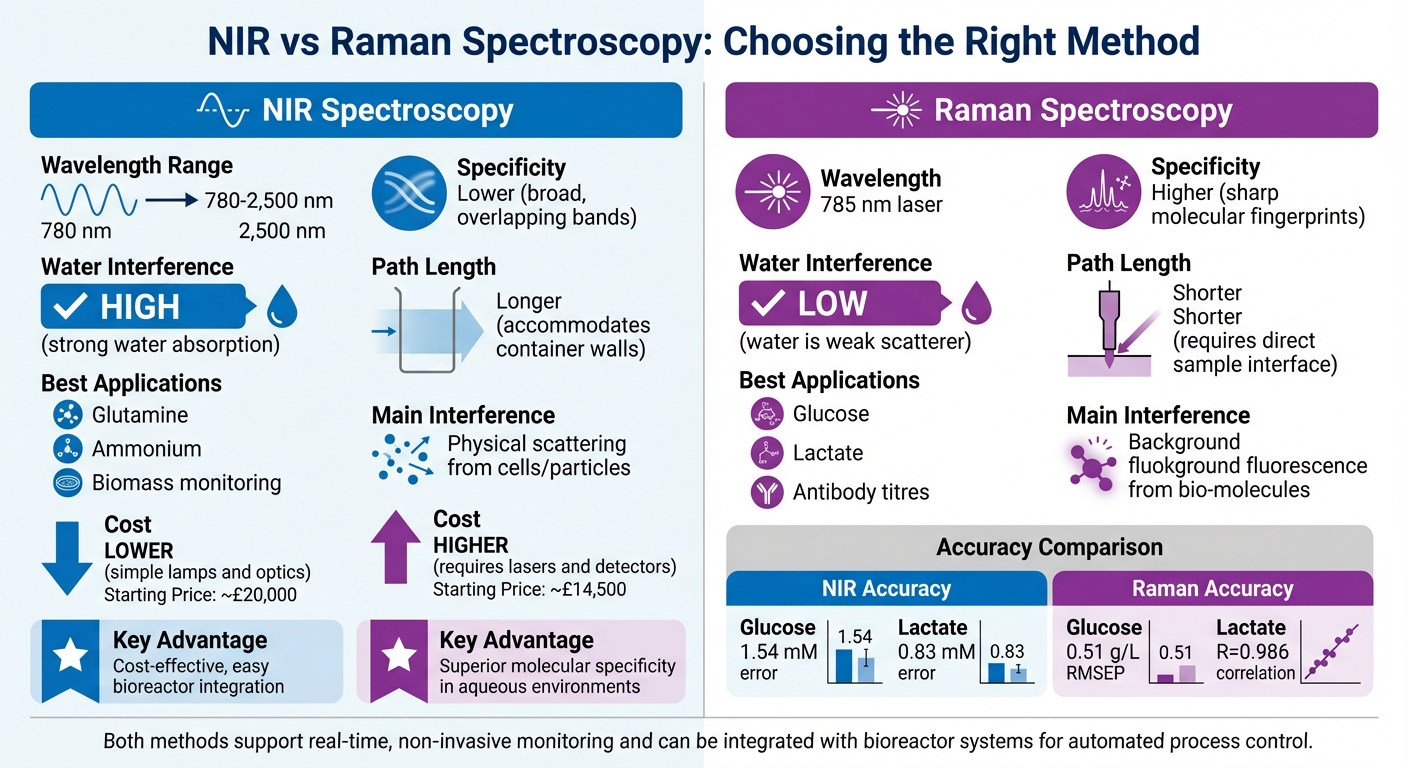
Jämförelse mellan NIR och Raman-spektroskopi för analys av tillväxtmedia
Att välja mellan NIR och Raman-spektroskopi beror på dina specifika analyter, budget och systemets uppsättning.Detta val är avgörande när man planerar att skala upp processer för odlat kött.
Jämförelsefaktorer
Raman-spektroskopi utmärker sig för sin förmåga att leverera mycket specifik molekylär information. Den genererar skarpa, distinkta spektrala "fingeravtryck", vilket gör det lättare att identifiera enskilda föreningar. Å andra sidan producerar NIR-spektroskopi breda, överlappande band som kräver avancerade kemometriska verktyg för analys [1]. Detta gör Raman särskilt användbar för att noggrant spåra specifika metaboliter.
Vattenabsorption i NIR kan dölja näringssignaler, medan Ramans låga känslighet för vatten säkerställer tydligare detektion. Dock är Raman inte utan sina utmaningar - den kan stöta på störningar från bakgrundsfluorescens orsakad av biologiska föreningar som proteinhydrolysat [1].
Forskning som involverar CHO-cellbioreaktorer har visat att Raman överträffar NIR i att förutsäga glukos, laktat och antikroppar, medan NIR är mer effektivt för glutamin och ammoniumjoner [2]. En studie genomförd i mars 2017 av R.C. Rowland-Jones vid University of Leeds stödde ytterligare Ramans styrkor och visade att det var mer tillförlitligt för att mäta laktat (RMSECV 1,11 g/L) och glukos (RMSECV 0,92 g/L) i 15 mL miniatyrbioreaktorer [16].
Ur ett kostnadsperspektiv är NIR-system vanligtvis mer prisvärda på grund av deras enklare ljuskällor. Raman-system kräver dock avancerade lasrar och detektorer, vilket gör dem dyrare [1]. Tabellen nedan belyser dessa viktiga skillnader:
| Faktor | NIR-spektroskopi | Raman-spektroskopi |
|---|---|---|
| Specificitet | Lägre; breda, överlappande band [1] | Högre; skarpa molekylära "fingeravtryck" [1] |
| Vattenstörning | Hög; stark vattenabsorption [2] | Låg; vatten är en svag spridare [2] |
| Bäst för | Glutamin, ammonium, biomassaövervakning [2] | Glukos, laktat, antikroppstitrar [2, 19] |
| Kostnad | Generellt lägre; enkla lampor och optik [1] | Generellt högre; kräver lasrar och detektorer [1] |
| Banlängd | Längre; rymmer behållarväggar [6] | Kortare; kräver ett direkt provgränssnitt [6] |
| Huvudstörning | Fysisk spridning från celler/partiklar [6] | Bakgrundsfluorescens från biomolekyler [2] |
Nästa gång kommer vi att utforska hur man tillämpar spektroskopidata för realtidsoptimering av media i produktion.
sbb-itb-ffee270
Använda spektroskopidata i produktion
Optimering av media i realtid
Spektroskopi omvandlar rådata till handlingsbara insikter, vilket effektiviserar näringstillförseln i produktionsprocesser. Genom att möjliggöra samtidig, icke-invasiv övervakning av nyckelparametrar som glukos, laktat, glutamin och ammonium, säkerställer det kontinuerlig optimering av kulturer. Till exempel, när glukosnivåerna sjunker under det ideala intervallet, utlöser systemet automatiskt näringstillförsel. Detta förhindrar cellsvält och minskar risken för ackumulering av giftiga biprodukter [2].
Skapandet av "Golden Batch"-banor från optimala produktionskörningar möjliggör tidig identifiering av problem, såsom kontaminering eller luftningsproblem [4]. För perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstids perstidsNedsänkta sonder, som kan motstå sterilisationscykler och högt tryck, överför realtidsdata direkt till bioreaktorernas kontrollenheter [6].
En studie genomförd i september 2018 vid Université de Lorraine jämförde in situ Raman- och NIR-sonder som opererade parallellt i en 2-liters CHO-cellbioreaktor. Resultaten visade att Ramanspektroskopi utmärkte sig vid detektering av glukos och laktat, medan NIR var mer effektiv för att övervaka glutamin och ammonium. Att kombinera styrkorna hos båda metoderna ger den mest omfattande realtidsövervakningen för odlad köttproduktion [2].
Spektroskopidata matas också in i Multivariat Statistisk Processkontroll (MSPC) system, som kontinuerligt jämför pågående batcher med etablerade Golden Batch-standarder.Detta tillvägagångssätt gör det möjligt för operatörer att upptäcka avvikelser - oavsett om de orsakas av kontaminering, näringsbrist eller utrustningsfel - inom timmar istället för dagar. Resultatet är förbättrad effektivitet och större konsekvens i produktionen [4].
Inköp av spektroskopiutrustning via Cellbase
Varför använda Cellbase för spektroskopiutrustning
Att välja rätt spektroskopiutrustning för produktion av odlat kött kan kännas som att navigera i en labyrint av tekniska detaljer. Med allmänna spektrometrar som erbjuder tusentals konfigurationer [18], är det lätt att bli överväldigad utan rätt expertis.
Det är här
Nyckelfunktioner för Cellbase vid upphandling av utrustning
Dessutom hjälper
Slutsats
NIR- och Ramanspektroskopi spelar en kritisk roll i att förfina tillväxtmedia för odlat kött. Dessa avancerade tekniker möjliggör realtids, icke-invasiv övervakning av viktiga analyter som glukos, laktat och ammonium.Detta innebär att produktionsteamen kan göra snabba justeringar utan att avbryta processen - en viktig fördel med tanke på att mediedesign förblir en av de största utmaningarna vid skalning av odlad köttproduktion [16][19] .
Varje metod har sina egna styrkor. NIR-spektroskopi utmärker sig i att bedöma biomassa och övergripande sammansättning, medan Raman-spektroskopi ger detaljerad insikt i specifika metaboliter i vattenlösningar [1]. Under studier med miniatyrbioreaktorer visade Raman-spektroskopi imponerande prediktiv noggrannhet, vilket gör det till ett pålitligt val för precisa mätningar [16]. Båda teknikerna stöder också utvecklingen av en "gyllene batch"-profil, vilket gör det möjligt för operatörer att upptäcka problem som bakteriell kontaminering eller luftningsproblem så snart de uppstår [4].
När det gäller att välja rätt spektroskopiutrustning kan processen vara skrämmande. Det är här
Professor Alan G. Ryder lyfter fram vikten av dessa metoder:
Snabba spektroskopiska metoder, om de tillämpas korrekt, kan användas för snabb och effektiv screening av cellodlingsmedia för att identifiera molekylär variation och potentiella problem med mediatillverkning [1] .
Vanliga frågor
Vilka är fördelarna med att använda spektroskopi i produktionen av odlat kött?
Spektroskopitekniker som nära-infraröd (NIR) och Raman ger värdefulla verktyg till den odlade köttindustrin. De möjliggör realtids, icke-invasiv övervakning av tillväxtmedia, vilket gör det möjligt att kontinuerligt spåra näringsämnen, metaboliter och celldensitet - utan att behöva ta prover eller använda extra reagenser. Denna nivå av övervakning hjälper till att upprätthålla stramare processkontroll och påskyndar justeringar av mediesammansättningen, vilket är avgörande för att säkerställa konsekvent kvalitet vid uppskalning av produktionen.
Dessa metoder är också effektiva och kostnadsbesparande. Med en enda mätning kan de analysera flera komponenter samtidigt - såsom aminosyror, sockerarter och lipider - vilket eliminerar behovet av separata kemiska tester. Detta minskar både arbets- och materialkostnader samtidigt som det ger data som kan förbättra prediktiva modeller, vilket hjälper till att standardisera kvalitet och minska variationen mellan partier.
En annan fördel är hur lätt spektroskopi kan integreras med automatiserade system. Till exempel kan NIR-prober installeras direkt i bioreaktorer för att leverera kontinuerliga data, vilket möjliggör automatiska justeringar av kritiska parametrar som matningshastigheter eller temperatur. För dem som behöver specialiserad utrustning,
Vilka är de viktigaste skillnaderna mellan NIR- och Ramanspektroskopi för att analysera tillväxtmedia i odlad köttproduktion?
Närinfraröd (NIR) spektroskopi är perfekt för snabb, icke-invasiv övervakning av den övergripande sammansättningen av tillväxtmedia. Dess förmåga att tillhandahålla online- eller inline-kontroll innebär att den kan leverera realtidsdata, vilket hjälper producenter att göra omedelbara justeringar under produktionsprocessen.
Å andra sidan erbjuder Ramanspektroskopi ett precist molekylärt fingeravtryck, vilket gör det till ett utmärkt val för att identifiera och mäta specifika metaboliter som glukos och laktat. Denna nivå av precision är särskilt användbar för att finjustera mediesammansättningen för att passa de specifika behoven i odlad köttproduktion.
Varför är realtidsövervakning av tillväxtmedia viktigt för produktion av odlat kött?
Realtidsövervakning spelar en nyckelroll i att hålla tillväxtmediet precis rätt för produktion av odlat kött. Genom att noggrant övervaka näringsämnen, metaboliter och cellhälsa kan producenter snabbt justera förhållandena för att upprätthålla stadig celltillväxt och förbättra kvaliteten på slutprodukten.
Denna praktiska metod eliminerar väntetiden som är förknippad med traditionell offline-testning, vilket leder till bättre avkastning och mindre avfall. Det säkerställer också att resurser används mer effektivt, vilket effektiviserar produktionsprocessen och ökar tillförlitligheten.











