Produktion af dyrket kød er dyrt, hvor vækstmedier er den største omkostningsdriver. Metabolomics, en detaljeret analyse af cellulær metabolisme, erstatter gætterier med præcise data for at forfine mediesammensætningen. Denne tilgang identificerer næringsstofmangler, sporer hvordan celler bruger ressourcer, og fremhæver affaldsophobning, der hæmmer vækst.
Vigtige fund:
- 40,72% stigning i celletæthed opnået i en undersøgelse fra 2019 ved at optimere medier til kyllingefibroblaster.
- Metabolomics værktøjer identificerede kritiske næringsstoffer som glukose, aminosyrer og energirelaterede forbindelser, der er nødvendige for effektiv cellevækst.
- Justeringer i næringsstofniveauer (e.g. , kreatin, inosine-5'-monophosphat) forbedrede celleproliferation samtidig med at affald blev reduceret.
Analyse af brugt medie for at lette optimering af dyrket kødmedie - Ted O'Neill - ISCCM9
Indledende vækstmedieproblemer
Forskerteamet stod over for store udfordringer med den oprindelige medieformulering for C2C12 muskelceller. Det standard DMEM/F12 medie kunne simpelthen ikke opretholde de celletætheder eller udbytter, der kræves til storskalaproduktion af dyrket kød. Cellerne forbrugte næringsstoffer langt hurtigere, end mediet kunne genopfylde, hvilket førte til tidlig udtømning af kritiske komponenter og dårlig biomassevækst. For at løse disse problemer vendte teamet sig mod datadrevne strategier for optimering.
Næringsstofmangler i den oprindelige formulering
En analyse af det brugte medie afslørede nogle åbenlyse næringsstofmangler. Glukose og specifikke aminosyrer blev brugt op i et uholdbart tempo.For at producere blot 1 kg C2C12 muskelceller, krævede cellerne mellem 1.100–1.500 g glukose og 250–275 g aminosyrer[2]. Blandt disse var glutamin, glycin og cystin i særlig høj efterspørgsel, hvilket begrænsede cellevækst og -proliferation.
Den metaboliske profil afslørede også ineffektivitet i, hvordan næringsstoffer blev behandlet. For eksempel var energirelaterede metabolitter som kreatin og inosine-5'-monophosphat nedreguleret, mens metabolitter involveret i membransyntese - såsom fosfoethanolamin og cholin - var opreguleret[3]. Dette skift indikerede, at cellerne prioriterede øjeblikkeligt energiforbrug frem for energilagring. Selv når næringsstoffer var tilgængelige, var deres proportioner langt fra optimale for effektiv biomasseproduktion. Denne ubalance gjorde det klart, at en mere præcis og analytisk tilgang var nødvendig.
Hvorfor Metabolomics Blev Valgt
Traditionelle forsøg-og-fejl metoder kunne have taget måneder af testning for at identificere disse specifikke problemer. I stedet valgte teamet metabolomics, en teknik, der identificerer og måler metabolitter i brugt medie med bemærkelsesværdig præcision. Denne metode gav et detaljeret øjebliksbillede af cellulær metabolisme i en enkelt analyse[2].
"Tidligere data fra metaboliske studier udført ved brug af serumholdige medier kan muligvis ikke direkte oversættes til serumfrie systemer." – ScienceDirect[2]
Metabolomics viste sig at være uvurderlig til at opdage subtile biokemiske ændringer, især da teamet arbejdede på at udvikle serumfrie formuleringer. Mens standard vækstvurderinger - som celletællinger eller levedygtighedstests - kun kunne tilbyde overfladiske indsigter, afslørede metabolomics cellernes dybere metaboliske behov. Dette gjorde det muligt for teamet at forfine mediesammensætningen baseret på faktiske data frem for antagelser, hvilket banede vejen for mere målrettede og effektive forbedringer.
Resultater fra Metabolomisk Analyse
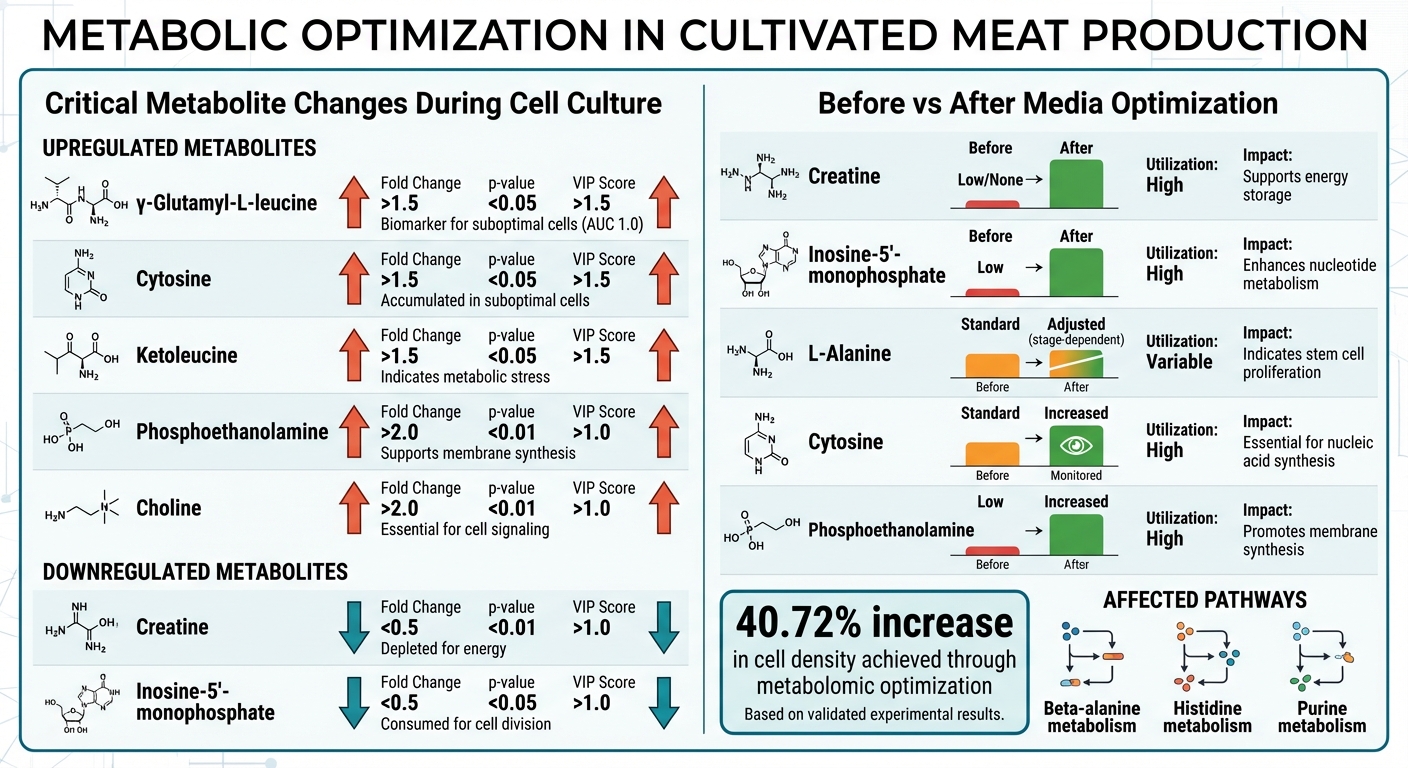
Metabolitændringer og Næringsstofoptimering i Dyrket Kødproduktion
Metabolitændringer Under Cellekultur
En detaljeret metabolomisk analyse identificerede syv kritiske metabolitter, der viste bemærkelsesværdige ændringer under svinemuskel stamcellekultur. I april 2024 identificerede et team ledet af Doo Yeon Jung ved Seoul National University γ‑glutamyl‑L‑leucin, cytosin og ketoleucin som nøglebiomarkører til at genkende suboptimale cellestater [5]. Disse tre metabolitter opnåede en AUC på 1,0, hvilket demonstrerer perfekt nøjagtighed i forudsigelsen af fald i celleproliferation [5].
Undersøgelsen afslørede også ændringer i energistyring inden for cellerne. Metabolitter som fosfoethanolamin og cholin var markant opreguleret, hvilket afspejler den øgede efterspørgsel efter membransyntese under hurtig celledeling [6]. På den anden side var kreatin og inosine-5′-monophosphat nedreguleret, hvilket indikerer et skift væk fra energilagring mod øjeblikkeligt energiforbrug [6]. Disse fund giver et stærkt grundlag for yderligere undersøgelse af metaboliske veje.
Metabolisk Vejanalyse
Vejanalysen afslørede øget aktivitet i tre nøglesystemer: beta-alanin metabolisme, histidin metabolisme og purin metabolisme [5][6]. Hver af disse veje spiller en vital rolle - proteinsyntese, pH-buffering og DNA/RNA-produktion, henholdsvis.Blandt disse skilte histidinvejen sig ud ved at vise konsekvent aktivitet under både de prolifererende og differentierende stadier. Dette antyder, at det kan være en begrænsende faktor i den oprindelige medieformulering [6].
Purinstofskiftevejen gav yderligere indsigt. En betydelig udtømning af nukleotid-relaterede forbindelser indikerede, at cellerne brugte disse byggesten hurtigere, end de kunne genopfyldes af kulturmediet. Dette blev yderligere understøttet af ophobningen af affaldsmetabolitter som cytosin i senere passager, hvilket faldt sammen med reduceret cellevækst [5].
Metabolit Sammenligningstabel
| Metabolitnavn | Foldændring | p-værdi | VIP Score | Status |
|---|---|---|---|---|
| γ‑Glutamyl‑L‑leucin | > 1.5 | < 0.05 | > 1.5 | Opreguleret (akkumuleret i suboptimale celler) [5] |
| Cytosin | > 1.5 | < 0.05 | > 1.5 | Opreguleret (akkumuleret i suboptimale celler) [5] |
| Ketoleucin | > 1.5 | < 0.05 | > 1.5 | Opreguleret (akkumuleret i suboptimale celler) [5] |
| Fosfoethanolamin | > 2.0 | < 0.01 | > 1.0 | Opreguleret (understøtter membransyntese) [6] |
| Kolin | > 2.0 | < 0.01 | > 1.0 | Opreguleret (essentiel for cellesignalering) [6] |
| Kreatin | < 0,5 | < 0,01 | > 1,0 | Nedreguleret (udtømt for energi) [6] |
| Inosin-5′-monofosfat | < 0,5 | < 0,05 | > 1,0 | Nedreguleret (forbrugt til celledeling) [6] |
Justeringer af vækstmedier
Ændringer i næringsstofkoncentrationer
Forskere ved Seoul National University, ledet af Doo Yeon Jung, brugte metabolomisk analyse til at finjustere vækstmediet til produktion af kultiveret kød.Ved at undersøge brugt medie identificerede de, hvilke næringsstoffer der blev udtømt under dyrkning, og hvilke affaldsprodukter der ophobede sig [5]. Dette gjorde det muligt for dem at justere næringsstofniveauerne for bedre at matche cellernes behov.
Teamet fokuserede på tre hovedfaktorer: næringsstoffer, som cellerne hurtigt forbrugte, affaldsprodukter, der indikerede metabolisk stress, og omkostningerne ved ingredienser (med henblik på at erstatte dyre komponenter uden at gå på kompromis med ydeevnen) [7]. For eksempel blev L-alanin-niveauerne ændret afhængigt af cellernes vækststadie, mens kreatin og inosin-5′-monofosfat blev øget for at støtte et skift fra energilagring til direkte energiforbrug.
"Overvågning af niveauerne af disse nøglemetabolitter i kulturmedier kunne tjene som en kvalitetskontrolforanstaltning for produktion af kultiveret kød ved at muliggøre indirekte detektion af suboptimale PSC'er." - Doo Yeon Jung, Forsker, Seoul National University [5]
Fosfoethanolamin-niveauerne blev øget for at hjælpe med membransyntese under celledeling, mens cytosinkoncentrationerne blev nøje overvåget for at undgå overdreven ophobning [5][6]. Disse justeringer havde til formål at skabe en metabolisk balance, hvor næringsstoffer blev effektivt omdannet til biomasse, hvilket reducerede spild og forbedrede foderkonverteringsforholdet [7].
Tabellen nedenfor fremhæver de vigtigste ændringer foretaget i næringsstofkoncentrationerne og deres indvirkning på cellevækst.
Før og efter sammenligning
| Næringsstof | Initial koncentration | Optimeret koncentration | Udnyttelsesgrad | Indvirkning på cellevækst |
|---|---|---|---|---|
| Kreatin | Lav/Ingen | Øget | Høj | Understøtter energilagring; stemmer overens med konventionelle kød egenskaber [6] |
| Inosin‑5′‑monophosphat | Lav | Øget | Høj | Forbedrer nukleotidmetabolisme og energiproduktion [6] |
| L-Alanin | Standard | Justeret (faseafhængig) | Variabel | Indikerer stamcelleproliferationskapacitet [5] |
| Cytosin | Standard | Øget/Overvåget | Høj | Essentiel for nukleinsyresyntese under hurtig celledeling [5] |
| Fosfoethanolamin | Lav | Øget | Høj | Fremmer membransyntese og cellestrukturens integritet [6] |
Disse forbedringer adresserede specifikke metaboliske udfordringer, især i purin-, histidin- og sfingolipidmetabolisme [6]. Ved at tilpasse næringsstof tilgængelighed til at matche cellulært forbrug, reducerede teamet spild og opnåede mere konsistent celleproliferation på tværs af flere vækstcyklusser.
sbb-itb-ffee270
Resultater: Forbedret Dyrkningspræstation
Cellevækst og Biomasseforbedringer
Den metabolomiske tilgang medførte klare gevinster i cellepræstation. En 2025-undersøgelse fra Texas A&M University fremhævede dette ved at teste to serumfrie formuleringer: LM7 (kemisk defineret) og LM8 (kemisk udefineret, indeholdende mungbønneprotein isolat). Imponerende nok matchede LM8-formuleringen præstationen af 20% FBS - en sjælden præstation i muskelcellekultur [8] . Dette markerede et stort fremskridt, da de fleste serumfrie medier kæmper for at matche selv 10% FBS præstation.
Yderligere undersøgelser ved brug af C2C12-celler viste, at optimering af næringsstof-forhold ikke kun reducerede affald, men også forbedrede biomassekonvertering [2] [7]. Lignende fordele blev observeret i studier af lamme-, C2C12- og svinemuskelceller, hvilket demonstrerer, hvor bredt anvendelig denne metabolomik-drevne medieoptimering kan være.
Skaleringen af disse fund blev valideret i 3D-mikrocarriersystemer, hvor LM8 viste overlegen ydeevne i rystekolbesystemer ved brug af CellBIND mikrocarriers [8]. Derudover fandt forskning i svinemuskelstamceller i april 2024, at celler ved passage 2 (PSC2) havde de højeste vækstrater. I modsætning hertil viste celler ved passage 3 (PSC3) et betydeligt tab af myogene markørgener, hvilket gør PSC2 til en pålidelig kvalitetskontrolbenchmark for skalering af produktion [5]. Disse fremskridt bekræfter ikke kun effektiviteten af metabolomics-tilgangen, men åbner også døren for betydelige omkostningsbesparelser.
Produktionsskala og omkostningsfordele
Disse forbedringer oversattes til betydelige omkostningsreduktioner. Da medieomkostninger ofte udgør over 60% af produktionsudgifterne, havde det en meningsfuld indvirkning at fjerne dyre komponenter og finjustere næringsstofleveringen [8].
Udover omkostninger styrker disse fremskridt det miljømæssige løfte ved dyrket kød. Med en forventet stigning i den globale efterspørgsel efter kød på omkring 70% inden 2050 [8], tilbyder dyrket kød en måde at reducere jord- og vandforbrug med op til 90% sammenlignet med konventionel husdyrbrug [8]. Ved at sikre, at næringsstoffer effektivt rettes mod biomasseproduktion, hjælper den metabolomiske tilgang med at opretholde denne miljømæssige fordel, mens spild forårsaget af metaboliske ineffektiviteter undgås.
Hvordan Cellbase Understøtter Medieoptimering

Metabolomics-baseret medieoptimering kræver specialiserede værktøjer og materialer, som kan være udfordrende at skaffe.
Platformen kategoriserer sine tilbud for at imødekomme specifikke behov:
- Vækstmedier & Kosttilskud: Leverer højkvalitets, serumfrie formuleringer.
- Labudstyr & Instrumentering: Indeholder metabolomikværktøjer og analytisk udstyr til analyse af brugt medie.
- Sensorer & Overvågning: Tilbyder værktøjer til at spore næringsstofudnyttelsesrater, hvilket er essentielt, da produktion af 1 kg C2C12-celler forbruger omkring 250–275 g aminosyrer og 1.100–1.500 g glukose [2] .
Det, der adskiller
Ud over at levere udstyr tilbyder
Konklusion
Metabolomics spiller en nøglerolle i at forfine vækstmedier til produktion af dyrket kød. Ved at identificere metaboliske flaskehalse og næringsstofhuller kan forskere foretage målrettede justeringer, der betydeligt forbedrer celleydelsen. For eksempel viste en undersøgelse fra East China University of Science and Technology, hvordan komparativ metabolomisk analyse førte til bemærkelsesværdige stigninger i celletæthed og virusproduktion [1].
Ved at bruge indsigter fra metabolomics bevæger analyse af brugt medie sig ud over gætterier.Denne præcision gør det muligt for forskere at skabe medieformuleringer, der maksimerer celleproliferation, samtidig med at de reducerer spild og omkostninger.
Fordelene spænder over forskellige aspekter af produktionen. Metabolomics hjælper med kvalitetskontrol gennem biomarkører som γ-glutamyl-L-leucin og ketoleucin [5]. Det letter også overgangen fra dyre, udefinerede serum-baserede formuleringer til overkommelige, serumfrie muligheder - kritisk for opskalering af produktionen. Som fremhævet af Good Food Institute:
"Cell culture media is currently the largest cost and environmental impact driver of cultivated meat production" [7].
Disse fremskridt understreger potentialet for data-drevet medieoptimering til at transformere feltet.
Ofte stillede spørgsmål
Hvad er metabolomics i optimering af vækstmedier?
Metabolomics spiller en nøglerolle i optimering af vækstmedier ved at analysere de metaboliske profiler af celler, der anvendes i produktionen af dyrket kød. Ved at forstå, hvordan disse celler udnytter næringsstoffer og deres metaboliske veje, kan forskere designe serumfrie medier, der både er mere effektive og omkostningseffektive, specifikt skræddersyet til behovene i produktionen af dyrket kød.
Hvilke metabolitter er de bedste tidlige indikatorer for dårlig vækst?
Vigtige metabolitter forbundet med dårlig vækst i dyrket kød inkluderer γ-glutamyl-L-leucine, cytosin, og ketoleucin. Disse biomarkører fungerer som indikatorer for underpræsterende primærceller og fremhæver metaboliske skift, der kan påvirke celleproliferation.
Hvordan bruges data om forbrugt medie til at reducere medieomkostninger?
Analyse af forbrugt medie spiller en vigtig rolle i at reducere omkostningerne ved produktion af dyrket kød. Ved at identificere næringsstoffer, der enten er udtømt eller i overskud, hjælper det med at forfine medieformuleringer for bedre effektivitet. Værktøjer som spektroskopi muliggør realtidsmonitorering, hvilket reducerer spild og forhindrer overforbrug af dyre komponenter. Derudover giver metabolomik værdifulde indsigter, der kan understøtte genbrug eller genanvendelse af medie, hvilket yderligere reducerer udgifterne. Denne målrettede tilgang sikrer, at ressourcer bruges klogt, samtidig med at den understøtter robust, høj kvalitet cellevækst.











