Asegurarse de que su personal de carne cultivada cumpla con los estándares GMP es esencial para la seguridad del producto, el cumplimiento normativo y una producción fluida. Este proceso requiere capacitación específica, evaluaciones de competencia y documentación exhaustiva. Aquí le mostramos cómo puede comenzar:
- Capacitación Básica: Enseñe al personal los principios de GMP, protocolos de higiene, técnicas asépticas y prevención de contaminación.
- Capacitación Específica por Rol: Adapte los programas a diferentes funciones laborales, como la operación de biorreactores o el control de calidad.
- Evaluaciones de Competencia: Utilice pruebas escritas y evaluaciones prácticas para confirmar conocimientos y habilidades.
- Documentación: Mantenga registros detallados de capacitación y documentos listos para auditoría para el cumplimiento normativo.
- Capacitación Continua: Programe requalificaciones regulares y actualizaciones de capacitación para cambios normativos.
- Sistemas de Seguimiento: Implementar herramientas digitales para monitorear las calificaciones y los plazos de recertificación.
Con programas estructurados y una supervisión adecuada, puede minimizar riesgos como la contaminación o la inestabilidad de las líneas celulares mientras cumple con los requisitos regulatorios, incluyendo Reglamento (CE) 853/2004.
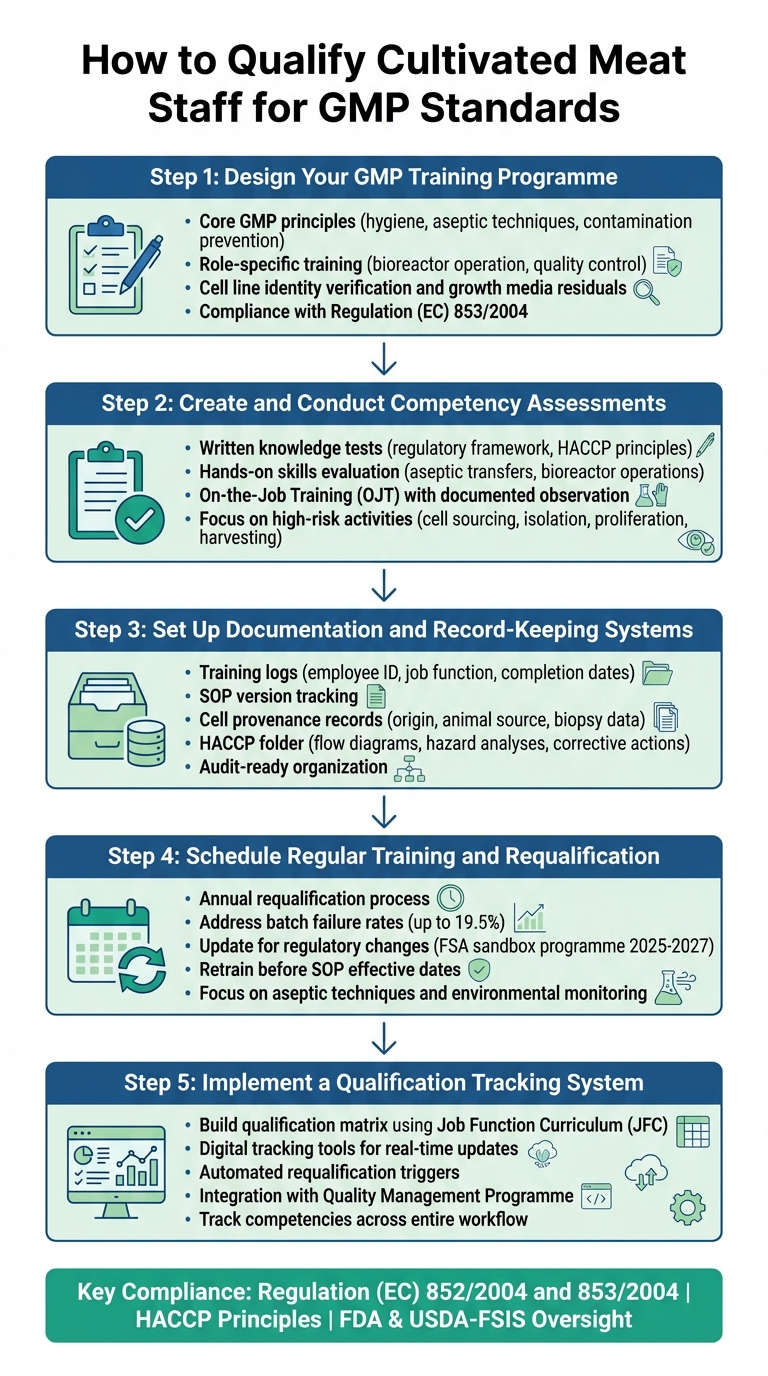
Proceso de 5 Pasos para Calificar al Personal de Carne Cultivada para Estándares GMP
¿Qué es GMP? | Buenas Prácticas de Manufactura en la Industria Alimentaria | SafetyCulture
Paso 1: Diseñe su Programa de Capacitación GMP
Crear un programa de capacitación estructurado comienza con los principios básicos de GMP que todo el personal debe comprender, sin importar su función.Según GMPSOP, la formación inicial debe incluir regulaciones esenciales, prácticas de salud e higiene, procesos de documentación y los valores fundamentales que apoyan el cumplimiento de GMP [5]. Para las instalaciones de carne cultivada, esta base también debe incorporar técnicas asépticas y prevención de contaminación a lo largo de todo el ciclo de vida celular, desde la obtención de materiales de partida hasta la fabricación, pruebas, almacenamiento y distribución [3].
Los requisitos específicos de la producción de carne cultivada significan que su formación también debe abordar la verificación de la identidad de la línea celular, los residuos del medio de crecimiento y los peligros únicos del bioprocesamiento [1]. A diferencia de la producción de carne tradicional, donde el sacrificio puede mitigar los riesgos de patógenos, la carne cultivada depende completamente del control de contaminación en cada etapa del cultivo celular.Las secciones a continuación describen estos principios y muestran cómo pueden adaptarse para diferentes roles dentro de su instalación.
Principios y Fundamentos de las BPM
Para cumplir con los requisitos del Reglamento (CE) 853/2004 en el contexto de la carne cultivada, su programa de capacitación debe asegurar que el personal sea competente en protocolos de higiene, procedimientos de vestimenta y comportamiento en salas limpias antes de ingresar a las áreas de producción. Dado que la carne cultivada se clasifica como un Producto de Origen Animal (POAO), la capacitación debe alinearse con estándares específicos de higiene mientras se reconocen los desafíos únicos de trabajar con células vivas [1]. Esto incluye comprender cómo prevenir la contaminación microbiana durante etapas críticas como el aislamiento y proliferación celular, donde las medidas convencionales de seguridad alimentaria pueden ser insuficientes.
Los empleados deben volverse hábiles en prácticas de higiene, vestimenta y documentación rigurosa para satisfacer el Reglamento (CE) 853/2004.La documentación en las instalaciones de carne cultivada va más allá del registro estándar: el personal debe registrar meticulosamente los detalles sobre la aislamiento y proliferación celular, creando un rastro de auditoría claro para las inspecciones regulatorias. Como destaca GMPSOP:
"Los sitios GMP deben cumplir con los requisitos GMP para la capacitación definiendo el conocimiento, habilidades y atributos que los colegas deben tener para realizar competentemente tareas GMP y otras actividades" [5].
Capacitación Personalizada para Diferentes Roles
Una vez que se establecen las competencias básicas de GMP, la capacitación debe adaptarse a funciones laborales específicas. Un enfoque único para todos no funciona en las instalaciones de carne cultivada, donde las responsabilidades varían enormemente. Un Currículo de Función Laboral (JFC) ofrece una solución al proporcionar una lista personalizada de SOPs, capacitación en el trabajo y temas específicos del rol [5]. Por ejemplo, un operador de biorreactor necesita formación práctica en técnicas de transferencia aséptica y operación de equipos, mientras que un analista de control de calidad requiere experiencia en caracterización de líneas celulares y protocolos de pruebas analíticas.
También es esencial diferenciar entre la formación basada en el conocimiento para roles de supervisión y "Entrenamiento de Habilidades/Rendimiento" para aquellos que realizan tareas prácticas [5]. Por ejemplo, un supervisor de producción que supervisa los procedimientos de cosecha de células necesita formación teórica para proporcionar una supervisión efectiva. Por otro lado, el técnico que lleva a cabo la cosecha debe demostrar su competencia a través de una formación en el trabajo observada y documentada. Este enfoque escalonado asegura que la profundidad e intensidad de la formación correspondan al nivel de riesgo que cada rol representa para la calidad del producto.
Paso 2: Crear y Realizar Evaluaciones de Competencia
Una vez que su programa de capacitación esté en marcha, el siguiente paso es evaluar el conocimiento y las habilidades prácticas de su personal en los estándares de GMP. Esto implica el uso de pruebas escritas para evaluar la comprensión teórica y la observación directa para evaluar el desempeño en el trabajo. Estas evaluaciones deben basarse en la capacitación personalizada proporcionada para diferentes roles, asegurando que los empleados puedan tanto recordar como aplicar los procedimientos de GMP de manera efectiva. Para la carne cultivada, la Agencia de Normas Alimentarias destaca la necesidad de abordar peligros específicos como la identidad de la línea celular, la consistencia, la divergencia y el medio de crecimiento residual en el producto final [1].
Al combinar evaluaciones teóricas y prácticas, crea un sistema de evaluación integral.Por ejemplo, comprender las técnicas asépticas en papel no siempre se traduce en mantener la esterilidad durante tareas del mundo real, como transferir células entre biorreactores bajo presión. Este enfoque dual fortalece su programa de capacitación y asegura una documentación exhaustiva y preparación para inspecciones regulatorias.
Pruebas de Conocimiento Escritas
Las pruebas escritas son un excelente punto de partida para evaluar el conocimiento fundamental de las GMP. Estas pruebas pueden verificar que los empleados entienden el marco regulatorio para la carne cultivada, incluidos sus requisitos específicos de higiene [1]. Son particularmente útiles para evaluar la información que el personal necesita para realizar o supervisar tareas de manera rutinaria. Como explica GMPSOP, las evaluaciones pueden incluir formatos escritos, verbales o basados en computadora, así como estudios de caso y simulaciones [5].
Para la producción de carne cultivada, es crucial probar el conocimiento de riesgos como la divergencia de líneas celulares, una preocupación clave de seguridad. Las preguntas también deben cubrir los principios de HACCP y los Puntos Críticos de Control, especialmente durante las etapas de proliferación y cosecha celular [1]. Las preguntas basadas en escenarios pueden ser particularmente efectivas, como pedir a los empleados que identifiquen la respuesta correcta a la contaminación del biorreactor detectada durante el monitoreo.
Adapte sus preguntas de prueba para abordar desafíos específicos de su instalación. Por ejemplo, si su sitio ha tenido problemas recurrentes en el manejo de líneas celulares o documentación, incluya preguntas que apunten a estas áreas [5]. Cuando se introducen Procedimientos Operativos Estándar (SOPs) nuevos o actualizados, las pruebas escritas pueden confirmar que los empleados entienden los cambios antes de que se implementen.No pase por alto temas fundamentales como los protocolos de limpieza, la higiene personal y la gestión de residuos: son esenciales para apoyar los sistemas basados en HACCP [1].
Evaluación de Habilidades Prácticas
Las evaluaciones prácticas son esenciales para verificar que los empleados puedan realizar correctamente las tareas de BPM en un entorno de producción. Estas evaluaciones implican observar al personal mientras llevan a cabo tareas específicas de acuerdo con sus SOPs [5]. En la producción de carne cultivada, esto podría incluir la supervisión de técnicos mientras realizan transferencias asépticas, operan biorreactores en condiciones estériles o cosechan células sin introducir contaminación.
La Capacitación en el Trabajo (OJT) es un componente clave de las evaluaciones prácticas. Este enfoque uno a uno permite a los formadores observar a los empleados realizando tareas y evaluar sus habilidades según criterios predefinidos.Según GMPSOP, este proceso incluye "una actividad presenciada y documentada" donde un colega demuestra su capacidad para realizar una tarea o habilidad específica descrita en un SOP [5]. La competencia solo se confirma cuando el empleado cumple con todos los criterios, con la documentación adecuada para respaldar la evaluación.
Enfoca tus evaluaciones prácticas en actividades de alto riesgo que impactan directamente la calidad del producto. Para la carne cultivada, esto incluye etapas críticas como la obtención de células, aislamiento, proliferación y cosecha, donde la contaminación microbiana representa riesgos significativos [1]. Antes de abordar tareas complejas como las operaciones de biorreactores, asegúrate de que el personal sea competente en prácticas básicas de higiene como el uso de vestimenta adecuada, comportamiento en salas limpias y la sanitización de equipos.Asigne entrenadores experimentados que no solo sean hábiles en realizar estas tareas, sino también capaces de evaluar el desempeño de otros según el estándar requerido [5].
Paso 3: Establecer Sistemas de Documentación y Registro
Una vez que se completen las evaluaciones de competencia, tener un sistema de documentación sólido es crucial para demostrar las calificaciones del personal y el cumplimiento con los estándares GMP.
Una buena documentación distingue a un programa de capacitación que puede resistir el escrutinio regulatorio. Los registros deben demostrar claramente que cada individuo que realiza tareas relacionadas con GMP ha completado la capacitación necesaria antes de trabajar de manera independiente. Como destaca GMPSOP: "Los registros o informes de capacitación deben estar fácilmente disponibles para demostrar que todos los empleados que realizan funciones relacionadas con GMP han completado los requisitos de capacitación" [5]. En la producción de carne cultivada, esta documentación es especialmente crítica para cumplir con las regulaciones de higiene, como el Reglamento (CE) 852/2004 y 853/2004 [1][2].
Gestión del Registro de Capacitación
Su sistema de registro de capacitación debe capturar detalles clave para cada empleado, incluyendo su nombre, ID, función laboral y el Currículo de Función Laboral (JFC) asignado que cubre toda la capacitación requerida. Esto incluye SOPs, capacitación en el trabajo y temas específicos del rol. Para la capacitación en SOP, el registro debe detallar el título del SOP, número de versión, fecha de finalización (que siempre debe ser antes de la fecha de vigencia de cualquier procedimiento nuevo o actualizado), y la firma del aprendiz. También debe documentar los resultados de las pruebas escritas (Nivel II) y evaluaciones prácticas (Nivel III), así como cualquier exención de capacitación [5] . Para la carne cultivada, asegúrese de que los registros cubran áreas esenciales como la obtención de células, aislamiento, proliferación y la gestión de medios de crecimiento y componentes residuales [1].
Prepare la Documentación para Auditorías
Para asegurar inspecciones fluidas, organice los registros para que puedan ser recuperados rápidamente. Establezca un sistema formal para crear, archivar y almacenar documentación de capacitación [5]. Todos los materiales de capacitación y herramientas de evaluación deben ser aprobados por el liderazgo de Calidad del Sitio y Producción. Asigne un Propietario del Sistema de Capacitación para supervisar el cumplimiento de los estándares de documentación [5]. Para la producción de carne cultivada, la documentación lista para auditoría debe incluir registros de personal y seguimiento de la procedencia de las células, detallando información como el origen de las células, fuente animal, detalles del proveedor y datos de biopsia [4]. Esto es especialmente importante porque, a finales de 2025, no existen procedimientos estandarizados para gestionar bancos de células en la producción de carne cultivada [4]. Además, su carpeta HACCP debe contener diagramas de flujo, análisis de peligros, procedimientos de monitoreo y registros de cualquier acción correctiva [1]. La Agencia de Normas Alimentarias aconseja: "Establezca documentos y registros acordes con la naturaleza y el tamaño del negocio alimentario para demostrar la aplicación efectiva de las medidas [de seguridad]" [1].
sbb-itb-ffee270
Paso 4: Programar Capacitación y Recalificación Regular
Mantener el cumplimiento de las GMP es un proceso continuo. A medida que evolucionan las regulaciones y los procesos, es esencial actualizar regularmente las calificaciones del personal y mantener un control estricto sobre su sistema de capacitación. Esto incluye revisar constantemente los Currículos de Funciones de Trabajo individuales para asegurar que todos los materiales de capacitación estén actualizados [5]. Para la producción de carne cultivada, esto es especialmente importante debido a la naturaleza emergente de la industria y su entorno regulatorio en constante cambio.
Proceso Anual de Recalificación
La frecuencia de la recalificación puede variar entre sitios, pero la mayoría de los sistemas GMP incluyen "Capacitación en Conceptos GMP" periódica para reforzar la comprensión y la aplicación adecuada de los estándares [5]. Las sesiones anuales deben adaptarse a las necesidades específicas de su instalación, incorporando datos como incidentes de contaminación o hallazgos de auditoría para abordar áreas que requieren mejora. Para las operaciones de carne cultivada, donde las tasas de fallos por lote pueden alcanzar hasta el 19.5% [7], los esfuerzos de reentrenamiento deben centrarse en técnicas asépticas y monitoreo ambiental.
Más allá de estos cursos de actualización anuales, la recualificación también debe ser activada por cualquier cambio en los productos, procesos o SOPs. La capacitación debe completarse antes de la fecha de vigencia de la SOP actualizada [5]. Para citar a la Agencia de Normas Alimentarias:
"Cuando se realice cualquier modificación en el producto, proceso o cualquier paso, los operadores de empresas alimentarias deberán revisar el procedimiento y realizar los cambios necesarios en él" [1].
Por ejemplo, si un nuevo protocolo de limpieza de biorreactores está programado para entrar en vigor el 15 de marzo, todo el personal relevante debe completar su capacitación y demostrar competencia antes de esa fecha. Estos cursos de actualización regulares, combinados con actualizaciones por cambios regulatorios, aseguran que el cumplimiento siempre esté a la altura del estándar.
Actualización de la Formación con Cambios Regulatorios
Además de la recualificación anual, es importante actualizar los programas de formación para reflejar los cambios en los requisitos regulatorios. La industria de la carne cultivada opera dentro de un marco regulatorio complejo y en evolución. En el Reino Unido, por ejemplo, los productos cultivados se clasifican como Productos de Origen Animal (POAO) y deben cumplir con las regulaciones de higiene bajo el Reglamento (CE) 852/2004 y 853/2004 [1]. Los programas de formación deben adaptarse para cumplir con estos estándares e incorporar iniciativas como el programa sandbox de la FSA, que se llevará a cabo de 2025 a 2027 [1].
El personal también debe comprender el panorama regulatorio más amplio. Para las empresas que operan internacionalmente o que obtienen materiales de los EE. UU., es crucial estar familiarizado con el modelo de supervisión conjunta.En este sistema, la FDA supervisa la recolección, almacenamiento y cultivo de células, mientras que el USDA-FSIS se encarga de la cosecha, procesamiento, empaquetado y etiquetado de ganado, aves de corral y bagre [6] [8]. A medida que la industria avanza hacia la producción sin antibióticos y el uso de materiales de grado alimenticio, también será necesario capacitarse nuevamente en técnicas asépticas más estrictas [7].
Para asegurar transiciones fluidas, programe actualizaciones con anticipación, notifique a los empleados de inmediato y organice sesiones obligatorias de recuperación para cualquiera que falte a la capacitación inicial [5]. Este enfoque proactivo mantiene a su equipo preparado para cambios regulatorios y operativos.
Paso 5: Implementar un Sistema de Seguimiento de Calificaciones
Una vez que sus programas de capacitación están en su lugar, las evaluaciones están completas y la documentación está organizada, el siguiente paso es implementar un sistema de seguimiento de calificaciones confiable. Este sistema asegura que las calificaciones del personal y los plazos de recertificación se monitoreen de manera efectiva. Para las instalaciones de carne cultivada, donde la producción involucra procesos complejos como la obtención y cosecha de células, este tipo de supervisión es esencial. Conecta la capacitación, las evaluaciones y la preparación para auditorías, asegurando que el cumplimiento se lleve a cabo sin problemas en toda su cadena de producción.
Construir una Matriz de Calificaciones
La matriz de calificaciones es una extensión de los programas de capacitación personalizados discutidos anteriormente. Proporciona un desglose detallado de las competencias específicas de cada rol, utilizando el Currículo de Función Laboral (JFC) como guía [5]. El JFC describe toda la capacitación necesaria: Procedimientos Operativos Estándar (SOPs), capacitación en el trabajo y principios de GMP, que deben mantenerse actualizados. Para la producción de carne cultivada, la matriz debe cubrir todo el flujo de trabajo, incluyendo la gestión de líneas celulares, técnicas de proliferación, manejo de medios de crecimiento, protocolos de cosecha y almacenamiento [1].
Su matriz también debe categorizar la capacitación en diferentes niveles de profundidad. Por ejemplo:
- Capacitación en comunicación: Se enfoca en la conciencia general.
- Capacitación en conocimiento: Proporciona la información necesaria para la supervisión rutinaria.
- Capacitación en habilidades/desempeño: Involucra tareas prácticas con evaluaciones de competencia [5].
Por ejemplo, un gerente de aseguramiento de calidad podría necesitar capacitación a nivel de conocimiento sobre operaciones de biorreactores, mientras que un técnico de producción requeriría capacitación a nivel de habilidades, completa con evaluaciones documentadas. Este enfoque asegura que su capacitación se alinee con los requisitos de documentación de HACCP [1].
Utilice Herramientas de Seguimiento Digital
Si bien los registros manuales pueden funcionar para equipos más pequeños, las herramientas de seguimiento digital son mucho más eficientes a medida que las operaciones crecen. Estas herramientas no solo automatizan el mantenimiento de registros, sino que también proporcionan actualizaciones en tiempo real sobre los estados de capacitación y le alertan sobre los próximos plazos de recualificación [5]. Integrar estas herramientas en su Programa de Gestión de Calidad asegura una cobertura integral del ciclo de vida de producción [3]. En las instalaciones de carne cultivada, los sistemas digitales pueden rastrear la competencia del personal en el manejo de desafíos únicos como nuevos alérgenos, residuos de medios de crecimiento y riesgos de contaminación microbiana [1].
Una característica clave de las herramientas digitales es la capacidad de establecer disparadores de recualificación automatizados. Por ejemplo, si hay un cambio en un producto, proceso o SOP, el sistema puede marcar automáticamente a los miembros del equipo relevantes para la reentrenamiento [1]. Esto asegura el cumplimiento del Reglamento (CE) 852/2004, que obliga a las empresas alimentarias a mantener procedimientos basados en los principios de HACCP [1]. Herramientas como MyHACCP de la FSA pueden complementar su sistema al ayudar a gestionar los registros de seguridad alimentaria junto con los registros de capacitación [1].
Conclusión
Garantizar que el personal cumpla con los estándares de GMP en la producción de carne cultivada es un pilar de cumplimiento normativo, seguridad del producto y preparación para el mercado. Cada paso en el proceso construye un marco que protege estos elementos críticos. Como se destaca en Mejores Prácticas & Investigación en Hematología Clínica, "Implementar regulaciones y principios actuales de Buenas Prácticas de Manufactura (GMP) incluso en las fases iniciales de estudios de terapias basadas en células es crucial para garantizar la seguridad y calidad reproducible de estos productos" [3].
La industria de la carne cultivada enfrenta desafíos únicos, particularmente en la gestión de riesgos biológicos y químicos en todas las etapas de producción.Las apuestas son altas, y las iniciativas como el programa de sandbox regulatorio de la FSA han permitido a empresas como Mosa Meat, BlueNalu, y Roslin Technologies influir en el desarrollo de futuros estándares de seguridad [2]. Para mantenerse competitivo y cumplir con las normativas, es esencial que los programas de formación interna se alineen con estos requisitos en evolución.
Adoptar prácticas estandarizadas beneficia más que solo la aprobación regulatoria; también agiliza el camino al mercado. Según la Investigación y Evidencia de la FSA, "Estandarizar tales métodos también podría facilitar los procesos de aprobación de productos, para que los productos de carne cultivada puedan llegar al mercado más rápido" [4]. Sin embargo, a finales de 2025, no existen reglas estandarizadas a nivel mundial para gestionar bancos de células en la producción de carne cultivada. Establecer estas prácticas es crucial para integrar la formación y la adquisición sin problemas en sus operaciones.
Un programa de calificación sólido también depende de obtener los materiales y equipos adecuados.
Preguntas Frecuentes
¿Qué significa 'competente' para los roles de GMP en carne cultivada?
Estar preparado para los roles de GMP en carne cultivada implica tener la capacitación, habilidades y conocimientos adecuados para cumplir con los estándares GMP. Esto significa estar familiarizado con los sistemas de calidad, reconocer los riesgos de contaminación y comprender los requisitos regulatorios. Estas expectativas se detallan en las directrices relacionadas con las calificaciones del personal y los sistemas de capacitación.Asegurarse de que el personal esté bien capacitado es crucial para cumplir con las normativas y mantener altos estándares de producción en las instalaciones de carne cultivada.
¿Con qué frecuencia debe llevarse a cabo la recualificación de GMP?
La recualificación bajo las directrices de GMP debe seguir intervalos establecidos por evaluaciones de riesgo exhaustivas. Generalmente, se recomienda un ciclo de dos años. Sin embargo, ciertos equipos, como las prensas de tabletas, podrían justificar extender esto a tres años según su uso y procesos específicos. Es crucial adaptar los horarios de recualificación para cumplir tanto con las demandas operativas como con los requisitos regulatorios.
¿Qué registros de capacitación esperan ver primero los inspectores?
Los inspectores a menudo examinan los registros de capacitación para confirmar que el personal ha completado la capacitación requerida de GMP (Buenas Prácticas de Manufactura). Estos registros deben reflejar claramente la comprensión, habilidades y capacidades de los empleados relevantes a sus responsabilidades específicas.Es esencial asegurar que toda la formación esté completamente documentada y muestre adherencia a los requisitos de GMP.











