Elegir entre líneas celulares bovinas y porcinas es una decisión crítica para la producción de carne cultivada. Cada tipo de célula ofrece ventajas y desafíos distintos, que afectan la escalabilidad, los requisitos de medios y la capacidad de crear productos cárnicos estructurados. Aquí hay un resumen rápido:
- Líneas celulares bovinas son adecuadas para la producción de tejido muscular, particularmente para productos como bistecs. Sobresalen en el marmoleo, pero enfrentan desafíos con la diferenciación a largo plazo y requieren modificaciones genéticas para la escalabilidad.
- Líneas celulares porcinas son ideales para la producción de grasa, con inmortalización espontánea y crecimiento estable durante cientos de duplicaciones. Son rentables para la producción a gran escala, pero pueden requerir un tiempo preciso para la co-diferenciación con células musculares.
Comparación Rápida
| Atributo | Líneas Celulares Bovinas | Líneas Celulares Porcinas |
|---|---|---|
| Tiempo de Duplicación | ~39 horas (pasajes tempranos) | 20–24 horas (pasajes tempranos) |
| Inmortalización | Requiere modificación genética | Espontánea |
| Diferenciación | Fuerte al principio, disminuye después de ~25 duplicaciones | Eficiencia adipogénica estable (>200 duplicaciones) |
| Costos de Medios | Más altos debido a factores de crecimiento recombinantes | Más bajos con medios suplementados con hemo |
| Adecuación para Carne Estructurada | Adecuado para marmoleo y separación músculo-grasa | Efectivo para co-diferenciación grasa-músculo |
Ambas líneas celulares tienen fortalezas y limitaciones únicas, lo que hace que la elección dependa de los objetivos del producto y las estrategias de producción.
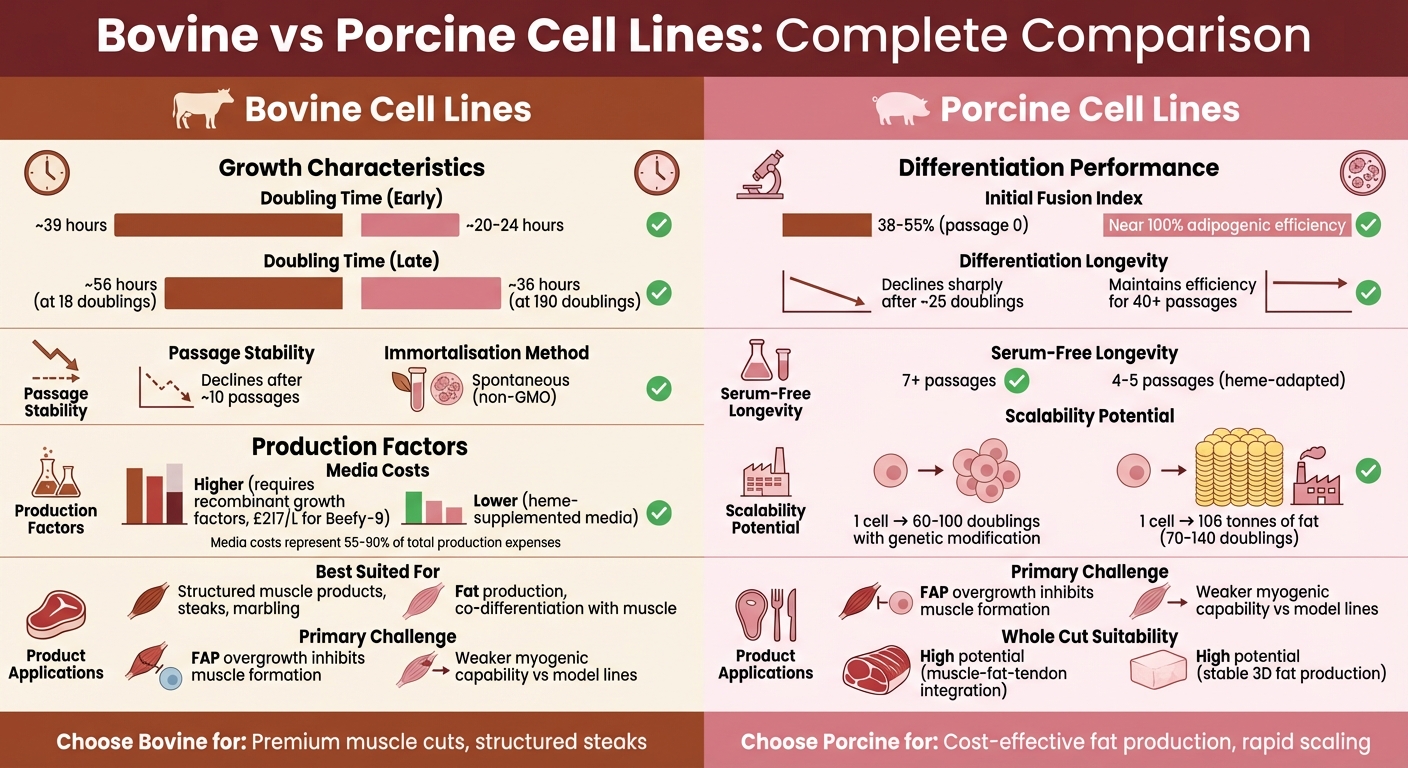
Comparación de Líneas Celulares Bovinas vs Porcinas para la Producción de Carne Cultivada
Líneas Celulares Bovinas
Aplicaciones en Carne Cultivada
Las líneas celulares bovinas son particularmente adecuadas para producir productos cárnicos estructurados como filetes y otros cortes premium. Una de sus características destacadas es su capacidad para desarrollar un marmoleado auténtico: la grasa intramuscular responsable del sabor y la textura distintivos de la carne de res. Este marmoleado se logra a través del papel de células satélite bovinas (BSCs), que forman el componente muscular, y progenitores fibro-adipogénicos (FAPs), que generan grasa con un perfil de ácidos grasos casi idéntico a la grasa subcutánea bovina natural [2].
Crear un marmoleado adecuado requiere una coordinación cuidadosa durante la diferenciación.A diferencia de los sistemas porcinos, que pueden diferenciar simultáneamente músculo y grasa, los sistemas bovinos generalmente manejan la diferenciación de células miogénicas (formadoras de músculo) y adipogénicas (formadoras de grasa) por separado. Estos componentes se combinan luego para lograr un control preciso sobre la proporción de grasa a músculo. Si bien este método permite una mayor personalización, también introduce una complejidad adicional al proceso de producción [2].
Características de Crecimiento
Aunque las células bovinas son efectivas para generar tanto músculo como grasa, su dinámica de crecimiento presenta desafíos para la producción a gran escala. Un problema clave surge con las células satélite bovinas, que pierden su capacidad de diferenciarse a medida que continúan proliferando. Por ejemplo, los mioblastos bovinos primarios pueden experimentar entre 60 y 100 duplicaciones de población mientras mantienen un cariotipo normal.Sin embargo, su capacidad para fusionarse en miotubos, un paso esencial para la formación de tejido muscular, disminuye significativamente después de aproximadamente 25 duplicaciones. Esta limitación crea un cuello de botella para escalar la producción, que requiere aproximadamente 2.9×10¹¹ células por kilogramo de masa húmeda [7].
En mayo de 2023, investigadores del Centro de Agricultura Celular de la Universidad de Tufts abordaron este problema desarrollando células satélite bovinas genéticamente inmortalizadas (iBSCs). Al introducir la transcriptasa inversa de Telomerasa bovina (TERT) y la quinasa dependiente de ciclina 4 (CDK4), estas células pudieron superar las 120 duplicaciones mientras seguían formando miotubos multinucleados. Andrew J.Stout de la Universidad de Tufts enfatizó la importancia de este avance:
"Para que la carne cultivada tenga éxito a gran escala, las células musculares de especies relevantes para la alimentación deben expandirse in vitro de manera rápida y confiable para producir millones de toneladas métricas de biomasa anualmente." [5]
El rendimiento del crecimiento también está fuertemente influenciado por factores como la densidad de siembra y la formulación del medio. Por ejemplo, las células madre derivadas de tejido adiposo bovino (bASCs) mostraron un crecimiento óptimo a una densidad de siembra de 1,500 células/cm², logrando una expansión de 28 veces en matraces de agitación al usar una estrategia de intercambio de medio del 80% [1]. Además, los medios químicamente definidos sin suero han demostrado apoyar el crecimiento exponencial de los mioblastos bovinos a tasas que alcanzan el 97% de las logradas con medios tradicionales que contienen suero [6] . Esto no solo reduce costos, sino que también se alinea con consideraciones éticas, lo que lo convierte en un enfoque prometedor para la producción futura.
Estos rasgos de crecimiento específicos de bovinos proporcionan una base sólida para compararlos con líneas celulares porcinas en el contexto de la producción de carne cultivada.
sbb-itb-ffee270
Líneas Celulares Porcinas
Aplicaciones en Carne Cultivada
Las líneas celulares porcinas son fundamentales en la producción de adipocitos uniloculares maduros que se asemejan estrechamente a la grasa de cerdo natural[9].
Un ejemplo destacado es la línea celular FaTTy, creada a través de la inmortalización espontánea. Esta línea celular demuestra una impresionante eficiencia adipogénica de ~100% a lo largo de 200 duplicaciones, produciendo perfiles de ácidos grasos que se alinean estrechamente con los encontrados en la grasa de cerdo nativa. Los adipocitos cultivados derivados de esta línea pueden alcanzar volúmenes de lípidos de hasta 96,670 μm³.Como explica el equipo de investigación FaTTy:
"FaTTy es una línea celular de ganado única con un fenotipo adipogénico distintivo caracterizado por la capacidad de diferenciarse de manera confiable con alta eficiencia bajo una variedad de condiciones de cultivo, y de generar adipocitos maduros que muestran perfiles de ácidos grasos comparables a la grasa nativa." [9]
Otra línea celular notable, PK15H, prospera en concentraciones de medios altos en hemo de hasta 40 mM. Esta característica ayuda a replicar el color rico y el sabor cargado de hierro típico del cerdo tradicional[3]. Además, la grasa porcina cultivada puede ajustarse para composiciones lipídicas más saludables, logrando relaciones de ácidos grasos monoinsaturados a saturados de 3.2, en comparación con la relación de 1.4 que se encuentra comúnmente en el tejido nativo[9].
Características de Crecimiento
Las líneas celulares porcinas no solo son hábiles en la producción de grasa, sino que también destacan en términos de crecimiento y escalabilidad. Exhiben una expansión estable y rápida, lo que las hace particularmente adecuadas para la producción a gran escala. Por ejemplo, la línea FaTTy comienza con un tiempo de duplicación poblacional de 20–24 horas, que solo se ralentiza ligeramente a 22–36 horas entre las duplicaciones 140 y 190. Esta consistencia es un cambio de juego, ya que una sola célula FaTTy expandida de 70 a 140 duplicaciones poblacionales podría teóricamente producir 106 toneladas de grasa dentro de un período de diferenciación de 11 días[9] .
Una ventaja importante de estas líneas celulares es su inmortalización espontánea, lo que permite una expansión a largo plazo sin la necesidad de modificación genética. Este estado no transgénico es una victoria regulatoria.Destacando esto, la Universidad de Ulsan College of Medicine señaló:
"Nuestro estudio informa sobre una célula porcina cultivable en medios ricos en hemo que puede mantenerse en condiciones sin suero." [3]
Además, las células madre musculares porcinas muestran una escalabilidad notable, con tasas de expansión de 10⁶ a 10⁷ veces, capaces de producir entre 100 g y 1 kg de carne cultivada[10]. Los avances en técnicas de clasificación celular, utilizando marcadores como CD31, CD45, JAM1, ITGA5 e ITGA7, han mejorado significativamente el aislamiento de células madre musculares de alta pureza. Estos métodos ofrecen un aumento del 20% en las tasas de positividad de PAX7 en comparación con técnicas anteriores[11]. Esta mejora asegura que el potencial miogénico se preserve a través de múltiples pasajes, abordando el problema común de la capacidad de diferenciación disminuida durante la expansión prolongada.
Estas ventajas de crecimiento y diferenciación hacen que las células porcinas sean una opción destacada sobre las células bovinas para la producción de carne cultivada.
ICAN Seminario web sobre Líneas Celulares y Medios de Cultivo para Aplicaciones de Carne Cultivada
Tasas de Crecimiento y Proliferación Comparadas
Vamos a profundizar en cómo se comparan las líneas celulares porcinas y bovinas en términos de crecimiento y proliferación. líneas celulares porcinas, como la línea FaTTy inmortalizada espontáneamente, son notablemente más rápidas. Su tiempo de duplicación de población inicial es de solo 20–24 horas [9]. En contraste, las células satélite bovinas, incluso cuando se cultivan en medios optimizados sin suero como Beefy-9, tardan alrededor de 39 horas por duplicación [12].
Las diferencias se vuelven aún más claras a lo largo de múltiples pasajes.Las células satélite bovinas primarias tienden a perder tanto su capacidad de proliferación como de diferenciación después de aproximadamente 10 pasajes [2]. Por otro lado, la línea porcina FaTTy ha mantenido casi un 100% de eficiencia adipogénica a lo largo de más de 200 duplicaciones de población. Incluso en etapas posteriores, su tiempo de duplicación solo aumenta modestamente a 22–36 horas [9]. Un estudio de mayo de 2022 de la Universidad de Tufts destacó que las células bovinas en Beefy-9 lograron 18.2 duplicaciones de población en siete pasajes (28 días) mientras mantenían más del 96% de stemness Pax7⁺ [12]. Mientras tanto, un informe de enero de 2025 de la Universidad de Edimburgo confirmó que la línea FaTTy superó las 200 duplicaciones sin perder su potencial de diferenciación [9].
También hay un marcado contraste en cómo estas células logran la inmortalización.Las células bovinas típicamente necesitan ingeniería genética - comúnmente a través de la sobreexpresión de TERT y CDK4 - para sostener una expansión a largo plazo más allá de 120 duplicaciones [5]. En comparación, las células porcinas como la línea FaTTy logran inmortalización espontánea sin modificación genética. Esto ofrece una clara ventaja regulatoria, especialmente en mercados cautelosos con los OGM [9].
htmlTabla de Comparación
| Característica | Células Satélite Bovinas | MSCs Porcinas (Línea FaTTy) |
|---|---|---|
| Tiempo Promedio de Duplicación | ~39 horas (optimizado sin suero) [12] | 20–24 horas (pasajes tempranos) [9] |
| Tiempo de Duplicación en Pasajes Tardíos | ~56 horas (a 18 duplicaciones) [12] | ~36 horas (a 190 duplicaciones) [9] |
| Estabilidad de Pasaje | Declina después de ~10 pasajes [2] | Estable para >200 duplicaciones [9] |
| Método de Inmortalización | Ingeniería (TERT/CDK4) [2] | Espontáneo [9] |
| Capacidad de célula madre/Diferenciación | >96% Pax7⁺ (hasta el pasaje 6) [12] | Cerca del 100% de eficiencia adipogénica [9] |
Vale la pena señalar que las células satélite in vivo se duplican en aproximadamente 17 horas, lo que resalta la dificultad de igualar las tasas de crecimiento natural in vitro [12].
Requisitos de medios y eficiencia de diferenciación
Dependencia de medios comparada
Los costos de los medios pueden dominar la producción de carne cultivada, a menudo representando del 55% al 90% de los gastos, y en algunos sistemas, incluso superando el 99% [3][12].
Para las células bovinas, un requisito común es el 20% de suero fetal bovino, lo que puede ser un gasto significativo en medios [12]. Una alternativa sin suero, Beefy-9, utiliza un medio basal B8 combinado con albúmina humana recombinante. Los costos varían según la fuente y el volumen del pedido, por lo que es mejor consultar al proveedor o la página del producto para obtener detalles actuales de precios [12]. Sin embargo, los altos niveles de albúmina en medios sin suero pueden obstaculizar la adhesión celular, por lo que la albúmina recombinante se agrega típicamente 24 horas después del pase [12].
Las líneas celulares porcinas adoptan un enfoque diferente para la adaptación sin suero. Las células PK15, por ejemplo, utilizan extractos de hemo bacteriano de Corynebacterium [3]. El hemo no solo reduce la dependencia del suero, sino que también mejora el sabor y el color. Dicho esto, concentraciones superiores a 10 mM pueden volverse tóxicas, aunque las células porcinas pueden tolerar hasta 40 mM debido a la regulación al alza de los genes de desintoxicación [3]. A pesar de esta tolerancia, las células porcinas cultivadas en medios suplementados con hemo generalmente permanecen viables solo durante 4-5 pasajes, mientras que las células bovinas cultivadas en Beefy-9 pueden mantener el crecimiento durante siete o más pasajes [3][12].
Ambos tipos de células dependen en gran medida del factor de crecimiento de fibroblastos-2 (FGF-2).Las células bovinas, por ejemplo, pueden mantener el crecimiento a corto plazo incluso cuando los niveles de FGF-2 se reducen de 40 ng/mL a 5 ng/mL [12]. Además, el uso de medios con bajo contenido de glucosa (1 g/L) ayuda a retener los marcadores de pluripotencia en las células bovinas [13].
Estos requisitos específicos de los medios son críticos al escalar la producción e influyen directamente en la eficiencia de diferenciación.
Eficiencia de Diferenciación
Aunque los costos de los medios son un factor significativo, la eficiencia de diferenciación también juega un papel importante en la determinación de la escalabilidad de la carne cultivada.
Las células bovinas enfrentan desafíos con la eficiencia de diferenciación a medida que se expanden. Por ejemplo, los mioblastos bovinos de ganado Belgian Blue inicialmente logran un índice de fusión de alrededor del 55% a las 14 duplicaciones de población, pero esto cae bruscamente a menos del 10% a las 25 duplicaciones [7]. De manera similar, las células bovinas derivadas de fetos comienzan con índices de fusión más altos (alrededor del 54.6%) en comparación con las células derivadas de adultos (aproximadamente 38.0%), sin embargo, ambas experimentan una disminución en la capacidad de diferenciación de aproximadamente 6.81% por pasaje [7].
Las células porcinas, por otro lado, muestran un rendimiento más estable. La cepa inmortalizada de preadipocitos porcinos ISP-4 mantiene una alta eficiencia de diferenciación adipogénica durante más de 40 pasajes, logrando un aumento de 100 veces en la acumulación de lípidos durante un protocolo de diferenciación de 8 días [8]. Esto hace que las células porcinas sean particularmente atractivas para la producción de grasa, mientras que las células bovinas son más adecuadas para la diferenciación muscular en los primeros pasajes pero tienen dificultades con el mantenimiento a largo plazo.
| Característica | Células Satélite Bovinas | Líneas Celulares Porcinas |
|---|---|---|
| Índice de Fusión Inicial | 38–55% (pasaje 0) [7] | No especificado para músculo |
| Longevidad de Diferenciación | Disminuye drásticamente después de ~25 duplicaciones [7] | Mantiene eficiencia por más de 40 pasajes (ISP-4 adipogénico) [8] |
| Longevidad sin Suero | Sostiene el crecimiento por más de 7 pasajes [12] | Viable por 4–5 pasajes (adaptado a hemo) [3] |
| Suplementos Clave | Albúmina recombinante, FGF-2 [12] | Extracto de hemo, insulina, dexametasona [3][8] |
| Producción de lípidos | Mínimo (enfoque muscular) | Aumento de 100 veces (ISP-4) [8] |
Adecuación para productos cárnicos estructurados
La elección de las líneas celulares juega un papel fundamental en la configuración no solo de las condiciones de crecimiento y medios, sino también de la estructura de los productos cárnicos cultivados.Cuando se busca replicar la textura y apariencia de un filete o chuleta de cerdo, es esencial equilibrar las células de grasa y músculo en las proporciones correctas.
Co-Diferenciación de Grasa-Músculo
Las líneas celulares bovinas y porcinas se comportan de manera diferente cuando se trata de co-diferenciación. Los cultivos celulares bovinos a menudo enfrentan desafíos como el sobrecrecimiento de FAP (progenitor fibro-adipogénico), que interrumpe el desarrollo muscular al reducir el índice de fusión. Además, los adipocitos en estos cultivos liberan señales, como la miostatina e IL-6, que bloquean la expresión de miogenina, deteniendo efectivamente la formación de fibras musculares[16].
Para abordar esto, los investigadores de Mosa Meat crearon un medio de crecimiento optimizado sin suero (i-SFGM). Este medio incluye triyodotironina (T3) y un aumento de HGF mientras excluye PDGF-BB para controlar el sobrecrecimiento de FAP.También utilizan adiposferas modulares (200–400 µm) para mantener las células de grasa y músculo físicamente separadas durante las etapas iniciales de crecimiento[4][14] .
Las líneas celulares porcinas, por otro lado, muestran un enfoque más coordinado para la co-diferenciación. La cepa de preadipocitos ISP-4, por ejemplo, funciona bien con células satélite musculares porcinas, produciendo un veteado que se asemeja a la carne convencional. Este proceso implica una fase de inducción adipogénica de 48 horas, seguida de 96 horas en suero de caballo al 2% para desencadenar la miogénesis. Esto da como resultado fibras musculares maduras entrelazadas con adipocitos[8]. Sin embargo, las células satélite musculares porcinas tienden a tener capacidades miogénicas más débiles en comparación con líneas modelo estándar como C2C12, requiriendo un tiempo preciso para asegurar que los adipocitos no dominen el cultivo[8].
Estas diferencias en la diferenciación destacan los desafíos y oportunidades únicos que cada tipo de célula presenta para escalar la producción.
Escalabilidad y Desafíos de Producción
Escalar la producción de carne cultivada estructurada requiere un rendimiento celular consistente. Las líneas celulares porcinas tienden a ser más escalables. Por ejemplo, la línea FaTTy inmortalizada espontáneamente mantiene casi un 100% de eficiencia adipogénica durante 200 duplicaciones de población[9]. Expandir una línea celular porcina de 70 a 140 duplicaciones podría producir teóricamente hasta 106 toneladas de grasa[9]. Además, la cepa ISP-4 ha demostrado un aumento de 40 veces en la densidad celular en seis días cuando se cultiva en microportadores en un sistema de matraz agitador[8].
"FaTTy es una línea celular de ganado única con un fenotipo adipogénico distintivo...estas características, junto con su naturaleza no transgénica, hacen de FaTTy una herramienta fundamental muy prometedora." – Nature Food, 2025[9]
Las líneas celulares bovinas enfrentan más obstáculos. La contaminación por FAP reduce su capacidad para diferenciarse eficazmente en tejido muscular[4]. Además, el alto costo de factores de crecimiento como FGF-2 y TGF-β - que a menudo representan más del 90% de los gastos de medios - hace que escalar líneas celulares bovinas sea más caro[17]. Estas células también requieren recubrimientos especializados, como Laminin-521, para promover la adhesión de células satélite y minimizar la interferencia de FAP[4].
La producción de una tonelada de carne cultivada involucra alrededor de 10¹³ células, y los productos estructurados como los cortes enteros requieren sistemas de producción avanzados, como reactores de perfusión o de lecho empacado, para soportar los andamios 3D y biomateriales necesarios para su desarrollo[15].
htmlTabla de Comparación
| Atributo | Líneas Celulares Bovinas | Líneas Celulares Porcinas |
|---|---|---|
| Desafío Principal de Escalabilidad | Crecimiento excesivo de FAP en cultivos musculares[4] | Adaptación a cultivo en suspensión/sin suero[9] |
| Estabilidad de Diferenciación | Declina después de ~10 pasajes[2] | Cepas como FaTTy estables para >200 duplicaciones[9] |
| Co-Diferenciación | Los adipocitos inhiben la miogénesis[16] | Prototipos exitosos de marmoleo logrados[2][8] |
| Resistencia Estructural | Alta; capaz de integrar músculo-grasa-tendón[14] | Moderada; enfoque en el crecimiento de fibras alineadas[14] |
| Aptitud para Corte Completo | Alto potencial, limitado por la interferencia de FAP[4] | Alto potencial debido a la producción estable de grasa 3D[9] |
| Desafío de Textura | Reducción de cohesividad después de cocinar[14] | Tiende a ser más suave que el cerdo comercial[14] |
Conclusión
Decidir entre líneas celulares bovinas y porcinas implica equilibrar sus distintos beneficios y desafíos en la producción de carne cultivada.Las células satélite bovinas son una vía directa para crear tejido muscular esquelético y se benefician de las formulaciones de medios sin suero existentes como Beefy-9 [2]. Por otro lado, las líneas celulares porcinas ya se han utilizado para desarrollar prototipos de cerdo cultivado y muestran potencial en la co-diferenciación con células satélite para crear estructuras de carne marmoleada [2].
La escalabilidad sigue siendo un obstáculo importante. Los costos de los medios y la escalabilidad de los biorreactores representan del 55% al 90% de los gastos totales de producción, y la disponibilidad de líneas celulares optimizadas sigue siendo limitada, lo que ralentiza el progreso comercial [3][2] .
"Las líneas celulares utilizadas en la producción de carne cultivada determinan en última instancia muchas de las variables posteriores a considerar." – GFI [2]
Preguntas Frecuentes
¿Qué línea celular es mejor para productos de corte entero como filetes o chuletas?
Las líneas celulares derivadas de células progenitoras residentes en el músculo, como las células satélite, son a menudo ideales para producir productos de corte entero como filetes o chuletas. Estas células tienen la capacidad de desarrollarse en tejido muscular maduro, creando la textura y forma estructurada necesaria para estos tipos de productos.
¿Cómo elijo entre inmortalización genética e inmortalización espontánea?
Elegir cómo inmortalizar células para la producción de carne cultivada depende de sus prioridades, incluyendo seguridad, escalabilidad y consideraciones regulatorias.
Inmortalización genética implica introducir genes específicos, como la telomerasa, para lograr un control preciso sobre la capacidad de las células para dividirse indefinidamente.Si bien este método ofrece previsibilidad y consistencia, puede generar preocupaciones sobre la modificación genética y los riesgos potenciales, como la tumorigenicidad.
Por otro lado, la inmortalización espontánea ocurre naturalmente con el tiempo en cultivos celulares a largo plazo. Este enfoque evita la ingeniería genética, lo que podría facilitar la aprobación regulatoria y aumentar la aceptación entre los consumidores que desconfían de la modificación genética.
Ambos métodos tienen sus fortalezas y desafíos, ofreciendo diferentes caminos hacia la producción escalable de carne cultivada. La elección depende en última instancia de equilibrar el control, los obstáculos regulatorios y la confianza del consumidor.
¿Cuál es el mayor impulsor de costos en los medios para células bovinas frente a porcinas?
El mayor gasto en la producción de medios para células bovinas y porcinas se reduce al costo y la complejidad de sus componentes.Desarrollar y ajustar formulaciones de medios es un gran obstáculo, especialmente porque los medios representan al menos el 50% de los costos operativos variables. Además, los ajustes adaptados a cada especie añaden otra capa de complejidad. Estos aspectos juegan un papel importante en la configuración de los costos de producción generales de la carne cultivada.











