מעבר מסרום עוברי של בקר (FBS) למדיה ללא סרום (SFM) הוא קריטי להגדלת ייצור בשר מתורבת. הסתמכות על FBS יוצרת אתגרים כמו עלויות גבוהות, אספקה מוגבלת ואיכות לא עקבית. SFM מציע חלופה בטוחה ומבוקרת יותר, אך הוא מגיע עם מכשולים:
- בעיות היצמדות תאים: מיובלסטים מתקשים להיצמד ללא סרום, ולעיתים נדרשים ציפויים יקרים כמו למינין או Matrigel. מדיה מותנית או תוספים ספציפיים יכולים לשפר את ההיצמדות.
- קצב גידול איטי יותר: מערכות ללא סרום חסרות חומרים מזינים חיוניים, מה שמוביל להפחתת התרבות ולהצטברות אמוניה. הוספת גורמי גידול והחלפת גלוטמין באלטרנטיבות יכולות לעזור.
- ביצועי מדיה לא עקביים: רבים מה-SFM המסחריים, המותאמים לתאי אדם, אינם תומכים ביעילות בגידול מיובלסטים של בעלי חיים. בדיקה על פני מינים ובמשך תקופות ארוכות יותר עם ערכת גילוי אופטימיזציית מדיה היא קריטית.
הפתרונות כוללים נוסחאות מותאמות, החלפה חלקית של המדיום, ומערכות תרבית משותפת כדי לדמות תנאים דמויי סרום. בעוד ש-SFM יכול להתקרב לביצועים של מערכות FBS, המעבר לביוראקטורים תלת-ממדיים מציג מורכבויות כמו הידבקות וניהול פסולת. ניטור קפדני של איכות התאים מבטיח הצלחה בייצור בקנה מידה גדול.
המעבר ל-SFM אינו רק עניין של מדע טוב יותר - הוא הופך להכרח ככל שמחירי ה-FBS ממשיכים לעלות. חוקרים ויצרנים חייבים להתמקד באופטימיזציה של המדיום ובמקור חומרים אמינים כדי להפוך את ייצור הבשר המתורבת לבר-קיימא ולחסכוני.
פיגומים מבוססי צמחים המשרים הידבקות תאים ללא סרום לבשר מתורבת - אינדי גורס - ISCCM9
sbb-itb-ffee270
בעיות נפוצות במדיה ללא סרום למיובלסטים
מעבר מנוסחאות מבוססות סרום לנוסחאות ללא סרום יכול להציג מספר אתגרים טכניים שמפריעים לזרימות עבודה ומעלים עלויות. בעיות אלו מופיעות לעיתים קרובות בדרכים ספציפיות, החל מהידבקות תאים.
הפחתת הידבקות והישרדות תאים
אחד המכשולים הגדולים ביותר הוא שמיובלסטים לא נצמדים היטב במדיה ללא סרום. סרום מספק באופן טבעי תערובת של חלבונים, גורמי גדילה וליפידים שעוזרים לתאים להידבק למשטחים. ללא רכיבים אלו, מיובלסטים מתקשים להידבק, מה שמוביל לעיתים קרובות למוות תאי מוקדם.
כדי להתמודד עם זה, מערכות רבות ללא סרום מסתמכות על חומרי ציפוי יקרים כמו למינין 511 או Matrigel. אבל גם עם הציפויים האלה, רמות ההצמדה לעיתים קרובות נופלות ממה שנראה בתרביות מבוססות סרום. לדוגמה, מחקר מ-2024 מצא שמדיה סטנדרטית ללא סרום תמכה רק ב-2,210 ± 319 תאים/סמ"ר על כלים לא מצופים. לעומת זאת, מדיה מותנית ללא סרום - שהושלמה עם גורמים מופרשים מקווי תאים אחרים - כמעט שילשה את המספר הזה ל-5,985 ± 1,558 תאים/סמ"ר [2].
בעיה נוספת היא רגישות מוגברת לאנטיביוטיקה. בהגדרות ללא סרום, אנטיביוטיקות כמו פניצילין, סטרפטומיצין ואמפוטריצין B יכולות להפחית את ההתרבות עד 62%, בהשוואה להפחתה של 20–26% במערכות מבוססות סרום [1]. ללא האלמנטים המגנים של הסרום, תאים פגיעים יותר ללחץ, מה שמקשה עוד יותר על הישרדותם וצמיחתם.
צמיחת תאים איטית יותר
גם אם תאים מצליחים להיצמד, קצב הצמיחה לעיתים קרובות מפגר מאחור.סרום מספק חומרים מזינים חיוניים כמו גורמי גדילה, ציטוקינים, כולסטרול וחומצות שומן - רבים מהם חסרים או לא מספקים ברוב הפורמולציות המסחריות ללא סרום. פער תזונתי זה מוביל לתפוקות תאים נמוכות יותר וזמני ייצור ארוכים יותר.
סיבוך נוסף הוא הצטברות אמוניה כתוצאה מחילוף החומרים של גלוטמין. אמוניה מעכבת גדילה ובתנאים ללא סרום, שבהם התאים כבר נמצאים במתח מטבולי, רעילות זו יכולה להפריע באופן חמור להתרחבות. מדיה מסחרית רבות תוכננו במקור עבור תאים אנושיים, ולכן ייתכן שלא יענו על הצרכים התזונתיים הספציפיים של מיובלסטים בקריים או חזיריים [1][3].
החלפה חלקית של המדיום, כמו החלפת 75% מהמדיום במהלך ההאכלה, יכולה לעזור לשמור על חלק מגורמי הגדילה האנדוגניים. אמנם זה משפר במעט את שיעורי הצמיחה, אך זה לא סוגר לחלוטין את הפער בין מערכות ללא סרום למערכות מבוססות סרום [1].
ביצועים משתנים בין מוצרים מסחריים
לא כל המדיות המסחריות ללא סרום מבצעות באופן שווה. במחקר שהשווה שבע פורמולציות, רק שלוש - FBM™, Essential 8™, ו-TeSR™-E8™ - תמכו בצמיחה עקבית של מיובלסטים בקריים במשך שישה ימים. אחרים, כמו StemPro™ ו-mTeSR1™, תמכו בצמיחה רק במשך ארבעה ימים לפני שנעצרו, בעוד STEMmacs™ נכשל לחלוטין בתמיכה בפרוליפרציה [1].
הבעיה נעוצה בעובדה שרוב המדיות המסחריות מותאמות לתאי גזע אנושיים או פיברובלסטים, ולא למיובלסטים של בעלי חיים. מה שעובד היטב במחקר ביו-רפואי לעיתים קרובות לא מספיק לייצור בשר מתורבת. חוסר העקביות הזה מדגיש את הצורך בפורמולציות המותאמות במיוחד למיובלסטים של בעלי חיים.נתוני יצרן עבור תאי אדם לא יכולים לנבא באופן מהימן עד כמה מדיום יפעל היטב עם תאים של בקר או חזיר.
כדי למצוא את המדיום הנכון ללא סרום, חשוב לבצע בדיקות ממושכות - רצוי במשך שישה עד עשרה ימים - כדי להבטיח שהוא תומך בהתרחבות תאים מתמשכת ולא רק בצמיחה לטווח קצר.
השוואת אפשרויות מסחריות של מדיום ללא סרום
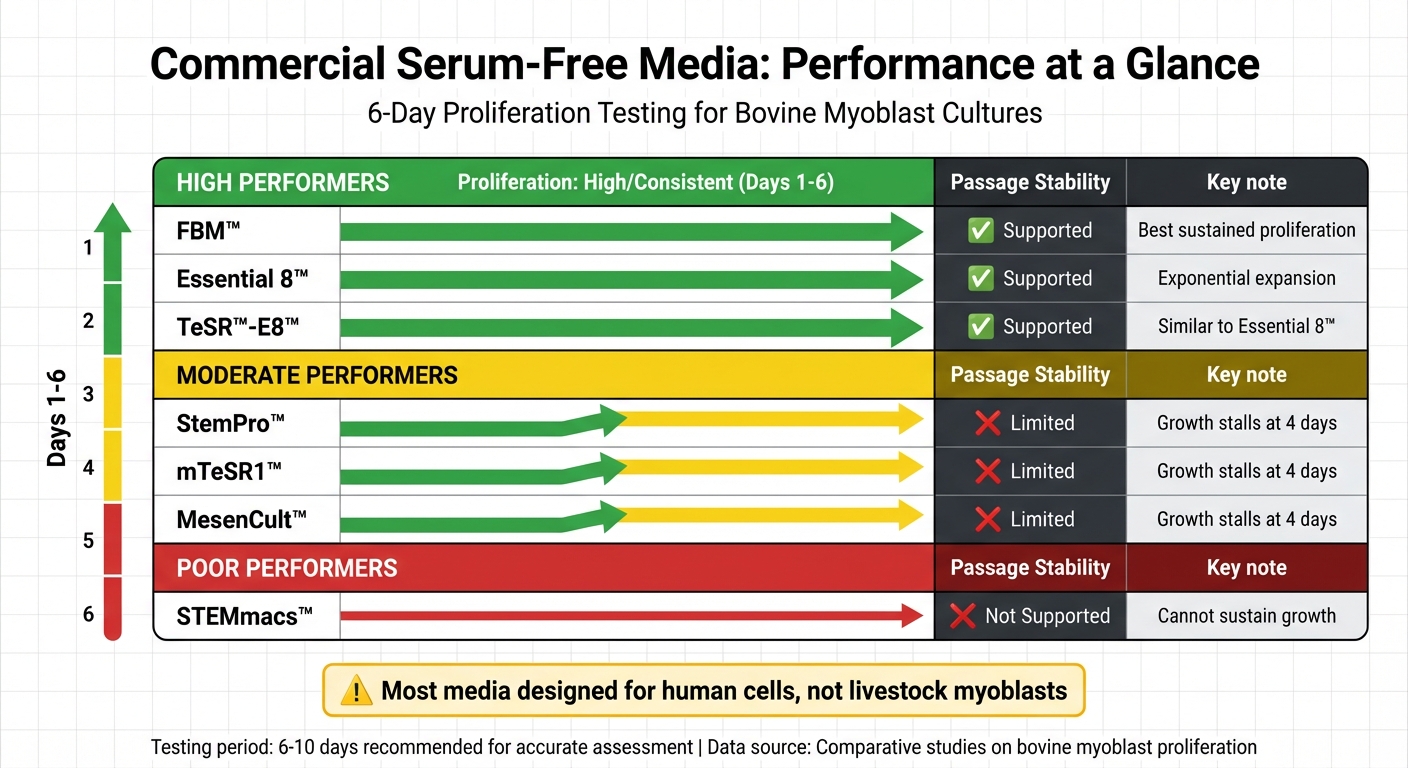
השוואת ביצועים של מדיום מסחרי ללא סרום לתרביות מיובלסטים של בקר
נתוני ביצועים למדיום נפוץ
כשמדובר במדיום ללא סרום לתרביות מיובלסטים, הביצועים יכולים להשתנות באופן נרחב. חלק מהמוצרים, כמו FBM™, Essential 8™, ו-TeSR™-E8™, תומכים בעקביות בהתרבות מיובלסטים של בקר במשך שישה ימים. לעומת זאת, אחרים, כמו StemPro™, mTeSR1™, ו-MesenCult™, נוטים להיעצר לאחר ארבעה ימים בלבד.בינתיים, STEMmacs™ נכשל לשמור על צמיחה בכלל [1].
להלן השוואה מהירה של מדדי ביצועים עבור המדיות הללו:
| מדיה | שגשוג (ימים 1–6) | יציבות מעבר | תצפיות מפתח |
|---|---|---|---|
| FBM™ | גבוה/עקבי | נתמך | מציע את הפוטנציאל הטוב ביותר לשגשוג מתמשך [1] |
| Essential 8™ | גבוה/עקבי | נתמך | תומך בהתרחבות אקספוננציאלית, אם כי פחות מבוסס על סרום [1] |
| TeSR™-E8™ | גבוה/עקבי | נתמך | דומה ל-Essential 8™ עבור מיובלסטים של בקר [1] |
| StemPro™ | מתון | מוגבל | הצמיחה נעצרת לאחר ארבעה ימים [1] |
| mTeSR1™ | מתון | מוגבל | הצמיחה נעצרת לאחר ארבעה ימים [1] |
| MesenCult™ | מתון | מוגבל | הצמיחה נעצרת לאחר ארבעה ימים [1] |
| STEMmacs™ | נמוך/אין | לא נתמך | לא מסוגל לתמוך בצמיחת מיובלסטים של בקר [1] |
מעניין, רוב המדיות - למעט FBM™ - מראות ספירת תאים נמוכה משמעותית בתוך 24 שעות מהזריעה בהשוואה לבקרות מבוססות סרום. זה מדגיש את החשיבות של הערכת מדדים אלה בעת בחירת מדיום, במיוחד בהתחשב במגמות רגולטוריות במדיום גידול לבטיחות מזון.
כיצד לבחור את המדיום הנכון ללא סרום
בחירת המדיום הטוב ביותר ללא סרום אינה רק על שיעורי גידול; היא דורשת איזון של מספר גורמים כמו פרוליפרציה, הצמדה ויעילות עלות. בדיקת מדיום על פני תקופה של שישה ימים היא קריטית, שכן בדיקות קצרות יותר עשויות לספק תוצאות מטעות [1].
ספציפיות למינים היא שיקול חשוב נוסף. אפשרויות רבות ללא סרום מתוכננות עם תאי אדם בראש, מה שאומר שהן עשויות לא לעמוד בדרישות התזונתיות של מיובלסטים של בעלי חיים כמו תאים של בקר או חזיר. הצרכים התזונתיים של מינים ומצבי תאים שונים יכולים להשתנות באופן משמעותי, ולכן בדיקה היא חיונית [3] .
דרישות ציפוי גם משחקות תפקיד גדול. חלק מהמדיות זקוקות לציפויים יקרים כמו למינין או Matrigel כדי להבטיח הידבקות תאים. אם התהליך שלך כולל משטחים לא מצופים או חומרים בדרגת מזון, כדאי לבדוק האם המדיה יכולה לתמוך בהידבקות ללא תוספים אלו. מדיה מותנית או פורמולציות המותאמות לכלים לא מצופים יכולות להיות חלופה חסכונית [2] .
גורם קריטי נוסף הוא שימוש באנטיביוטיקה. קוקטיילים אנטיביוטיים סטנדרטיים, כמו פניצילין/סטרפטומיצין, יכולים להפחית את התרבות המיובלסטים ב-20–26% במדיות המכילות סרום ובכ-62% במערכות ללא סרום. הסרת אנטיביוטיקה יכולה להוביל לתפוקות תאים גבוהות משמעותית [1].
לבסוף, אל תתעלם מניהול פסולת מטבולית. הצטברות אמוניה יכולה להיות רעילה לתרביות, ולכן זה רעיון טוב להוסיף לתקשורת תרכובות שאינן מייצרות אמוניה כמו α-ketoglutarate או pyruvate. תוספים אלו עוזרים להפחית את רעילות האמוניה ולהאריך את חיי התרביות [3].
שיטות לשיפור תרביות מיובלסטים ללא סרום
התמודדות עם האתגרים של תרביות מיובלסטים ללא סרום דורשת אסטרטגיות ממוקדות. הנה כמה שיטות מעשיות לשיפור הביצועים שלהם.
הוספת תוספים מרכזיים
שילוב תוספים ספציפיים יכול לשפר באופן משמעותי את צמיחת המיובלסטים. תערובת של FGF-2 (10 ng/ml), EGF (5 ng/ml), IGF (5 ng/ml), ו-אינסולין (10 μg/ml) הוכחה כמגבירה את התפשטות התאים בתקשורת בסיסית כמו FBM [1] . גורמי הגדילה הללו פועלים יחד כדי לקדם את התרבות התאים תוך שמירה על המצב הבלתי מבודל הנחוץ לייצור.
חומצות אמינו וויטמינים הם גם קריטיים. תרכובות כמו פירידוקסמין (ויטמין B6), אספרגין, וחומצה גלוטמית משחקות תפקיד מפתח בעידוד הידבקות והתרבות תאים, במיוחד על משטחים לא מצופים [2]. תוספים אלו עוזרים להחליף את התמיכה המטבולית המסופקת בדרך כלל על ידי סרום, ומטפלים באתגרים הקשורים להידבקות.
"ניתוח רכיבים וניסויי אימות הציעו כי פירידוקסמין, אספרגין וחומצה גלוטמית תרמו לרכישת פונקציית התרבות של המדיום המפותח." - npj Science of Food [2]
עם זאת, יש לנקוט בזהירות עם תוספי תזונה מבוססי שומן כמו LipoGro. בעוד שהם יכולים לעורר צמיחה, הם עשויים גם לגרום להתמיינות אדיפוגנית, מה שגורם למיובלסטים לפתח חללי שומן ולאבד את זהותם כתאי שריר [1].
התאמת פורמולציות מדיה
התאמה אישית של פורמולציות מדיה יכולה לאופטימיזציה של תרביות ללא סרום באמצעות ערכת גילוי גורמי גדילה. גישה יעילה אחת כוללת שימוש ב-מדיה מותנית. מדיה מותנית על ידי קו-תרבות של HepG2 (הפטומה אנושית) ו-NIH/3T3 (פיברובלסט עכברי) משחזרת את הפרופיל המטבולי של כבד עוברי. שיטה זו משיגה צפיפות תאים של 5,985 ± 1,558 תאים/סמ"ר על כלים לא מצופים, דומה ל-6,722 ± 1,500 תאים/סמ"ר שהושגו עם מדיה המכילה סרום [2] . האינטראקציה בין סוגי תאים אלו מקדמת הפרשת רכיבים דמויי סרום, ומשפרת את הצמיחה.
אסטרטגיה חסכונית נוספת היא החלפה חלקית של המדיום. על ידי החלפת 75% בלבד מהמדיום במקום שינוי מלא, נשמרים גורמי גדילה אנדוגניים המיוצרים על ידי התאים, מה שמשפר את שיעורי הגדילה ללא צורך בתוספים נוספים [1].
מניעת התמיינות מוקדמת עם מעכבים
שמירה על מצב פרוליפרטיבי דורשת שליטה זהירה באותות התמיינות. לדוגמה, מדיה מותנית מתאי HepG2 יכולה לדכא את הביטוי של סמן ההתמיינות המיוגני דסמין, ולשמור על תאים לא ממוינים ומוכנים להתרחבות [2].
בנוסף, מעקב אחר סמנים כמו CD29 (אינטגרין בטא-1) ו-Ki67 עוזר להבטיח שהפורמולציה יעילה בשמירה על פרוליפרציית תאים, ומפחיתה את הסיכון להתמיינות מוקדמת.סמנים אלה מספקים דרך אמינה לניטור והתאמת תנאי התרבות לתוצאות מיטביות.
הגדלת תרביות מיובלסטים ללא סרום לייצור
מעבר למערכות תרבות תלת-ממדיות
העברת תרביות מיובלסטים ללא סרום מכלים שטוחים דו-ממדיים למערכות ביוריאקטור תלת-ממדיות מגיעה עם סט אתגרים משלה, במיוחד כשמדובר בהידבקות תאים. ציפוי רכיבי ביוריאקטור עם חומרים יקרים כמו למינין אינו מעשי לייצור בקנה מידה גדול. עם זאת, שימוש במדיה מותנית מתרביות משותפות של HepG2 ו-NIH/3T3 או העשרת מדיה בסיסית עם תרכובות כמו פירידוקסמין, אספרגין וחומצה גלוטמית הוכח כיעיל. שיטות אלו מאפשרות למיובלסטים להידבק למבנים תלת-ממדיים לא מצופים ולנשאים מיקרוסקופיים, לטפל בבעיות ההידבקות מבלי להיזקק לציפויים יקרים [2].
גורם קריטי נוסף בהגדלה הוא ניהול פסולת מטבולית. תרביות ביוריאקטור צפופות יכולות לחוות הצטברות רעילה של אמוניה, שניתן להימנע ממנה על ידי החלפת גלוטמין באלטרנטיבות שאינן מייצרות אמוניה כמו α-ketoglutarate, גלוטמט או פירובט [3]. התאמות אלו חיוניות כאשר עוברים מעבר למערכות בקנה מידה קטן ודורשות בקרת איכות ומעקב חיישנים קפדניים כדי לשמור על שלמות המיובלסטים במהלך הייצור.
אישור איכות התאים בתרביות מותאמות
כאשר התרביות מותאמות לייצור בקנה מידה גדול יותר, הבטחת איכות התאים היא קריטית. טכניקות כמו בדיקות טרנסקריפטומיות, מטבולומיות ופונקציונליות משמשות לאימות שהתאים שומרים על רמות גבוהות של CD29 ו-Ki67 תוך דיכוי ביטוי Desmin. סמנים אלו מצביעים על כך שהתאים נשארים במצב פרוליפרטיבי, לא מבודל במהלך תהליך ההגדלה [2]. מעקב אחר מדדים אלו חשוב במיוחד כאשר ננקטים אמצעי חיסכון, כגון מעבר לרכיבים בדרגת מזון או שימוש בשינויים חלקיים במדיה. שלב זה מבטיח שהמעבר ממערכות בדרגת מחקר למערכות בדרגת ייצור לא יפגע באיכות התאים. כיוונון עדין של פרמטרים אלו הוא שלב קריטי לקראת הפיכת ייצור בשר מתורבת למדרגי ויעיל מבחינת עלות.
ביצועי תרבית ללא סרום לעומת תרבית מבוססת סרום
כאשר מותאמים, מערכות ללא סרום יכולות להשיג תוצאות הקרובות לתרביות מסורתיות מבוססות סרום.הטבלה למטה מדגישה מדדים מרכזיים מתרביות מיובלסטים של בקר שגודלו על משטחים לא מצופים:
| מדד | מבוסס סרום (20% FBS + 10% HS) | ללא סרום מותנה |
|---|---|---|
| הידבקות תאים (24 שעות) | ~6,722 תאים/סמ"ר | ~5,985 תאים/סמ"ר |
| שגשוג תאים (72 שעות) | ~10,050 תאים/סמ"ר | ~8,998 תאים/סמ"ר |
| ביטוי CD29 | גבוה | גבוה |
| ביטוי Ki67 | גבוה | גבוה |
| ביטוי דסמין | מדוכא | מדוכא |
הנתונים נלקחו מ-npj Science of Food [2]
בעוד שלמערכות מבוססות סרום יש עדיין יתרון קל בצפיפות התאים, מדיה ללא סרום מספקת תוצאות דומות בביטוי סמני הדבקה ושומרת על תאים לא ממוינים - גורמים מרכזיים לייצור.הפער מצטמצם עוד יותר כאשר מוסיפים תוספים ספציפיים כדי לייעל את הנוסחאות, מה שהופך מערכות ללא סרום לאופציה מעשית יותר ויותר לייצור בשר מתורבת בקנה מידה גדול.
סיכום
מעבר תרביות מיובלסטים למדיה ללא סרום מגיע עם חלקו ההוגן של מכשולים: בעיות חיבור מוקדמות, צמיחת תאים איטית יותר ותוצאות לא עקביות ממוצרים מסחריים. עם זאת, שינויים פשוטים - כמו הסרת אנטיביוטיקה ובחירה בהחלפות מדיה חלקיות - יכולים לשפר משמעותית את שיעורי ההתרבות [1]. על ידי בחירה קפדנית של מדיה והוספת גורמי גדילה ספציפיים, חוקרים יכולים לסגור את הפער בין מערכות ללא סרום למערכות מבוססות סרום מבחינת ביצועים. התקדמות זו סוללת את הדרך להגדלת הייצור.
עם זאת, הגדלת תרביות ללא סרום מציגה שכבות חדשות של מורכבות.מעבר תאים למערכות ביוריאקטור תלת-ממדיות תוך הבטחת שמירה על הפנוטיפ שלהם דורש בקרת איכות קפדנית. עם זאת, ישנן עדויות לכך שמערכות ללא סרום המותאמות היטב יכולות להשיג צפיפות תאים דומה לאלו שגדלו במדיה מבוססת סרום. זה הופך את השיטות ללא סרום ליותר ויותר מעשיות לייצור בשר מתורבת מסחרי.
הטיעון הכלכלי למדיה ללא סרום קשה להתעלם ממנו. עם עליית מחירי FBS, השיטות המבוססות על סרום הופכות לבלתי אפשריות מבחינה כלכלית [1] . השינוי הזה אינו רק על שיפורים טכניים - הוא על הישרדות כלכלית עבור תעשיית הבשר המתורבת.
עבור חוקרים וצוותי ייצור שעושים את המעבר הזה, השגת החומרים הנכונים היא חיונית. ממדיה מוגדרת כימית ועד גורמי גדילה רקומביננטיים, גישה לאספקה אמינה היא המפתח.This is where
שאלות נפוצות
כיצד ניתן לשפר את הצמדת המיובלסטים במדיום ללא סרום ללא שימוש בלמינין או Matrigel?
כדי לשפר את הצמדת המיובלסטים במדיום ללא סרום ללא שימוש בלמינין או Matrigel, שקול להשתמש ב-מדיום מותנה ללא סרום. גישה זו יכולה לקדם הידבקות והתרבות גם על כלים לא מצופים. אפשרות נוספת היא לאופטימיזציה של המדיום על ידי הוספת רכיבים כגון FGF2, פאטואין, ו-BSA. התאמות אלו יכולות לעשות הבדל ניכר בשיפור הצמדת התאים והצמיחה, ולבטל את הצורך בציפויים של מטריצה חוץ-תאית.
מהי הדרך המהירה ביותר להפחית הצטברות אמוניה בתרביות מיובלסטים ללא סרום?
כדי להפחית הצטברות אמוניה בתרביות מיובלסטים ללא סרום, יש להתמקד בשיפור הרכב המדיום. גישה אחת היא להשתמש במדיום מותנה שמקדם גם הידבקות וגם התרבות תאים תוך שמירה על רמות אמוניה נמוכות. בנוסף, שיפור תנאי התרבות יכול לעזור למזער את ייצור האמוניה. זה עשוי לכלול התאמת גורמים כמו pH, טמפרטורה או ריכוזי חומרים מזינים כדי להתאים טוב יותר לצרכים המטבוליים של התאים.
כיצד אוכל לוודא שהמיובלסטים נשארים בלתי ממוינים לאחר המעבר למדיום ללא סרום?
כדי להבטיח שהמיובלסטים יישארו במצבם הבלתי ממויין כאשר הם מתורבתים במדיום ללא סרום, חשוב לעקוב אחר סמנים ספציפיים.Pax7 הוא אינדיקטור אמין למיובלסטים לא ממוינים, בעוד שהיעדר סמני התמיינות כמו שרשרת כבדה של מיוזין (MHC) מאשר שהם לא התחילו להתמיין.
ניתן להשתמש בטכניקות כגון:
- אימונוציטוכימיה: להמחשת ביטוי חלבונים בתאים.
- ציטומטריית זרימה: לניתוח ביטוי סמנים באוכלוסיית תאים גדולה.
- qPCR: למדידת רמות mRNA של סמנים מרכזיים.
בנוסף, התבוננות בתאים תחת מיקרוסקופ היא חיונית. מיובלסטים צריכים לשמור על המראה האופייני שלהם, ולהימנע מהיווצרות מיוטיובים רב-גרעיניים, שהם סימן ברור להתמיינות. על ידי שילוב של שיטות אלו ומעקב קבוע, ניתן להבטיח שהתאים יישארו לא ממוינים.











