סקרינינג CRISPR בתפוקה גבוהה משנה את תחום הבשר המתורבת על ידי אפשרות לשינויים גנטיים מדויקים לשיפור ביצועי קווי התאים. הנה מה שאתה צריך לדעת:
- אתגר מרכזי: ייצור בשר מתורבת דורש קווי תאים שגדלים ביעילות, עמידים להזדקנות ומתמיינים לרקמות שריר ושומן.
- תפקיד CRISPR: על ידי מיקוד לאלפי גנים בו זמנית, פלטפורמות אלו מזהות עריכות גנטיות שמשפרות צמיחה, מעכבות הזדקנות ותומכות בהתמיינות.
- ממצאים בולטים: מחקרים הראו שדפיקה של גנים כמו TP53 ו-PTEN ב-תאי גזע מזנכימליים של בקר יכולה להגדיל את הפרוליפרציה עד פי 1,000 תוך 30 ימים ולהאריך את תוחלת החיים שלהם מ-100 ל-200 ימים.
- יישומים: כלי CRISPR כמו מסכי knockout, CRISPRi ו-CRISPRa משמשים לאופטימיזציה של צמיחת תאים, ויסות ביטוי גנים ואיזון בין פרוליפרציה לדיפרנציאציה.
- כלים לתעשייה: טכניקות מתקדמות כמו RMCE, RNA-seq ופלטפורמות תא בודד משלבות תוצאות CRISPR עם נתוני מולטי-אומיקס, ומבטיחות שיפורים מדויקים וניתנים להרחבה.
עבור מהנדסי ביופרוסס ואנשי מקצוע בתחום מו"פ, חידושים אלו מטפלים בצווארי בקבוק קריטיים בהגדלת תהליכי בשר מתורבת תוך שמירה על איכות התאים ותפקודם. השילוב של CRISPR עם מערכות אוטומטיות ומשאבים מותאמים כמו
יסודות CRISPR-Cas9 למסכי נוקאאוט ברחבי הגנום
כיצד CRISPR-Cas9 פועל בעריכת גנים בקנה מידה גדול
מערכת CRISPR-Cas9 מסתמכת על נוקלאז Cas9 המשולב עם RNA מנחה יחיד (sgRNA) כדי למקד רצפי DNA ספציפיים. ברגע שה-sgRNA מכוון את Cas9 למיקום הגנומי הרצוי, האנזים יוצר שבירה דו-גדילית ב-DNA. שבירה זו מתוקנת בעיקר באמצעות חיבור קצוות לא הומולוגי (NHEJ), תהליך נטול דיוק שלעיתים קרובות מכניס הוספות או מחיקות קטנות (indels). ה-indels הללו יכולים לגרום למוטציות של שינוי מסגרת, ובכך לשבש את תפקוד הגן הממוקד [1]. מנגנון מדויק זה הוא הבסיס לביצוע מסכי נוקאאוט ברחבי הגנום, שהם חיוניים בזיהוי רגולטורים קריטיים של התנהגות תאית.
לסינון בקנה מידה גדול, חוקרים משתמשים בספרייה מגוונת של sgRNAs, בדרך כלל מועברת לאוכלוסיית תאים מעורבת באמצעות טרנסדוקציה לנטיויראלית. כדי להבטיח שכל תא יקבל רק שינוי גנטי אחד, נשמרת רמת זיהום נמוכה (MOI של כ-0.3) [1]. עם הזמן, תאים עם מוטציות מועילות נוטים להתרבות בהצלחה רבה יותר מאחרים, תופעה שנצפתה במגוון סוגי תאים ותנאי ניסוי.
שיטות מסירה חלופיות, כגון החלפת קלטת בתיווך רקומבינאז (RMCE), מציעות דיוק נוסף על ידי מיקוד ל"משטחי נחיתה" גנומיים ספציפיים כדי להפחית את השונות באתרים האינטגרציה. לדוגמה, מחקר שהשתמש בתאי CHO-K1 יישם שיטת RMCE ללא וירוסים כדי לסנן 111,651 gRNAs ייחודיים על פני 21,585 גנים. גישה זו זיהתה גנים החיוניים לכושר התא לאורך תקופות של 16 ו-37 ימים [7].
יתרונות הסריקה הגנומית הרחבה
סריקות נוק-אאוט גנומיות רחבות מנצלות את הדיוק של CRISPR-Cas9 כדי לחקור באופן שיטתי אלפי גנים. זה מאפשר לחוקרים לגלות גנים שמשפיעים על הישרדות תאים, צמיחה ותגובות ללחץ. מעבר לגורמים גנטיים, אופטימיזציה של פונקציונליזציה של פני השטח היא קריטית לשיפור הצמדות וצמיחת תאים במערכות אלו. חקירה בלתי מוטה כזו רלוונטית במיוחד לייצור בשר מתורבת, שבה תאי גזע מזנכימליים (שמהווים כ-25% ממקורות התאים) לעיתים קרובות מתמודדים עם אתגרים כמו פרוליפרציה מוגבלת והזדקנות מוקדמת [1].
sbb-itb-ffee270
שיטות סריקה של ספריות CRISPR מאוגדות
בניית ספריות CRISPR מאוגדות
ספריות CRISPR מאוגדות מתחילות עם אוסף שנבחר בקפידה של RNA חד-גדילי מנחה (sgRNAs).בהקשר של מחקר בשר מתורבת, ספריות ממוקדות מתוכננות לעיתים קרובות להתמקד במשפחות גנים ספציפיות, כגון גורמי שעתוק או רגולטורים של התפשטות תאים. גישה זו מסייעת לאזן בין עלות לסקלביליות תוך שמירה על המיקוד בתכונות הרלוונטיות לפנוטיפ הרצוי [1].
התהליך מתחיל בסינתזה של אוליגונוקלאוטידים כבריכה, הגברתם באמצעות PCR ושיבוטם לווקטור משלוח. לדוגמה, ספרייה ספציפית לבקר שנבנתה בתחילת 2025 כללה 3,000 sgRNAs המכוונים ל-603 גנים כדי לזהות גורמים המשפיעים על התפשטות תאי גזע [1]. בקנה מידה גדול יותר, מסכים גנומיים רחבי היקף יכולים להגיע למורכבות גבוהה בהרבה. דוגמה אחת היא מסך תאי שחלה של אוגר סיני (CHO), שהשתמש ב-111,651 gRNAs ייחודיים כדי למקד ל-21,585 גנים [7].
העברה באמצעות וירוסים לנטיויראליים משמשת בדרך כלל להעברת ספריות אלו במכפיל זיהום נמוך (כ-0.3), מה שמבטיח שכל תא עובר שינוי גנטי יחיד בלבד [1]. לחלופין, שיטות ללא וירוסים כמו החלפת קלטות בתיווך רקומבינאז (RMCE) משלבות את ספריית ה-gRNA ב"משטחי נחיתה" גנומיים שנקבעו מראש בתוך קו תאים ראשי. טכניקה זו משיגה כיסוי gRNA של 99.9% עם עיוות מינימלי [7].
כדי לשמור על אמינות סטטיסטית, חוקרים מבטיחים כיסוי גבוה - בדרך כלל 500 עד 600 תאים לכל sgRNA [1] [7]. חלק מהפלטפורמות משתמשות במערכות Cas9 מושרות (iCas9), המאפשרות שליטה מדויקת על מועד התרחשות העריכה הגנטית. לדוגמה, ניתן להפעיל את העריכה לאחר שהתאים מגיעים למצב מסוים, כמו צפיפות גבוהה או תחילת הזדקנות.שליטה זמנית זו שימושית במיוחד לחקר שלבים לא-מתרבים, שהם קריטיים להתגברות על מחסומי הזדקנות על ידי בחירה בין קווי תאים ראשוניים לעומת קווי תאים בני אלמוות להגדלת ייצור בשר מתורבת [4].
לאחר בניית הספרייה, חוקרים עוברים לבדיקות סינון ממוקדות להערכת תפקוד גנים.
גישות סינון לקווי תאים של בשר מתורבת
לאחר בניית הספרייה, חוקרים מעריכים את ביצועי התאים באמצעות מבחני תחרות וטכניקות מיון פונקציונליות. שיטה נפוצה היא מבחן התרבות מבוסס תחרות, המזהה שינויים גנטיים המעניקים עמידות לצמיחה או להזדקנות - תכונות מפתח לאופטימיזציה של קווי תאים לבשר מתורבת.
מסכים לטווח קצר (הנמשכים כ-30 ימים) מזהים גנים שמשפיעים מיד על מחזור התא, בעוד שמסכים לטווח ארוך (עד 200 ימים) מתמקדים בגנים שעוזרים לתאים להתגבר על הזדקנות רפליקטיבית. זהו אתגר קריטי בהגדלת ייצור בשר מתורבת [1]. לתכונות מורכבות יותר, כמו הפרשת חלבון מוגברת או ביטוי של סמנים ספציפיים, נעשה שימוש במיון תאים מופעל פלואורסצנטית (FACS). דוגמה אחת היא "מבחן הפרשת לכידה קרה", שמבודד אוכלוסיות תאים פרודוקטיביות על ידי לכידת חלבונים מופרשים על פני שטח התא לפני המיון [7] [5].
אימות הוא שלב קריטי באישור תוצאות הסינון. מבחן הכושר התאי (CelFi), למשל, עוקב אחר היחס בין מוטציות מחוץ למסגרת למוטציות במסגרת לאורך זמן.אם תאים עם מוטציות מחוץ למסגרת נעלמים מהאוכלוסייה, זה מצביע על כך שהגן הממוקד חיוני לכושר התאים [2].
ביוני 2025, חוקרים בהובלת שיג'י דינג ב-אוניברסיטת נאנג'ינג לחקלאות השתמשו ב-CRISPR/Cas9 ליצירת CDKN2A–/– קווי תאי לוויין חזיריים . תאים מותאמים אלו שמרו על פרוליפרציה יציבה לפחות 15 מעברים בתנאים ללא סרום תוך שמירה על סמני גזע. כאשר נזרעו על פיגום אכיל תלת-ממדי מבוסס צמח, הם יצרו מבנים דמויי בשר עם מרקם משופר, כולל לעיסות וגמישות מוגברת [8].
"ממצאים אלו מדגימים את השימושיות של סריקת CRISPR לאופטימיזציה של תכונות תאי גזע בקר ומציעים דרך לייצור בשר מתורבת בקנה מידה גדול יותר בעתיד." – Communications Biology [1]
מסכי CRISPR-גנטיים משולבים בתאי יונקים | תצוגה מקדימה של פרוטוקול
CRISPRi ו-CRISPRa למסכי רגולציה גנטית הפיכים
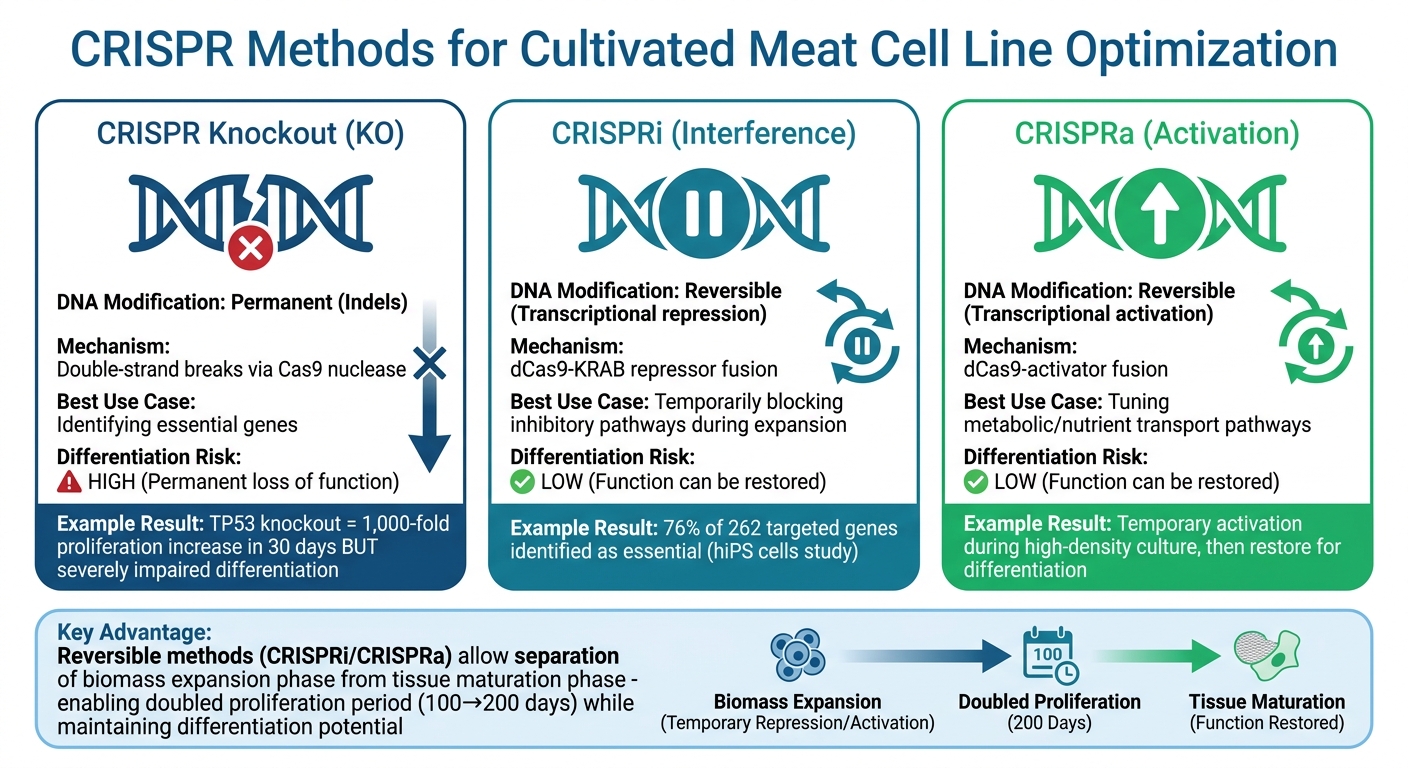
שיטות עריכת גנים CRISPR לבשר מתורבת: השוואה בין Knockout ל-CRISPRi/CRISPRa
שימוש ב-CRISPRi ו-CRISPRa בגנומיקה פונקציונלית
כשמדובר בשיפור ייצור בשר מתורבת, הפרעה ב-CRISPR (CRISPRi) והפעלה ב-CRISPR (CRISPRa) מספקות כלים חזקים. טכניקות אלו משתמשות בחלבון Cas9 לא פעיל יחד עם מדכאים או מפעילים, ומאפשרות לחוקרים להתאים את ביטוי הגנים באופן זמני מבלי לבצע שינויים קבועים ב-DNA [10].
הפיכות זו חשובה במיוחד להתמודדות עם אתגר מרכזי: גנים שמקדמים צמיחת תאים מהירה לעיתים קרובות מפריעים לשלבים המאוחרים של התמיינות לרקמת שריר או שומן. לדוגמה, השבתה קבועה של הגן TP53 בתאי גזע מזנכימליים של בקר יכולה להגדיל את ההתרבות ביותר מ-1,000 פעמים תוך 30 ימים בלבד אך פוגעת קשות ביכולתם להתמיין [1]. CRISPRi מציע פתרון גמיש יותר על ידי חסימה זמנית של מסלולים שמעכבים התמיינות במהלך התרחבות הביומסה בביוריאקטורים לבשר מתורבת . ברגע שהתאים מוכנים להבשלה של הרקמה, ניתן לשחזר את תפקוד הגנים הרגיל.
באוקטובר 2025, חוקרים כמו גבריאלה קאסגרנדה ראפי ורודריק ל. בייג'רסברגן ממכון הסרטן של הולנד פיתחו מערכת CRISPR ניתנת להשראה.גישה זו מעכבת עריכת גנים עד שהתאים מגיעים למצבים ספציפיים - כמו צפיפות גבוהה או שלב לא פרוליפרטיבי - ועוזרת לשמור על חיות התאים [4].
CRISPRi גם מתבלט בדיוק שלו בהשוואה להפרעה מסורתית של RNA (RNAi). RNAi לעיתים קרובות מוביל לתוצאות לא עקביות ולהשפעות מחוץ למטרה, בעוד ש-CRISPRi מספק דיכוי גנים אמין ומדויק יותר [2]. יתרון נוסף הוא ש-CRISPRi נמנע מהפעלת רעילות הקשורה ל-p53, שנגרמת לעיתים קרובות על ידי תגובות נזק ל-DNA. במחקר משנת 2025 בהובלת ליקין וואנג ב-Sun Yat-sen University Cancer Centre, חוקרים השתמשו במערכת KRAB–dCas9 הניתנת להשראה על ידי דוקסיציקלין כדי לסרוק 262 גנים בתאי גזע פלוריפוטנטיים מושרים אנושיים (תאי hiPS). הם מצאו כי 76% מהגנים הקשורים לתרגום (200 מתוך 262) היו חיוניים לצמיחה, מה שמדגים את יעילות המערכת [10].
היכולת לכוונן את ביטוי הגנים הופכת את CRISPRi ו-CRISPRa לכלים בעלי ערך לאיזון בין התרבות תאים להתמיינות במחקר גנומיקה פונקציונלית.
התאמת מסכים הפיכים ליישומים בבשר מתורבת
רגולציה גנטית הפיכה מציעה פתרונות לאתגרים מרכזיים בייצור בשר מתורבת. לדוגמה, CRISPRa יכול להפעיל באופן זמני גנים המעורבים בהובלת חומרים מזינים או במסלולים מטבוליים במהלך תרבות בצפיפות גבוהה. ברגע שהתאים מגיעים לצפיפות הרצויה, המערכת יכולה להחזיר את ביטוי הגנים לרמות נורמליות, תומכת בהתמיינות נכונה לרקמת שריר או שומן.
מערכות ניתנות להשראה מאפשרות גם להפריד בין שלב התרחבות הביומסה לבין הבשלת הרקמה. CRISPRi יכול לדכא גנים הקשורים להזדקנות במהלך תהליך ההגדלה, ובכך להכפיל את תקופת ההתרבות של תאי בקר מכ-100 ימים ליותר מ-200 ימים [1]. לאחר השגת ביומסה מספקת, חוקרים יכולים לשחזר ביטוי גנים נורמלי כדי לאפשר התמיינות. גישה זו שימושית במיוחד עבור תאי גזע מזנכימליים, הנוטים להיכנס להזדקנות מוקדמת בתרבית [1].
"עריכת גנים ממוקדת של תהליכים כפולים אלו יכולה למקסם את יעילות ההתרחבות של MSC תוך שמירה על הרב-פוטנטיות והפוטנציאל ההתמיינות החיוניים שלהם, ובסופו של דבר לקדם מערכות בשר מתורבת בקנה מידה." – Communications Biology [1]
הטבלה למטה מדגישה את ההבדלים בין שיטות רגולציה גנטית הפיכות וקבועות:
| תכונה | CRISPR Knockout (KO) | CRISPRi / CRISPRa |
|---|---|---|
| שינוי DNA | קבוע (Indels) | הפיך (תעתוקי) |
| מנגנון | שבירות דו-גדיליות | מיזוג dCas9-effector |
| מקרה שימוש מיטבי | זיהוי גנים חיוניים | כוונון מסלולי מטבוליזם/צמיחה |
| סיכון להבדלה | גבוה (אובדן תפקוד קבוע) | נמוך (ניתן לשחזר תפקוד) |
השוואה זו ממחישה כיצד ניתן להתאים שיטות רגולציה גנטית הפיכות כדי להתמודד עם האתגרים הספציפיים של פיתוח קווי תאים לייצור בשר מתורבת.
שילוב מסכי CRISPR עם טכנולוגיות פאנל תאים וגנטיפיקציה
קישור מסכי CRISPR עם ניתוח מולטי-אומיקס
שילוב מולטי-אומיקס וגנטיפיקציה אוטומטית במסכי CRISPR משפר את השימושיות שלהם, במיוחד בקידום פיתוח קווי תאים לבשר מתורבת.
שילוב מסכי CRISPR עם מולטי-אומיקס, כגון ריצוף RNA, מאפשר לחוקרים למפות את ההשפעות של נוקאאוטים גנטיים ספציפיים על מסלולים תאיים. זה רלוונטי במיוחד לבשר מתורבת, שבו הבנת האיזון בין פרוליפרציה ודיפרנציאציה של תאים היא קריטית.
לדוגמה, מסך נוקאאוט CRISPR משולב המכוון ל-600 גנים ב-תאי גזע מזנכימליים שמקורם ברקמת שומן של בקר, בשילוב עם RNA-seq, חשף שנוקאאוט של TP53 ו-PTEN עיכב הזדקנות.תאים אלה שמרו על פרופיל ביטוי גנים צעיר, עם גנים של מחזור התא שהוגברו, מה שהוביל לעלייה של 50% בקצב הכפלה עד היום ה-50 לאחר הטרנסדוקציה [1].
פלטפורמות תא בודד כמו CROP-seq לוקחות זאת רחוק יותר על ידי זיהוי בו-זמני של שינויים ב-sgRNA ובטרנסקריפטום בתאים בודדים [6]. רמת דיוק זו היא בעלת ערך רב לזיהוי שינויים גנטיים המשפרים התמיינות שרירים או סינתזת חלבונים - גורמים קריטיים להשגת המרקם והתכונות התזונתיות הרצויות בבשר מתורבת.
גישה מבטיחה נוספת כוללת סריקת פאנל תאים, שבה נבדקות הפרעות CRISPR על פני קווי תאים מגוונים מתורמים, אתרים אנטומיים ומינים שונים. לדוגמה, חוקרים אימתו את ספריית MyoCRISPR-KOLib על קווי מיאלובלסט אנושיים משבעה תורמים.באמצעות מערכת בחירה של רעלן מפוצל, הם זיהו 250 גנים החיוניים למיזוג מיובלסטים. מתוך אלה, 41 גנים אושרו דרך מאגרי מידע רפואיים כמשחקים תפקיד במורפולוגיה של שריר שלד [6]. אימות רב-שכבתי זה מבטיח שמטרות גנטיות יישארו חזקות על פני וריאציות ביולוגיות, שיקול מפתח להרחבת ייצור בשר מתורבת.
תובנות אלו סוללות את הדרך לפלטפורמות אוטומטיות וניתנות להרחבה המשלבות מסכים גנטיים עם גנוטיפ מפורט ליישומים תעשייתיים.
אוטומציה והרחבה בפלטפורמות משולבות
האוטומציה חיונית לטיפול במאגרי הנתונים והדגימות העצומים שנוצרים על ידי פלטפורמות CRISPR וגנוטיפ משולבות. מערכות RMCE, המאפשרות מסירה ספציפית לאתר של ספריות sgRNA ללא וירוסים, הן צעד משמעותי קדימה. פלטפורמות אלו מבטיחות שכל תא יקבל עותק sgRNA יחיד ועקבי, מה שמפחית את השונות.RMCE כבר הוכיח כיסוי ספרייה גבוה עם הטיה מינימלית בתאי שחלה של אוגר סיני (CHO) [5].
"פלטפורמת סריקה גנטית בלתי מוטה בעלת תפוקה גבוהה חיונית לפיתוח מפעלי CHO מהדור הבא." - צוות מחקר שחלה של אוגר סיני [5]
היכולת להתרחב משופרת עוד יותר על ידי כלי אימות כמו מבחן הכושר התאי (CelFi). מבחן זה משתמש בריצוף עמוק ממוקד כדי לעקוב אחר פרופילי אינדל לאורך זמן, ולעקוב אחר היחס בין מוטציות במסגרת לעומת מחוץ למסגרת. על ידי קישור מוטציות אלו ליתרונות או חסרונות בצמיחה, חוקרים יכולים לאמת ביעילות מטרות גנטיות בקווי תאי בשר מתורבת [2].
| טכנולוגיה | שיטת אינטגרציה | היתרון העיקרי לבשר מתורבת |
|---|---|---|
| RNA-seq / Multi-omics | קישור פגיעות CRISPR לפרופילים טרנסקריפטומיים | הבנת האופן שבו גנים מווסתים צמיחה והתמיינות[1][6] |
| מערכות רעלן מפוצלות | קישור איחוי תאים לבחירת קיימות | בחירה כמותית של תאים המסוגלים או לא מסוגלים לאיחוי[6] |
| פלטפורמות RMCE | אינטגרציה ספציפית לאתר של ספריות gRNA | סינון בקצב גבוה, ללא וירוסים, עם מספרי עותקים גנטיים עקביים[5] |
| CROP-seq | CRISPR חד-תאי + RNA-seq | זיהוי סימולטני של sgRNA ושינויים טרנסקריפטומיים [6] |
| CelFi Assay | ריצוף עמוק ממוקד של אינדלים | אימות מהיר של מטרות גנטיות על ידי מעקב אחר שינויים בתדירות האללים [2] |
פלטפורמות מתקדמות אלו מייעלות את התהליך מזיהוי מטרות גנטיות ועד לאימות השפעתן על כושר התא.יעילות זו תומכת בפיתוח של קווי תאים חזקים מספיק לייצור בשר מתורבת בקנה מידה גדול.
שימוש במסכי CRISPR לשיפור צמיחה והתרבות של קווי תאים
שיטות סריקת CRISPR הפכו לכלי חזק לשיפור ביצועי קווי תאים, ומציעות יתרונות ישירים לייצור בשר מתורבת.
דוגמאות לשיפורים בקווי תאים מבוססי CRISPR
מסכי CRISPR שיפרו בהצלחה את ביצועי קווי התאים במחקר בשר מתורבת. לדוגמה, מסך נוקאאוט משולב המכוון ל-600 גנים בתאי גזע מזנכימליים שמקורם בשומן בקר זיהה את TP53 ו-PTEN כמעכבים מרכזיים של צמיחה. נוקאאוט של TP53 הגדיל באופן משמעותי את כמות התאים בתוך 30 ימים[1]. בנוסף, תאי הגזע המזנכימליים הערוכים הראו קצב הכפלה גבוה ב-12% בממוצע [1] .
על ידי מיקוד גנים מדכאי גידול, החוקרים האריכו את תוחלת החיים הפרוליפרטיבית של התאים מכ-100 ליותר מ-200 ימים, ובכך עקפו למעשה את מגבלת הייפליק. עיכוב זה בסננסנס מאפשר הרחבת ביומסה על פני מסגרות זמן רלוונטיות תעשייתית[1].
בדוגמה נוספת, חוקרים מאוניברסיטת החקלאות נאנג'ינג, בראשות שיג'י דינג, צ'ונבאו לי וגואנגהונג ג'ואו, השתמשו ב-CRISPR/Cas9 לפיתוח CDKN2A−/− קווי תאי לוויין חזיריים. תאים מהונדסים אלו שמרו על פרוליפרציה יציבה לפחות ב-18 מעברים במדיום מותאם ללא סרום המורכב מ-19 רכיבים (A19). הם גם נזרעו בהצלחה על פיגומים אכילים, יצירת מבנים דמויי בשר עם שיפור בלעיסות ובגמישות[8]. התאים שמרו על חיוניות של מעל 90% במעברים מרובים בתנאים ללא סרום[8].
"תאי נוקאאוט מבוססי CRISPR של CDKN2A מספקים מקור מתחדש של תאי אב לשריר, ומפחיתים את התלות בביופסיות חוזרות מבעלי חיים."
דוגמאות אלו מדגישות כיצד מסכי CRISPR יכולים לזהות שינויים גנטיים שמשפרים את קצב הצמיחה, מעכבים את הזדקנות התאים, ומאפשרים תרבית ללא סרום - שלושה היבטים חיוניים להגדלת ייצור בשר מתורבת.
אתגרי הגדלה עבור קווי תאים מותאמים ל-CRISPR
בעוד שקווי תאים מותאמים ל-CRISPR מראים יתרונות ברורים, הגדלתם לשימוש תעשייתי מציבה אתגרים. פרוליפרציה מוגברת לעיתים קרובות באה על חשבון ההתמיינות.לדוגמה, TP53 נוקאאוטים בתאי גזע מזנכימליים של בקר נקשרו לביטוי מופחת של גנים להבדלת שרירים, מה שיכול להפריע ליכולתם להבשיל לרקמה אכילה[1]. כדי להתמודד עם זה, ייתכן שיהיה צורך באסטרטגיות נוספות, כגון הוספת תוספי מדיה או הפעלת גורמי שעתוק ספציפיים, כדי לשחזר את ההבדלה לאחר ההתרחבות[1].
נושא קריטי נוסף הוא שמירה על יציבות גנטית. וריאציות במספרי עותקי גנים (אנאופלואידיה) והשפעות מחוץ למטרה במהלך עריכת CRISPR יכולות להוביל לתוצאות לא עקביות או חיוביות שגויות במחקרי סינון [2]. כלים כמו מבחן הכושר התאי (CelFi) מסייעים להפחית סיכונים אלה על ידי ניטור היחס של אינדלים מחוץ למסגרת לאורך זמן, ומבטיחים שהיתרונות בצמיחה שנצפו קשורים ישירות לעריכות המיועדות[2].
חסמים כלכליים וטכניים עדיין קיימים. תאי גזע מזנכימליים, המהווים כ-25% ממקורות התאים בתעשיית הבשר המתורבת, מתמודדים עם אתגרים כמו העלות הגבוהה של גורמי גדילה, הצורך במדיה ללא סרום מותאמת, ופיתוח ביוריאקטורים בקנה מידה גדול (קיבולות של 10,000–50,000 ליטר)[1][9][11]. בנוסף, הבטחת המרקם הרצוי כאשר תאים נזרעים על גבי פיגומים תלת-ממדיים ממשיכה להיות משימה מורכבת[11].
"המצב הנוכחי של בשר מתורבת מתמודד עם אתגרים משמעותיים, כולל עלויות גבוהות, בעיות בקנה מידה והצורך בהתקדמות טכנולוגית נוספת."
- ביולוגיה של תקשורת [1]
התגברות על אתגרים אלו דורשת גישה מקיפה שמשלבת אופטימיזציה גנטית עם התקדמות בניסוח מדיה, טכנולוגיית ביוריאקטורים ופרוטוקולי דיפרנציאציה. בעוד שמסכי CRISPR מספקים תובנות גנטיות קריטיות, תרגום ממצאים אלו לפתרונות ניתנים להרחבה ידרוש מערכות משולבות ותהליכי אימות קפדניים. מאמצים אלו חיוניים להעברת ייצור בשר מתורבת מהמעבדה לכדאיות מסחרית.
כיצד Cellbase תומך במחקר CRISPR בבשר מתורבת
הקרנת CRISPR כבר הראתה את הפוטנציאל שלה, אך הרחבתה לשימוש תעשייתי דורשת גישה לכלים ומשאבים מיוחדים. כאן נכנס
גישה למשאבי CRISPR דרך Cellbase
בניגוד לספקי תרופות רחבי טווח,
בנובמבר 2025,
"כל חברת בשר מתורבת שדיברנו איתה בזבזה זמן על אותה בעיית רכש. מציאת ספקים לרכיבים קריטיים דרשה חיפוש בגוגל בין דפי ספקי פארמה שלא הבינו את יישומי המזון."
- דוד בל, מייסד קבוצת Cultigen [15]
על ידי ריכוז המשאבים הללו,
הפעלת שיתוף פעולה בפיתוח בשר מתורבת
הפלטפורמה מעוצבת להתמודד עם הדרישות של פרויקטים מסחריים בקנה מידה גדול, כמו אלה שמבוצעים על ידי Believer Meats ו-Aleph Farms. מיזמים אלה דורשים תשתית לביורי-אקטורים של 50,000 ליטר ו שרשראות אספקה אופטימליות לייצור, אשר
סיכום
הקרנת CRISPR בתפוקה גבוהה עברה מרעיון מבטיח לכלי קריטי בקידום פיתוח בשר מתורבת. ההשפעה של טכנולוגיה זו על אופטימיזציה של קווי תאים היא בלתי ניתנת להכחשה. לדוגמה, פריצות דרך אחרונות הראו ששינויים גנטיים יכולים להכפיל את אורך החיים של תאי גזע בקר מ-100 ל-200 ימים, להפחית את אוכלוסיות התאים הסניליים מ-60% ל-10% בלבד, ולהשיג עלייה מדהימה פי 1,000 בשפע התאים בתוך חודש אחד [1]. התקדמויות אלו מסמנות מעבר ברור ממחקר ניסיוני ליישומים תעשייתיים מעשיים.
פלטפורמות קומפקטיות וספריות ממוקדות מתמודדות עם חלק מהאתגרים הדחופים ביותר בתחום. מערכות מיקרופלואידיות דיגיטליות מאפשרות כעת הקרנה עם עד 3,000 תאים בלבד לכל תנאי, מה שהופך את זה לאפשרי לעבוד עם תאי בעלי חיים ראשוניים מוגבלים שאינם זמינים מסחרית.בינתיים, ספריות ממוקדות כמו MyoCRISPR-KOLib מכוונות ביעילות ל-90% מהתמלילים הרלוונטיים תוך כיסוי של רק שליש מהגנום [3][6]. רמת דיוק ויעילות זו היא קריטית להתגברות על מגבלות משאבים והגדלת הייצור.
"ממצאים אלו מדגימים את התועלת של סריקת CRISPR לאופטימיזציה של תכונות תאי גזע בקר ומציעים דרך לייצור בשר מתורבת יותר בקנה מידה בעתיד." [1]
למרות ההתקדמות הללו, ההצלחה תלויה בגישה לתשתית הנכונה. חוקרים זקוקים לספריות gRNA ספציפיות למינים, מדיה גידול המיועדת ליישומי מזון, ביוריאקטורים תואמים, וכלים אנליטיים המותאמים לייצור בשר מתורבת ולא לשימוש פרמצבטי.Addressing these needs,
עבור צוותים העובדים על הנדסת הדור הבא של קווי תאי בשר מתורבת, הכלים והטכנולוגיות מוכנים. האתגר כעת טמון בפריסה מהירה ויעילה של סריקת CRISPR כדי לממש את מלוא הפוטנציאל שלה.
שאלות נפוצות
כיצד לבחור בין CRISPR knockout, CRISPRi ו-CRISPRa עבור סריקה?
הבחירה בין מערכות אלו תלויה בשאלה הביולוגית הספציפית שלך ובתוצאה שאתה שואף להשיג:
- CRISPR knockout: שיטה זו משבשת את תפקוד הגן לחלוטין, מה שהופך אותה לאידיאלית לחקר ההשפעות של אובדן או השבתת גן.
- CRISPRi: על ידי דיכוי ביטוי גנים ללא חיתוך ה-DNA, גישה זו מתאימה במיוחד לחקר גנים חיוניים או כאשר נדרש דיכוי הפיך.
- CRISPRa: אם אתה צריך להגביר את ביטוי הגנים, מערכת זו היא הבחירה המועדפת. היא שימושית במיוחד לבחינת ההשפעות של ביטוי יתר, כמו קידום פרוליפרציה או התמיינות של תאים.
בעת קבלת החלטה, קח בחשבון את המודל התאי שלך, את הגנים שאתה מכוון אליהם ואת המטרות הכלליות של הניסוי שלך.
כיצד ניתן להגביר את הפרוליפרציה מבלי לפגוע בהתמיינות של שריר או שומן?
הגברת הפרוליפרציה של תאי שריר או שומן תוך שמירה על יכולתם להתמיין היא אתגר מרכזי בייצור בשר מתורבת.גישה מבטיחה אחת כוללת עריכת גנים מבוססת CRISPR, שמאפשרת מניפולציה מדויקת של גנים לשיפור הצמיחה או להארכת חיי התא. לדוגמה, מיקוד ב-מיוסטטין (MSTN) יכול לקדם צמיחת תאים, בעוד שעריכת CDKN2A מסייעת לתאים לעקוף הזדקנות.
עם זאת, השגת איזון בין פרוליפרציה לדיפרנציאציה היא קריטית. ניהול לא נכון של מטרות מסוימות, כמו P53 (TP53), עלול לפגוע בדיפרנציאציה, ובכך לפגוע באיכות הרקמה. כדי לנווט במורכבויות אלו, סינון CRISPR בתפוקה גבוהה הוא כלי חשוב. טכניקה זו מזהה את הרגולטורים הגנטיים היעילים ביותר, וסוללת את הדרך לפיתוח רקמות בריאות וניתנות להרחבה בייצור בשר מתורבת.
מה נדרש כדי לאמת פגיעות במסך CRISPR לפני הגדלת קו תאים?
אימות פגיעות במסך CRISPR לייצור בשר מתורבת דורש גישה שיטתית. ראשית, יש לאשר את תפקוד הגן באמצעות ניסויים עצמאיים, כגון נוקאאוט של גנים, כדי להבטיח שההשפעות הנצפות ניתנות לשחזור. לאחר מכן, חשוב להעריך את הרלוונטיות הביולוגית של גנים אלה על ידי בחינת השפעתם על גורמים כמו התרבות תאים, חיות ואריכות ימים.
הערכות בטיחות חשובות באותה מידה כדי לשלול השפעות מחוץ למטרה או חוסר יציבות גנטית שעלולות לפגוע בתהליך. אימות פונקציונלי בתנאים המדמים סביבות תעשייתיות, כגון ביוריאקטורים, הוא שלב קריטי נוסף. זה מבטיח שהעריכות הגנטיות מתפקדות כמצופה בסביבות ייצור בקנה מידה גדול. בדיקות יסודיות בכל שלב הן הכרחיות לפני ששוקלים הגדלה.











