Screening CRISPR throughput tinggi mengubah sektor daging budidaya dengan memungkinkan modifikasi genetik yang tepat untuk meningkatkan kinerja garis sel. Berikut adalah yang perlu Anda ketahui:
- Tantangan Utama: Produksi daging budidaya memerlukan garis sel yang tumbuh secara efisien, tahan terhadap penuaan, dan berdiferensiasi menjadi jaringan otot dan lemak.
- Peran CRISPR: Dengan menargetkan ribuan gen secara bersamaan, platform ini mengidentifikasi pengeditan genetik yang meningkatkan pertumbuhan, menunda penuaan, dan mendukung diferensiasi.
- Temuan Penting: Studi telah menunjukkan bahwa menonaktifkan gen seperti TP53 dan PTEN dalam sel punca mesenkimal sapi dapat meningkatkan proliferasi hingga 1.000 kali lipat dalam 30 hari dan memperpanjang masa hidup mereka dari 100 hingga 200 hari.
- Aplikasi: Alat CRISPR seperti knockout screens, CRISPRi, dan CRISPRa digunakan untuk mengoptimalkan pertumbuhan sel, mengatur ekspresi gen, dan menyeimbangkan proliferasi dengan diferensiasi.
- Alat Industri: Teknik canggih seperti RMCE, RNA-seq, dan platform sel tunggal mengintegrasikan hasil CRISPR dengan data multi-omik, memastikan peningkatan yang tepat dan dapat diskalakan.
Untuk insinyur bioproses dan profesional R&D, inovasi ini mengatasi hambatan kritis dalam peningkatan proses daging budidaya sambil mempertahankan kualitas dan fungsionalitas sel. Integrasi CRISPR dengan sistem otomatis dan sumber daya yang disesuaikan seperti
Dasar-Dasar CRISPR-Cas9 untuk Skrining Knockout Seluruh Genom
Cara Kerja CRISPR-Cas9 dalam Pengeditan Gen Skala Besar
Sistem CRISPR-Cas9 bergantung pada nuklease Cas9 yang dipasangkan dengan RNA pemandu tunggal (sgRNA) untuk menargetkan urutan DNA tertentu. Setelah sgRNA mengarahkan Cas9 ke lokasi genom yang diinginkan, enzim tersebut menciptakan kerusakan untai ganda pada DNA. Kerusakan ini sebagian besar diperbaiki melalui penyambungan ujung non-homolog (NHEJ), sebuah proses yang rentan terhadap kesalahan yang sering kali memperkenalkan sisipan atau penghapusan kecil (indel). Indel ini dapat menyebabkan mutasi pergeseran bingkai, yang secara efektif mengganggu fungsi gen yang ditargetkan [1]. Mekanisme yang tepat ini adalah dasar untuk melakukan skrining knockout seluruh genom, yang sangat penting dalam mengidentifikasi pengatur kritis perilaku seluler.
Untuk penyaringan skala besar, peneliti menggunakan perpustakaan sgRNA yang beragam, biasanya dikirimkan ke dalam populasi sel campuran melalui transduksi lentiviral. Untuk memastikan bahwa setiap sel hanya menerima satu perubahan genetik, tingkat infeksi yang rendah (MOI sekitar 0,3) dipertahankan [1]. Seiring waktu, sel dengan mutasi yang menguntungkan cenderung berkembang biak lebih sukses daripada yang lain, fenomena yang diamati di berbagai jenis sel dan kondisi eksperimental.
Metode pengiriman alternatif, seperti pertukaran kaset yang dimediasi rekombinase (RMCE), menawarkan presisi tambahan dengan menargetkan "landasan" genomik tertentu untuk mengurangi variabilitas di situs integrasi. Sebagai contoh, sebuah studi menggunakan sel CHO-K1 menggunakan metode RMCE bebas virus untuk menyaring 111.651 gRNA unik di 21.585 gen. Pendekatan ini mengidentifikasi gen yang penting untuk kebugaran sel selama periode 16 dan 37 hari [7].
Manfaat Penyaringan Seluruh Genom
Penyaringan knockout seluruh genom memanfaatkan akurasi CRISPR-Cas9 untuk menyelidiki ribuan gen secara sistematis. Ini memungkinkan peneliti untuk mengungkap gen yang mempengaruhi kelangsungan hidup sel, pertumbuhan, dan respons terhadap stres. Selain faktor genetik, mengoptimalkan fungsionalisasi permukaan sangat penting untuk meningkatkan keterikatan dan pertumbuhan sel dalam sistem ini. Eksplorasi tanpa bias seperti ini sangat relevan untuk produksi daging budidaya, di mana sel punca mesenkimal (yang membentuk sekitar 25% dari sumber sel) sering menghadapi tantangan seperti proliferasi terbatas dan penuaan dini [1].
sbb-itb-ffee270
Metode Penyaringan Perpustakaan CRISPR Gabungan
Membangun Perpustakaan CRISPR Gabungan
Perpustakaan CRISPR gabungan dimulai dengan koleksi RNA pemandu tunggal (sgRNA) yang dipilih dengan cermat.Dalam konteks penelitian daging budidaya, perpustakaan yang ditargetkan sering dirancang untuk fokus pada keluarga gen tertentu, seperti faktor transkripsi atau regulator proliferasi sel. Pendekatan ini membantu menyeimbangkan biaya dengan skalabilitas sambil tetap fokus pada sifat yang relevan dengan fenotipe yang diinginkan [1].
Proses dimulai dengan mensintesis oligonukleotida sebagai kumpulan, memperbanyaknya melalui PCR, dan mengkloningnya ke dalam vektor pengiriman. Misalnya, perpustakaan spesifik sapi yang dibangun pada awal 2025 mencakup 3.000 sgRNA yang menargetkan 603 gen untuk mengidentifikasi faktor yang mempengaruhi ekspansi sel punca [1]. Dalam skala yang lebih besar, skrining seluruh genom dapat mencapai kompleksitas yang jauh lebih tinggi. Salah satu contohnya adalah skrining sel Ovarium Hamster Cina (CHO), yang menggunakan 111.651 gRNA unik untuk menargetkan 21.585 gen [7].
Transduksi lentiviral umumnya digunakan untuk mengirimkan perpustakaan ini pada tingkat infeksi yang rendah (sekitar 0.3), memastikan setiap sel hanya mengalami satu modifikasi genetik [1]. Sebagai alternatif, metode bebas virus seperti pertukaran kaset yang dimediasi rekombinase (RMCE) mengintegrasikan perpustakaan gRNA ke dalam "landasan" genomik yang telah ditentukan dalam garis sel master. Teknik ini mencapai cakupan gRNA 99.9% dengan distorsi minimal [7].
Untuk menjaga keandalan statistik, peneliti memastikan cakupan tinggi - biasanya 500 hingga 600 sel per sgRNA [1] [7] . Beberapa platform menggunakan sistem Cas9 yang dapat diinduksi (iCas9), memungkinkan kontrol yang tepat kapan pengeditan gen terjadi. Misalnya, pengeditan dapat dipicu setelah sel mencapai keadaan tertentu, seperti kepadatan tinggi atau awal penuaan.Kontrol temporal ini sangat berguna untuk mempelajari fase non-proliferatif, yang penting untuk mengatasi hambatan penuaan dengan memilih antara garis sel primer vs garis sel yang diabadikan untuk meningkatkan produksi daging budidaya [4] .
Setelah perpustakaan dibangun, peneliti melanjutkan ke uji saring terarah untuk mengevaluasi fungsi gen.
Pendekatan Penyaringan untuk Garis Sel Daging Budidaya
Setelah membangun perpustakaan, peneliti menilai kinerja sel menggunakan uji kompetisi dan teknik penyortiran fungsional. Metode yang banyak digunakan adalah uji proliferasi berbasis kompetisi, yang mengidentifikasi perubahan genetik yang memberikan ketahanan pertumbuhan atau penuaan - sifat kunci untuk mengoptimalkan garis sel untuk daging budidaya.
Layar jangka pendek (berlangsung sekitar 30 hari) mengidentifikasi gen yang segera mempengaruhi siklus sel, sementara layar jangka panjang (hingga 200 hari) berfokus pada gen yang membantu sel mengatasi penuaan replikasi. Ini adalah tantangan kritis dalam meningkatkan produksi daging budidaya [1]. Untuk sifat yang lebih kompleks, seperti sekresi protein yang ditingkatkan atau ekspresi penanda spesifik, digunakan fluorescence-activated cell sorting (FACS). Salah satu contohnya adalah "cold capture secretion assay", yang mengisolasi populasi sel produktif dengan menangkap protein yang disekresikan di permukaan sel sebelum disortir [7] [5].
Validasi adalah langkah penting dalam mengonfirmasi hasil penyaringan. Uji Cellular Fitness (CelFi), misalnya, melacak rasio mutasi out-of-frame terhadap in-frame dari waktu ke waktu.Jika sel dengan mutasi out-of-frame menghilang dari populasi, ini menunjukkan bahwa gen yang ditargetkan penting untuk kebugaran seluler [2].
Pada Juni 2025, peneliti yang dipimpin oleh Shijie Ding di Universitas Pertanian Nanjing menggunakan CRISPR/Cas9 untuk membuat CDKN2A–/– garis sel satelit babi . Sel yang dimodifikasi ini mempertahankan proliferasi stabil setidaknya selama 15 kali pasase dalam kondisi bebas serum sambil mempertahankan penanda stemness. Ketika ditanam pada scaffold 3D yang dapat dimakan berbasis tanaman, mereka membentuk konstruksi seperti daging dengan tekstur yang ditingkatkan, termasuk kekenyalan dan kelengketan yang lebih baik [8].
"Temuan ini menunjukkan kegunaan penyaringan CRISPR untuk mengoptimalkan sifat sel induk sapi dan menawarkan jalur menuju produksi daging kultur yang lebih dapat diskalakan di masa depan." – Komunikasi Biologi [1]
CRISPR-Genetic Screens Gabungan dalam Sel Mamalia | Pratinjau Protokol
CRISPRi dan CRISPRa untuk Skrining Regulasi Gen Reversibel
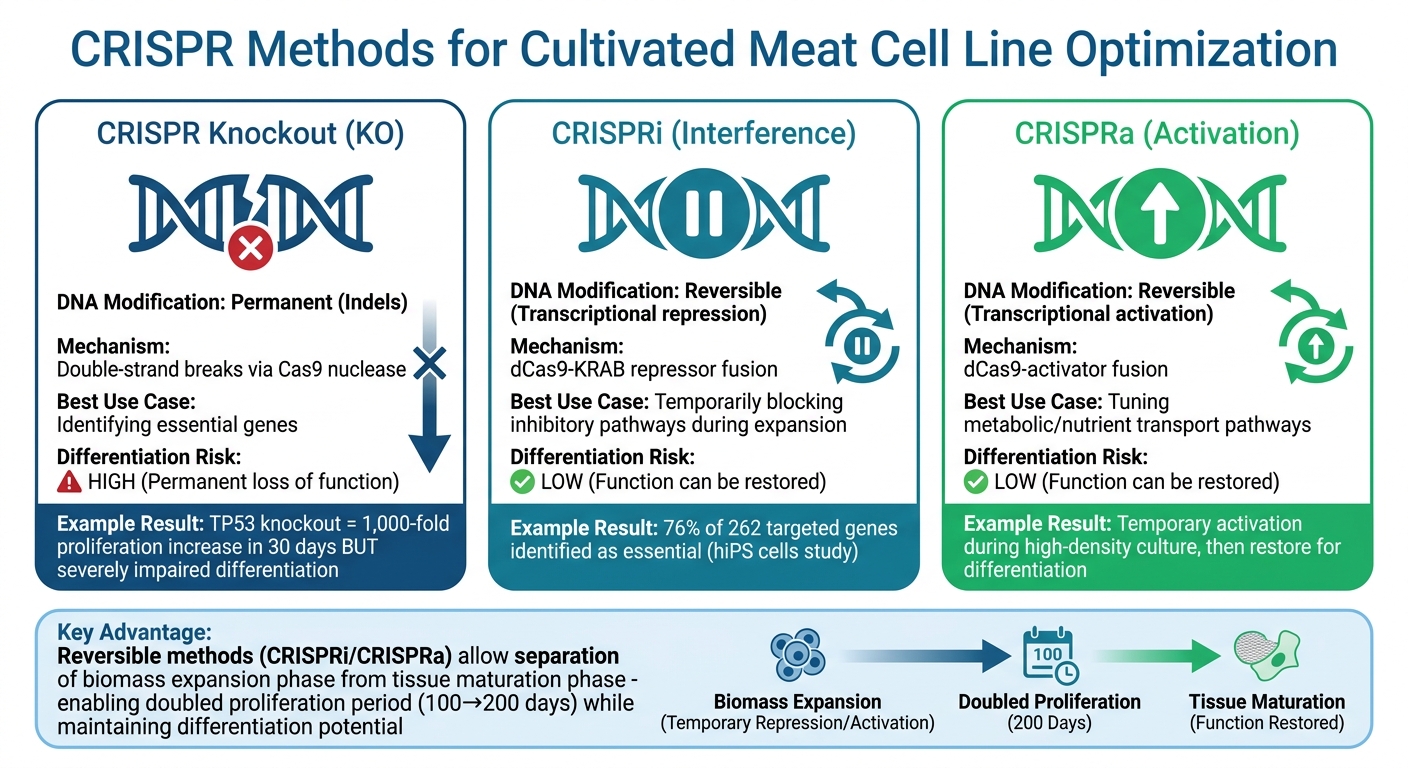
Metode Pengeditan Gen CRISPR untuk Daging Budidaya: Perbandingan Knockout vs CRISPRi/CRISPRa
Menggunakan CRISPRi dan CRISPRa dalam Genomik Fungsional
Ketika datang untuk meningkatkan produksi daging budidaya, interferensi CRISPR (CRISPRi) dan aktivasi CRISPR (CRISPRa) menyediakan alat yang kuat. Teknik-teknik ini menggunakan protein Cas9 yang tidak aktif dipasangkan dengan represor atau aktivator, memungkinkan peneliti untuk menyesuaikan ekspresi gen sementara tanpa membuat perubahan permanen pada DNA [10].
Reversibilitas ini sangat penting untuk mengatasi tantangan besar: gen yang mendorong pertumbuhan sel cepat sering mengganggu tahap akhir diferensiasi menjadi jaringan otot atau lemak. Misalnya, menonaktifkan secara permanen gen TP53 pada sel punca mesenkimal sapi dapat meningkatkan proliferasi lebih dari 1.000 kali lipat hanya dalam 30 hari tetapi sangat menghambat kemampuan mereka untuk berdiferensiasi [1]. CRISPRi menawarkan solusi yang lebih fleksibel dengan memblokir sementara jalur yang menghambat diferensiasi selama ekspansi biomassa dalam bioreaktor untuk daging budidaya. Setelah sel siap untuk pematangan jaringan, fungsi gen normal dapat dipulihkan.
Pada Oktober 2025, peneliti seperti Gabriele Casagrande Raffi dan Roderick L. Beijersbergen dari Netherlands Cancer Institute mengembangkan sistem CRISPR yang dapat diinduksi.Pendekatan ini menunda pengeditan gen hingga sel mencapai keadaan tertentu - seperti kepadatan tinggi atau fase non-proliferatif - membantu menjaga kelangsungan hidup sel [4].
CRISPRi juga menonjol karena presisinya dibandingkan dengan interferensi RNA tradisional (RNAi). RNAi sering menghasilkan hasil yang tidak konsisten dan efek di luar target, sementara CRISPRi memberikan represi gen yang lebih andal dan spesifik [2]. Keuntungan lain adalah bahwa CRISPRi menghindari pemicu toksisitas terkait p53, yang sering disebabkan oleh respons kerusakan DNA. Dalam studi tahun 2025 yang dipimpin oleh Liqin Wang di Sun Yat-sen University Cancer Centre, peneliti menggunakan sistem KRAB–dCas9 yang dapat diinduksi oleh doksisiklin untuk menyaring 262 gen dalam sel induk pluripoten manusia (sel hiPS). Mereka menemukan bahwa 76% dari gen terkait translasi yang ditargetkan (200 dari 262) penting untuk pertumbuhan, menunjukkan efektivitas sistem ini [10].
Kemampuan untuk menyetel ekspresi gen ini membuat CRISPRi dan CRISPRa menjadi alat yang berharga untuk menyeimbangkan proliferasi dan diferensiasi sel dalam penelitian genomik fungsional. Menyesuaikan Layar Reversibel untuk Aplikasi Daging Budidaya Regulasi gen reversibel menawarkan solusi untuk tantangan utama dalam produksi daging budidaya. Misalnya, CRISPRa dapat mengaktifkan sementara gen yang terlibat dalam transportasi nutrisi atau jalur metabolisme selama kultur dengan kepadatan tinggi. Setelah sel mencapai kepadatan yang diinginkan, sistem dapat mengembalikan ekspresi gen ke tingkat normal, mendukung diferensiasi yang tepat menjadi jaringan otot atau lemak. Sistem yang dapat diinduksi juga memungkinkan pemisahan fase ekspansi biomassa dari pematangan jaringan. CRISPRi dapat menekan gen yang terkait dengan penuaan selama proses peningkatan skala, secara efektif menggandakan periode proliferasi sel sapi dari sekitar 100 hari menjadi lebih dari 200 hariSetelah mencapai biomassa yang cukup, peneliti dapat mengembalikan ekspresi gen normal untuk memungkinkan diferensiasi. Pendekatan ini sangat berguna untuk sel punca mesenkimal, yang cenderung memasuki penuaan dini dalam kultur [1]."Pengeditan genetik yang ditargetkan dari kedua proses ini dapat mengoptimalkan efisiensi ekspansi MSC sambil mempertahankan multipotensi dan potensi diferensiasi esensial mereka, yang pada akhirnya memajukan sistem daging kultur yang dapat diskalakan." – Biologi Komunikasi [1]
Tabel di bawah ini menyoroti perbedaan antara metode regulasi gen yang dapat dibalik dan permanen:
| Fitur | CRISPR Knockout (KO) | CRISPRi / CRISPRa |
|---|---|---|
| Modifikasi DNA | Permanen (Indels) | Dapat dibalik (Transkripsi) |
| Mekanisme | Pemutusan untai ganda | Fusi dCas9-effector |
| Kasus Penggunaan Terbaik | Mengidentifikasi gen esensial | Menyetel jalur metabolik/pertumbuhan |
| Risiko Diferensiasi | Tinggi (Kehilangan fungsi permanen) | Rendah (Fungsi dapat dipulihkan) |
Perbandingan ini menggambarkan bagaimana metode regulasi gen yang dapat dibalik dapat disesuaikan untuk memenuhi tantangan spesifik dalam mengembangkan garis sel untuk produksi daging budidaya.
Menggabungkan Layar CRISPR dengan Panel Sel dan Teknologi Genotip
Menghubungkan Layar CRISPR dengan Analisis Multi-Omik
Mengintegrasikan multi-omik dan genotip otomatis ke dalam layar CRISPR menyempurnakan kegunaannya, terutama dalam memajukan pengembangan lini sel daging budidaya.
Menggabungkan layar CRISPR dengan multi-omik, seperti pengurutan RNA, memungkinkan peneliti memetakan efek dari penghapusan gen spesifik pada jalur seluler. Ini sangat relevan untuk daging budidaya, di mana memahami bagaimana sel menyeimbangkan proliferasi dan diferensiasi sangat penting.
Misalnya, layar penghapusan CRISPR terpooling yang menargetkan 600 gen dalam sel punca mesenkimal yang berasal dari adiposa sapi, dipasangkan dengan RNA-seq, mengungkapkan bahwa penghapusan TP53 dan PTEN menunda penuaan.Sel-sel ini mempertahankan profil ekspresi gen yang muda, dengan gen siklus sel yang terupregulasi, yang mengarah pada peningkatan 50% dalam tingkat penggandaan pada hari ke-50 pasca-transduksi [1].
Platform sel tunggal seperti CROP-seq membawa ini lebih jauh dengan secara simultan mendeteksi perubahan sgRNA dan transkriptomik dalam sel individu [6]. Tingkat presisi ini sangat berharga untuk mengidentifikasi modifikasi genetik yang meningkatkan diferensiasi otot atau sintesis protein - faktor kritis untuk mencapai tekstur dan sifat nutrisi yang diinginkan dalam daging yang dibudidayakan.
Pendekatan menjanjikan lainnya melibatkan penyaringan panel sel, di mana gangguan CRISPR diuji di berbagai garis sel dari berbagai donor, situs anatomi, dan spesies. Misalnya, peneliti memvalidasi perpustakaan MyoCRISPR-KOLib pada garis myoblast manusia dari tujuh donor.Menggunakan sistem seleksi toksin-terpisah, mereka mengidentifikasi 250 gen yang penting untuk fusi mioblas. Dari jumlah tersebut, 41 gen dikonfirmasi melalui basis data medis berperan dalam morfologi otot rangka [6] . Validasi multi-garis ini memastikan bahwa target genetik tetap kuat di berbagai variasi biologis, pertimbangan kunci untuk meningkatkan produksi daging budidaya.
Wawasan ini membuka jalan bagi platform otomatis dan dapat diskalakan yang menggabungkan skrining genetik dengan genotipe terperinci untuk aplikasi industri.
Otomatisasi dan Skalabilitas dalam Platform Terintegrasi
Otomatisasi sangat penting untuk menangani dataset dan sampel yang luas yang dihasilkan oleh platform CRISPR dan genotipe terintegrasi. Sistem RMCE, yang memungkinkan pengiriman perpustakaan sgRNA yang spesifik lokasi dan bebas virus, adalah langkah maju yang besar. Platform ini memastikan setiap sel menerima satu salinan sgRNA yang konsisten, mengurangi variabilitas.RMCE telah menunjukkan cakupan perpustakaan yang tinggi dengan bias minimal pada sel ovarium hamster Cina (CHO) [5].
"Platform penyaringan genetik throughput tinggi yang tidak bias sangat penting untuk pengembangan pabrik CHO generasi berikutnya." - Tim Penelitian Ovarium Hamster Cina [5]
Skalabilitas lebih ditingkatkan oleh alat validasi seperti uji Cellular Fitness (CelFi). Uji ini menggunakan pengurutan dalam yang ditargetkan untuk memantau profil indel dari waktu ke waktu, melacak rasio mutasi in-frame versus out-of-frame. Dengan mengaitkan mutasi ini dengan keuntungan atau kerugian pertumbuhan, peneliti dapat dengan efisien memverifikasi target genetik dalam garis sel daging yang dibudidayakan [2].
| Teknologi | Metode Integrasi | Manfaat Utama untuk Daging Budidaya |
|---|---|---|
| RNA-seq / Multi-omics | Menghubungkan hasil CRISPR dengan profil transkriptomik | Memahami bagaimana gen mengatur pertumbuhan dan diferensiasi [1][6] |
| Sistem Toksin Terpisah | Menghubungkan fusi sel dengan seleksi viabilitas | Seleksi kuantitatif sel yang mampu fusi atau cacat [6] |
| Platform RMCE | Integrasi spesifik situs dari perpustakaan gRNA | Penyaringan throughput tinggi, bebas virus dengan jumlah salinan gen yang konsisten [5] |
| CROP-seq | Single-cell CRISPR + RNA-seq | Deteksi simultan sgRNA dan perubahan transkriptomik [6] |
| CelFi Assay | Pengurutan dalam yang ditargetkan dari indel | Validasi cepat target genetik dengan melacak pergeseran frekuensi alel [2] |
Platform canggih ini menyederhanakan proses dari mengidentifikasi target genetik hingga memvalidasi dampaknya pada kebugaran sel. Efisiensi ini mendukung pengembangan lini sel yang cukup kuat untuk produksi daging budidaya skala besar.
Menggunakan CRISPR Screens untuk Meningkatkan Pertumbuhan dan Proliferasi Lini Sel
Metode penyaringan CRISPR telah menjadi alat yang kuat untuk meningkatkan kinerja lini sel, menawarkan manfaat langsung untuk produksi daging budidaya.
Contoh Peningkatan Lini Sel Berbasis CRISPR
CRISPR screens telah berhasil meningkatkan kinerja lini sel dalam penelitian daging budidaya. Sebagai contoh, sebuah screen knockout terpilih yang menargetkan 600 gen dalam sel punca mesenkimal yang berasal dari adiposa sapi mengidentifikasi TP53 dan PTEN sebagai penghambat pertumbuhan utama. Menghilangkan TP53 secara signifikan meningkatkan kelimpahan sel dalam 30 hari[1]. Selain itu, sel punca mesenkimal sapi yang telah diedit menunjukkan tingkat penggandaan rata-rata 12% lebih tinggi[1].
Dengan menargetkan gen penekan tumor, para peneliti memperpanjang umur proliferatif sel dari sekitar 100 menjadi lebih dari 200 hari, secara efektif melewati batas Hayflick. Penundaan penuaan ini memungkinkan ekspansi biomassa selama jangka waktu yang relevan secara industri[1].
Dalam contoh lain, peneliti dari Universitas Pertanian Nanjing, yang dipimpin oleh Shijie Ding, Chunbao Li, dan Guanghong Zhou, menggunakan CRISPR/Cas9 untuk mengembangkan garis sel satelit babi CDKN2A −/−. Sel-sel yang direkayasa ini mempertahankan proliferasi yang stabil setidaknya selama 18 kali pasase dalam medium bebas serum 19-komponen khusus (A19). Mereka juga berhasil ditanamkan pada rangka yang dapat dimakan , menciptakan konstruksi mirip daging dengan peningkatan kekenyalan dan kelengketan[8]. Sel-sel tersebut mempertahankan viabilitas lebih dari 90% di berbagai pasase dalam kondisi bebas serum[8].
"Sel-sel knockout CDKN2A berbasis CRISPR menyediakan sumber yang dapat diperbarui dari progenitor otot, mengurangi ketergantungan pada biopsi hewan yang berulang."
Contoh-contoh ini menyoroti bagaimana layar CRISPR dapat mengidentifikasi modifikasi genetik yang meningkatkan laju pertumbuhan, menunda penuaan seluler, dan memungkinkan kultur bebas serum - tiga aspek penting untuk meningkatkan produksi daging yang dibudidayakan.
Tantangan Penskalaan untuk Garis Sel yang Dioptimalkan CRISPR
Sementara garis sel yang dioptimalkan CRISPR menunjukkan keuntungan yang jelas, penskalaan mereka untuk penggunaan industri menghadirkan tantangan. Peningkatan proliferasi sering kali mengorbankan diferensiasi.Sebagai contoh, TP53 knockouts dalam sel punca mesenkimal sapi telah dikaitkan dengan penurunan ekspresi gen diferensiasi otot, yang dapat menghambat kemampuan mereka untuk matang menjadi jaringan yang dapat dimakan[1]. Untuk mengatasi hal ini, strategi tambahan, seperti menambahkan suplemen media atau mengaktifkan faktor transkripsi tertentu, mungkin diperlukan untuk memulihkan diferensiasi setelah ekspansi [1].
Masalah kritis lainnya adalah menjaga stabilitas genetik. Variasi dalam jumlah salinan gen (aneuploidy) dan efek di luar target selama pengeditan CRISPR dapat menyebabkan hasil yang tidak konsisten atau positif palsu dalam studi penyaringan[2]. Alat seperti uji Cellular Fitness (CelFi) membantu mengurangi risiko ini dengan memantau rasio indel di luar bingkai dari waktu ke waktu, memastikan bahwa manfaat pertumbuhan yang diamati secara langsung terkait dengan pengeditan yang dimaksudkan[2].
Hambatan ekonomi dan teknis juga tetap ada. Sel punca mesenkimal, yang membentuk sekitar 25% dari sumber sel dalam industri daging budidaya, menghadapi tantangan seperti biaya tinggi faktor pertumbuhan, kebutuhan untuk media bebas serum yang dioptimalkan, dan pengembangan bioreaktor skala besar (kapasitas 10.000–50.000 L) [1][9][11]. Selain itu, memastikan tekstur yang diinginkan ketika sel ditanam pada scaffold 3D terus menjadi tugas yang kompleks[11].
"Keadaan saat ini dari daging budidaya menghadapi tantangan signifikan, termasuk biaya tinggi, masalah skalabilitas, dan kebutuhan untuk kemajuan teknologi lebih lanjut."
- Biologi Komunikasi [1]
Mengatasi tantangan ini memerlukan pendekatan komprehensif yang menggabungkan optimasi genetik dengan kemajuan dalam formulasi media, teknologi bioreaktor, dan protokol diferensiasi. Sementara layar CRISPR memberikan wawasan genetik yang kritis, menerjemahkan temuan ini menjadi solusi yang dapat diskalakan akan menuntut sistem terintegrasi dan proses validasi yang ketat. Upaya ini sangat penting untuk memindahkan produksi daging budidaya dari laboratorium ke kelayakan komersial.
Bagaimana Cellbase Mendukung Penelitian CRISPR dalam Daging Budidaya
Penyaringan CRISPR telah menunjukkan potensinya, tetapi untuk menskalakannya ke penggunaan industri memerlukan akses ke alat dan sumber daya khusus. Di sinilah
Mengakses Sumber Daya CRISPR Melalui Cellbase
Tidak seperti pemasok farmasi spektrum luas,
Pada November 2025,
"Setiap perusahaan daging budidaya yang kami ajak bicara membuang waktu pada masalah pengadaan yang sama. Mencari pemasok untuk komponen penting berarti mencari melalui halaman pemasok farmasi yang tidak memahami aplikasi makanan."
- David Bell, Pendiri Cultigen Group [15]
Dengan memusatkan sumber daya ini,
Mengaktifkan Kolaborasi dalam Pengembangan Daging Budidaya
Platform ini dirancang untuk menangani tuntutan proyek komersial berskala besar, seperti yang dilakukan oleh Believer Meats dan Aleph Farms. Usaha ini memerlukan infrastruktur untuk bioreaktor 50.000 liter dan rantai pasokan produksi yang dioptimalkan, yang
Kesimpulan
Screening CRISPR throughput tinggi telah beralih dari konsep yang menjanjikan menjadi alat penting dalam memajukan pengembangan daging budidaya. Dampak teknologi ini dalam mengoptimalkan garis sel tidak dapat disangkal. Misalnya, terobosan terbaru telah menunjukkan bahwa modifikasi genetik dapat menggandakan umur proliferasi sel induk sapi dari 100 menjadi 200 hari, mengurangi populasi sel penuaan dari 60% menjadi hanya 10%, dan mencapai peningkatan jumlah sel yang luar biasa sebanyak 1.000 kali lipat dalam satu bulan [1]. Kemajuan ini menandai pergeseran yang jelas dari penelitian eksperimental ke aplikasi industri praktis.
Platform kompak dan perpustakaan yang ditargetkan sedang mengatasi beberapa tantangan paling mendesak di bidang ini. Sistem mikrofluida digital sekarang memungkinkan untuk screening dengan hanya 3.000 sel per kondisi, membuatnya layak untuk bekerja dengan sel hewan primer terbatas yang tidak tersedia secara komersial.Sementara itu, perpustakaan terfokus seperti MyoCRISPR-KOLib secara efisien menargetkan 90% transkrip yang relevan sambil mencakup hanya sepertiga dari genom [3] [6]. Tingkat presisi dan efisiensi ini sangat penting untuk mengatasi keterbatasan sumber daya dan meningkatkan produksi.
"Temuan ini menunjukkan kegunaan penyaringan CRISPR untuk mengoptimalkan sifat sel punca sapi dan menawarkan jalur menuju produksi daging budidaya yang lebih dapat diskalakan di masa depan." [1]
Terlepas dari kemajuan ini, keberhasilan bergantung pada akses ke infrastruktur yang tepat. Peneliti memerlukan perpustakaan gRNA spesifik spesies, media pertumbuhan yang dirancang untuk aplikasi makanan, bioreaktor yang kompatibel, dan alat analisis yang disesuaikan untuk produksi daging budidaya daripada penggunaan farmasi.Menjawab kebutuhan ini,
Untuk tim yang bekerja untuk merekayasa gelombang berikutnya dari garis sel daging budidaya, alat dan teknologi sudah siap. Tantangannya sekarang terletak pada penerapan penyaringan CRISPR yang cepat dan efektif untuk mewujudkan potensinya secara penuh.
FAQ
Bagaimana Anda memilih antara CRISPR knockout, CRISPRi, dan CRISPRa untuk sebuah penyaringan?
Pilihan antara sistem-sistem ini bergantung pada pertanyaan biologis spesifik Anda dan hasil yang Anda tuju:
- CRISPR knockout: Metode ini mengganggu fungsi gen sepenuhnya, menjadikannya ideal untuk mempelajari efek dari kehilangan atau inaktivasi gen.
- CRISPRi: Dengan menekan ekspresi gen tanpa memotong DNA, pendekatan ini sangat cocok untuk menyelidiki gen esensial atau ketika diperlukan penekanan yang dapat dibalik.
- CRISPRa: Jika Anda perlu meningkatkan ekspresi gen, sistem ini adalah pilihan utama. Ini sangat berguna untuk memeriksa efek dari overekspresi, seperti mempromosikan proliferasi atau diferensiasi sel.
Saat memutuskan, pertimbangkan model seluler Anda, gen yang Anda targetkan, dan tujuan keseluruhan dari eksperimen Anda.
Bagaimana Anda dapat meningkatkan proliferasi tanpa merusak diferensiasi otot atau lemak?
Meningkatkan proliferasi sel otot atau lemak sambil mempertahankan kemampuan mereka untuk berdiferensiasi adalah tantangan utama dalam produksi daging budidaya.Salah satu pendekatan menjanjikan melibatkan pengeditan gen berbasis CRISPR, yang memungkinkan manipulasi gen secara tepat untuk meningkatkan pertumbuhan atau memperpanjang umur sel. Misalnya, menargetkan myostatin (MSTN) dapat mendorong pertumbuhan sel, sementara mengedit CDKN2A membantu sel melewati penuaan.
Namun demikian, mencapai keseimbangan antara proliferasi dan diferensiasi sangat penting. Salah pengelolaan target tertentu, seperti P53 (TP53), dapat mengganggu diferensiasi, yang berpotensi mengorbankan kualitas jaringan. Untuk menavigasi kompleksitas ini, penyaringan CRISPR throughput tinggi sangat penting. Teknik ini mengidentifikasi pengatur gen yang paling efektif, membuka jalan untuk pengembangan jaringan yang dapat diskalakan dan sehat dalam produksi daging yang dibudidayakan.
Apa yang dibutuhkan untuk memvalidasi hasil layar CRISPR sebelum meningkatkan skala lini sel?
Memvalidasi hasil layar CRISPR untuk produksi daging budidaya memerlukan pendekatan yang metodis. Pertama, fungsi gen harus dikonfirmasi melalui eksperimen independen, seperti penghapusan gen, untuk memastikan efek yang diamati dapat direproduksi. Selanjutnya, penting untuk mengevaluasi relevansi biologis dari gen-gen ini dengan memeriksa dampaknya terhadap faktor-faktor seperti proliferasi sel, viabilitas, dan umur panjang.
Penilaian keamanan sama pentingnya untuk menyingkirkan efek di luar target atau ketidakstabilan genetik yang dapat mengganggu proses. Validasi fungsional di bawah kondisi yang meniru pengaturan industri, seperti bioreaktor, adalah langkah penting lainnya. Ini memastikan bahwa pengeditan genetik berfungsi seperti yang diharapkan dalam lingkungan produksi skala besar. Pengujian menyeluruh pada setiap tahap tidak dapat dinegosiasikan sebelum mempertimbangkan peningkatan skala.











