プロセス分析技術(PAT)は、製造プロセスにリアルタイムの品質監視を統合し、一貫性を向上させ、廃棄物を削減します。これは、pH、酸素、栄養素などの要因を正確に制御することが重要な培養肉の生産に特に有用です。PATは、インラインセンサー、ケモメトリックス、自動化システムを組み合わせて、規制基準を満たしながら製品の品質を確保します。
PATを実装するための重要なステップ:
- 重要なプロセスパラメータ(CPP)の特定: 温度、溶存酸素、pH、グルコースなどの要因に焦点を当てます。
- 監視ツールの選択: リアルタイムデータのためにインラインセンサー(e.g、ラマン分光法)を使用します。
- PATシステムの統合: センサーをバイオリアクターに接続して自動フィードバック制御を行います。
- 予測モデルの開発: データ分析を使用してプロセスを最適化します。
- コンプライアンスの確保: GMP、ISO 17025、その他の規制ガイドラインに従う。
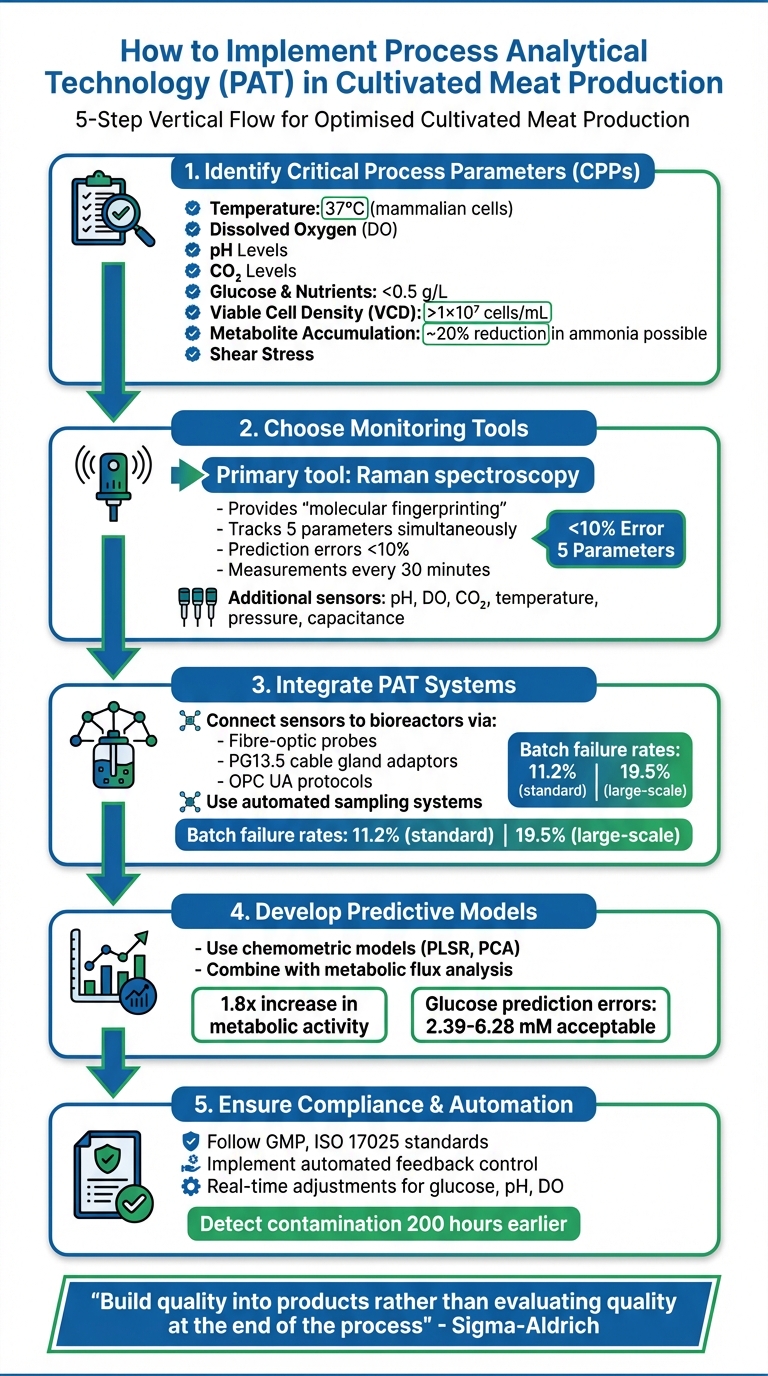
培養肉生産におけるPAT導入のための5ステッププロセス
バイオプロセス専門家パネルディスカッション I - PAT導入
重要プロセスパラメータ(CPP)の特定
培養肉生産の成功を確実にするためには、細胞の生存率、バイオマス収量、製品品質に影響を与える重要プロセスパラメータ(CPP)を特定することが不可欠です。これを誤管理すると、全生産が危険にさらされる可能性があります。
監視すべき主要パラメータ
温度は重要な要素です。哺乳類の細胞は約37°Cで最適に成長し、魚類や昆虫の細胞は最適な代謝活動を維持するために、より低温の環境を必要とします[2].
溶存酸素 (DO)は、好気性代謝にとってもう一つの重要な要素です。生産が拡大するにつれて、十分な酸素移動を確保することがより困難になります[2]。酸素が不足すると、細胞は嫌気性代謝に切り替わり、乳酸の蓄積を引き起こし、成長を妨げる可能性があります。
pHレベルは、培養の代謝状態を示す指標です。変動があると、酵素活性が妨げられ、細胞の健康が損なわれ、製品の特性(例えば、食感や保水性)に影響を与える可能性があります[2][3]。
二酸化炭素 (CO₂) のレベルは、特に大規模な運用において慎重に管理する必要があります。動物細胞はCO₂レベルの上昇に特に敏感であり、継続的な監視が不可欠です [2].
グルコースと栄養素 は細胞の主なエネルギー源です。グルコースレベルが低すぎると、細胞が飢餓状態になり、死滅や早期分化を引き起こす可能性があります [2]。グルコース濃度を低く保つこと (e.g., 0.5 g/L 以下) で、非効率な代謝を防ぎ、乳酸の蓄積を減少させることができます [4].
生存細胞密度 (VCD) は、培養の成長段階 - 遅滞期、対数期、定常期 - を追跡し、最適な収穫時期を決定するのに役立ちます [2]。培養肉の場合、高い細胞密度はしばしば1×10⁷ cells/mL以上と見なされます [2]。
代謝物の蓄積 - アンモニアや乳酸など - は成長を妨げ、細胞の生存率を低下させる可能性があります。これらの有害な副産物を監視し、制御することが重要です。例えば、ある方法では有害なアンモニアレベルを20%削減しました[2].
せん断応力は、インペラーやガスバブルによって引き起こされ、独特の課題をもたらします。微生物細胞とは異なり、動物細胞は保護細胞壁を持たないため、損傷を受けやすくなります。許容可能な応力レベルは種によって異なり、各細胞株に合わせて微調整する必要があります[2].
これらのパラメータは、培養肉生産を最適化するための基盤を提供します。
培養肉に特有のパラメータ
上記の要因は広く適用されますが、培養肉生産は特別な注意を要する独自の課題をもたらします。
CO₂感受性は特に重要です。動物細胞は微生物細胞に比べてCO₂阻害に対してより感受性が高く、これが管理すべき重要なパラメータとなっています[2].
生産の拡大は新たな優先事項をもたらします。バイオ医薬品では、バイオリアクターは通常、高価値製品のために20,000 Lで最大化されます。しかし、培養肉は経済的に実現可能であるために、はるかに大きな容量が必要です。視点を変えると、これまでに建設された最大の微生物バイオリアクターは1,500,000 Lを保持しており、培養肉生産がいつの日か到達する必要がある規模です[2].
熱管理は種によって異なります。非哺乳類細胞は全く異なる加熱および冷却システムを必要とし、温度制御は非常に種特異的です[2]。この変動性は柔軟なプロセス分析技術(PAT)システムを要求します。
これらのパラメータに適した監視機器を調達することは難しい場合があります。
これらのCPPを習得することは、PATツールを通じてリアルタイム制御システムを実装する前の必要なステップです。
PATツールの選択と統合
重要なプロセスパラメータを特定したら、次のステップは、測定が行われる場所や応答速度に合ったセンサーを選択することです。インラインモニタリングはここで際立っています。センサーがプロセスストリーム内に留まるため、アットラインやオフラインの方法と比較して、最も迅速で動的なリアルタイムの洞察を提供します。[6]。pHや溶存酸素のように即時のフィードバックが求められるパラメータに対して、インラインセンサーはサンプリングによる遅延を排除します。
センサーと技術の選択
この分野で際立ったツールの一つはラマン分光法であり、培養肉の生産における定番の選択肢です。「分子指紋」を提供する能力により、グルコースや乳酸のような有機分子を特定するのに特に効果的であり、水に影響されません[6][7]。2026年1月にMerck/Sigma-Aldrichによる研究では、ProCellics™ Raman AnalyserとBio4C® PAT Raman Softwareの有効性が強調されました。このシステムは、3Lの水ジャケット付きバイオリアクター内のCHO細胞培養を監視し、30分ごとに測定を行いました。特に、5つのパラメータを同時に追跡し、6日目の細胞希釈イベント中に総細胞密度と生存細胞密度を10%未満の誤差で正確に区別しました[11]。
「ラマンは、上流バイオプロセスの監視と制御のための第一選択のPATとなっています。これは、先進的なプロセス制御を促進し、一貫したプロセス品質を可能にするからです。」 - Karen A Esmonde-White, Endress+Hauser [8]
ラマン分光法は精密であるだけでなく、主要な代謝物レベルを10%未満の誤差で予測します [7][11]。しかし、ラマンだけでは不十分です。pH、溶存酸素、CO₂、温度、圧力、静電容量のための標準バイオリアクターセンサーも必要です [10][6]。特に培養肉生産におけるバッチ失敗率が11.2%で、大規模なセットアップでは19.5%に上昇するため、運用を合理化し、汚染リスクを低減するために、自動サンプリングシステムは不可欠です [5]。
センサーを選択する際は、多変量データ解析 (MVDA) および 実験計画法 (DOE) ソフトウェアと互換性があることを確認してください[1]。この互換性により、ツールは小規模な研究開発用バイオリアクターから商業生産規模まで拡張可能です[1]。
バイオリアクターシステムへのPATツールの統合
現代のバイオリアクターシステムは、PATツールの統合を簡素化します。非破壊のインライン測定は、光ファイバープローブを使用して可能になり、標準のPG13.5ケーブルグランドアダプターを介して取り付けられます。これらのプローブは、OPC UAプロトコルを通じてバイオリアクターシステムにシームレスに接続されます[8][9][11][1]。
データ面では、Bio4C® PAT Raman SoftwareやBioPAT® MFCSのようなプラットフォームが、センサーデータをリアルタイム制御のための実用的なインサイトに変換します[10][11]。これらのシステムは、主成分分析 (PCA)や部分最小二乗法 (PLS)のような高度なツールを使用して、複雑なスペクトルデータを意味のあるプロセスパラメータに変換します[9]。
「ラマン技術の応用は... バイオ医薬品製造における包括的なプロセスの理解と制御を可能にし、ユーザーが自信を持って正しい決定を下すことを支援します。" - Merck/Sigma-Aldrich [11]
ラマンモデルを構築する際、分析物スパイキング - 既知の濃度の分析物を追加する手法 - は、化合物間の相関を断ち切り、モデルが間接的な傾向に依存しないようにするのに役立ちます[1]。DOEを使用して幅広いプロセス条件を組み込むことで、モデルが商業規模の変動に対応できるほど堅牢であることを保証します[1]。
統合の課題が解決されたら、次のタスクは適切なPAT機器の調達です。
培養肉用PAT機器の調達
培養肉生産におけるリアルタイムモニタリングのための適切なツールを見つけるのは難しいことがあります。幸いなことに、
成長培地が生産コストの50%以上を占めることが多いことを考えると、栄養素の使用を最適化するための効果的なモニタリング機器の調達は、実用的であるだけでなく経済的にも賢明です。
sbb-itb-ffee270
プロセス最適化のための予測モデルの構築
PATツールを導入した後、次のステップは、細胞の生存率や代謝物レベルなど、直接測定が難しい変数を推定するために予測モデルを使用することです[12]。スペクトルデータを分析することで、より迅速でスマートなプロセス制御が可能になります。このデータを信頼性のある予測モデルに変換することが課題です。
ケモメトリックモデルの開発
部分最小二乗回帰(PLSR)は、培養肉の生産でよく見られる重なり合ったノイズの多い信号に対処するための優れた出発点です[7][13]。1,000~3,000の変数を含むことがあるラマン分光を精緻化するために、データを微分計算で前処理します。 これは、重要なピークを保持しながらノイズを低減するのに役立ちます。ただし、データを過度に平滑化しないように注意してください。そうしないと、モデルが依存する信号が消えてしまう可能性があります。
変数選択も同様に重要です。主成分分析(PCA)は、ターゲットパラメータと最も強く関連するスペクトル領域を特定するのに役立ちます。例えば、2018年の研究では、第8主成分(PC8)がグルコース濃度と高い相関があることが明らかになりました。研究者たちはこの洞察を利用して、PLSRモデルを微調整しました[7]。この焦点を絞ったアプローチは、過学習のリスクを減らし、モデルが意味のあるデータに集中することを保証します。
培養肉の生産においては、データ駆動型モデルとフラックスバランス解析(FBA)などのメカニスティックモデルを組み合わせることが特に効果的です。2023年に、オックスフォード・バイオメディカは、HEK293T細胞培養を監視するために屈折計ベースのPATシステム(レンジャーシステム)を使用しました。実時間データと代謝フラックス解析を統合することにより、pHが細胞内酸素レベルと代謝活動に直接影響を与えることを明らかにしました。このハイブリッド戦略により、最適化されていないプロセスと比較して代謝活動を1.8倍に向上させるpH運用計画が開発されました。[12][14].
モデルが構築されたら、次のステップは実際の運用条件下で正確かつ信頼性のあるパフォーマンスを確保することです。
生産用途のためのモデルの検証
モデルの真の試験はその検証にあります。まず、トレーニングフェーズの一部ではなかった独立したデータセットに対して評価を開始します。予測の精度を測るために、予測の二乗平均平方根誤差(RMSEP)などの指標を使用します。培養肉プロセスにおけるグルコースモニタリングでは、予測誤差は2.39 mMから6の範囲です。28 mMは、リアルタイムの自動制御において通常許容される範囲です[7].
スケーラビリティも重要な要素です。モデルは、小規模なR&Dバイオリアクターでも大規模な商業システムでも、一貫した結果を提供する必要があります。2018年の研究では、PLSRモデルが10 Lから100 Lシステムにスケールアップしても予測精度を維持したことが示されました[7].
最後に、「パラメータプロービング」を使用して動的条件でモデルをテストします。これは、pHや溶存酸素などの変数を調整して、モデルが変化を正確に追跡できるかどうかを確認する方法です[14]。オックスフォード・バイオメディカは、この方法を使用して自律的なpH制御システムを検証しました[12]。その後、PATシステムがパラメータを希望の範囲内に維持できることを確認するために、クローズドループテストを実施します[14]。
リアルタイムプロセス制御の実装
リアルタイムプロセス制御は、予測モデルをさらに一歩進め、継続的なデータを使用して最適なパフォーマンスを維持します。ライブセンサーデータを自動調整に変換することで、栄養レベル、pH、溶存酸素などの重要な条件が一貫して調整されることを保証し、手動介入を必要としません。これにより、労働コストと人的エラーが削減されるだけでなく、より一貫した製品品質が保証されます。培養肉の生産において、このような自動化はリアルタイムプロセス最適化を達成するためのゲームチェンジャーです。
これを実現するためには、重要なプロセスパラメータ(CPP)を直接測定し、それらの信号を制御システムに入力することが重要です。ダン・コペック、Sartorius Stedim BiotechのPAT専門家は、このアプローチの重要性を強調しています:
重要なプロセスパラメータ(CPP)を制御する最良の方法は、その特定のパラメータを測定し、ライブ信号を制御システムに統合し、スマートフィードバックアルゴリズムを適用して自動制御ループを実現することです。[4]
これらのフィードバックループは、リアルタイムのセンサー読み取り値を事前に定義された設定値と比較します。PIDアルゴリズムを使用して、栄養供給、pH、溶存酸素などの重要なパラメータを自動的に調整し、すべてがスムーズに動作するようにします。
例えば、培養肉の生産では、インシチュセンサーがほぼ瞬時に測定を行います。例えば、キャパシタンスセンサーは、細胞をラジオ周波数フィールド内のマイクロキャパシタとして扱うことで、生細胞体積を追跡できます。このデータは、連続灌流プロセスにおける自動化されたセルブリード制御をトリガーし、安定したセル密度を維持するのに役立ちます。[4]
フィードバック制御システムの設定
培養肉の生産において、グルコース、pH、溶存酸素などのパラメータは、細胞の成長と代謝効率に直接影響を与えます。グルコースレベルを低く保つこと(約0.1–0.5 g/L)は、乳酸の蓄積を防ぐために特に重要です。[4] これに対処するために、Sartorius Stedim BiotechはBioPAT Traceシステムを開発しました。この技術は、酵素バイオセンサーと10 kDa膜を持つ透析プローブを使用して、体積を失うことなく1分ごとにグルコース測定を提供します。これにより、灌流バイオリアクターでの高い細胞密度が確保されます。[4]
pH制御の自動化もまた、重要な改善をもたらす可能性があります。ある研究では、オックスフォード・バイオメディカとWattBEイノベーションズの研究者が、レンジャー屈折率(RI)PATシステムを使用してHEK293T細胞培養を監視しました。「代謝率指数」(MRI)を開発し、pHの設定値を調整することで、代謝活動が1.8倍に増加しました。この技術は「パラメータプロービング」とも呼ばれ、変数を調整してシステムの反応を観察し、運用条件を改善することを含みます。[12]
信頼性をさらに向上させるために、仮想センサーがハードウェアセンサーのバックアップとして機能することができます。例えば、静電容量の読み取りに基づく仮想センサーが、ラマンプローブからのグルコースデータをクロスチェックするかもしれません。この冗長性は、プロセスの変動性が高い場合に特に有用なセンサーのドリフトや故障をプロセスを妨げる前に検出するのに役立ちます。
培養肉におけるリアルタイムオートメーションの例
リアルタイム制御戦略は、すでにさまざまなアプリケーションで印象的な結果をもたらしています。例えば、Sartorius Stedim Biotechは、GSK Medicine Research Centreと協力して、CHO細胞培養における自動閉ループ給餌のためにBioPATプラットフォームを使用しました。これにより、手動サンプリングが排除され、栄養素の安定供給が確保されました。[4]
別の例では、Oxford BiomedicaがRanger RIシステムを代謝フラックス分析と統合し、自律的なpH制御戦略を作成しました。このシステムは細胞の代謝状態に適応し、従来の方法よりも最大200時間早く微生物汚染を検出し、リアルタイムモニタリングの可能性を示して高価なバッチ失敗を防ぎます。[12]
Kopecが適切にまとめているように:
自動化とリアルタイムモニタリングは、品質と収率の向上、労働コスト、リスク、廃棄物の削減とともにプロセスを改善するはずです。[4]
始めるには、最も重要なパラメータ、通常はグルコース、pH、溶存酸素に焦点を当て、プロセスの理解が深まるにつれて自動化を徐々に拡大します。この段階的なアプローチは、リアルタイム制御を通じて培養肉の生産を最適化するために不可欠です。
結論: PAT導入のステップ
プロセス分析技術(PAT)を培養肉の生産に導入するには、明確で体系的なアプローチが必要です。最初に、重要プロセスパラメータ(CPP)を特定します。これには、グルコースレベル、pH、溶存酸素が含まれ、いずれも製品の品質に直接影響を与えます。これらが定義されたら、ラマン分光法や静電容量センサーのようなPATツールを選択し、リアルタイムモニタリングを可能にします。
次のステップは、これらのセンサーをバイオリアクターシステムに統合し、収集したデータを理解するための予測モデルを作成することです。可能な限りインラインモニタリングを優先してください。これにより、遅延が排除され、プロセス中の汚染リスクが低減されます。
自動フィードバックシステムはここで重要な役割を果たし、生データを即時の実行可能な調整に変換します。シグマアルドリッチが適切に述べているように:
PATの主要な目的は、プロセスの終わりで品質を評価するのではなく、製品に品質を組み込むことです。[6]
この積極的なアプローチは、労働コストを削減するだけでなく、廃棄物を削減しながら一貫した製品品質を確保します。
自動化されたフィードバックシステムが稼働したら、次に注目すべきは適切なPAT機器の調達です。信頼性の高い機器は成功の鍵であり、
プロセスの理解が深まるにつれて、規制基準を満たしながらスケーラブルで一貫した生産を達成するために自動化を徐々に拡大してください。これらの手順に従うことで、PATの実装は、より効率的で信頼性の高い培養肉生産プロセスの基盤となることができます。
よくある質問
培養肉生産におけるプロセス分析技術(PAT)の利点は何ですか?
プロセス分析技術(PAT)は、培養肉生産におけるプロセス制御と製品の一貫性を向上させる上で重要な役割を果たします。温度、pHレベル、溶存酸素などの重要な要素のリアルタイムモニタリングにより、PATは細胞の最適な成長条件を確保し、予期しないプロセスの問題の発生を最小限に抑えます。その結果、より高い収率、一貫した品質、そして生産コストの削減が実現します。
PATのもう一つの利点は、品質設計(QbD)フレームワークをサポートすることです。分析データを製品の特定の品質特性に直接結びつけることで、従来のエンドポイントテスト方法への依存を減らします。このアプローチは、検証プロセスを迅速化するだけでなく、再現性を向上させ、予測制御戦略を可能にするデータ駆動型の意思決定を可能にします。
培養肉分野の企業にとって、ラマン分光法は、培養肉生産のためのPATシステムにおけるリアルタイムモニタリングをどのように改善しますか?
ラマン分光法は、PAT(プロセス分析技術)システム内でのリアルタイムモニタリングにおいて、重要なプロセスパラメータの迅速で非侵襲的なインライン測定を提供することで重要な役割を果たします。これは、より厳密なプロセス制御を維持し、製品の品質を一貫して確保するのに役立ちます。
その際立った特徴の一つは、複数の分子を同時に検出する能力です。例えば、グルコース、乳酸、アンモニウムのレベルを監視しながら、細胞の生存率や製品の特性を評価することができます - すべてを単一の測定で行います。現代のラマンプローブは、バイオリアクターストリームに直接設置できるように設計されており、サンプルを抽出することなく継続的なデータ収集を可能にします。
もう一つの利点は、自動フィードバック制御をサポートしていることです。リアルタイムデータを提供することで、ラマン分光法は栄養供給の正確な調整を可能にし、最適な生産条件を維持します。さまざまなリアクターサイズにわたってモデルをスケーリングおよび転送する柔軟性は、培養肉の生産におけるその有用性をさらに高め、効率を向上させ、エラーのリスクを最小限に抑えます。
培養肉生産のためのプロセス分析技術(PAT)のスケールアップにおける主な課題は何ですか?
大規模な培養肉生産のためのPAT(プロセス分析技術)のスケールアップには、綿密な計画と実行を要求する多くの課題が伴います。主な問題は、PAT機器によって生成される膨大なデータ量の管理と統合にあります。生産が拡大するにつれて、データの正確性を維持しながら制御システムへのスムーズな統合を確保することが、より複雑な作業となります。
もう一つの重要な障害は、産業規模のバイオリアクターにおけるセンサーの性能です。小規模なセットアップでうまく機能するセンサーは、せん断力や温度変動などの要因がリアルタイム測定の精度を損なう可能性がある大規模なシステムでは課題に直面することがよくあります。
また、培養肉生産の独自の要求に合わせた専門機器の調達の問題もあります。
信頼性のあるセンサーを選択し、スケーラブルなデータシステムを構築し、戦略的に調達を計画することで、これらの課題に早期に取り組むことができ、商業規模の生産への移行をより効率的に進めることができます。











