自動化サンプリングシステムは、特に培養肉の生産において、バイオプロセスの監視方法を変革しています。これらのシステムは、栄養素レベル、代謝物、細胞の健康状態などの重要な要素に関する頻繁で正確かつリアルタイムのデータを提供し、手動サンプリングでは実現できないものです。手動では1日1回のところを、2~3時間ごとに実行することで、代謝の変化をより明確に把握し、コストのかかる生産エラーを防ぐのに役立ちます。
主なポイントは以下の通りです:
- 効率性: サンプリング、分析、洗浄サイクルは15分以内で完了します。
- 無菌性: システムは370時間以上無菌状態を維持し、汚染リスクを低減します。
- 正確性: グルコース測定の偏差はわずか1.1%で、アミノ酸分析はほぼリアルタイムの洞察を提供します。
- 労働節約: 手動介入を最小限に抑え、スタッフが他の作業に専念できるようにします。
- アプリケーション: 培養肉生産における一貫性とスケーラビリティを向上させます。
これらのシステムは、HPLCやラマン分光法のような高度なツールとシームレスに統合され、正確な栄養素のモニタリングとリアルタイムのプロセス調整を可能にします。その結果、品質管理の向上、変動の削減、より効率的な生産ワークフローをサポートします。
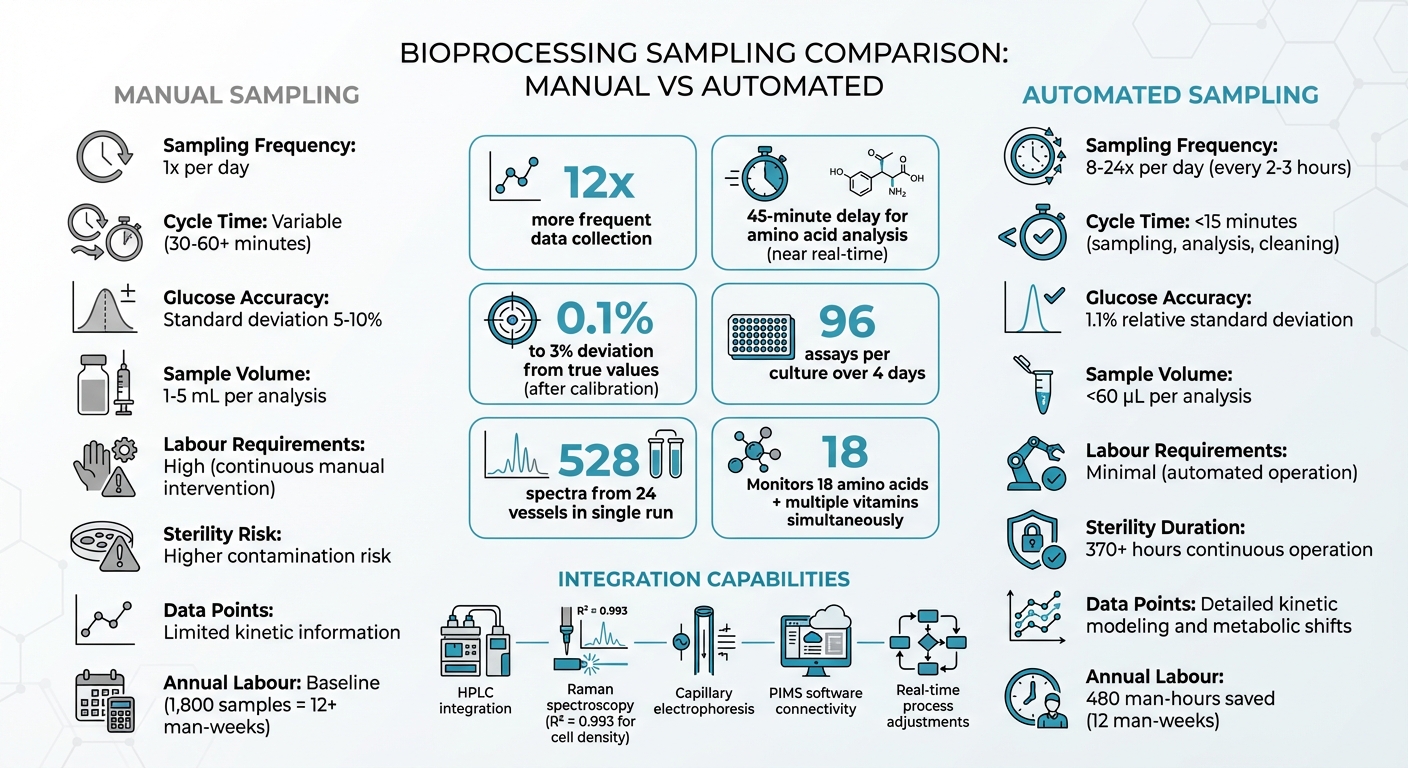
手動 vs 自動サンプリングシステム: バイオプロセスにおける性能比較
自動サンプリング技術に関する研究
研究方法とアプローチ
自動サンプリング技術の最近の進歩により、培養肉生産におけるその応用が大幅に洗練されました。これらの研究は、プロセス全体での無菌性を維持しながら、分析ツールと自動サンプリングシステムの統合に焦点を当てています。研究者は通常、HPLCや キャピラリー電気泳動のような確立された方法と自動サンプラーを組み合わせて、インラインセンサーでは正確に測定するのが難しい複雑な代謝物を監視します。
2020年5月、ウィーン工科大学のチームは、 Numeraシステムを Securecell AGによって調査し、CHOフィードバッチ培養中にLucullus PIMSソフトウェアを利用しました。彼らは18種類のアミノ酸とIgG製品レベルを監視し、連続運転 370時間の間、無菌状態を維持しました [2]。細胞密度が増加するにつれて、「プッシュアウトタイム」などのシステム設定の調整が重要になりました[2]。
同様に、2017年8月、ロザンヌ・M。Guijtは タスマニア大学で、ジュルカット細胞の5つの並行懸濁培養を監視するために 逐次注入キャピラリー電気泳動(SI-CE)を使用しました。4日間にわたり、システムは各培養で 96のアッセイを実施し、各電気泳動分離にはわずか12分しかかかりませんでした。驚くべきことに、フラスコあたりわずか5.78 mL(分析あたり60 µL未満)しか必要とせず、培養量を大幅に減らすことなくハイスループットスクリーニングに理想的です[6]。これらの正確で体系的な方法は、パフォーマンスデータへのより深い洞察の基盤を築きます。
研究結果とパフォーマンスデータ
これらの研究から得られた発見は、自動サンプリングシステムの効率と精度を強調しています。例えば、ウィーンのチームは、グルコース測定で1.1%の相対標準偏差を達成しました。さらに、サンプル希釈によって引き起こされる系統的誤差が修正され、真の値からの偏差が 0.1%から3%にまで低減されました [2]。この精度のレベルは、通常の手動サンプリングが提供するものよりもはるかに優れています。
サンプリング頻度は、もう一つの重要な利点です。手動サンプリングが通常1日1回に制限されているのに対し、自動化システムは1日8回から24回サンプリングでき、見逃されがちな代謝変化を捉えることができます。ウィーンの研究では、アミノ酸分析がサンプル採取から45分遅れで完了し、栄養素の枯渇に関するほぼリアルタイムの洞察を提供しました [2]。
タスマニアの研究は、もう一つの重要な利点を強調しました。リアルタイムの細胞密度測定に対して乳酸データを正規化することにより、研究者はロテノンやクリオキノールのような化合物の薬理学的効果を単純なバイオマスの変化から区別することができました[6]。このレベルの詳細は、従来の手動サンプリングではほぼ不可能であり、まばらなデータポイントが重要な代謝パターンをしばしば隠してしまいます。
メディアモニタリングのためのセンサー技術
センサーと分析ツールの種類
センサー技術は、特に培養肉の生産において、リアルタイムのメディアモニタリングを洗練する上で重要な役割を果たします。さまざまなセンサーが、メディアの組成と細胞の健康状態を注意深く監視するために使用されます。例えば、標準のインラインセンサーは、pH、温度、および溶存酸素を継続的に測定し、細胞成長に理想的な条件を維持します[7]。生細胞密度を測定する際には、キャパシタンスプローブが唯一の商業的に利用可能なオンラインソリューションです。これらのプローブは電場を使用して生細胞を検出し、健全な細胞膜が小さなコンデンサーとして機能するため、生細胞を死細胞やデブリから区別します[7]。
分光センサーは、代謝活動を非侵襲的に追跡する方法を提供します。例えば、UV–vis分光法は光の吸収と散乱(200–740 nm)を分析し、細胞密度を推定し、損傷した細胞からの核酸を識別します [7]。蛍光分光法は、NADH、NADPH、トリプトファンのような自然に存在する蛍光体を監視し、プロセスに干渉することなく、培養の代謝状態に関する貴重なリアルタイムの洞察を提供します [7]。一方、ラマン分光法は、メディアの分子指紋を生成し、グルコース、乳酸、アミノ酸レベルを最小限の誤差で正確に追跡することを可能にします [7][2]。実際、インラインラマンセンサーは、複雑なメディアにおいてチロシンの0.41 mM、トリプトファンの0.24 mMの二乗平均平方根誤差で顕著な精度を示しています[2]。これらの分光ツールは、高速で非破壊的な代謝分析を提供することにより、自動サンプリングシステムを補完します。
自動化システムは、バイオリアクターを高度な分析装置に接続することで、精度をさらに向上させます。このセットアップにより、アミノ酸やビタミンのような複雑な栄養素のリアルタイムモニタリングが可能になりますが、これらは現在のインラインセンサーでは正確に測定するのが難しいです[1][2]。例えば、UV–vis吸収分光法モデルは、細胞密度予測においてR²値が0.993に達し、その信頼性を示しています[7]。
センサー統合の例
技術開発者と研究者の協力により、センサー統合において印象的な進歩が見られました。その一例が、Sartorius Stedim Biotechと Tornado Spectral Systemsのパートナーシップです。彼らは、Ambr 250 高スループットミニバイオリアクターシステムにラマンフローセルプロトタイプを組み込みました。それを BioProfile FLEX2アナライザーと Nova Biomedical からの自動参照測定のために組み合わせることで、CHO細胞培養におけるグルコース、乳酸、グルタミンを追跡するための堅牢なモデルを作成しました。このセットアップにより、スペクトルデータと参照データの間の時間差がわずか5分に短縮され、ほぼ瞬時のデータ相関が可能になりました [8]。
"ラマン分光法は、細胞培養分析物を非破壊的にインシチュで測定するのに適したPATツールです...調査された分子の共有結合に関する構造情報を高い分子特異性と堅牢性で提供します。"
– Marek Hoehse, Sartorius Stedim Biotech [8]
別の例はウィーン工科大学から来ており、研究者たちはセンサー統合が精度をどのように向上させるかを実証しました。3を使用して。6 Lバイオリアクターを、Thermo Fisher Ultimate 3000 HPLCおよび Roche Cedex Bio HTアナライザーにNumeraシステムを介して接続しました。このセットアップにより、CHOフィードバッチ培養中に18種類のアミノ酸とナイアシンアミド、葉酸、B12、リボフラビンなどのビタミンをリアルタイムで監視することができました [2]。自動化システムは、単一のランで24の容器から528のスペクトルを生成し、従来のパイロットスケールモデル構築と比較してコストを削減し、時間を節約しました[8]。
プロセス最適化と品質管理
リアルタイムプロセス調整
自動サンプリングシステムは、ラボ分析とライブ生産のギャップを埋め、プロセス分析技術 (PAT)をリアルタイムで使用できるようにします [2]。これらのシステムは、2~3時間ごとにデータを提供し、細胞代謝と栄養素の使用に関する包括的なビューを作成します[2]。この高頻度データは、手動サンプリングでは見落とされがちな乳酸シフトなどの動的な値や重要なイベントを捉えます[2][6]。
プロセス情報管理システム (PIMS)と組み合わせると、これらの分析結果は必要に応じて給餌戦略を自動的に調整することができます[2]。動的アルゴリズムは反応のプラトーを特定し、プロセスのタイムリーな修正を可能にします[5]。この機能は、培養肉の生産において特に価値があり、高い細胞密度と収量を達成するために最適な栄養バランスを維持することが重要です。
"手動サンプリングと比較してサンプリング頻度が高いため、生成される情報の内容が増加し、代謝の解釈が容易になり、プロセスイベントの検出がより正確になります。"
– Paul Kroll, Business Development Manager, Securecell AG [1]
注目すべき例として、2020年にウィーン工科大学が3.6リットルのバイオリアクターをNumeraシステムを介して自動HPLCおよびCedex Bio HTアナライザーに接続したケースがあります。このセットアップでは、370時間にわたり18種類のアミノ酸と複数のビタミンを監視し、偏差は0.1%から3%と非常に低く抑えられました[2]。頻繁なデータ収集により、手動の方法では完全に見逃してしまう反応速度論を観察することが可能になりました。
利点と課題の比較
自動サンプリングシステムに関連する主な利点と課題の内訳は次のとおりです。
| 特徴 | 利点 | 課題 |
|---|---|---|
| 精度 & 正確性 | 高精度を実現 (1.1% RSD) とサンプル調製における人的エラーを排除します [2] | 希釈係数のための綿密な校正と調整が必要です [2] |
| データ頻度 | 1日8サンプル以上を可能にし、詳細な動力学モデリングを可能にします [2] | 高データ量は管理のために高度なソフトウェア (PIMS) を必要とします [2] |
| 労働 & コスト | 手動サンプリングと誘導体化の作業負荷を削減します [2] | 高額な初期設備費用と複雑な設置 [2][5] |
| サンプル量 | 最小限のメディアを消費します(<分析あたり60 µL未満)、リアクターボリュームを長時間の運転のために保持します[6] | チューブ内の小さなボリュームは、残留物の蓄積や表面比効果を受けやすいです[2] |
| プロセス制御 | リアルタイムの給餌と栄養調整を促進します[2][3] | サンプラー、アナライザー、バイオリアクターコントローラー間のシームレスな統合が求められます[2] |
自動化システムは、370時間以上の無菌状態を維持するだけでなく、分析あたり60マイクロリットル未満のメディアを必要とします[2][6]。しかし、オペレーターは液体処理における潜在的な系統的誤差に対処する必要がありますが、自動キャリブレーションにより偏差を0.1%まで低減することができます[2]。さらに、ろ過モジュールの「プッシュアウト時間」(POT)は、プロセスの進行に伴い一貫したサンプル供給を確保するために、生細胞密度に基づいて調整する必要があるかもしれません[2]。
これらの戦略は、自動化システムが培養肉の生産を反応的な監視からより積極的で制御されたプロセスに移行させ、センサー技術と研究の初期の進歩を補完する方法を強調しています。
sbb-itb-ffee270
Cellbase 自動サンプリングシステムのリソース
認定サプライヤーリスト
このプラットフォームは、bbi-biotechのbioPROBEのような特殊な無菌サンプリングツールも強調しています。このツールは、「設計による無菌性」を誇り、バイオフィルムの形成と詰まりを防ぐ特許取得済みのガスクッション輸送メカニズムを採用しています[9]。さらに、
簡素化された機器調達
検証済みリストを紹介するだけでなく、
R&Dチーム向けに、検証済みリスティングは、サンプリングとイベントベースの調整の両方を自動化するソリューションを提供します。これは、0.5 mlのような小さなサンプル量を管理するのに特に役立ち、メディアの損失を最小限に抑えるのに役立ちます[9][10]。時間節約の可能性は大きく、1,800サンプルを処理する際に、自動サンプリングは手動方法と比較して年間約480人時(12人週に相当)の労働需要を削減できます[9]。設備の取得を合理化し、精度を向上させることにより、
結論
要約と今後の展望
自動サンプリングシステムは、培養肉のバイオプロセスの監視方法を変革しています。バイオリアクターを分析ツールと直接リンクすることで、従来の1日1回のアプローチに比べて12倍も頻繁に - 2~3時間ごとに高品質なデータを提供します[1][2] 。この頻繁なデータ収集により、細胞代謝の深い理解、栄養素枯渇の迅速な特定、および給餌戦略の最適化に重要な動的パラメータの計算が可能になります。
これらのシステムは、長期間の無菌状態を維持し、高精度の測定を提供するため、バイオプロセシングにおけるゲームチェンジャーとなっています。これらの利点がしっかりと確立されたことで、さらなる進歩の舞台が整いました。
培養肉生産の未来はスマートバイオマニュファクチャリングに向かっています。これは、自動サンプリングを予測モデルとクローズドループプロセス制御と統合することを含みます。このような進歩により、事後のデータ分析からリアルタイムのプロセス最適化へと焦点が移ります。これにより、給餌戦略をその場で調整でき、生産時間を短縮し、製品の品質を一貫して確保し、重要な品質属性の継続的な監視を通じて市場投入までの時間を加速します。[2][3]生産者にとって、これらのシステムは競争力のあるスケーラブルな運営の基盤となりつつあります。
この進化において、
(English) Numera PAT: バイオプロセスにおける自動サンプリング

よくある質問
自動サンプリングシステムは、培養肉の生産における一貫性をどのように向上させますか?
自動サンプリングシステムは、手動サンプリングに伴う予測不可能性を排除することで、培養肉の生産における一貫性を確保する上で重要な役割を果たします。これらのシステムは、スケジュールされた間隔で正確なサンプル量を収集するように設計されており、人為的なエラーを減らし、均一性を確保します。この安定した正確なサンプリングは、栄養素、代謝物、細胞の健康状態に関するリアルタイムの洞察を提供し、生産プロセスの制御を向上させ、製品の品質を向上させます。
サンプリング、準備、転送などのタスクを自動化することで、汚染の可能性が大幅に減少します。さらに、データ収集は標準的な勤務時間外でも継続でき、生産プロセスのより包括的なビューを提供します。この継続的な監視により、フィード、温度、その他の重要な要素などのパラメータを迅速に調整でき、一貫したバッチ品質とより信頼性の高い生産結果が得られます。培養肉セクターで働く人々にとって、
センサーは培養肉生産におけるリアルタイムモニタリングにどのように貢献しますか?
センサーはリアルタイムモニタリングに不可欠であり、溶存酸素、pH、温度、細胞密度、細胞生存率などの重要なプロセスパラメータ(CPP) を継続的に追跡します。瞬時のフィードバックを提供することにより、これらのセンサーはオペレーターが逸脱を迅速に発見し、タイムリーに調整を行い、製品品質を損なう可能性のある問題を回避するのに役立ちます。
近赤外線(NIR)やラマンプローブなどの最新技術は、グルコースのような栄養素や乳酸のような副産物をリアルタイムで監視することで、手動サンプリングの必要性を削減し、さらに一歩進んでいます。インシチュ顕微鏡のような高度な光学ツールは、形態や生存率に関する詳細な単一細胞データを提供します。これらの革新は、プロセス分析技術(PAT)の中心であり、自動化を可能にし、培養肉生産における一貫した制御を確保します。
自動サンプリングシステムは、バイオプロセシングにおける労働をどのように削減しますか?
自動サンプリングシステムは、サンプルの採取、準備、分析機器への提供といったルーチンタスクを処理することで、バイオプロセシングの重労働を軽減します。これらのシステムは事前に設定されたスケジュールで動作し、技術者がバイオリアクターやサンプルと手動でやり取りする必要をなくします。その結果、反復作業が減り、人為的なエラーの可能性が減少し、熟練したスタッフがデータ分析やプロセスの改善といったタスクに集中する時間が増えます。
さらに、これらのシステムは手動の方法と比べて、はるかに頻繁なサンプリング、時にはほぼ連続的なサンプリングを可能にします。これにより、豊富なデータが生成され、リアルタイムのモニタリングと重要なパラメータの厳密な制御が可能になります。組み込みのデータ管理ツールにより、サンプルのメタデータが自動的に整理され、書類作業や手動データ入力が削減されることで、ワークフローがさらにスムーズになります。
培養肉産業に携わる方々にとって、











