哺乳類細胞を育てるためには、pHと温度を正確に維持することが特に培養肉の生産において重要です。細胞は増殖(増殖)し、筋繊維に発達(分化)するために制御された環境を必要とします。ここでの重要なポイントは次のとおりです:
- 最適条件: pHは7.2–7.4の間に保ち、温度は37°Cにする必要があります。わずかな偏差(e.g., pHが0.3単位下がるなど)でも成長が遅くなり、生産性が低下します。
- なぜ重要か: 細胞は不均衡を修正するために余分なエネルギーを消費し、それが成長効率に影響を与えます。高密度培養は特に乳酸の蓄積によるpH低下に陥りやすいです。
- スケールでの課題: 大型バイオリアクターはpHの急上昇やCO₂の蓄積など不均一な条件に直面し、正確な制御が難しくなります。
- ソリューション: 高度なバイオリアクターは、自動化システムと信頼性の高いセンサーを備えており、安定性を維持し、細胞の成長と一貫性を向上させます。
ラボで細胞を育てる場合でも、生産のためにスケールアップする場合でも、pHと温度を安定させることは成功のために不可欠です。
バイオリアクター内のセンサー
pHと温度が細胞成長に与える影響
バイオリアクター設計におけるpHと温度の役割は、理論的な重要性を超えて、細胞の代謝と成長に直接影響を与えます。このセクションでは、これら2つの要因が細胞の行動と生産性をどのように形作るかを探ります。
pHが細胞代謝と生存率に与える影響
pHレベルが最適範囲から逸脱すると、細胞はバランスを維持するためにより多くの労力を要します。例えば、Na⁺/H⁺アンチポーターのようなメカニズムを活性化し、成長に使われるはずのエネルギーを消費します。[3].このエネルギーの再配分は、遺伝子活動の大きな変化を引き起こす可能性があります。ある研究では、培地のpHを6.7に下げると、わずか24時間以内に2,000以上の遺伝子がその発現レベルを変化させました[3].
pHと代謝の相互作用は悪循環を生み出す可能性があります。高い解糖活性は乳酸を生成し、培地のpHを下げます。いくつかの高密度培養では、最大90%のグルコースが乳酸に変換され[2]、急速な酸性化を引き起こします。この酸性化は最終的にさらなる乳酸生成を停止させますが、細胞成長が著しく減少するという代償を伴います[5].
酸性およびアルカリ性の極端な条件は有害です。pH 7.1未満の酸性条件が成長を妨げることは広く知られていますが、アルカリ性条件 - pH 7.7から9の範囲。0 - は、増殖を遅らせ、製品の収量を減少させることもあります[2][4]。ほとんどの哺乳類細胞にとって、重要な下限pHは6.6から6.8の間です。この範囲を超えると、細胞はアポトーシスやネクローシスのリスクが高まります[5]。
これらのpHによる代謝の混乱は、温度が細胞の挙動にさらに影響を与える役割を果たす舞台を設定します。
細胞増殖と分化に対する温度の影響
温度は代謝活動とガスの溶解度において重要な役割を果たします。ほとんどの培養において37°Cが標準ですが、わずかな偏差でも成長やタンパク質生産に影響を与える可能性があります[3][5]。2017年にウィーン工科大学で行われた研究がこの効果を示しました。研究者たちは、pHの不均一性をシミュレートするために10–12 m³の撹拌タンクバイオリアクターでCHO細胞を使用しました。指数増殖期におけるpH 9.0ゾーンへの一時的な曝露は、最大生存細胞密度と最終製品収率の両方を著しく低下させました[4].
培養肉生産の分野では、温度管理は二重の目的を果たします。増殖期には、安定した37°Cを維持することで効率的な細胞増殖が確保されます。しかし、細胞の接着と剥離を制御することで、足場のない組織層を形成するための高度な温度応答システムが開発されています[6].
明らかに、正確な温度調整は、細胞の成長と分化の成功において最適なpHを維持することと同様に重要です。
pHと温度の複合効果
pHと温度の相互作用は、CO₂化学と密接に関連しています。温度の変化はCO₂の溶解度に影響を与え、それが重炭酸緩衝系の酸塩基平衡に影響を及ぼします[3]。高温は細胞代謝を加速し、乳酸やCO₂のような副産物の生成を増加させます。これにより培地がさらに酸性化し、細胞へのストレスが増大します[2][3]。
"溶解ガスの溶解度、したがってCO₂が酸塩基化学に与える影響は、温度、浸透圧、湿度、圧力に強く依存します。" - Shannon G. Klein et al., King Abdullah University of Science and Technology[3]
pHと温度が同時に逸脱すると、結果として生じる代謝ストレスが細胞の増殖と分化の両方を著しく妨げる可能性があります。例えば、標準的なバッチ培養では、中央値のpHシフトが0.425単位であることがよくあります[3]。高密度培養では、この変化は0.9単位に達し、CO₂レベルが10.45%に上昇します[3]。これらの条件は、細胞が恒常性を維持するためにさらに多くのエネルギーを消費することを強いられ、バイオマス生産の効率が低下します。
これらのストレスを最小限に抑えるために、新しく調製した培地は使用前に少なくとも1時間、CO₂インキュベーターで平衡化する必要があります。これにより、CO₂の水和の遅い逆反応が安定します[2]。このような予防措置は、最適な細胞成長と生産性を達成するために不可欠です。
バイオリアクターにおけるpHと温度の制御方法
バイオリアクターでpHと温度を安定させるには、ハードウェア、センサー、および制御戦略の組み合わせが必要です。選択される技術は、しばしば生産規模、培養肉に使用される細胞の種類、およびプロセスが自動化または手動管理のどちらに傾いているかに依存します。
バイオリアクターの設計と制御方法
培養肉の生産に使用されるバイオリアクターは、37°Cの温度を維持するために熱交換システムに依存しています[1]。pHレベルは通常、CO₂スパージングによって調整され、CO₂濃度とヘッドスペースの流れを調整します[9]、または必要に応じて酸や塩基を追加する自動シリンジポンプによって調整されます[8]。
使い捨てバイオリアクター(SUB)は、洗浄の必要性を排除し、汚染リスクを低減することで実用的な解決策を提供します。これらのシステムは2,000 Lまでスケールアップできます。しかし、1 kgのバイオマスを生産するために必要な作業量は、バイオリアクターの設計によって大きく異なります:撹拌槽リアクター(STR)では約570 L、充填床バイオリアクター(PBB)では110 L、そして中空繊維バイオリアクター(HFB)ではわずか1.4 Lです[1]。
モニタリングのためのセンサー技術
バイオリアクターがセットアップされると、正確なセンサーがリアルタイムでpHと温度をモニタリングする上で重要な役割を果たします。pH測定には、電気化学センサー、特にガラス電極がその耐久性と効果的な性能から広く使用されています[7]。温度に関しては、抵抗温度計が業界標準です[7]。
近年、光学センサーが特に使い捨てシステムで人気を集めています。これらのセンサーは、蛍光色素 - 例えば6,8-ジヒドロキシピレン-1,3-ジスルホン酸二ナトリウム塩 - をハイドロゲルパッチに埋め込んで利用します。コンパクトで、汚染リスクを最小限に抑えるのに役立ちます[7]。
非接触センサーは、セルロースのような透過性膜を使用して外部でpHを測定する別のオプションであり、汚染リスクをさらに低減します[7]。一方、比色システムは、培地内のフェノールレッド指示薬の色変化を検出してpHを追跡します。これらのシステムは、LED光源と環境光センサーを使用して検出を行います[8]。光学センサーは侵襲性が低いですが、指示薬-タンパク質結合や培地の濁りなどの問題に影響されることがあります。対照的に、電気化学センサーは、かさばるものの、そのような状況ではより堅牢で信頼性があります[7]。
自動化とフィードバックシステム
自動化はバイオリアクター制御に革命をもたらし、人為的なエラーを削減し、一貫性を向上させました。自動化システムとクローズドループ制御は、長期的な培養肉生産に特に価値があります[8]。例えば、チェンマイ大学の2022年の研究では、色素pHモニタリングを備えた3Dプリントの自動バイオリアクターが紹介されました。このシステムはpH 7.4 ± 0.2を維持し、手動の培地交換と比較して72時間で細胞増殖を大幅に向上させ、80%以上の細胞生存率を達成しました[8]。
もう一つの注目すべき例は、フランスのマルティラックにあるメルク・バイオデベロップメントからです。2013年12月、チームはパーフュージョンプロセス用のMobius CellReady 3L使い捨てバイオリアクターをテストしました。自動細胞保持と培地交換のためにオルタナティブタンジェンシャルフロー(ATF)技術を使用し、バッチモードと比較してモノクローナル抗体生産を2.9倍に増加させました。研究者のAurore Polès-LahilleとFlavien Thuetは、この自動化システムがpHレベルを6.80から7.10の間に維持しながら、細胞密度を3300万細胞/mLでサポートしたと報告しました[10]。これらのシステムは連続データを提供し、細胞の成長と生産性を最適化するためのリアルタイム調整を可能にします[8]。
培養肉生産のための先進的なバイオリアクター、センサー、および制御システムは、
sbb-itb-ffee270
研究結果: pHと温度制御の成果
自動制御システムと手動制御システム
2022年4月、チェンマイ大学のSuruk Udomsom、Pathinan Paengnakorn、およびそのチームは、L929マウス線維芽細胞を使用して自動プログラム可能なバイオリアクターをテストしました。このシステムは、72時間の期間中、6時間ごとに部分的なメディアのリフレッシュを実行しました。その結果は?自動化システムでは、従来の手動培養法と比較して細胞増殖が有意に高かった。バイオリアクターはpH7.4 ± 0.2の安定した状態を維持し、実験を通じて細胞の生存率は一貫して80%以上であった[8].
一方、手動システムは課題に直面している。CO₂インキュベーターから培地を取り出して検査すると、ほぼ即座にアルカリ化が始まり、時間定数は2~3時間である。インキュベーターに戻すと、正しいpHに戻るまでに約45分かかる[2]。これらの変動は細胞を不安定にする可能性がある。しかし、自動化システムはそのような不一致を排除するように設計されており、細胞成長のためのより安定した環境を確保する。
異なるpHと温度範囲のテスト
2019年4月、ジョアンナ・ミヒルと彼女のチームは、オックスフォード大学でDLD1細胞の代謝活動を6日間のインキュベーション期間にわたって調査しました。グルコースレベルが12 mM以上に保たれた場合、細胞は約20 mMの乳酸を生成し、培地の酸性化を引き起こしました。この研究では、最適なpH 7.4からのわずかな逸脱、具体的には0.3単位以上の変化が、3つの哺乳類細胞株(NCI-H747、DLD1、Caco2)の増殖率を低下させることがわかりました。[2][3].
"細胞の成長...はpH 7.4で最適でしたが、培地のpHが7.4から> 0.3単位逸脱すると、3つの細胞株すべてで増殖率が低下しました。" – シャノン・G・クラインら[3]
標準的なバッチ培養では、代謝活動によりpHの変化が一般的です。特に高密度培養では、溶存酸素レベルが0.95%まで低下することがあります。[3]これらの発見は、培養肉の生産を拡大する際に環境の安定性を維持することがいかに重要であるかを強調しています。
培養肉細胞タイプの結果
制御された研究を拡大し、スケールダウンシミュレーションは、大規模なバイオリアクターシステムでpHと温度の安定性を維持することの課題を明らかにしました。2017年7月、ウィーン工科大学のMatthias BrunnerとJens Frickeが率いる研究者たちは、10–12 m³の撹拌タンクバイオリアクターの条件を模倣するために、二室スケールダウンモデルを使用しました。彼らは、大規模システムでの塩基添加による不均一性をシミュレートするために、CHO細胞をpH 9.0の短期間にさらしました。短期間の高pHレベルへの曝露でも、指数増殖期の特定成長率が乱れ、最大生存細胞密度の減少と製品収量の低下を引き起こしました[4].
「大規模プロセス中の細胞の高pH値への短期間の曝露でも、細胞の生理学と全体的なプロセス性能に影響を与える可能性があります。」 – Matthias Brunner et al. [4]
一部の哺乳類細胞培養では、約90%のグルコースが乳酸に代謝されており、活発なpH緩衝の必要性を強調しています。これらの発見は、最適な細胞成長と生産性を確保するために、生産プロセス全体での正確な環境制御の重要な役割を強調しています。
装置の選択とバイオリアクターのスケールアップ
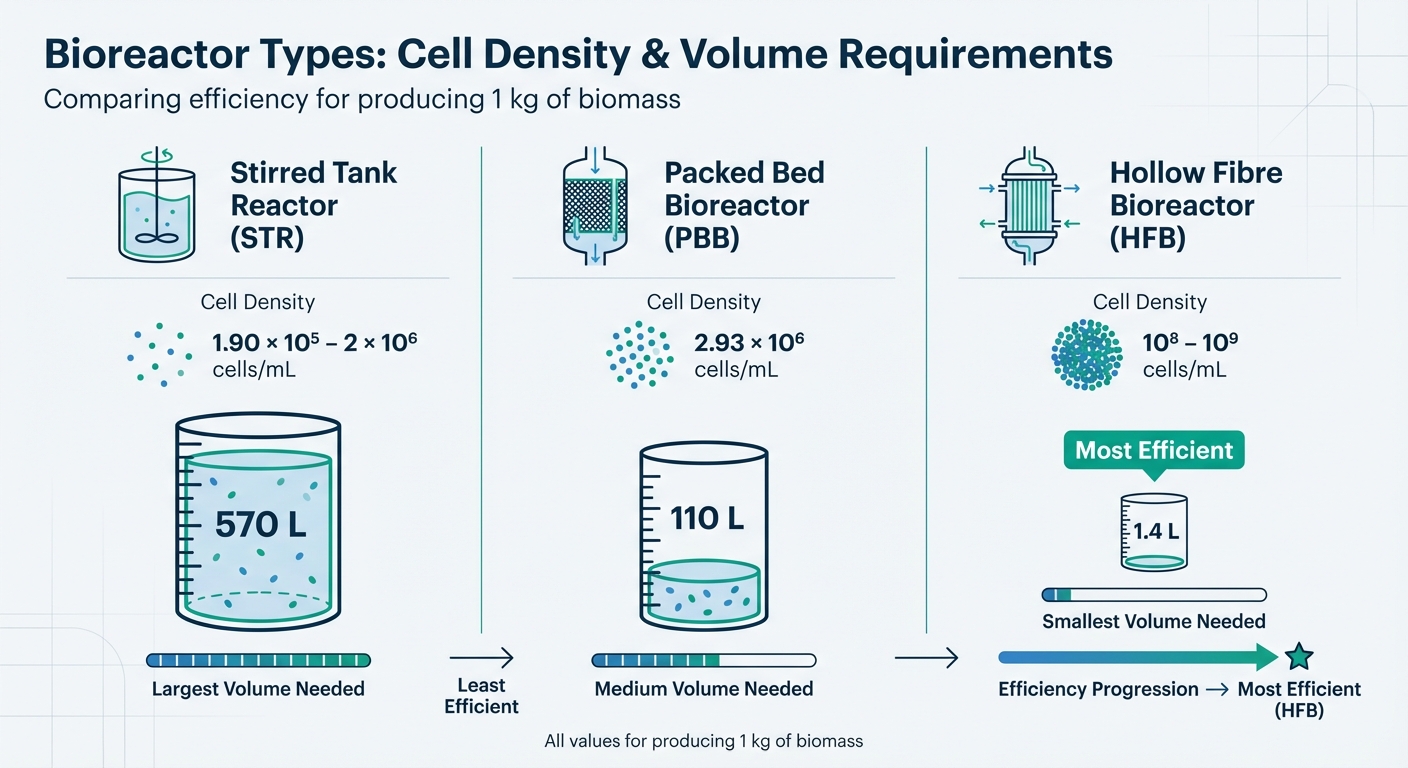
培養肉生産のためのバイオリアクタータイプの比較
pHと温度制御の設計要件
培養肉生産に使用されるバイオリアクターは、7.2–7.4の狭いpH範囲を維持するために正確な制御システムを備えている必要があります[1]。非線形モデル予測制御(NMPC)や適応制御のような高度なシステムは、pHと温度を安定させながら給餌率を調整するのに特に効果的です[12]。自動フィードバックシステムも、手動調整による不一致を排除する上で重要な役割を果たします。
安定したpH調整のためには、CO₂/重炭酸塩バッファリングが非常に効果的です。CO₂は中性pH付近で自己緩衝剤として作用し、腐食性がないため、適切な選択肢となります[1][2][11]。細胞成長中に発生する代謝熱を処理するために、バイオリアクターは熱交換器やサービス流体流システムを備えている必要があります[1][12]。
培養肉細胞、特に筋細胞前駆体は、その付着依存性のために流体力学的ストレスに非常に敏感です。これらの細胞は、懸濁適応細胞よりもはるかに壊れやすいです[1]。それらを保護するために、ガス透過性シリコンチューブのような泡のない曝気方法が、損傷を引き起こす剪断応力を伴う従来のスパージング技術よりも好まれます[1][11]。さらに、高品質のセンサーを統合することにより、pHや溶存酸素(pO₂)のインラインプローブ、二酸化炭素張力(pCO₂)を監視するオフガスセンサーなどが、リアルタイムの環境制御を可能にします[13].
これらの制御戦略は小規模なシステムではうまく機能しますが、バイオリアクターのサイズが大きくなるにつれて、同じレベルの精度を維持することがますます複雑になります。
大規模バイオリアクターにおけるスケーリングの課題
バイオリアクターを研究室の設定から商業生産にスケールアップすることは、多くの課題をもたらします。大きな体積では、水素イオン濃度、二酸化炭素、溶存酸素の勾配が生じ、不均一な環境条件を引き起こす可能性があります[13][14]。これらの不一致は、均一な細胞成長が重要な培養肉にとって特に問題です。例えば、大規模なフィードバッチプロセスでは、溶存CO₂(dCO₂)レベルが75–225 mg/Lに達することがあり、溶存酸素は8.0 mg/L未満のままです[11]。このCO₂の蓄積は、pHレベルを6.8まで低下させる可能性があります[13]。
「プロセスパラメータの相互作用の理解は、プロセスのスケールアップ時に特に有用であり、pH、溶存酸素張力(pO₂)、二酸化炭素張力(pCO₂)の望ましくない変動が最も発生しやすい。」– Matthias Brunner et al. [13]
37°Cの一定温度を維持することも重要な要素であり、代謝熱の継続的な除去が必要です[1]。このバランスを達成するには、均一性を確保するための十分な攪拌が必要ですが、過度のインペラ速度は剪断に敏感な細胞を損傷する可能性があります[1]。これらの問題に商業規模で対処するためには、pHとpCO₂の制御を分離する必要があるかもしれません。例えば、CO₂ガスにのみ依存するのではなく、HClやNaOHを使用してpHを調整することで、CO₂の毒性を防ぎながら安定したpHレベルを維持することができます[13].
| バイオリアクターの種類 | 達成可能な細胞密度 (cells/mL) | 1 kgのバイオマスの作業量 |
|---|---|---|
| 撹拌タンク (STR) | 1.90 × 10⁵ – 2 × 10⁶ | 570 L |
| 充填床 (PBB) | 2.93 × 10⁶ | 110 L |
| 中空糸 (HFB) | 10⁸ – 10⁹ | 1.4 L |
機器の調達 Cellbase
培養肉生産の特定の要求を満たすバイオリアクターを見つけることは、困難な作業となることがあります。
一般的なラボ供給プラットフォームとは異なり、
結論
培養肉の生産において、正確なpHと温度の制御を維持することは非常に重要です。これらの要因は、細胞の生存率と成長の一貫性に直接影響を与えます。最適範囲からわずか0.3 pH単位の逸脱でも、細胞増殖を著しく妨げる可能性があります[3]。同様に、安定した温度は、細胞成長を支える代謝バランスを維持するために不可欠です。オックスフォード大学のジョアンナ・ミヒルはこの感受性を強調し、次のように述べています:
"生物学的プロセスは酸塩基化学に非常に敏感です" [2]
この精度は商業規模ではさらに困難になり、大量の体積でホメオスタシスを維持することは、重要なエンジニアリングの課題を引き起こします。
手動の実験室方法から自動化されたバイオプロセスへの移行は、培養肉の生産を経済的に持続可能で再現可能にするための重要なマイルストーンです。自動化は手動監視に伴う不一致を排除します。先進的なバイオリアクターシステム - 撹拌タンクから中空繊維のセットアップまで - は、施設の物理的なフットプリントとメディア効率に影響を与えながら、さまざまな細胞密度の能力を提供します。
しかし、スケールアップには独自の複雑さがあります。大規模なバイオリアクターは、しばしば10〜12 m³の範囲で、pHの不一致が特に起こりやすいです。例えば、塩基添加時に局所的なpHスパイクが9.0に達することがあり、強力な制御メカニズムの必要性を強調しています。紅海研究センターのShannon G. Kleinは、安定した条件を維持することの重要性を強調しています:
"細胞培養における関連する生理学的条件を維持することは、発表された研究結果の再現性を確保し、実験データの臨床応用への翻訳的関連性を保証するために極めて重要です" [3]
これらの課題に取り組むためには、専門的な機器と高度な監視システムが不可欠です。
現在、6大陸で175社以上が培養肉産業に参入し、投資額は24億ポンドを超えています[15]。商業的成功のためには、最適なpHと温度条件の維持が重要です。バイオリアクターの設計、オートメーション、専門的な調達における革新が、研究室から大規模生産施設への移行を可能にしています。これらの進歩は培養肉の未来を形作り、業界が最も差し迫った課題を克服するのを助けています。
よくある質問
培養肉の生産中にpHと温度を制御することが重要なのはなぜですか?
培養肉を生産する際には、pHと温度を正確に制御することが非常に重要です。哺乳類の細胞は、わずかな環境の変化にも非常に敏感です。このプロセスで使用されるほとんどの細胞株は、約37°Cの最適な温度で繁栄します。しかし、38°Cを超える温度や低すぎる温度などのわずかな変動でも、細胞の生存率に大きな影響を与え、成長を遅らせたり、代謝機能を妨げたりする可能性があります。同様に、pHを7.0から7.4の範囲内で安定させることも同様に重要です。CO₂や乳酸のような代謝副産物によって引き起こされるこの範囲の変動は、細胞の成長を害し、組織の品質を損なう可能性があります。
大規模なバイオリアクターでは、システム全体で均一なpHと温度を維持することがさらに重要になります。バイオリアクター全体で一貫した調整を行うことで、予測可能な細胞の発展を確保し、最終製品の成長、分化、質感をサポートします。また、生産中の高価な試行錯誤の調整を最小限に抑えるのにも役立ちます。培養肉産業の研究者や製造業者にとって、
自動化されたバイオリアクターは、手動システムと比較してどのように細胞成長を促進しますか?
自動化されたバイオリアクターは、温度、pH、溶存酸素などの重要なパラメータを管理するための新たな精度をもたらし、細胞成長に理想的な条件を確保します。例えば、これらのシステムは通常、温度を37°C前後、pHレベルを7.0から7.4の間に維持します。高度なセンサーを備えたこれらは、これらの変数を継続的に監視し、迅速に調整を行います。加熱、冷却、ガス流量の調整、酸と塩基のバランス調整などです。このほぼ瞬時の反応により、手動介入でよく見られる遅延や不正確さが排除されます。その結果、細胞ストレスを最小限に抑え、代謝効率を高め、成長率と細胞密度を向上させる安定した環境が実現します。
さらに、現代のバイオリアクターはクラウドベースの分析を利用して、パフォーマンスを追跡し、給餌スケジュールを最適化し、異なる生産ランにわたってプロセスを微調整します。培養肉の文脈では、これらの革新により、より高い細胞収量、組織発達の加速、そして生産費用の削減が実現します。この分野の方々にとって、
培養肉生産のためのバイオリアクターのスケールアップにおける主な課題は何ですか?
培養肉を生産するためのバイオリアクターのスケールアップは容易ではありません。これらのリアクターのサイズが大きくなるにつれて、pH、温度、溶存ガスなどの要因を厳密に制御することがますます困難になります。これらの変動は、細胞の不均一な成長や最終製品の一貫性の欠如を引き起こす可能性があります。一般的な障害には、非効率的な混合、限られた酸素移動、センサーの応答の遅れが含まれ、これらはすべて最適な細胞培養に必要な微妙なバランスを乱す可能性があります。
もう一つの複雑さの層は、接着性細胞株の使用から来ています。これらの細胞は繁栄するために大きな表面積または特殊なマイクロキャリアシステムを必要とします。システムがスケールアップするにつれて、これらの細胞を適切にサポートし、損傷を引き起こす可能性のある機械的ストレスを与えないようにすることが重要です。その上、産業規模のバイオリアクターは、均一な温度分布を確保し、無菌状態を維持し、厳しい食品安全基準を遵守しながら、コストを管理可能に保つ必要があります。
これらの課題に取り組むために、











