- Propósito: Garante que os biorreatores atendam aos padrões regulatórios e de produção, mantendo a esterilidade, controle ambiental preciso, e segurança alimentar.
- Características Principais: Biorreatores de tanque agitado foram escolhidos por sua adequação para células musculares bovinas, oferecendo forças de cisalhamento controladas e escalabilidade.
- Desafios: Escalar biorreatores para altas densidades celulares e reduzir custos exigiu repensar materiais, métodos de esterilização e design de processos.
- Soluções: Trocar para materiais de grau alimentício, usar métodos de esterilização econômicos e integrar software de controle de bioprocessos para otimização de processos reduziu significativamente os custos.
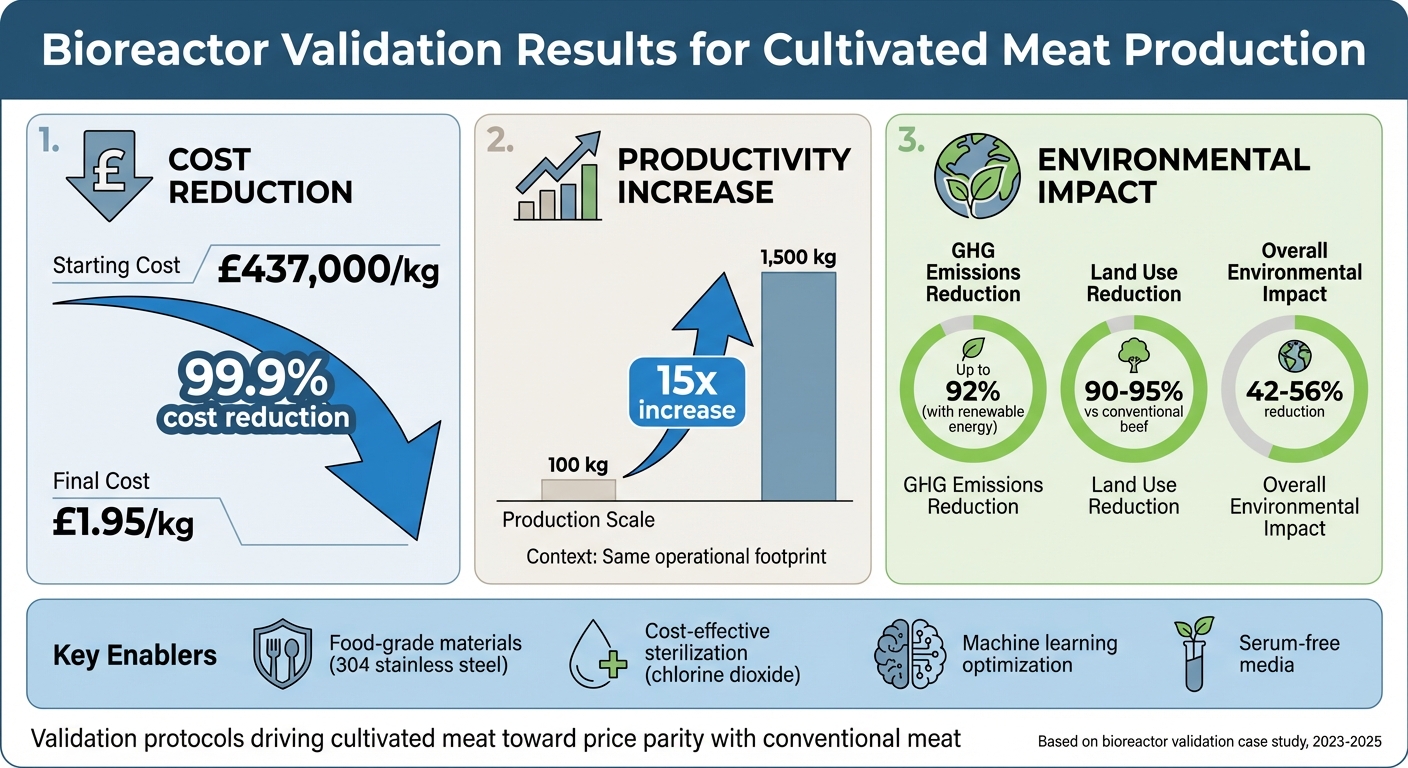
- Resultados: Os custos de produção caíram drasticamente, com um aumento de 15 vezes na produtividade e até 92% de redução nas emissões de gases de efeito estufa quando alimentados por energia renovável.
Este estudo descreve como protocolos de validação e escolhas de design inteligentes estão aproximando a carne cultivada da paridade de preço com a carne convencional.
Impacto da Validação de Biorreatores: Redução de Custos e Benefícios Ambientais na Produção de Carne Cultivada
Requisitos Regulatórios para Validação de Biorreatores
Padrões Regulatórios Aplicáveis
No setor de carne cultivada, atender a padrões regulatórios rigorosos é uma parte crítica do processo de validação de biorreatores. No Reino Unido, a Food Standards Agency (FSA) e a Food Standards Scotland (FSS) categorizam a carne cultivada como "produtos de origem animal" (POAO). Esta classificação garante que as regulamentações de segurança alimentar e higiene se apliquem em todas as etapas de produção, incluindo as operações de biorreatores.No entanto, de acordo com a orientação do Reino Unido (dezembro de 2025), embora esses produtos se enquadrem na categoria POAO, eles não se qualificam legalmente como "carne". Essa distinção significa que certos requisitos convencionais de bem-estar animal e microbiológicos são excluídos, moldando os protocolos específicos de validação necessários no Reino Unido.
Globalmente, as avaliações de segurança variam em duração. Singapura e os Estados Unidos normalmente concluem as revisões em 12 meses, enquanto a União Europeia tem uma média de cerca de 18 meses. O Reino Unido traçou seu próprio caminho com o Programa Sandbox CCP, financiado até fevereiro de 2027. Esta iniciativa permite que os reguladores colaborem diretamente com empresas como Gourmey, Hoxton Farms, e Mosa Meat, simplificando os requisitos de dados e acelerando as avaliações de segurança.
"O programa sandbox está nos permitindo acelerar o conhecimento regulatório para reduzir barreiras para tecnologias alimentares emergentes sem comprometer os padrões de segurança."
– Dr. Thomas Vincent, Diretor Adjunto de Inovação, FSA [3]
Independentemente da jurisdição, as empresas devem enviar dossiês de segurança detalhados antes de entrar no mercado. Esses dossiês descrevem os processos de produção, a composição do produto e os dados de segurança. Eles também devem confirmar que a carne cultivada é nutricionalmente comparável à carne convencional, incluindo análises de macro e micronutrientes, bem como perfis de aminoácidos e ácidos graxos.
Requisitos do Protocolo de Validação
Os padrões regulatórios exigem protocolos rigorosos de validação de biorreatores para garantir operações seguras e controladas. Um componente chave é a implementação de um plano de Análise de Perigos e Pontos Críticos de Controle (HACCP).Este framework identifica e mitiga riscos em cada estágio da produção, desde a biópsia inicial da célula até a colheita final da massa celular. Dada a novidade da produção de carne cultivada, as avaliações de segurança devem abordar potenciais perigos ao longo do processo.
Os protocolos de validação devem provar que os sistemas de biorreatores mantêm condições estéreis durante os ciclos de produção, prevenindo efetivamente a contaminação microbiana. Além disso, esses protocolos precisam avaliar se as proteínas na carne cultivada poderiam desencadear reações alérgicas nos consumidores.
"Nossa nova orientação fornece clareza para as empresas, ajudando-as a entender e demonstrar corretamente aos reguladores de alimentos do Reino Unido como seus produtos são seguros. Especificamente, esta orientação garante que as empresas tenham avaliado os riscos alérgicos potenciais e que são nutricionalmente apropriados antes de serem autorizados para venda."
– Dr.Thomas Vincent, Diretor Adjunto de Inovação, FSA [2]
No Reino Unido, a validação se concentra em fornecer dados suficientes para uma avaliação de risco científica, em vez de conceder autorização de mercado. Nicolas Morin-Forest, Co-fundador & CEO da GOURMEY, destacou essa distinção:
"A validação da Grã-Bretanha marca um passo crítico em nossa jornada regulatória de novos alimentos e confirma que agora estamos progredindo para uma avaliação completa de risco, nos aproximando de disponibilizar nossos produtos aos consumidores." [4]
sbb-itb-ffee270
Seleção de Biorreator e Especificações do Sistema
Tecnologia de Biorreator Selecionada
A instalação optou por um biorreator de tanque agitado, uma escolha impulsionada por seu desempenho confiável com células progenitoras de músculo bovino. Fatores-chave que influenciaram essa decisão incluíram as necessidades específicas das células, a escala de produção desejada e considerações gerais de custo.
Células musculares bovinas, sendo dependentes de ancoragem, requerem forças de cisalhamento baixas - abaixo de 0,1 N/m² - para evitar danos durante o cultivo. O design de tanque agitado atendeu a esse requisito, além de se mostrar adaptável tanto para experimentos em escala piloto quanto para produção comercial. O custo foi outro fator importante, com unidades em escala piloto posicionadas como mais acessíveis para orçamentos típicos no setor de carne cultivada do que na indústria farmacêutica[5][7].
A escala de produção visava volumes entre 100 e 1.000 litros para garantir a viabilidade comercial. Sistemas modulares de tanque agitado foram escolhidos em vez de alternativas de leito empacotado devido à sua capacidade de aumentar a escala em um fator de 10 sem ultrapassar os limites de transferência de massa, mantendo valores de kLa acima de 50 h⁻¹.Esses sistemas visam produzir 1–10 kg de carne cultivada por lote enquanto equilibram o investimento de capital para capacidade escalável [7][8].
Recursos de Design do Sistema
Uma vez selecionado o biorreator de tanque agitado, seu design incorporou recursos avançados para promover o crescimento celular ideal. O sistema de troca de gás emprega tecnologia de micro-sparger, entregando bolhas entre 20–100 µm. Esta configuração atinge valores de kLa de 100–200 h⁻¹ a 37°C, mantendo níveis de oxigênio dissolvido em 30–50% de saturação. Para gerenciar a remoção de CO₂, a aeração do espaço de cabeça é combinada com contatores de membrana e sensores antiespuma[5][6].
Para mistura eficiente, o biorreator usa impulsores duplos Rushton, operando em velocidades de 50–150 rpm.Isso garante uma mistura uniforme com taxas de cisalhamento abaixo de 5.000 s⁻¹, protegendo as células de danos enquanto mantém gradientes de nutrientes abaixo de 10%. A agitação é controlada por PID, com feedback em tempo real sobre os níveis de pH e oxigênio dissolvido, suportando taxas de perfusão de 1–5 volumes de vaso por dia[5][7].
A escalabilidade foi um foco principal do design. O biorreator mantém semelhança geométrica em diferentes escalas, aderindo a uma proporção altura-diâmetro de 2:1. Impulsores otimizados por CFD garantem uma ampliação linear, e testes piloto mostraram uma retenção de 95% na viabilidade celular ao escalar de 10 litros para 200 litros. O design modular permite a integração em sistemas de produção maiores enquanto atende aos padrões de conformidade GxP [7][8].
Tecnologia analítica de processos também está integrada, apresentando espectroscopia Raman para monitoramento em tempo real de parâmetros críticos como pH (6,8–7,2) e lactato (mantido abaixo de 2 g/L). Modelos preditivos, adaptados da produção de anticorpos monoclonais, monitoram os níveis de glicose com valores de R² acima de 0,95, garantindo controle preciso do processo[5] [6][7].
Essas características não apenas melhoram o cultivo celular, mas também atendem aos rigorosos padrões de validação exigidos pelos órgãos reguladores do Reino Unido.
Execução do Protocolo de Validação
Procedimentos de Validação Principais
Para garantir a integridade operacional, um protocolo de validação completo foi realizado, incorporando recursos de design avançados. O monitoramento em tempo real desempenhou um papel fundamental, com tecnologia analítica de processos (PAT) sensores rastreando continuamente parâmetros críticos como oxigênio dissolvido, pH e níveis de CO₂ durante cada execução de cultivo[6] . O processo começou com células semeadas a uma densidade de 1×10⁵ células/mL, cultivadas por uma semana em um meio contendo 3 g/L de glicose. A espectroscopia Raman foi empregada para monitorar os níveis de lactato e glicose ao longo do tempo[5].
A análise de estresse de cisalhamento confirmou que as forças de agitação permaneceram abaixo de 0,1 Pa, que é o limite crítico para células musculares bovinas. O teste pós-estresse demonstrou que a viabilidade celular permaneceu acima de 90%[6].
O teste de esterilidade foi estendido a todas as matérias-primas, com atenção especial ao meio de crescimento. Os fornecedores foram obrigados a fornecer certificados de análise, verificados por meio de testes de terceiros, em conformidade com os padrões das instalações do Reino Unido.O protocolo incluiu imunoensaios ELISA para detectar endotoxinas de bactérias gram-negativas, juntamente com citometria de fluxo para identificar contaminantes com base no tamanho, forma e propriedades de fluorescência das células[9] .
Métodos de Otimização de Processos
Uma vez confirmada a estabilidade do sistema, os esforços se concentraram em refinar o processo usando análises avançadas. Algoritmos de aprendizado de máquina ajustaram dinamicamente as taxas de fluxo de mídia e velocidades de agitação com base em dados contínuos de PAT. Esses modelos, treinados em conjuntos de dados de design de experimentos (DoE), identificaram estratégias de alimentação econômicas correlacionando medições de permissividade com a qualidade da biomassa[6] . Essa abordagem foi particularmente eficaz durante a fase de proliferação, onde taxas de crescimento consistentes são cruciais para a produção comercial.
A espectroscopia Raman, inicialmente desenvolvida para a produção de anticorpos monoclonais, foi adaptada com sucesso para aplicações em carne cultivada. Sua especificidade de analito permitiu que a instalação adotasse protocolos de validação estabelecidos, mantendo a precisão necessária para o monitoramento em tempo real ao longo do ciclo de cultivo[5].
Desafios Técnicos e Soluções
Questões de Escalonamento e Produtividade
Escalonar biorreatores de ambientes de laboratório para produção comercial não foi uma tarefa fácil. A instalação tinha como objetivo produzir 10–100 kg de carne cultivada, exigindo um enorme número de 10¹²–10¹³ células para atingir essa meta [11]. No entanto, alcançar altas densidades celulares provou ser um obstáculo significativo.Embora os biorreatores de fibra oca possam teoricamente alcançar densidades de 10⁸ a 10⁹ células/mL [13], os designs convencionais de biorreatores não atenderam à produção de carne cultivada.
Matt McNulty, um Pesquisador do GFI, explicou a raiz do problema: "Os biorreatores usados na carne cultivada ainda são amplamente adaptados de designs convencionais de alimentos e farmacêuticos. Esses designs não são especificamente adaptados às necessidades de produção de carne cultivada e, portanto, geram custos mais altos devido a ineficiências nessa falta de adequação" [12]. Essa incompatibilidade entre design e propósito exigiu uma reavaliação completa dos equipamentos e processos.
Soluções Implementadas e Dados de Desempenho
Para enfrentar esses desafios, a instalação reformulou seus equipamentos e protocolos para se alinhar mais de perto com as demandas específicas da produção de carne cultivada.Uma das principais mudanças envolveu a transição de padrões de grau farmacêutico para padrões de grau alimentício. Por exemplo, a equipe substituiu os vasos de aço inoxidável 316 por alternativas de aço inoxidável 304, que atendiam aos requisitos de segurança alimentar enquanto reduziam significativamente os custos de capital [12]. Além disso, o processo tradicional de esterilização no local a vapor foi substituído pelo tratamento com gás dióxido de cloro. Este ajuste permitiu o uso de vasos de paredes mais finas feitos de materiais alternativos, reduzindo ainda mais os custos [12].
Outra medida de economia de custos envolveu a troca de água de grau farmacêutico para água de grau alimentício classificada como "Geralmente Reconhecida como Segura" (GRAS) para preparação de meios [12]. A equipe também introduziu microcarregadores e suportes comestíveis, que não apenas resolveram problemas de desprendimento celular, mas também cumpriram com os regulamentos de segurança alimentar [11].
Para otimizar ainda mais as operações, a instalação implementou sistemas de sensores multiplexados. Esses sensores forneceram dados de desempenho em tempo real, que poderiam ser utilizados em aplicações de aprendizado de máquina para ajustar processos [12]. Coletivamente, essas mudanças tiveram um impacto dramático nos custos de produção, reduzindo-os substancialmente [10]. Essa notável redução de custos destaca como alinhar protocolos de produção com padrões regulatórios pode alcançar escalabilidade comercial sem sacrificar segurança ou qualidade.
Resultados de Validação e Impacto na Indústria
Resultados de Desempenho Medidos
Através de testes rigorosos, o sistema demonstrou um impressionante salto na produtividade. Usando tecnologia de biorreator contínuo sem bolhas, a produtividade do crescimento celular aumentou 15 vezes, impulsionando a produção de 100 kg para 1.500 kg - tudo dentro do mesmo espaço operacional[16]. Durante a fase de diferenciação, ajustes para otimizar a biomassa celular levaram a um aumento de 128%, o que reduziu significativamente o impacto ambiental geral em 42–56%. A transição do metabolismo de células C2C12 para CHO também desempenhou um grande papel na redução dos impactos ambientais, alcançando reduções de até 67% quando alimentado por fontes de energia renováveis[14]. Ainda mais impressionante, o uso de energia renovável reduziu as emissões de gases de efeito estufa em até 92% e reduziu o uso de terra em 90–95% em comparação com os métodos tradicionais de produção de carne bovina [15] [16]. Esses resultados abrem caminho para uma adoção mais ampla em toda a indústria.
Contribuições para Práticas da Indústria
Os resultados de validação redefiniram os padrões para design de biorreatores e conformidade regulatória na produção de carne cultivada. Ao mostrar que padrões de qualidade alimentar podem substituir efetivamente os farmacêuticos sem comprometer a segurança, o processo introduziu um roteiro de economia de custos para a indústria. Por exemplo, a troca do aço inoxidável 316 para o 304, combinada com a esterilização por dióxido de cloro e o uso de água classificada como GRAS, reduziu significativamente os custos de capital enquanto mantinha a conformidade.
Além de provar a viabilidade técnica, esses avanços estão mudando os padrões da indústria. Modelos econômicos sugerem que processamento contínuo vs fed-batch poderia proporcionar economias de 55% nos custos de capital e operacionais ao longo de uma década [1]. Para equipes de compras, plataformas como
Conclusão
Principais Descobertas
Esta análise destaca como a produção de carne cultivada pode avançar em direção ao sucesso comercial fazendo escolhas inteligentes de equipamentos e refinando protocolos operacionais. Optar por materiais de grau alimentício como aço inoxidável 304 em vez do mais caro aço inoxidável 316 garante segurança e conformidade enquanto reduz custos. A mudança para meios sem soro, como validado pela Agência de Alimentos de Cingapura's aprovação das formulações da GOOD Meat no início de 2023, elimina os desafios éticos e financeiros ligados a insumos derivados de animais[15].
O aumento da produção com reatores de elevação, particularmente em 260.000 L, mostrou um forte potencial para reduzir custos em comparação com reatores de tanque agitado menores de 42.000 L[17]. No entanto, alcançar altas densidades celulares - até 2 × 10⁸ células/mL - requer sistemas de perfusão avançados para lidar com resíduos metabólicos como amônia e lactato. A otimização de processos provou ser essencial para enfrentar esses desafios[11]. Para equipes de compras, plataformas como
Desenvolvimentos Futuros
Com a eficiência de custos e o controle de processos validados, o foco agora se desloca para biorreatores em mega-escala, que prometem redefinir a economia de produção.O anúncio da GOOD Meat em maio de 2022 sobre uma instalação com dez biorreatores de 250.000 L - capazes de produzir 13.700 toneladas métricas de frango e carne cultivados anualmente - marca um movimento significativo dos projetos piloto para a produção em escala industrial[11][15]. Isso está alinhado com o parâmetro econômico estabelecido por Patrick G. Negulescu et al. da Universidade da Califórnia, Davis:
"Para ser diretamente competitivo com a carne bovina, os produtos CM, ou pelo menos o custo de produção, devem cair para um nível comercialmente competitivo"[17]
As projeções indicam que esse objetivo está ao alcance, especialmente à medida que os custos de mídia continuam a diminuir ainda mais.
Inovações como microcarregadores comestíveis e sistemas híbridos, que combinam expansão e diferenciação celular em um único recipiente, devem simplificar os processos de validação e reduzir os riscos de contaminação. Os protocolos descritos neste estudo de caso oferecem um modelo replicável para empresas que estão ampliando suas operações, provando que testes rigorosos podem coexistir com a redução de custos. À medida que mais instalações adotam esses métodos validados, a indústria de carne cultivada se aproxima da paridade de preços com a carne tradicional. Juntamente com isso, o setor oferece benefícios ambientais notáveis, incluindo até 92% de redução nas emissões de gases de efeito estufa quando alimentado por fontes de energia renováveis[15].
Recapitulação de biorreatores: sensores, modelagem, ampliação e design alternativo de reatores
Perguntas Frequentes
Que evidências os reguladores esperam em um dossiê de validação de biorreator para carne cultivada?
Os órgãos reguladores exigem dossiês de validação de biorreatores para confirmar que os sistemas funcionam dentro de parâmetros definidos. Isso envolve garantir desempenho consistente do processo e monitoramento em tempo real de fatores chave como níveis de pH, oxigênio dissolvido, e temperatura. Além disso, o teste de esterilidade desempenha um papel crucial na prevenção de contaminação. A adesão a normas como ISO 14644-1 e EU GMP Anexo 1 é obrigatória para manter o controle microbiano e sustentar práticas de fabricação estéreis.
Como um biorreator de tanque agitado pode ser ampliado sem prejudicar as células musculares bovinas?
Ampliar um biorreator de tanque agitado para a produção de carne cultivada envolve o gerenciamento de tensão de cisalhamento , que pode prejudicar as células musculares bovinas. Para enfrentar isso, ferramentas como dinâmica de fluidos computacional (CFD) e modelos de escala reduzida são usadas para prever padrões de fluxo. Esses insights orientam ajustes no design do impulsor e nas velocidades de agitação, ajudando a reduzir danos às células.
Igualmente importante é garantir a distribuição uniforme de nutrientes e oxigênio. Sistemas de monitoramento avançados, combinados com técnicas de mistura eficazes, são fundamentais para criar condições consistentes. Essa abordagem ajuda a minimizar o estresse localizado e apoia a saúde celular durante a produção em larga escala.
Quais mudanças de validação de redução de custos têm o maior impacto na economia unitária?
A adoção de biorreatores de uso único tem um efeito perceptível na redução de custos medidos em £/kg. Embora esses sistemas reduzam os investimentos iniciais de capital e despesas com mão de obra, eles vêm com custos mais altos de consumíveis. Além disso, a introdução de monitoramento em tempo real e tecnologias de reciclagem de meios aumenta a eficiência operacional. Esses avanços não apenas simplificam os processos, mas também levam a economias de custos a longo prazo.











