Kryopreservering är processen att frysa och lagra levande celler vid ultralåga temperaturer för att bevara deras livskraft över tid. Denna metod är avgörande för produktion av odlat kött, vilket säkerställer konsekventa, stabila cellinjer och skyddar mot förluster från kontaminering eller utrustningsfel. Viktiga steg inkluderar:
- Förberedelse: Skörda celler under deras tillväxtfas, kontrollera livskraft (sikta på ≥90%) och förbered dem i frysningsmedium med kryoskyddsmedel som DMSO eller glycerol.
- Nedfrysning: Använd en kontrollerad kylhastighet (-1°C till -3°C per minut) för att förhindra skador från iskristaller. Förvara celler i flytande kväveånga (-135°C till -190°C) för långtidsbevaring.
- Upptining: Tina snabbt celler i ett 37°C vattenbad för att minimera kryoskyddsmedelstoxicitet, överför dem sedan till tillväxtmedium för återhämtning.
- Kvalitetskontroll: Märk flaskor noggrant, övervaka lagringsförhållanden och testa livskraften efter upptining för att säkerställa framgångsrik bevarande.
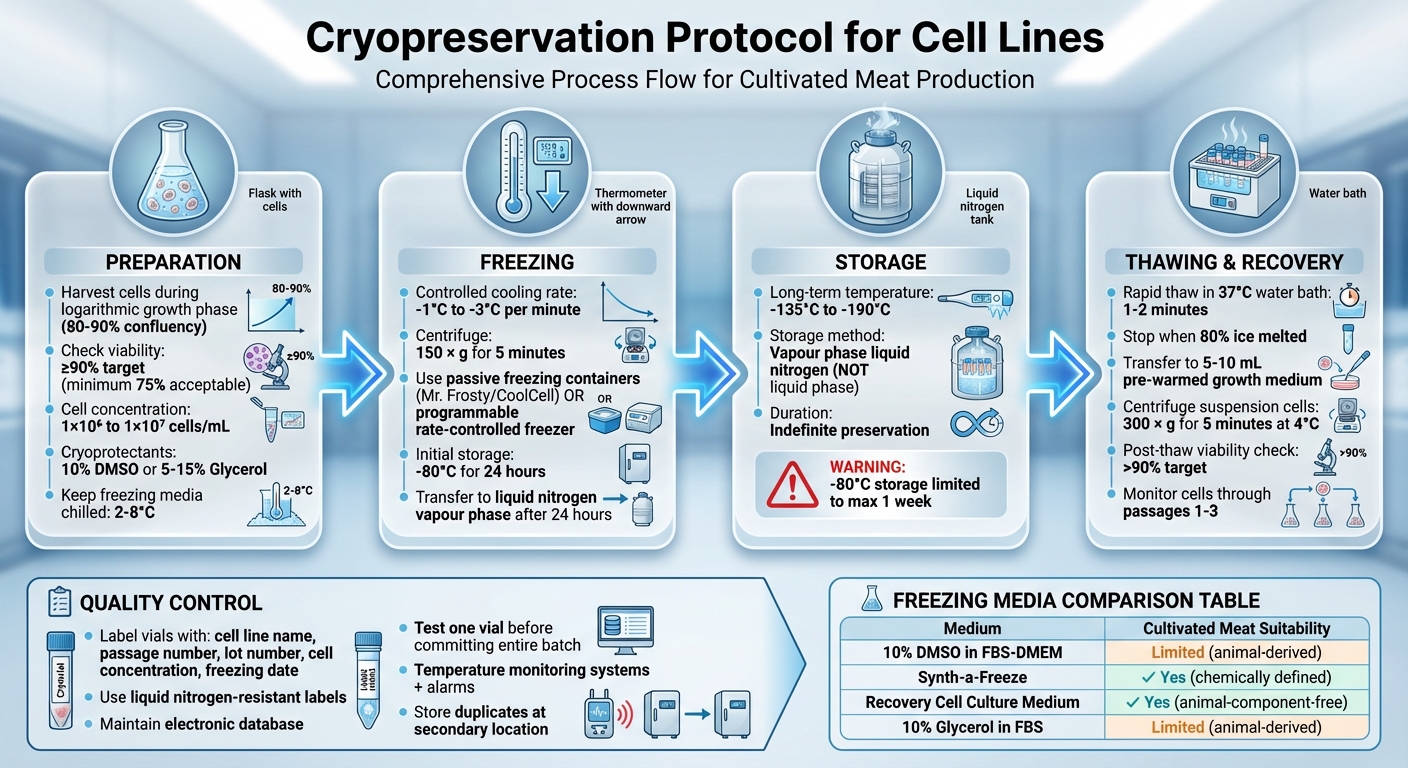
Fullständigt Kryopreserveringsprotokoll för Cellinjer: 4-stegsprocess från Förberedelse till Lagring
Förbereda Celler för Kryopreservering
Cellskörd och Livskraftskontroller
För att säkerställa bästa återhämtning efter upptining, skörda celler under deras logaritmiska (log) tillväxtfas. För adherenta cellinjer är detta vanligtvis när de når 80–90% konfluens [2][3][6].
Kontrollera cellernas livskraft med Trypan Blue-exklusionsmetoden. Blanda lika delar (1:1) av 0,4% Trypan Blue med cellsuspensionen, räkna sedan cellerna med en hemocytometer.Viabla celler kommer att utesluta färgen och framstå som ljusa under mikroskopet, medan icke-viabla celler kommer att färgas blå [4]. Sträva efter en livskraft på minst 90% för bästa återhämtningsgrad, även om vissa protokoll kan acceptera ett minimum på 75% [1][2][3][5].
Innan skörd, använd ett mikroskop för att kontrollera bakteriell eller svampkontaminering. Friska suspensionsceller bör framstå som ljusa, runda och refraktiva under ett inverterat faskontrastmikroskop [2][3].
När cellerna uppfyller de nödvändiga livskraftstandarderna, gå vidare till förfrysningsstegen.
Förberedelser före frysning
För adherenta celler, använd skonsamma dissociationsmetoder, såsom trypsin eller TrypLE Express, och begränsa inkubationstiden för att undvika att skada cellmembranen [5]. Förbered cellerna vid en koncentration av 1 × 10⁶ till 1 × 10⁷ celler/mL, beroende på cellinjen [1][6]. Vid aliquotering, se till att cellsuspensionen blandas ofta för att bibehålla en jämn fördelning över kryorören [5].
Håll frysningsmediet kylt mellan 2°C och 8°C under resuspensionen för att minska kryoskyddsmedlets toxicitet innan frysningsprocessen börjar [5]. När cellerna är suspenderade i frysningsmediet, gå snabbt vidare till frysningsprotokollet [1]. Alltid kryokonservera celler vid det lägsta möjliga passagenumret för att minska risken för genetisk drift eller morfologiska förändringar [5][7].
Val av kryoskyddsmedel och frysningsmedia
Kryoskyddsmedelsalternativ och deras funktioner
Dimetylsulfoxid (DMSO) används ofta som ett kryoskyddsmedel, vanligtvis vid en koncentration av 10% [2]. Det fungerar genom att tränga in i cellmembran och minska isbildning under frysning. Dock kan DMSO vara giftigt för celler vid rumstemperatur, så snabb upptining är nödvändig för att minimera exponering och snabbt späda ut det [1].
Glycerol fungerar som ett användbart alternativ för cellinjer känsliga för DMSO, vanligtvis används i koncentrationer från 5% till 15% [8].Det är särskilt effektivt för celltyper där DMSO kan orsaka oönskad differentiering [3], och det tenderar att ha lägre toxicitet jämfört med DMSO.
Inom odlat kött-applikationer använder traditionella frysningsprotokoll ofta en blandning av 90% Fetal Bovine Serum (FBS) och 10% DMSO [1]. Dock begränsar beroendet av djurhärledda komponenter dessa metoder när det gäller skalbarhet och regulatoriskt godkännande [9]. För att hantera dessa problem, kemiskt definierade medier - som Synth-a-Freeze eller Recovery Cell Culture Medium - erbjuder ett alternativ utan djurkomponenter. Dessa medier bibehåller hög cellviabilitet efter upptining samtidigt som de övervinner utmaningarna med komponenter av animaliskt ursprung [9].
Jämförelse av frysningsmedier
Här är en översikt över fördelarna och begränsningarna med olika frysningsmedier som används i odlad köttproduktion:
| Medium | Fördelar | Nackdelar | Lämplighet för odlat kött |
|---|---|---|---|
| 10% DMSO i FBS-DMEM | Etablerade protokoll [1] | Innehåller komponenter från djur; batchvariabilitet [9] | Begränsad skalbarhet |
| Synth-a-Freeze | Kemiskt definierad; konsekvent kvalitet; fri från djurkomponenter [9] | Högre initial kostnad [9] | Ja |
| Recovery Cell Culture Medium | Lätt att använda; designad för snabb återhämtning [9] | Kan behöva optimeras för specifika cellinjer | Ja |
| 10% Glycerol i FBS | Alternativ för DMSO-känsliga celler [1] | Beroende av serum med animaliskt ursprung [9] | Begränsad skalbarhet |
I februari 2023 visade forskare vid Tokyo Women's Medical University, ledda av Hironobu Takahashi, vikten av att välja rätt frysningsmedium. Using commercial options like CELLBANKER 1 and 2, they successfully cryopreserved primary bovine myogenic cells at –80°C for up to a year. Remarkably, these cells retained their ability to proliferate and differentiate into contractile muscle tissue with intact sarcomere structures after thawing [10] .
För produktion av odlat kött föredras alltmer kemiskt definierade och GMP-kompatibla medier. Som STEMCELL Technologies betonar:
Inom starkt reglerade områden som cell- och genterapi rekommenderas det att använda ett GMP-tillverkat, fullt definierat kryokonserveringsmedium för att säkerställa att produkterna konsekvent produceras och kontrolleras enligt kvalitetsstandarder [9].
Plattformar som
Kryopreserveringsprocedur och kylhastigheter
Steg-för-steg frysningsprotokoll
Nyckeln till framgångsrik kryopreservering ligger i att upprätthålla en jämn kylhastighet på -1°C till -3°C per minut[2]. Denna gradvisa process tillåter vatten att lämna cellerna långsamt, vilket förhindrar bildandet av skadliga intracellulära iskristaller som kan spräcka cellmembran[1].
Börja med att centrifugera cellerna vid 150 x g i 5 minuter[3]. När centrifugeringen är klar, resuspendera cellpelleten i ett kallt frysningsmedium innehållande 10% DMSO vid en koncentration av 2–4×10⁶ celler/mL [3].För att minska exponeringen för DMSO, gå snabbt vidare till nästa steg - frysning.
Distribuera cellsuspensionen i förmärkta kryogena vialer. Varje vial bör tydligt ange viktiga detaljer som cellinje namn, passage nummer, lot nummer, cellkoncentration och datum för frysning[3]. Med vialerna förberedda är det dags att välja och använda lämplig kylutrustning.
Kylutrustning och tekniker
Placera vialerna omedelbart i en kontrollerad kylanordning. Passiva fryskontainrar, som Nalgene "Mr Frosty" (som använder isopropanol) eller Corning "CoolCell", är populära val. Dessa verktyg kan uppnå en kylhastighet på ungefär 1°C per minut när de placeras i en -80°C frys[2] .
För storskaliga operationer där konsekvens är avgörande är en programmerbar hastighetskontrollerad frys det bästa alternativet. Som Sigma-Aldrich anger:
ECACC använder rutinmässigt en programmerbar hastighetskontrollerad frys. Detta är det mest tillförlitliga och reproducerbara sättet att frysa celler[3].
Efter cirka 24 timmar vid -80°C, överför vialerna till ångfasen av flytande kväve, där temperaturerna varierar mellan -135°C och -190°C, för långtidsförvaring [4]. Undvik att lagra celler vid -80°C längre än en vecka, eftersom detta kan äventyra deras livskraft. Temperaturer under -135°C är nödvändiga för obegränsad bevarande[2]. Att använda ångfasen istället för den flytande fasen minskar risken för korskontaminering samtidigt som tillräckligt låga temperaturer bibehålls.
Upptinings- och återhämtningsprotokoll
Upptiningsprocess
Snabb upptining av celler är avgörande för att begränsa exponeringen för giftiga kryoskyddsmedel och förhindra att iskristaller orsakar skador. Se till att bära ett helt ansiktsskydd och isolerade handskar för säkerhet. Börja med att ta bort kryoröret från flytande kväve och lossa locket något för att släppa ut eventuell uppbyggd tryck. Dra sedan åt locket igen.
Placera röret i ett 37°C vattenbad och se till att locket håller sig ovanför vattenlinjen. Låt det tina i 1–2 minuter, eller tills endast några få iskristaller återstår. När det har tinat, torka av rörets utsida med 70% alkohol för att bibehålla sterilitet.
Överför innehållet i röret till ett rör som innehåller 5–10 mL förvärmd tillväxtmedium. Tillsätt mediet långsamt för att minska osmotisk chock. Om du arbetar med suspensionscellinjer, centrifugera cellupphängningen omedelbart vid 300 × g i 5 minuter vid 4°C.Detta steg hjälper till att pelletera cellerna och avlägsnar kryoskyddsmedlet. Efter centrifugering, resuspendera cellerna i färskt medium. För adherenta celler är centrifugering vanligtvis onödig. Istället, så cellerna direkt i ett lämpligt odlingskärl och avlägsna eventuellt kvarvarande DMSO vid det första mediebytet, vanligtvis efter 24 timmar.
Bedömningar efter upptining
Omedelbart efter upptining, kontrollera cellviabiliteten för att säkerställa att återhämtningen har varit framgångsrik. Använd Trypan Blue-exklusionsmetoden för denna bedömning. Idealiskt bör cellviabiliteten överstiga 90% [11], men ett minimum av 75% är acceptabelt. Efter 24 timmar, inspektera cellerna under ett faskontrastmikroskop för att bekräfta vidhäftning, utvärdera celldensitet och kontrollera tecken på kontaminering.
Fortsätt övervaka cellerna genom passager 1–3 för att säkerställa normal proliferation och att de behåller sina förväntade egenskaper.För cellinjer som återhämtar sig långsammare kan du förbättra överlevnaden genom att öka den initiala koncentrationen av fetalt bovint serum till cirka 20% v/v.
sbb-itb-ffee270
Lagring och långsiktig livskraft
Lagringsförhållanden och varaktighet
För att bibehålla cellinjers livskraft på lång sikt är det viktigt att lagra dem vid temperaturer under -135°C [7][2]. Detta säkerställer att de förblir bevarade på obestämd tid.
Den föredragna metoden för att lagra odlade köttcellinjer är ångfas flytande kväve. Denna teknik håller temperaturerna mellan -135°C och -190°C, vilket gör den idealisk för långsiktig bevaring samtidigt som den erbjuder ökad säkerhet jämfört med lagring i vätskefas.
Om du behöver lagra celler vid -80°C, begränsa detta till en period av 24 timmar till en vecka. Utöver detta kan cellernas livskraft minska.För tillfällig förvaring vid denna temperatur, överför cellerna till flytande kväveförvaring så snart som möjligt.
Använd standard sterila kryogena vialer (1–2 mL) med intern gänga och en O-ring för säker förvaring [4][5]. Placera alltid förseglade kryovialer i gasfasen snarare än i den flytande fasen av kväve för att minska risken för vialexplosioner under upptining [5]. Se dessutom till att behållare med flytande kväve hålls minst halvfulla för att upprätthålla en säkerhetsbuffert.
Slutligen är rigorösa kvalitetskontrollåtgärder avgörande för att säkerställa cellernas långsiktiga livskraft.
Kvalitetskontrollkontroller
För att säkerställa tillförlitligheten hos lagrade cellinjer, följ strikta protokoll för kvalitetskontroll. Börja med att noggrant märka varje vial med flytande kväveresistenta etiketter. Inkludera viktiga detaljer såsom cellinjeidentitet, lotnummer, passagenummer och frysningsdatum. Upprätthåll en elektronisk databas för att registrera den exakta platsen för varje vial, vilket minskar den tid lagringskärlen behöver förbli öppna [7][2].
Innan hela partier åläggs långtidslagring, testa en vials livskraft efter korttidslagring i gasfas. Detta steg hjälper till att bekräfta att frysningsprocessen var framgångsrik och identifierar eventuella problem [4][7][2]. För mycket värdefulla cellbestånd är det klokt att lagra dubbletter på en sekundär plats för att skydda mot utrustningsfel eller lokala katastrofer [7][2].
Utrusta alla förvaringskärl med temperaturövervakningssystem och larm för att upptäcka låga nivåer av flytande kväve [7]. Installera dessutom syrelarm i förvaringsområden, inställda att utlösas vid 18% syre (v/v), för att minimera kvävningsrisker för personal som arbetar med flytande kväve [7][2].
Cryopreservation of mammalian cell lines video protocol
Slutsats och viktiga insikter
Här är en snabb sammanfattning av de väsentliga stegen och rekommendationerna för effektiv kryokonservering i odlad köttproduktion:
- Cellskörd: Samla in celler under deras logaritmiska tillväxtfas, säkerställ att livskraften överstiger 90%. Använd 10% DMSO som kryoskyddsmedel, även om glycerol kan vara ett alternativ för mer känsliga cellinjer [11][1].
- Kylning och Förvaring: Upprätthåll en kontrollerad kylhastighet och överför snabbt vialer till ångfas flytande kväveförvaring för att skydda cellernas integritet [11]
En studie av Roka Kakehi et al. belyser vikten av precision vid kryokonservering [10]:
"Att säkerställa en pålitlig och konsekvent källa av celler genom att använda kryokonservering kommer att tillåta oss att öka den stabila tillgången på lovande celler för odlad köttproduktion." - Roka Kakehi et al., Tokyo Women's Medical University
- Upptiningsprocess: Tina celler i ett 37°C vattenbad i cirka två minuter, och stoppa när 80% av isen har smält. Detta minskar DMSO-toxicitet och förbättrar cellåterhämtning [1]. Följ upp med livskraftskontroller efter upptining för att säkerställa framgång och finjustera framtida procedurer.
Dessa metoder fungerar hand i hand med strikta kvalitetskontrollrutiner. Märk alltid flaskor noggrant, håll organiserade register och genomför noggranna kontroller innan långtidslagring [11]. För specialiserade kryopreserveringsbehov, plattformar som
Vanliga frågor
Vilka är fördelarna med att använda kemiskt definierade medier för kryopreservering av cellinjer i odlad köttproduktion?
Kemiskt definierade medier ger flera fördelar när det gäller kryopreservering av cellinjer för odlad köttproduktion. Genom att ta bort odefinierade komponenter, som serum från djur, säkerställer de konsekventa och förutsägbara resultat - en avgörande faktor för att bibehålla cellinjernas långsiktiga tillförlitlighet.
En annan viktig fördel är den minskade risken för kontaminering och variation. Detta stöder inte bara högre kvalitets- och säkerhetsstandarder utan stämmer också perfekt överens med den precision och skalbarhet som krävs för att möta både regulatoriska krav och konsumentförväntningar inom den odlade köttindustrin.
Hur påverkar valet av kryoskyddsmedel cellöverlevnad under frysning och upptining?
Valet av kryoskyddsmedel är en nyckelfaktor för att bevara cellhälsan under frysning och upptining. Två allmänt använda alternativ är dimetylsulfoxid (DMSO) och glycerol, var och en med distinkta egenskaper. DMSO är känt för sin förmåga att snabbt tränga in i celler och ge starkt skydd. Dock kommer det med en varning: vid höga koncentrationer eller med långvarig exponering kan det bli toxiskt, vilket potentiellt kan sänka cellens livskraft.
Glycerol, däremot, är mindre toxiskt och kan appliceras direkt.Dess nackdel ligger i dess långsammare hastighet av cellpenetration, vilket kan resultera i mindre omedelbart skydd jämfört med DMSO.
Att uppnå rätt balans är avgörande. Att korrekt justera koncentrationen och exponeringstiden för kryoskyddsmedlet hjälper till att skydda celler samtidigt som risken för toxicitet minimeras. Dessutom är det viktigt att följa bästa praxis för kylhastigheter och lagringsförhållanden för att säkerställa högsta möjliga återhämtningsgrad efter upptining.
Varför är det viktigt att kontrollera kylhastigheten under kryopreservering?
Att upprätthålla en jämn kylhastighet, vanligtvis mellan –1°C och –3°C per minut, är nyckeln till att hålla cellerna livskraftiga. Att kyla gradvis gör att cellerna kan dehydrera i en kontrollerad takt, vilket minskar risken för att skadliga iskristaller bildas, som kan riva eller skada cellmembran.
Detta mätta tillvägagångssätt skyddar cellernas struktur, vilket ökar deras överlevnad och funktionalitet när de väl tinats.Att följa exakta kylprotokoll är avgörande för att säkerställa framgångsrik långtidslagring och återhämtning av cellinjer.











