Att byta från fetalt bovint serum (FBS) till serumfria medier (SFM) är avgörande för att skala upp produktionen av odlat kött. FBS-beroende skapar utmaningar som höga kostnader, begränsad tillgång och inkonsekvent kvalitet. SFM erbjuder ett säkrare, mer kontrollerat alternativ, men det kommer med hinder:
- Cellfästningsproblem: Myoblaster har svårt att fästa utan serum, vilket ofta kräver dyra beläggningar som laminin eller Matrigel. Konditionerat medium eller specifika tillsatser kan förbättra vidhäftningen.
- Långsammare tillväxthastigheter: Serumfria system saknar viktiga näringsämnen, vilket leder till minskad proliferation och ammoniakuppbyggnad. Tillsats av tillväxtfaktorer och ersättning av glutamin med alternativ kan hjälpa.
- Inkonsekvent medieprestanda: Många kommersiella SFM, optimerade för humana celler, misslyckas med att effektivt stödja tillväxt av myoblaster från boskap. Testning över arter och under längre perioder med ett mediaoptimeringsupptäcktskit är avgörande.
Lösningar inkluderar skräddarsydda formuleringar, delvis mediebyte och samkultursystem för att efterlikna serumliknande förhållanden. Även om SFM kan närma sig prestandan hos FBS-system, introducerar skalning till 3D-bioreaktorer komplexiteter som vidhäftning och avfallshantering. Noggrann övervakning av cellkvalitet säkerställer framgång i storskalig produktion.
Att byta till SFM handlar inte bara om bättre vetenskap - det blir en nödvändighet eftersom FBS-priserna fortsätter att stiga. Forskare och producenter måste fokusera på att optimera medier och hitta pålitliga material för att göra produktionen av odlat kött genomförbar och kostnadseffektiv.
Växtbaserade ställningar som inducerar serumfri celladhesion för odlat kött - Indi Geurs - ISCCM9
sbb-itb-ffee270
Vanliga problem i serumfria medier för myoblaster
Att byta från serum-baserade till serumfria formuleringar kan innebära flera tekniska utmaningar som stör arbetsflöden och ökar kostnaderna. Dessa problem visar sig ofta på specifika sätt, med början i cellfästning.
Minskad cellfästning och överlevnad
En av de största hindren är att myoblaster inte fäster bra i serumfria medier. Serum ger naturligt en blandning av proteiner, tillväxtfaktorer och lipider som hjälper celler att fästa vid ytor. Utan dessa komponenter har myoblaster svårt att fästa, vilket ofta leder till tidig celldöd.
För att lösa detta förlitar sig många serumfria system på dyra beläggningsmedel som laminin 511 eller Matrigel. Men även med dessa beläggningar når fästningsnivåerna ofta inte upp till vad som ses i serum-baserade kulturer. Till exempel fann en studie från 2024 att standard serumfritt medium endast stödde 2,210 ± 319 celler/cm² på obelagda skålar. Däremot nästan tredubblade ett konditionerat serumfritt medium - kompletterat med utsöndrade faktorer från andra cellinjer - den siffran till 5,985 ± 1,558 celler/cm² [2].
Ett annat problem är ökad känslighet för antibiotika. I serumfria uppställningar kan antibiotika som Penicillin, Streptomycin och Amphotericin B minska proliferation med så mycket som 62%, jämfört med en minskning på 20–26% i serum-baserade system [1]. Utan serums skyddande element är celler mer sårbara för stress, vilket ytterligare hindrar deras överlevnad och tillväxt.
Långsammare celltillväxt
Även om celler lyckas fästa, släpar tillväxthastigheterna ofta efter.Serum tillhandahåller viktiga näringsämnen som tillväxtfaktorer, cytokiner, kolesterol och fettsyror - många av dessa saknas eller är otillräckliga i de flesta kommersiella serumfria formuleringar. Denna näringsbrist resulterar i lägre cellutbyten och längre produktionstider.
En annan komplikation är ammoniakuppbyggnad från glutaminmetabolism. Ammoniak hämmar tillväxt och, i serumfria förhållanden, där celler redan är under metabolisk stress, kan denna toxicitet allvarligt hindra expansion. Många kommersiella medier designades ursprungligen för humana celler, så de kanske inte uppfyller de specifika näringsbehoven hos bovina eller porcina myoblaster [1][3].
Delvis mediebyte, såsom att byta ut 75% av mediet under utfodring, kan hjälpa till att behålla några endogena tillväxtfaktorer. Även om detta blygsamt förbättrar tillväxttakterna, stänger det inte helt gapet mellan serumfria och serumbaserade system [1].
Variabel Prestanda Bland Kommersiella Produkter
Inte alla kommersiella serumfria medier presterar lika bra. I en studie som jämförde sju formuleringar, stödde endast tre - FBM™, Essential 8™ och TeSR™-E8™ - konsekvent tillväxt av bovina myoblaster över sex dagar. Andra, som StemPro™ och mTeSR1™, stödde tillväxt i bara fyra dagar innan de stannade, medan STEMmacs™ helt misslyckades med att upprätthålla proliferation [1].
Problemet ligger i att de flesta kommersiella medier är optimerade för mänskliga stamceller eller fibroblaster, inte för boskapsmyoblaster. Det som fungerar bra inom biomedicinsk forskning faller ofta kort för odlat köttproduktion. Denna inkonsekvens belyser behovet av formuleringar som är specifikt anpassade för boskapsmyoblaster.Tillverkarens data för mänskliga celler kan inte på ett tillförlitligt sätt förutsäga hur väl ett medium kommer att prestera med bovina eller porcina celler.
För att hitta rätt serumfritt medium är det avgörande att genomföra omfattande tester - helst över sex till tio dagar - för att säkerställa att det stödjer långvarig cellexpansion snarare än bara kortsiktig tillväxt.
Jämförelse av kommersiella serumfria mediealternativ
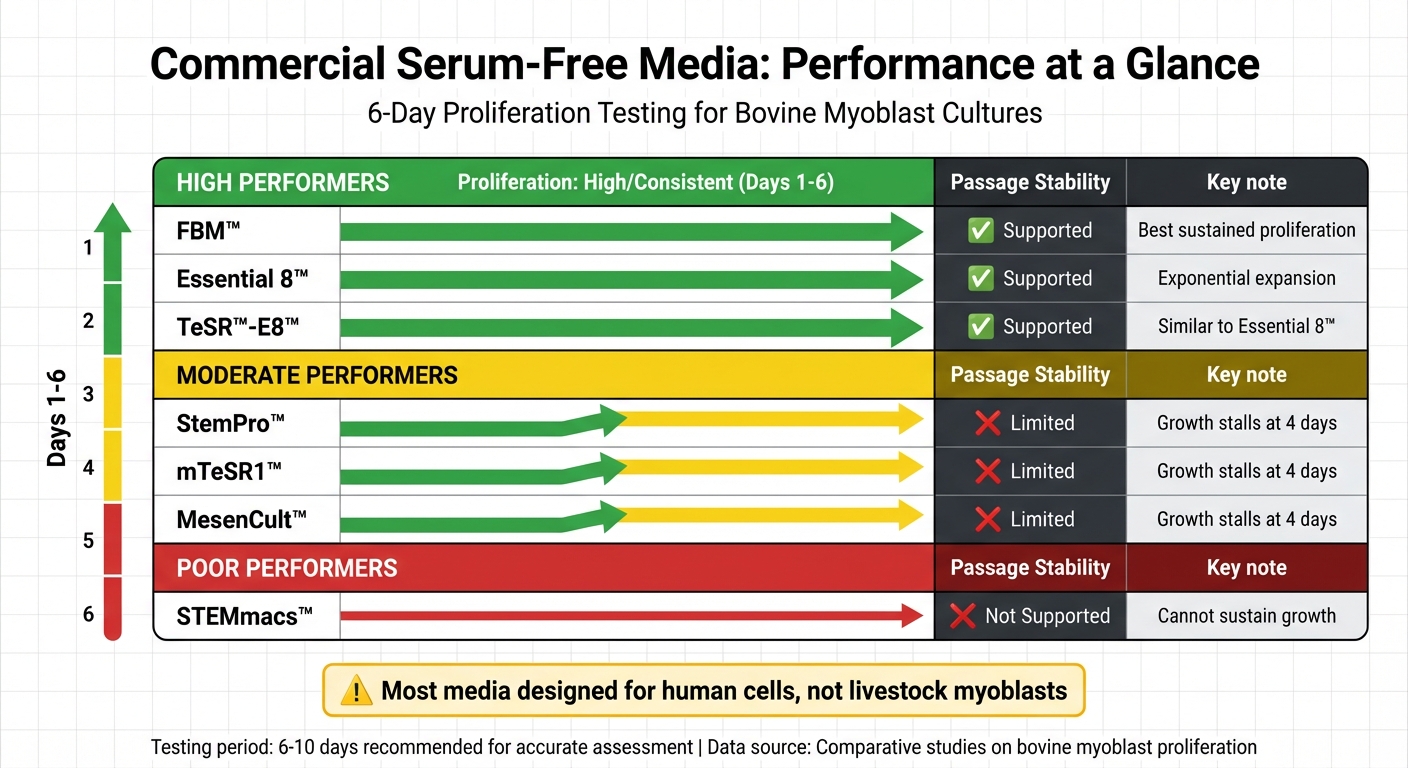
Prestandajämförelse av kommersiella serumfria medier för bovina myoblastkulturer
Prestandadata för vanliga medier
När det gäller serumfria medier för myoblastkulturer kan prestandan variera kraftigt. Vissa produkter, som FBM™, Essential 8™, och TeSR™-E8™, stödjer konsekvent bovin myoblastproliferation över sex dagar. I kontrast tenderar andra, såsom StemPro™, mTeSR1™, och MesenCult™, att stanna av efter bara fyra dagar.Under tiden misslyckas STEMmacs™ helt med att upprätthålla tillväxt [1].
Här är en snabb jämförelse av prestandamått för dessa medier:
| Medium | Proliferation (Dag 1–6) | Passagestabilitet | Viktiga observationer |
|---|---|---|---|
| FBM™ | Hög/Konsekvent | Stöds | Erbjuder den bästa potentialen för långvarig proliferation [1] |
| Essential 8™ | Hög/Konsekvent | Stöds | Stöder exponentiell expansion, dock mindre än serum-baserad [1] |
| TeSR™-E8™ | Hög/Konsekvent | Stöds | Liknande Essential 8™ för bovina myoblaster [1] |
| StemPro™ | Måttlig | Begränsad | Tillväxten avstannar efter fyra dagar [1] |
| mTeSR1™ | Måttlig | Begränsad | Tillväxten avstannar efter fyra dagar [1] |
| MesenCult™ | Måttlig | Begränsad | Tillväxten avstannar efter fyra dagar [1] |
| STEMmacs™ | Låg/Ingen | Inte stöds | Kan inte upprätthålla tillväxt av bovina myoblaster [1] |
Intressant nog visar de flesta medier - förutom FBM™ - betydligt lägre cellantal inom 24 timmar efter sådd jämfört med serum-baserade kontroller.Detta belyser vikten av att utvärdera dessa mätvärden när man väljer ett medium, särskilt med tanke på regulatoriska trender inom tillväxtmedier för livsmedelssäkerhet.
Hur man väljer rätt serumfritt medium
Att välja det bästa serumfria mediet handlar inte bara om tillväxthastigheter; det kräver en balans av flera faktorer som proliferation, vidhäftning och kostnadseffektivitet. Att testa medier under en sexdagarsperiod är avgörande, eftersom kortare tester kan ge missvisande resultat [1].
Artsspecificitet är en annan viktig faktor att överväga. Många serumfria alternativ är utformade med mänskliga celler i åtanke, vilket innebär att de kanske inte uppfyller de näringsmässiga kraven hos boskapsmyoblaster som bovina eller porcina celler. Näringsbehoven hos olika arter och celltillstånd kan variera avsevärt, så testning är nödvändig [3] .
Beläggningskrav spelar också en stor roll. Vissa medier behöver dyra beläggningar som laminin eller Matrigel för att säkerställa celladhesion. Om din process involverar obelagda ytor eller livsmedelsklassade material, är det värt att testa om mediet kan stödja vidhäftning utan dessa tillsatser. Konditionerat medium eller formuleringar anpassade för obelagda skålar kan vara ett kostnadseffektivt alternativ [2] .
En annan kritisk faktor är användningen av antibiotika. Standard antibiotikacocktails, såsom Penicillin/Streptomycin, kan minska myoblastproliferationen med 20–26% i serum-innehållande medier och med så mycket som 62% i serumfria system. Att eliminera antibiotika kan leda till betydligt högre cellytningar [1].
Slutligen, glöm inte hantering av metaboliskt avfall. Ammoniakansamling kan vara giftig för kulturer, så det är en bra idé att komplettera medier med icke-ammoniageniska föreningar som α-ketoglutarat eller pyruvat. Dessa tillsatser hjälper till att minska ammoniaktoxicitet och förlänger kulturernas livslängd [3].
Metoder för att Förbättra Serumfria Myoblastkulturer
Att hantera utmaningarna med serumfria myoblastkulturer kräver riktade strategier. Här är några praktiska metoder för att förbättra deras prestanda.
Tillsätta Nyckeltillskott
Inkorporering av specifika tillskott kan avsevärt förbättra myoblasttillväxt. En blandning av FGF-2 (10 ng/ml), EGF (5 ng/ml), IGF (5 ng/ml), och insulin (10 μg/ml) har visat sig förbättra cellexpansion i basmedier som FBM [1] . Dessa tillväxtfaktorer arbetar tillsammans för att främja cellproliferation samtidigt som de bibehåller det odifferentierade tillstånd som är nödvändigt för produktion.
Aminosyror och vitaminer är också avgörande. Föreningar som pyridoxamin (Vitamin B6), asparagin, och glutaminsyra spelar en nyckelroll i att främja celladhesion och proliferation, särskilt på obelagda ytor [2] . Dessa tillskott hjälper till att ersätta det metaboliska stöd som vanligtvis tillhandahålls av serum, vilket adresserar adhesionsrelaterade utmaningar.
"Komponentanalys och valideringsexperiment föreslog att pyridoxamin, asparagin och glutaminsyra bidrog till förvärvet av kulturfunktionen hos det utvecklade mediet." - npj Science of Food [2]
Men försiktighet behövs med lipidbaserade tillskott som LipoGro. Medan de kan stimulera tillväxt, kan de också inducera adipogen differentiering, vilket får myoblaster att utveckla fettvakuoler och förlora sin muskelcellidentitet [1].
Skräddarsy medieformuleringar
Anpassning av medieformuleringar kan optimera serumfria kulturer med hjälp av ett tillväxtfaktorupptäcktskit. Ett effektivt tillvägagångssätt involverar användning av konditionerat medium. Medium konditionerat genom samodling av HepG2 (mänsklig hepatom) och NIH/3T3 (musfibroblast) celler replikerar den metaboliska profilen hos fosterlever. Denna metod uppnår en celldensitet på 5,985 ± 1,558 celler/cm² på obelagda skålar, jämförbar med de 6,722 ± 1,500 celler/cm² som uppnås med serumhaltigt medium [2] . Interaktionen mellan dessa celltyper främjar utsöndringen av serumliknande komponenter, vilket förbättrar tillväxten.
En annan kostnadseffektiv strategi är delvis mediebyte. Genom att byta ut endast 75% av mediet istället för ett fullständigt byte, bevaras endogena tillväxtfaktorer som produceras av cellerna, vilket förbättrar tillväxthastigheterna utan behov av ytterligare tillskott [1].
Förhindra tidig differentiering med inhibitorer
Att upprätthålla ett proliferativt tillstånd kräver noggrann kontroll av differentieringssignaler. Till exempel kan konditionerat medium från HepG2-celler undertrycka uttrycket av den myogena differentieringsmarkören Desmin, vilket håller cellerna odifferentierade och redo för expansion [2].
Dessutom hjälper spårning av markörer som CD29 (integrin beta-1) och Ki67 till att säkerställa att formuleringen är effektiv för att upprätthålla cellproliferation, vilket minskar risken för för tidig differentiering.Dessa markörer ger ett tillförlitligt sätt att övervaka och justera odlingsförhållanden för optimala resultat.
Skalning av serumfria myoblastkulturer för produktion
Övergång till 3D-odlingssystem
Att flytta serumfria myoblastkulturer från platta 2D-skålar till 3D-bioreaktorsystem medför sina egna utmaningar, särskilt när det gäller celladhesion. Att belägga bioreaktorkomponenter med dyra ämnen som laminin är inte praktiskt för storskalig produktion. Däremot har användning av konditionerat medium från HepG2 och NIH/3T3 samkulturer eller berikning av basmedium med föreningar som pyridoxamin, asparagin och glutaminsyra visat sig vara effektivt. Dessa metoder tillåter myoblaster att fästa vid obelagda 3D-stödstrukturer och mikrobärare, hantera adhesionsproblemen utan att behöva använda kostsamma beläggningar [2].
En annan kritisk faktor vid skalning är hantering av metaboliskt avfall. Täta bioreaktorkulturer kan uppleva en giftig ammoniakansamling, vilket kan undvikas genom att ersätta glutamin med icke-ammoniageniska alternativ som α-ketoglutarat, glutamat eller pyruvat [3]. Dessa justeringar är nödvändiga när man går bortom småskaliga system och kräver noggrann kvalitetskontroll och sensormonitorering för att bibehålla myoblastens integritet under produktionen.
Bekräfta Cellkvalitet i Anpassade Kulturer
När kulturer anpassas för storskalig produktion är det avgörande att säkerställa cellernas kvalitet. Tekniker som transkriptomik, metabolomik och funktionella tester används för att verifiera att cellerna bibehåller höga nivåer av CD29 och Ki67 samtidigt som Desmin-uttrycket undertrycks. Dessa markörer indikerar att cellerna förblir i ett proliferativt, odifferentierat tillstånd under skalningsprocessen [2]. Övervakning av dessa indikatorer är särskilt viktigt när kostnadsbesparande åtgärder, såsom byte till livsmedelsklassade komponenter eller användning av delvisa mediebyten, införs. Detta steg säkerställer att övergången från forskningsklassade till produktionsklassade system inte komprometterar cellkvaliteten. Finjustering av dessa parametrar är ett kritiskt steg mot att göra produktionen av odlat kött skalbar och kostnadseffektiv.
Serumfri vs Serum-baserad Kulturprestanda
När de är optimerade kan serumfria system uppnå resultat som är nära traditionella serum-baserade kulturer.Tabellen nedan belyser nyckelmetrik från bovina myoblastkulturer odlade på obelagda ytor:
| Metrik | Serumbaserad (20% FBS + 10% HS) | Konditionerat serumfritt |
|---|---|---|
| Celladhesion (24h) | ~6,722 celler/cm² | ~5,985 celler/cm² |
| Cellproliferation (72h) | ~10,050 celler/cm² | ~8,998 celler/cm² |
| CD29-uttryck | Högt | Högt |
| Ki67-uttryck | Högt | Högt |
| Desmin-uttryck | Undertryckt | Undertryckt |
Data hämtad från npj Science of Food [2]
Även om serum-baserade system fortfarande har en liten fördel i celldensitet, ger serumfria medier jämförbara resultat i uttryck av adhesionsmarkörer och håller cellerna odifferentierade - nyckelfaktorer för produktion.Klyftan minskar ytterligare när specifika tillskott läggs till för att optimera formuleringar, vilket gör serumfria system till ett alltmer praktiskt alternativ för storskalig odling av kött.
Slutsats
Att byta myoblastkulturer till serumfritt medium medför sina egna utmaningar: tidiga fästningsproblem, långsammare celltillväxt och inkonsekventa resultat från kommersiella produkter. Men enkla förändringar - som att ta bort antibiotika och välja partiella mediebyten - kan avsevärt förbättra proliferationshastigheterna [1]. Genom att noggrant välja medium och lägga till specifika tillväxtfaktorer kan forskare minska skillnaden mellan serumfria och serumbaserade system när det gäller prestanda. Dessa framsteg banar väg för att skala upp produktionen.
Att skala upp serumfria kulturer introducerar dock nya lager av komplexitet.Övergången av celler till 3D-bioreaktorsystem samtidigt som de behåller sin fenotyp kräver rigorös kvalitetskontroll. Ändå visar bevis att väloptimerade serumfria system kan uppnå celldensiteter jämförbara med de som odlas i serumbaserade medier. Detta gör serumfria metoder alltmer praktiska för kommersiell produktion av odlat kött.
Det ekonomiska argumentet för serumfria medier är svårt att ignorera. Med FBS-priser som fortsätter att stiga blir serumbaserade metoder ekonomiskt ohållbara [1] . Denna förändring handlar inte bara om tekniska förbättringar - det handlar om ekonomisk överlevnad för den odlade köttindustrin.
För forskare och produktionsteam som gör denna övergång är det viktigt att hitta rätt material. Från kemiskt definierade medier till rekombinanta tillväxtfaktorer, är tillgång till pålitliga leveranser avgörande.Detta är där
Vanliga frågor
Hur kan jag förbättra myoblastfästning i serumfritt medium utan laminin eller Matrigel?
För att förbättra myoblastfästning i serumfritt medium utan att använda laminin eller Matrigel, överväg att använda konditionerat serumfritt medium. Denna metod kan främja adhesion och proliferation även på obehandlade skålar. Ett annat alternativ är att optimera mediet genom att tillsätta komponenter som FGF2, fetuin, och BSA. Dessa justeringar kan göra en märkbar skillnad i att förbättra cellfästning och tillväxt, vilket eliminerar behovet av extracellulära matrixbeläggningar.
Vad är det snabbaste sättet att minska ammoniakansamling i serumfria myoblastkulturer?
För att minska ammoniakansamling i serumfria myoblastkulturer, fokusera på att förbättra medieformuleringen. Ett tillvägagångssätt är att använda konditionerat medium som främjar både celladhesion och proliferation samtidigt som ammoniaknivåerna hålls låga. Dessutom kan förfining av odlingsförhållandena hjälpa till att minimera ammoniakproduktionen. Detta kan innebära att justera faktorer som pH, temperatur eller näringskoncentrationer för att bättre anpassa sig till cellernas metaboliska behov.
Hur validerar jag att myoblaster förblir odifferentierade efter övergång till serumfritt medium?
För att säkerställa att myoblaster förblir i sitt odifferentierade tillstånd när de odlas i serumfritt medium är det viktigt att spåra specifika markörer. Pax7 är en pålitlig indikator på odifferentierade myoblaster, medan frånvaron av differentieringsmarkörer som myosin heavy chain (MHC) bekräftar att de inte har börjat differentiera.
Du kan använda tekniker som:
- Immunocytokemi: För att visualisera proteinuttryck i celler.
- Flödescytometri: För att analysera marköruttryck i en stor cellpopulation.
- qPCR: För att mäta mRNA-nivåer av viktiga markörer.
Dessutom är det viktigt att observera cellerna under ett mikroskop. Myoblaster bör behålla sitt karakteristiska utseende och undvika bildandet av multinukleära myotuber, vilket är ett tydligt tecken på differentiering. Genom att kombinera dessa metoder och övervaka regelbundet kan du säkerställa att cellerna förblir odifferentierade.











