Biosikkerhedsinspektioner er afgørende for at sikre sikkerheden ved produktion af dyrket kød i Storbritannien og globalt. Disse inspektioner fokuserer på at forhindre kontaminering, verificere produktsikkerhed og opretholde hygiejnestandarder. Siden slutningen af 2025 har Storbritannien klassificeret dyrket kød som "Produkter af animalsk oprindelse", hvilket underlægger det de samme strenge sikkerhedsregler som traditionelt kød. Udfordringer inkluderer mikrobiel kontaminering (e.g. , mycoplasma påvirker 5%-35% af cellelinjer), kemiske rester og genetisk stabilitet.
Vigtige foranstaltninger inkluderer:
- Facilitetsdesign: Brug af HEPA-filtre, renrum og steriliseringsprotokoller som CIP og SIP.
- Personaleuddannelse: HACCP Niveau 4 certificering og aseptiske teknikker.
- Håndtering af materialer: Sporbar cellebanking, genetiske stabilitetstests og restovervågning.
Det britiske Food Standards Agency (FSA) og Food Standards Scotland (FSS) overvåger overholdelse med initiativer som Cultivated Meat Sandbox Programme, der blev lanceret i 2025 for at vejlede virksomheder. Globale tilgange varierer, hvor USA og EU anvender forskellige rammer, men alle sigter mod at opretholde sikkerhed. At føre detaljerede optegnelser, håndtere manglende overholdelse hurtigt og udnytte tredjepartsrevisioner er afgørende for at opfylde disse standarder.
Regulerende myndigheder ansvarlige for biosikkerhedsinspektioner
Food Standards Agency (FSA) Ansvar i Storbritannien
I Storbritannien overvåger Food Standards Agency (FSA) fødevaresikkerhed i England og Wales, mens Food Standards Scotland (FSS) håndterer lignende ansvar i Skotland.Begge organisationer kategoriserer dyrkede kødprodukter - dem der er afledt af dyreceller - som Produkter af animalsk oprindelse (POAO) under Forordning (EF) 853/2004. Denne klassifikation betyder, at faciliteter, der producerer sådanne produkter, skal følge hygiejne- og sikkerhedsstandarder, der ligner dem for traditionel kødproduktion [5][7].
FSA spiller en nøglerolle i at sikre sikkerheden, før disse produkter når markedet. Den udfører videnskabelige risikovurderinger og kræver, at fødevarevirksomhedsoperatører anvender Hazard Analysis and Critical Control Point (HACCP) principper. Disse foranstaltninger har til formål at forhindre biologiske, kemiske og fysiske farer. Derudover håndhæver FSA overholdelse gennem Officielle Kontroller under Forordning (EF) 2017/625 [5].
For at imødegå de specifikke udfordringer ved dyrket kød, introducerede FSA sit Cultivated Meat Sandbox Programme i februar 2025. Dette initiativ involverer otte virksomheder, der deltager i månedlige workshops, hvor de bruger reelle produktionsdata til at adressere biosikkerhedsspørgsmål som cellelinjeidentitet, mikrobiologi og toksikologi. Programmets mål er at skabe detaljeret vejledning for industrien. I begyndelsen af 2026 forventer FSA at modtage omkring 15 ansøgninger fra virksomheder inden for dyrket kød, med planer om at færdiggøre sikkerhedsvurderinger for mindst to af disse ansøgninger inden for en toårig tidsramme [6][7][8].
I Nordirland forbliver EU-reglerne i kraft, hvilket sikrer overensstemmelse med bredere europæiske standarder.Men produkter, der er godkendt i Storbritannien, kan transporteres til Nordirland under Northern Ireland Retail Movement Scheme (NIRMS) [7].
Disse skræddersyede britiske foranstaltninger fremhæver en særskilt reguleringsmetode sammenlignet med andre lande, hvilket afspejler de forskellige strategier, der anvendes globalt for biosikkerhedstilsyn.
Globale Reguleringsorganer
Biosikkerhedsregler for dyrket kød varierer meget på tværs af kloden, formet af forskellige filosofier og risikostyringsstrategier. I USA deler Food and Drug Administration (FDA) og USDA Food Safety and Inspection Service (USDA-FSIS) ansvaret under en aftale fra 2019. FDA overvåger de indledende faser, såsom celleindsamling og vækst, mens USDA-FSIS tager over under høst, forarbejdning og mærkning.Bemærkelsesværdigt kræver USDA-FSIS inspektioner mindst én gang pr. skift, hvilket afspejler processen for traditionelt kød og fjerkræ [9][10].
I Den Europæiske Union leder Den Europæiske Fødevaresikkerhedsautoritet (EFSA) sikkerhedsvurderinger for dyrkede kødprodukter. I mellemtiden giver organisationer som FN's Fødevare- og Landbrugsorganisation (FAO) og Verdenssundhedsorganisationen (WHO) bredere sikkerhedsvejledning. Deres fælles rapport fra april 2023 om sikkerheden ved dyrket kød har påvirket risikovurderinger i forskellige lande, herunder Storbritannien [7]. FSA samarbejder også med regulatorer i Singapore og Australien - to nationer, der allerede har godkendt dyrkede kødprodukter - for at fremme ensartede biosikkerhedspraksisser globalt [6].
Reguleringsrammer varierer betydeligt mellem lande. For eksempel kræver USDA, at faciliteter sikrer en "grant of inspection" og designgodkendelse, før produktionen begynder. I modsætning hertil bruger Storbritanniens FSA sin Regulatory Sandbox til at udvikle branchespecifik vejledning i partnerskab med virksomheder [9] [7]. Importregler varierer også; USA kræver en "equivalence" proces for at sikre, at udenlandske inspektionssystemer opfylder dets folkesundhedsstandarder [9][10].
Disse internationale forskelle former globale bedste praksis, der balancerer behovet for reguleringsmæssig konsistens med respekt for lokale tilgange til biosikkerhed.
Tendenser inden for opskalering og bioprocessering af dyrket kød
Biosikkerhedsstandarder og inspektionskrav
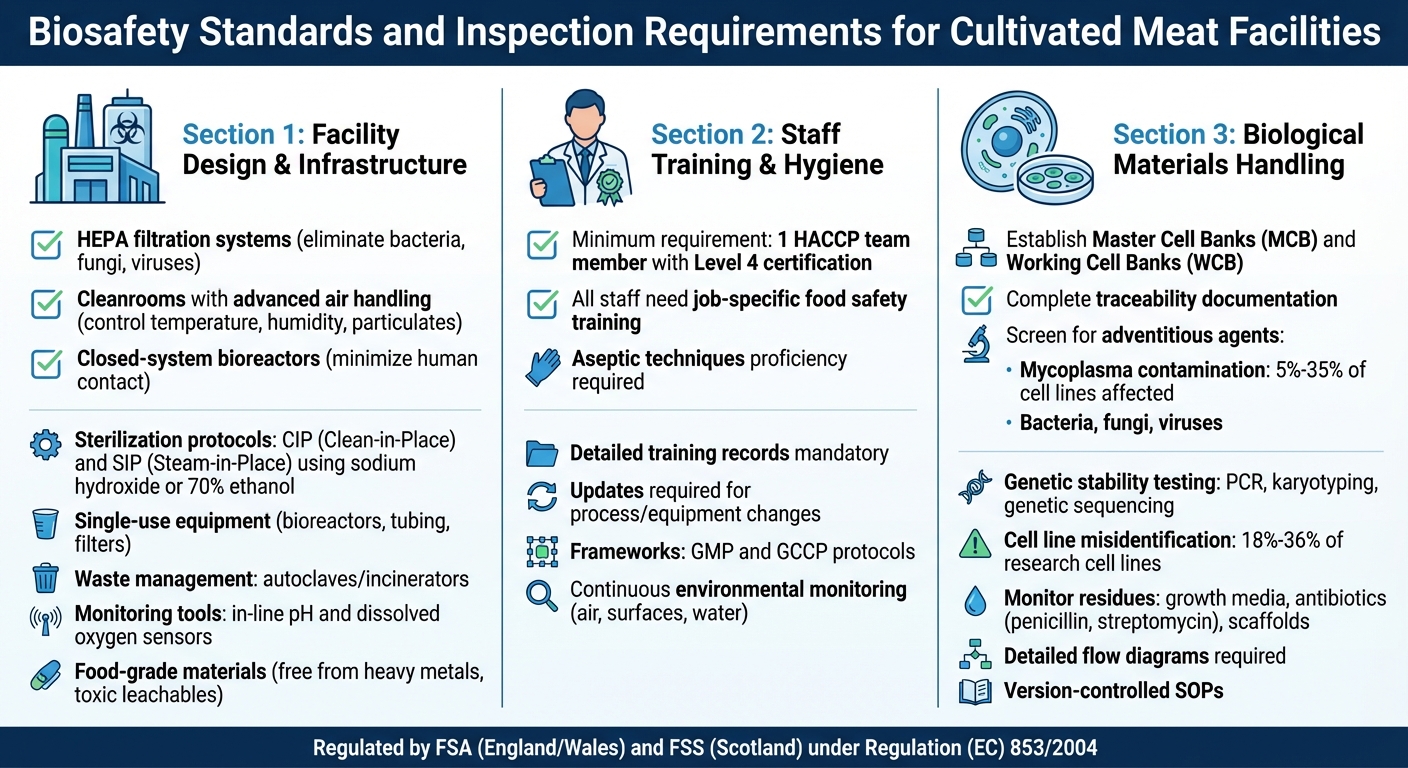
UK Biosikkerhedsinspektionskrav for faciliteter til dyrket kød
Facilitetsdesign og infrastruktur
Designet af en facilitet er grundlæggende for at opfylde biosikkerhedsinspektionsstandarder, som beskrevet i de regulerende retningslinjer. Faciliteter til dyrket kød skal implementere strenge strukturelle foranstaltninger for at forhindre kontaminering. For eksempel er HEPA-filtreringssystemer nødvendige for at eliminere bakterier, svampe og vira fra luften [3] . Renrum udstyret med avancerede luftbehandlingssystemer regulerer temperatur, fugtighed og partikler, hvilket reducerer mikrobielle risici [4].
For at begrænse menneskelig kontakt med cellekulturer - en almindelig kilde til kontaminering - stoler faciliteter ofte på lukkede system bioreaktorer og automatiseret udstyr [4] [3]. Derudover er Clean-in-Place (CIP) og Steam-in-Place (SIP) protokoller essentielle for sterilisering af udstyr mellem produktionskørsler, typisk ved brug af natriumhydroxid eller 70% ethanol [1] [3]. Brugen af engangsbioreaktorer, slanger og filtre minimerer yderligere risikoen for krydskontaminering mellem partier [4].
Korrekt affaldshåndtering og kontamineringsovervågning er også kritiske. Faciliteter skal inkludere systemer som autoklaver eller forbrændingsanlæg til bortskaffelse af brugt vækstmedie og biologiske biprodukter.Overvågningsværktøjer, såsom in-line pH og opløste iltsensorer, giver tidlige advarsler om potentiel forurening [1][4]. Desuden skal alle anvendte materialer - uanset om det er i bioreaktoroverflader eller rør - opfylde fødevaregodkendte standarder og være fri for skadelige stoffer som tungmetaller eller giftige udvaskninger, der kunne kompromittere produktsikkerheden [1][3].
Personaleuddannelse og hygiejnekrav
Mens robust facilitetdesign er vigtigt, er veluddannet personale lige så afgørende for at opretholde kontrollerede miljøer. Ifølge britiske hygiejneregler skal mindst ét medlem af HACCP-teamet have Level 4 træning i HACCP-principper. Derudover skal alt personale, der er involveret i overvågning og korrigerende handlinger, have job-specifik træning i fødevaresikkerhedsprotokoller [5] .
Personale, der arbejder med biologiske materialer, skal være dygtige i aseptiske teknikker for at undgå at introducere forurenende stoffer i cellekulturer [4]. Faciliteter er forpligtet til at føre detaljerede træningsregistre og opdatere personalet, når der er ændringer i produktionsprocesser, materialer eller udstyr [5]. Hygiejnestandarder understøttes yderligere af rammer som Good Manufacturing Practice (GMP) og Good Cell Culture Practice (GCCP), som fastsætter protokoller for opretholdelse af renlighed. Kontinuerlig miljøovervågning af luft, overflader og vand sikrer, at mikrobiel forurening opdages tidligt [4].
Håndtering og Opbevaring af Biologiske Materialer
Håndtering af biologiske materialer kræver omhyggelige protokoller for at sikre sikkerhed og overholdelse.Faciliteter skal etablere Master Cell Banks (MCB) og Working Cell Banks (WCB), med klar dokumentation for frossen opbevaring og fuldstændig sporbarhed af cellernes oprindelse [2]. Screening for adventive agenter, såsom bakterier, svampe, vira og mycoplasmer, er obligatorisk. Forskningsresultater indikerer, at 5% til 35% af cellelinjer kan bære mycoplasmainfektioner, der undgår standard filtreringssystemer [1].
For at overvåge genetisk drift under udvidede produktionscyklusser udfører faciliteter genetisk stabilitetstestning ved hjælp af metoder som PCR, karyotyping eller genetisk sekventering [1] [2]. Studier afslører, at 18–36% af forskningscellelinjer lider af fejlagtig identifikation eller kontaminering, hvilket understreger behovet for grundige kontroller [1]. Derudover skal faciliteter bekræfte, at rester fra vækstmedier, antibiotika (e.g. , penicillin og streptomycin), og stilladsmaterialer forbliver inden for sikre, fødevaregodkendte grænser [1][3].
Detaljerede flowdiagrammer er essentielle for at spore hvert trin i processen, fra cellekilde til endelig emballering. Versionskontrolsystemer sikrer, at Standard Operating Procedures (SOP'er) forbliver opdaterede, et krav der letter glattere inspektioner [5]. Disse strenge håndteringsprotokoller udgør rygraden i overholdelsesindsatsen, hvilket sikrer, at faciliteter er forberedt på grundige revisioner.
sbb-itb-ffee270
Revisionsprocedurer og overholdelsesverifikation
Inspektionschecklister og dokumentation
Revisioner i den britiske fødevaresektor drejer sig om de syv HACCP-principper, som alle fødevarevirksomheder er lovmæssigt forpligtet til at følge. Inspektører fokuserer typisk på tre nøgleområder af dokumentation:
- HACCP-planen: Dette inkluderer fareanalyse, procesflowdiagrammer og identificerede kritiske kontrolpunkter (CCP'er).
- Politikdokumenter: Disse beskriver hygiejneprocedurer og relaterede protokoller.
- Driftsoptegnelser: Disse dækker overvågningslogfiler, kalibreringsoptegnelser og anden dag-til-dag overholdelsesdokumentation.
For at demonstrere løbende overholdelse skal faciliteterne opretholde en velorganiseret sikkerhedsmappe.Dette bør inkludere overvågningsresultater for kritiske grænser, såsom pH-aflæsninger og temperaturlogfiler, sammen med optegnelser over korrigerende handlinger, der er taget, når disse grænser overskrides. Bevis for medarbejderuddannelse er også afgørende, hvor mindst ét medlem af HACCP-teamet skal have en Level 4-certificering. Derudover skal alle Standard Operating Procedures (SOP'er) være opdaterede, tydeligt daterede og versionskontrollerede.
Disse optegnelser danner grundlaget for verifikationsaudits, som sikrer fortsat overholdelse af sikkerhedsprotokoller. Faciliteter bør gennemføre verifikationsaudits årligt eller hyppigere, hvis arten af farer, produktionsvolumen eller tidligere problemer berettiger det. Regulatorer skelner mellem validering, som bekræfter, at sikkerhedsplanen er teoretisk effektiv før implementering, og verifikation, som involverer regelmæssige kontroller for at sikre, at planen fungerer i praksis.
Håndtering af manglende overholdelse
Undladelse af at opfylde biosikkerhedsstandarder medfører øjeblikkelige juridiske konsekvenser. Food Standards Agency (FSA) understreger dette med princippet:
"Fødevarer må ikke markedsføres, hvis de er usikre. Dette betyder, at de hverken må være skadelige for helbredet eller uegnede til menneskeføde."
Når manglende overholdelse opstår, skal faciliteter følge en tre-trins responsproces:
- Genopret øjeblikkelig kontrol: Adressér problemet hurtigt for at minimere risici.
- Afhjælp berørte produkter: Tag skridt til at håndtere og, om nødvendigt, fjerne usikre produkter fra markedet.
- Undersøg grundårsager: Identificér og ret de underliggende årsager til overtrædelsen.
Hver korrigerende handling skal være klart dokumenteret, inklusive hvem der er ansvarlig, og hvordan handlingens effektivitet verificeres.
Gentagen manglende overholdelse kan føre til alvorlige konsekvenser. Ifølge FSA's vejledning:
"Hvis korrigerende handlinger skal tages gentagne gange, betyder det, at der er en grundlæggende fejl i fødevaresikkerhedsstyringssystemet."
I sådanne tilfælde kan tilsynsmyndigheder iværksætte grundige undersøgelser, og driften kan blive suspenderet, indtil anlægget beviser, at det har adresseret systemiske fejl. Det er essentielt at føre detaljerede optegnelser over alle korrigerende foranstaltninger, inklusive årsagsanalyser, for at demonstrere, at langsigtede løsninger er blevet implementeret.
Industriressourcer til opfyldelse af biosikkerhedsstandarder
At sikre overholdelse af biosikkerhed kræver ofte mere end blot interne kontroller.Eksterne ressourcer spiller en nøglerolle i at hjælpe faciliteter med at opfylde lovgivningsmæssige standarder ved at give adgang til verificerede værktøjer og materialer, der er i overensstemmelse med inspektionsforventningerne.
Cellbase 's Rolle i Biosikkerhedsoverholdelse
For producenter af dyrket kød kommer håndtering af cellebanker - hjørnestenen i produktionen - med sine egne udfordringer, især da der ikke er standardiserede retningslinjer på plads [2]. Dette gør sourcing af overensstemmende udstyr og sporing af cellernes oprindelse særligt vanskeligt.
Arbejder med tredjepartsrevisorer
Tredjepartsrevisorer bringer et ekstra lag af sikkerhed ved at verificere HACCP-planer og øge tilliden til fødevaresikkerhedsstyringssystemer [5]. Deres ekspertise inkluderer udførelse af mikrobiologiske udfordringsstudier, såsom evaluering af vækstpotentialet for patogener som Listeria i dyrket kød. Disse studier giver kritiske sikkerhedsdata, hvilket er særligt vigtigt, da industrien oplever en gennemsnitlig mikrobiologisk kontaminationsbatchfejlrate på 11.2% [11].
At engagere sig med tredjepartsrevisorer tidligt kan også hjælpe faciliteter med at forberede sig til FDA præ-markedsanmeldelser og USDA inspektioner [12][9]. For at strømline overholdelsesprocessen bør revisionsrapporter tilføjes til permanente HACCP-mapper, hvilket sikrer, at faciliteter er klar til at demonstrere overholdelse af sikkerhedsstandarder under officielle inspektioner [5].
Konklusion
Biosikkerhedsinspektioner spiller en afgørende rolle i at beskytte folkesundheden og opretholde industriens tillid inden for sektoren for dyrket kød. Storbritanniens strenge hygiejneregler sætter en høj standard for faciliteter, hvilket sikrer, at de håndterer risici som mycoplasmaforurening og fejlagtig identifikation af cellelinjer direkte [5][1].
Programmer som CCP-sandkassen har hjulpet med at afklare regulatoriske forventninger, hvilket strømliner vejen for nye fødevareteknologier uden at gå på kompromis med sikkerheden. For at opfylde disse standarder skal producenter implementere robuste foranstaltninger, herunder autentificeret cellebanking, sikre at mindst ét teammedlem har Level 4 HACCP-uddannelse, og gennemføre årlige sikkerhedsplan-gennemgange [5][1][2]. Branchens gradvise skift mod serumfri medier og vedtagelse af realtids-overvågningsteknologier understreger dens dedikation til at adressere både konventionelle fødevaresikkerhedsproblemer og unikke risici forbundet med produktion af dyrket kød.
Ekstern støtte styrker også overholdelsesindsatsen. Platforme som
Stærke biosikkerhedspraksisser er essentielle - ikke kun for at opnå markedsgodkendelse, men også for at opretholde branchens omdømme og drive dens fremtidige vækst.
Ofte stillede spørgsmål
Hvad udløser en biosikkerhedsinspektion i et dyrket kød anlæg?
Biosikkerhedsinspektioner i dyrkede kød anlæg spiller en afgørende rolle i at sikre overholdelse af vigtige standarder såsom ISO 14644-1, EU GMP Annex 1, og EN 17141. Disse inspektioner udføres normalt på nøglestadier, herunder design-, konstruktions- og certificeringsfaserne.Det primære mål er at forhindre mikrobiel forurening og opretholde sikkerhed gennem hele processen.
Hvordan sikrer producenter, at deres cellelinjer forbliver autentiske og stabile over tid?
Producenter opretholder integriteten og pålideligheden af deres cellelinjer ved at implementere strenge cellebankprocedurer. Disse processer involverer bekræftelse af cellelinjernes identitet, regelmæssig vurdering af deres stabilitet og overholdelse af etablerede industristandarder og retningslinjer. Ved at følge disse protokoller sikrer de konsistente og pålidelige resultater i produktionen af dyrket kød.
Hvad sker der, hvis der findes forurening under produktionen?
Forurening under produktionen kan føre til alvorlige problemer, såsom manglende overholdelse af sikkerhedsstandarder, produkt tilbagekaldelser og øgede mikrobielle risici. Dette understreger behovet for strenge hygiejnepraksis og robuste certificeringsprocesser for at beskytte både produktsikkerhed og kvalitet.











