Genetisk stabilitet er afgørende for produktion af dyrket kød. Uden det kan cellelinjer mutere, hvilket fører til inkonsekvent kvalitet, sikkerhedsrisici og produktionsfejl. Skalering fra tusinder til billioner af celler forstærker disse risici, hvilket gør robuste kvalitetskontrolsystemer essentielle. Regulatorer som FDA og EMA kræver bevis for stabilitet, før de godkender produkter, da selv mindre genetiske ændringer kan udløse allergifremkaldende eller skadelige resultater.
Vigtige udfordringer inkluderer genetisk drift, mutationsakkumulering og aktivering af onkogener. Disse problemer opstår fra forlænget cellepassage, selektive pres og miljømæssige stressfaktorer under produktionen. Avancerede testmetoder, såsom karyotyping, SNP arrays og next-generation sequencing (NGS), hjælper med at opdage og adressere disse risici. Forebyggende strategier som struktureret cellebanking og målrettet genetisk engineering beskytter yderligere mod ustabilitet.
Producenter skal integrere kvalitetskontrol i alle produktionsfaser - fra cellebanking til storskala bioreaktorer. Værktøjer som STR-profiler, kontamineringstests og funktionelle assays sikrer konsistens og sikkerhed. Platforme som
Accelerating Cell Line Development from DNA to Master Cell Bank - AGC Biologics
Almindelige udfordringer i opretholdelse af genetisk stabilitet
At sikre genetisk stabilitet gennem hele produktionscyklussen af dyrket kød er ingen let opgave. Den store produktionsskala introducerer mange muligheder for genetiske ændringer at udvikle sig og sprede sig. At erkende disse udfordringer er nøglen til at implementere effektive kvalitetskontrolsystemer.
Genetisk drift og mutationsakkumulering
Forlænget cellepassage er en væsentlig kilde til genomisk ustabilitet i produktionen af dyrket kød. Immortaliserede cellelinjer er af deres natur tilbøjelige til genomiske ændringer, hvilket kan føre til spontane mutationer under langtidskultur [6][5]. Efterhånden som celler gennemgår flere populationfordoblinger, opbygges fejl i DNA-replikationen, hvilket resulterer i forskellige cellepopulationer og potentielt et tab af funktion. Christopher Frye og Luhong He fra BioPharm International fremhæver dette problem:
Klonalt afledte CHO-cellelinjer er ofte blevet observeret at divergere og blive en heterogen population over lange perioder med subkultur [6].
I industrielle miljøer viser omkring 20% af produktionscellelinjer betydelig transgen heterogenitet over successive generationer [6]. Disse mutationer kan opstå tidligt, under DNA-replikation efter transfektion, eller på grund af fejl, når fremmede gener integreres i værtsgenomet [5].
Selektive pres tilføjer et andet lag af kompleksitet. Midler som antibiotika og metaboliske markører (e.g. , MTX) brugt til at stabilisere cellelinjer kan faktisk øge mutationsraterne [6][5]. I nogle tilfælde, jo højere koncentrationen af disse midler er, desto højere er mutationsraten [6]. Miljømæssige stressfaktorer - såsom næringsstofmangel, suboptimale kulturforhold under opskalering, og fysisk stress fra ekspansion - kan yderligere destabilisere genetisk integritet [6][5].
Shuai Wang, direktør for cellelinjeudvikling hos WuXi Biologics, bemærker:
Mutationsniveauer vil sandsynligvis ændre sig over cellepassagering på grund af kinesiske hamsteræggestok (CHO) cellers genomiske plasticitet [5].
Epigenetiske ændringer spiller også en rolle. Transgener kan delvist eller helt gå tabt eller blive tavse under kulturprocessen, hvilket påvirker den langsigtede stabilitet. Disse akkumulerede mutationer skader ikke kun cellefunktionen, men øger også risikoen for at aktivere onkogener.
Risici ved Onkogen Aktivering
Onkogen aktivering repræsenterer en kritisk sikkerhedsbekymring for producenter af dyrket kød, da det kan kompromittere hele produktionspartier. Genetisk ustabilitet kan føre til onkogen aktivering gennem mekanismer som hypermethylering, hvilket kan resultere i tumor-lignende profiler [3][1]. Den hurtige udvidelse, der kræves i produktionen, øger yderligere sandsynligheden for at akkumulere disse skadelige mutationer [5][6].
Dette er en velkendt udfordring. Ifølge International Consortium for Innovation & Quality in Pharmaceutical Development (IQ) mener 67% af respondenterne, at genetiske mutationer udgør en større trussel end aminosyrefejl under produktionen [5] . Et tilfælde fra maj 2024 illustrerer alvoren af dette problem: WuXi Biologics opdagede, at 43% af klonerne fra et cellelinjeudviklingsprogram havde den samme genetiske punktmutation. Årsagen? Et 2,1%–2,2% variantniveau i plasmid-DNA'et brugt under transfektion, som ikke blev opdaget af traditionel Sanger-sekventering. For at løse dette inkorporerede virksomheden Next-Generation Sequencing (NGS) i sine kvalitetskontrolprocesser for at fange sådanne varianter tidligt [5].
Tidlig påvisning af genetiske abnormiteter er afgørende, da onkogene ændringer kan kompromittere hele partier. Standard G-bånd karyotypering kan identificere unormale subpopulationer med så lidt som 14% mosaik i tyve cellemetafaser [1]. Mere avancerede teknikker som NGS kan opdage genetiske mutationer i klonale celler med en følsomhed på 0,5% [5].
DNA-methyleringsanalyse er et andet værdifuldt værktøj til vurdering af tumorigenisk potentiale:
Fordi DNA-methyleringsniveauer og hypermethylering af visse gener forekommer ved kræftinitiering og -progression, kan analysen af DNA-methyleringsprofiler give supplerende information om cellers tumorigeniske potentiale [3].
Den virkelige udfordring ligger i at implementere robuste overvågningssystemer, der er i stand til at identificere disse ændringer, før de kompromitterer sikkerheden.For producenter af dyrket kød kræver opretholdelse af genetisk stabilitet under hurtig celleudvidelse avancerede kvalitetskontrolforanstaltninger. Specialiserede platforme som
Kvalitetskontrol Testmetoder
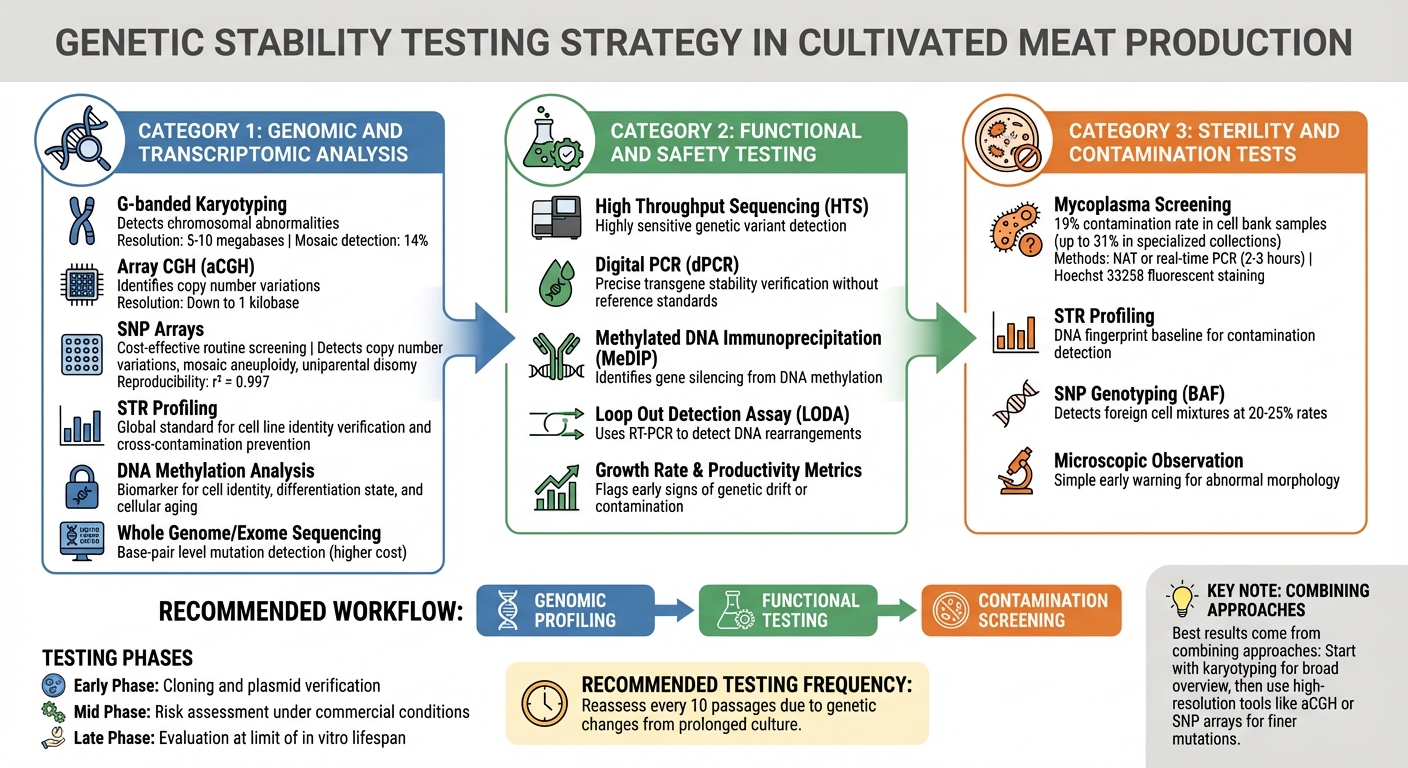
Kvalitetskontrol Testmetoder for Genetisk Stabilitet i Dyrkede Kød Cellelinjer
Identifikation af genetisk ustabilitet, før det påvirker produktionen, kræver en flerlags teststrategi. Producenter af dyrket kød er afhængige af metoder, der opdager alt fra store kromosomale ændringer til enkeltbase-mutationer. Valget af teknikker afhænger af de risici, der er til stede på hvert produktionsstadie. Disse genomiske værktøjer fungerer som den første kontrolpost, efterfulgt af detaljerede funktionelle og kontaminationsvurderinger.
Genomisk og transkriptomisk analyse
G-båndet karyotypering er et vigtigt værktøj til at identificere større kromosomale problemer som numeriske abnormiteter og store strukturelle omlejringer, såsom translokationer. Mens det kan detektere mosaikniveauer på omkring 14%, er dets opløsning begrænset til ændringer på 5–10 megabaser, hvilket betyder, at mindre ændringer kan gå ubemærket hen [1].
Array Komparativ Genomisk Hybridisering (aCGH) tilbyder højere opløsning, der identificerer kopiantalsvariationer ned til 1 kilobase. Tilsvarende giver Single Nucleotide Polymorphism (SNP) arrays en omkostningseffektiv mulighed for rutinemæssig screening, der detekterer kopiantalsvariationer, mosaik aneuploidi og uniparental disomi. Valideringsstudier har vist, at SNP arrays er meget reproducerbare, med B Allel Frekvens (BAF) målinger, der opnår en imponerende r² = 0.997 [8] [1].
Rocio Aguilar-Quesada fra Andalusian Public Health System Biobank fremhæver værdien af at kombinere metoder:
Karyotyping forbliver en alsidig test, især når den suppleres med højopløsnings test [1].
Short Tandem Repeat (STR) profilering er den globale standard for at verificere cellelinjeidentitet og forhindre krydskontaminering [1] [9]. I mellemtiden tjener DNA methyleringsanalyse som en biomarkør for celleidentitet, differentieringstilstand og cellulær aldring [1]. Til detektion af mutationer på baseparniveau er helgenom- eller exomsekventering en mulighed, selvom det kommer med højere omkostninger sammenlignet med array-baserede metoder [1].
De bedste resultater opnås ved at kombinere disse tilgange. Start med karyotyping for et bredt overblik, og brug derefter højopløsningsværktøjer som aCGH eller SNP arrays til at fange finere mutationer. Regelmæssig revurdering - ideelt set hver 10. passage - er kritisk, da forlænget kultur kan føre til genetiske ændringer [10]. Disse genomiske indsigter suppleres derefter med funktionelle assays for at sikre konsistent celleadfærd gennem hele produktionen.
Funktionel og Sikkerhedstestning
Genomisk profilering alene er ikke nok. Funktionelle tests bekræfter, at celler bevarer deres tilsigtede egenskaber under ekspansion. Metrikker som vækstrater og produktivitet kan advare om tidlige tegn på genetisk drift eller kontaminering [9].
High Throughput Sequencing (HTS) er meget følsom til at detektere genetiske varianter, mens digital PCR (dPCR) præcist verificerer transgen stabilitet uden behov for referencestandarder [11] . Christopher Frye og Luhong He fra BioPharm International understreger vigtigheden af dette trin:
Produktionscellelinjen er fundamentet for enhver bioproces, og derfor er passende genetisk karakterisering af produktionscellelinjen absolut afgørende for succes i procesudvikling [6].
Epigenetisk stabilitet er også kritisk. Methylated DNA Immunoprecipitation (MeDIP) hjælper med at identificere gendæmpning forårsaget af DNA-methylering, en almindelig årsag til produktivitetsnedgang [7]. Værktøjer som Loop Out Detection Assay (LODA) bruger RT-PCR til at detektere DNA-omlejringer, såsom når et gen af interesse slettes, mens den selektive markør forbliver [7].
Testning bør tilpasses produktionsfasen: tidlige fase-tests fokuserer på kloning og plasmidverifikation, mellemfase-tests vurderer risici under kommercielle forhold, og sene fase-tests evaluerer celler ved grænsen af deres in vitro levetid [6]. At starte eksperimenter med friske, lav-passage celler fra en master cellebank reducerer risikoen for genetisk drift [9].
Sterilitet og Kontamineringstests
Kontamineringstest er afgørende for at undgå faktorer, der kunne destabilisere genetikken. Mycoplasma er særligt bekymrende, da det ændrer cellens metabolisme og adfærd uden at forårsage synlige ændringer i kulturen [1]. Undersøgelser afslører mycoplasma-kontaminering i 19% af cellebankprøver, med nogle specialiserede samlinger, der viser rater så høje som 31% [1].
Regelmæssig mycoplasma-screening ved brug af følsomme Nukleinsyre Amplifikationsteknikker (NAT) eller real-time PCR kan give semi-kvantitative resultater inden for 2–3 timer [1]. Hoechst 33258 fluorescerende farvning er en anden metode, der afslører karakteristiske ekstracellulære fluorescensmønstre [9].
STR-profilering etablerer et DNA-fingeraftryk for cellelinjer, der fungerer som en baseline til at opdage krydskontaminering [9]. Derudover kan SNP-genotyping ved brug af B Allele Frequency (BAF) distributioner identificere kontaminering fra andre cellelinjer, og opdage fremmede celleblandinger ved rater på 20–25% [8].
Mikroskopisk observation er et simpelt, men effektivt tidligt advarselsværktøj, da unormal cellemorfologi ofte signalerer kulturproblemer [9]. Implementering af et kvalitetsstyringssystem, såsom ISO 9001:2015, sammen med Good In Vitro Method Practices (GIVIMP), hjælper med at opretholde standardiserede og reproducerbare kulturforhold, hvilket reducerer risikoen for genomisk ustabilitet [10].
For producenter af dyrket kød, der har brug for adgang til specialiseret testudstyr og materialer, tilbyder platforme som
sbb-itb-ffee270
Forebyggelsesstrategier for genetisk ustabilitet
At opdage genetisk ustabilitet er én ting; at forhindre det er en helt anden udfordring.For at holde genetisk stabilitet intakt, har producenter af dyrket kød brug for velovervejede systemer, der forhindrer cellelinjer i at drive, før problemer opstår. To nøglestrategier leder vejen her: struktureret cellebanking og målrettet genetisk ingeniørarbejde. Sammen tackler disse tilgange direkte risikoen for genetisk drift og aktivering af onkogener.
Cellebanking og Kryopræservering
Akkumulering af mutationer er en reel bekymring, så et pålideligt cellebankingsystem er et must. Industriens standard involverer et to-niveau system: en Master Cell Bank (MCB) og en Working Cell Bank (WCB). Denne opsætning sikrer et konsistent udgangspunkt for produktion. Begrænsning af antallet af passager er afgørende, da hver passage øger chancen for mutationer. Ved at opbevare celler i flydende nitrogen, pauses biologisk aktivitet effektivt, hvilket reducerer risikoen for genetiske ændringer under opbevaring.
I stedet for at spore tid, måles cellealder ved population fordoblinger. For eksempel involverer en typisk 5.000-liters produktionsbioreaktor omkring 30 population fordoblinger[6]. For at opretholde genetisk konsistens begrænser kommerciel produktion dette antal til mellem 45 og 60 fordoblinger[6].
Screeningsmetoder som RT-PCR og single-cell qPCR kan fange problemer tidligt, såsom usædvanlig mRNA splejsning eller transgen variabilitet. Cellelinjer, der viser stor variabilitet i kopiantal, bør kasseres for at undgå fremtidige problemer.
Kvalitetskontrol er ufravigelig. Alarmerende nok har undersøgelser fundet, at op til 31% af cellelinjerne i nogle banker var kontamineret med mycoplasma [3] . For at forhindre dette anvendes STR profilering til at bekræfte ægtheden af cellelinjer gennem hele bankprocessen.Som fremhævet af FSA Research and Evidence:
Fordi de bankede celler er udgangsmaterialet til det endelige produkt, kan høje standarder blive krævet af regulatorer i fremtiden for at sikre et sikkert kødprodukt af høj kvalitet[2].
Genetisk Ingeniørkunst for Stabilitet
Genetisk ingeniørkunst giver et ekstra lag af forsvar ved direkte at forbedre cellelinjens stabilitet. Teknikker som målrettet integration (TI), især Rekombinase-Mediated Cassette Exchange (RMCE), tillader præcis indsættelse af transgener i specifikke genomiske lokationer. Denne tilgang undgår uforudsigeligheden ved tilfældig integration, hvor positionseffekter og kopiantalsinstabilitet kan skabe kaos. Selvom RMCE i CHO-celler har effektivitetsrater under 0,1%[12], er de resulterende kloner mere forudsigelige og stabile.
Valget af ekspressionssystem er også vigtigt. For eksempel resulterer Glutamin Syntetase (GS) systemet typisk i omkring fem transgenkopier pr. celle, mens Dihydrofolat Reduktase (DHFR) systemet kan amplificere kopiantallet op til 1.000[6]. Selvom højere kopiantaller kan lyde tiltalende, øger de sandsynligheden for DNA-ændringer, hvilket gør GS-baserede systemer til et klogere valg for langvarig stabilitet.
For yderligere at minimere risici er site-specifik mutagenese og pre-transfektion NGS-screening afgørende. Da Sanger-sekventering har en højere detektionsgrænse, kan NGS fange plasmidmutationer under 0,5%, hvilket forbedrer klonscreeningssucces til over 90%[5].
Shuai Wang og kolleger fra WuXi Biologics understreger vigtigheden af denne årvågenhed:
Da procesoptimering ikke kan rette gen-niveau mutationer, overvåg mutationsniveauer i stabile kloner nøje[5].
For producenter, der har brug for specialiserede værktøjer - hvad enten det er til kryopræservering, genetisk engineering eller cellelinjekarakterisering -
Integration af kvalitetskontrol i produktionen
Inkorporering af kvalitetskontrol i hver produktionsfase er afgørende. Uden et struktureret system kan selv velvedligeholdte cellelinjer opleve ændringer under ekspansion og opskalering. Kvalitetskontrol bør ikke være en eftertanke - det skal være en central del af produktionen. Dette begynder på skaleringsstadiet, hvor strenge ledelsessystemer og kontrollerede miljøer spiller en nøglerolle.
Kvalitetskontrol under udvidelse og skalering
Som diskuteret tidligere, er genomiske og kontamineringstests vitale, især under skalering. Overgangen fra små volumener til tusindvis af liter introducerer nye risici, hvor hver cellepassage øger chancen for mutationer. Et Quality Management System (QMS) hjælper med at håndtere disse risici effektivt. For eksempel implementerede Josep M. Canals og hans team ved Universitetet i Barcelona ISO 9001:2015 QMS mellem 2017 og 2022 for at standardisere humane pluripotente stamcellekulturer. Deres retrospektive analyse af G-bånd og aCGH-data afslørede en betydelig reduktion i kromosomale abnormiteter sammenlignet med tilstande før tilpasning[10] [13]. Kanaler fremhævede vigtigheden af løbende overvågning:
Den genetiske ustabilitet, som hPSCs viser i kultur, gør den hyppige revurdering af genomisk integritet til et essentielt krav, når man planlægger at bruge dem til eksperimenter[10].
Rutinemæssig genomisk screening er et must. Teknikker som G-bånd karyotyping og aCGH opdager strukturelle ændringer, mens Next-Generation Sequencing (NGS) identificerer mutationer på niveauer under 0,5%[5]. Vækstkurveanalyse kan også tidligt påpege problemer, såsom kontaminering eller genetisk drift[9] . Miljøovervågning tilføjer et ekstra lag af sikkerhed, med praksisser som settle plate testning og halvårlige HEPA filterkontroller, der sikrer, at produktionsmiljøet forbliver stabilt og stressfrit for cellelinjer[4].
Konsistens i medier og reagenser er lige så vigtig. Brug af serumfri, definerede medier som mTeSR1, sammen med reagenser med et analysecertifikat, hjælper med at reducere variation fra batch til batch og begrænser risikoen for viral kontaminering[10][4]. Regelmæssige morfologiske kontrol - enkle mikroskopiske observationer ved forskellige kulturtætheder - kan fange tidlige tegn på differentiering eller stress[9]. Til sourcing af specialiseret udstyr eller reagenser, platforme som
Funktionelle Assays for Produktkonsistens
Mens genomisk overvågning beskytter processen, sikrer funktionelle assays, at cellerne fungerer som tilsigtet.Genetisk stabilitet alene er ikke nok; celler skal også opretholde deres evne til at fungere korrekt på tværs af produktionsbatcher. I dyrket kød betyder det at bekræfte, at stamceller, såsom muskel-satellitceller, stadig kan differentiere til moden muskel- eller fedtvæv efter ekspansion[2] . Differentiationsanalyser er essentielle for at verificere dette.
Metaboliske analyser som MTT, LDH og Resazurin giver indsigt i cellernes sundhed og levedygtighed[4][9]. Disse, kombineret med Short Tandem Repeat (STR) profilering, hjælper med at bekræfte, at cellelinjer forbliver autentiske og fri for krydskontaminering gennem hele produktionsprocessen[1][9].
Transkriptionel analyse er et andet kritisk skridt.Xiaoyue Chen og Sam Zhang anbefaler:
cDNA frem for genomisk-DNA sekventering anbefales til mutationsdetektion for at evaluere risici på transkriptionsniveauet[5].
Denne metode tilbyder et mere præcist billede af det endelige produkt, da det afspejler, hvordan gener udtrykkes frem for blot deres genomiske placeringer. Ved at parre genomisk screening med funktionelle assays kan producenter sikre, at hver batch opfylder strenge standarder for sikkerhed, kvalitet og ydeevne på hvert trin af produktionen.
Konklusion
Opretholdelse af genetisk stabilitet er afgørende for at producere dyrket kød sikkert og konsekvent. Francisco J. Molina-Ruiz og hans kolleger fra Laboratoriet for Stamceller og Regenerativ Medicin fremhæver risiciene:
Genetiske ændringer i hPSCs kunne bringe ikke kun sikkerheden af hPSC-baserede celleprodukter i fare...men også føre til heterogen differentieringspropensitet af udgangsmaterialet, ændrede genekspressionsprofiler og ineffektivitet af det endelige celleprodukt [10].
Indsatserne er betydelige - over 531 fejlagtigt identificerede cellelinjer er blevet registreret af International Cell Line Authentication Committee [1].
At tackle disse problemer kræver en robust kvalitetskontrolramme. Dette involverer kombination af metoder som STR-profiler, G-bånd karyotypering, aCGH og avanceret NGS [5], sammen med systemer som ISO 9001:2015 for at standardisere processer og minimere kromosomale abnormiteter [13].
Økonomiske faktorer driver også behovet for disse foranstaltninger.Genetisk drift kan resultere i, at muterede celler får en vækstfordel, hvilket potentielt kan ødelægge hele produktionspartier [10][11]. Med det voksende fokus på humane pluripotente stamceller har efterspørgslen efter stabile cellelinjer aldrig været større. Som professor David L. Kaplan fra Tufts University forklarer:
Immortaliserede cellelinjer betragtes generelt som en nødvendighed for genereringen af store mængder spiseligt væv fra en stabil, robust bioproces [14].
For producenter af dyrket kød skal kvalitetskontrol være indlejret i hvert trin - fra plasmidscreening til overvågning af storskalaproduktion. Ved at kombinere grundig testning med forebyggende strategier kan producenter sikre konsistente og pålidelige resultater.
Ofte stillede spørgsmål
Hvor ofte skal genetisk stabilitetstest udføres under opskalering?
Genetisk stabilitetstest er et afgørende skridt under opskalering og bør udføres regelmæssigt. Hvor ofte denne test udføres, afhænger i høj grad af den specifikke cellelinje og den pågældende proces. For at reducere risikoen for mutationer og opretholde cellernes stamcelleegenskaber er det klogt at etablere en passagegrænse baseret på genetisk analyse.
Hvilke tests opdager bedst små mutationer og store kromosomændringer?
Tests såsom SNP-array-analyse og genom-dækkende SNP-genotyping er e
Hvad er den enkleste måde at forhindre genetisk drift på tværs af produktionsbatcher?
For at minimere genetisk drift er det afgørende at udføre regelmæssige genetiske og funktionelle analyser af cellelinjer og begrænse antallet af passager, de gennemgår. Implementer praksisser som at etablere mastercellebanker og rutinemæssigt kontrollere genetisk stabilitet, som anbefalet i kvalitetskontrolprotokoller. Disse foranstaltninger er nøglen til at opretholde konsistens og sikre pålidelige resultater på tværs af forskellige produktionsbatcher.











