Bioreaktoreiden skaalaaminen viljellyn lihan tuotantoon on monimutkaista, erityisesti kun hallitaan leikkausjännitystä, mekaanista voimaa, joka voi vahingoittaa nisäkässoluja skaalausprosessin aikana. Toisin kuin mikrobisolut, nisäkässolut ovat hauraita ja herkkiä turbulenssille ja ilmastusvoimille. Kun leikkausjännitys ylittää 3 Pa, solut voivat rikkoutua, mikä vähentää elinkelpoisuutta ja tuottavuutta.
Näiden haasteiden ratkaisemiseksi insinöörit luottavat laskennalliseen virtausdynamiikkaan (CFD) ja skaalausmallit ennustamaan ja hallitsemaan leikkausjännitystä ennen täysimittaista tuotantoa. CFD analysoi virtauskuvioita, leikkausalueita ja sekoitustehokkuutta bioreaktoreissa, kun taas skaalausmallit vahvistavat nämä ennusteet kokeellisesti, minimoiden riskit skaalausprosessin aikana.
Keskeiset huomiot:
- Leikkausjännityksen rajat: Nisäkässolut sietävät enintään 3 Pa; tämän ylittäminen vahingoittaa soluja.
- CFD-työkalut: Kehittyneet menetelmät, kuten Large Eddy Simulations (LES) ja Lattice-Boltzmann -simulaatiot (LB-LES), mahdollistavat tarkan virtauksen ja turbulenssin mallinnuksen.
- Pienennysmallit: Nämä jäljittelevät suurten bioreaktoreiden olosuhteita pienemmissä kokoonpanoissa CFD-ennusteiden validointiin.
-
Suunnittelun huomioitavat seikat:
- Käytä kaltevan terän juoksupyöriä alhaisemman leikkausvoiman saavuttamiseksi.
- Pidä Kolmogorovin pyörteiden pituudet yli 20 μm soluvaurioiden estämiseksi.
- Pidä juoksupyörän kärjen nopeudet alle 1,5 m/s.
Yhdistämällä CFD-tietoa kokeelliseen validointiin, tiimit voivat optimoida bioreaktorien suunnittelua viljellyn lihan tuotantoon, varmistaen solujen selviytymisen ja tehokkaan skaalaamisen.
CFD-kompassi | Parhaat käytännöt bioreaktorin CFD:lle
Laskennallisen fluididynamiikan (CFD) käyttö leikkausjännityksen mallintamiseen
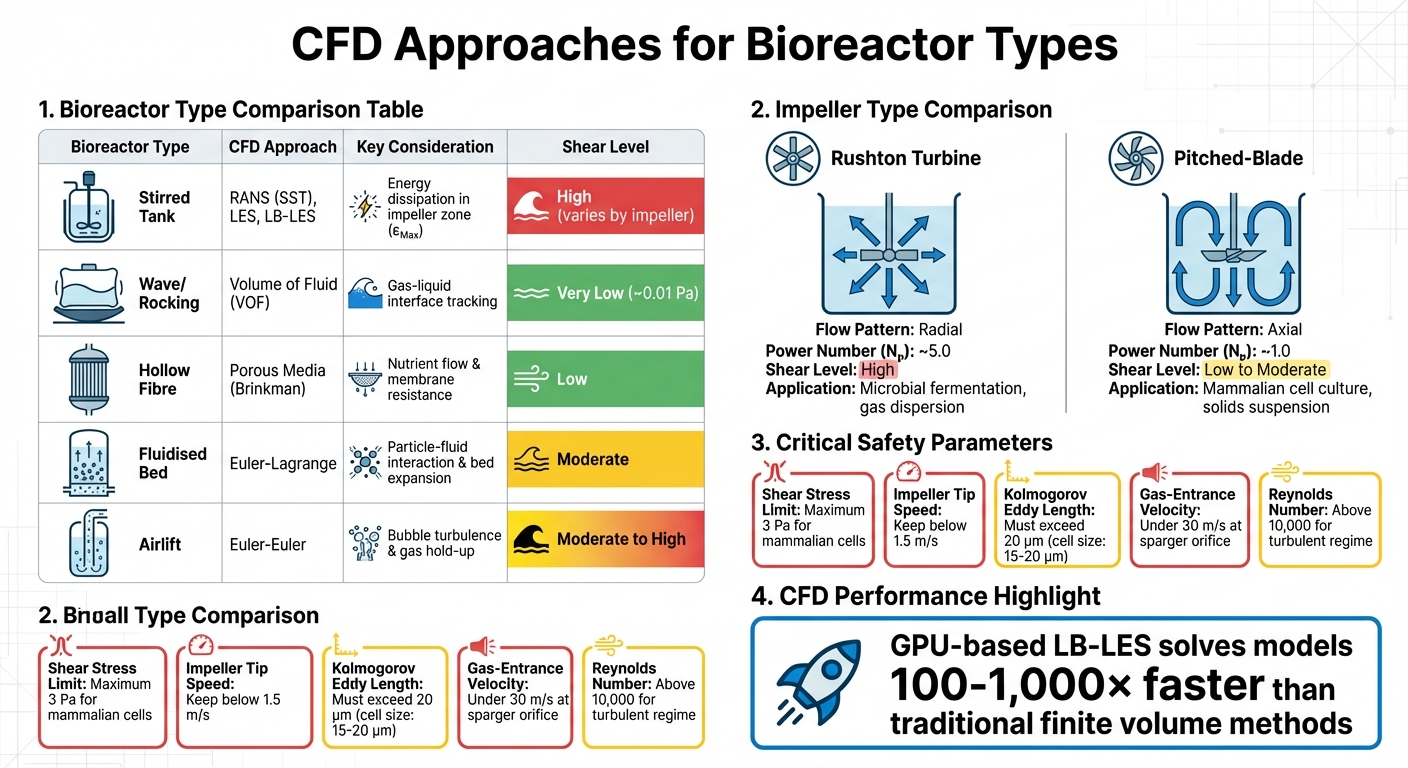
CFD-lähestymistavat ja keskeiset parametrit eri bioreaktorityypeille viljellyn lihan tuotannossa
CFD-simulaatiot antavat insinööreille työkalut kartoittaa fluididynamiikkaa ja leikkausvoimia bioreaktoreissa ennen niiden fyysistä rakentamista. Sen sijaan, että luotettaisiin kokeilu- ja erehdysmenetelmiin tuotantomittakaavassa, CFD auttaa ennustamaan kriittisiä tekijöitä, kuten korkean leikkauksen alueita, turbulentteja pyörteitä ja solujen elinkelpoisuutta tietyissä astian osissa. Tämä on erityisen tärkeää viljellyn lihan tuotannossa, jossa bioreaktorien mittakaava voi lopulta saavuttaa 200 000 litraa - paljon suurempia kuin perinteiset biofarmaseuttiset astiat [8]. Nämä ennakoivat näkemykset ohjaavat mittakaavan pienentämiskokeita ja vaikuttavat laitteiden valintaan.
Laskennallisten tekniikoiden kehitys on ollut merkittävää. Vaikka Reynolds-Averaged Navier-Stokes (RANS) -mallit, kuten k-ε, ovat edelleen laajalti käytössä teollisuudessa, edistyneet menetelmät, kuten Large Eddy Simulations (LES) ja GPU-tehostetut Lattice-Boltzmann -simulaatiot (LB-LES), rikkovat rajoja. Kuten professori Miroslav Soos Prahan kemian ja teknologian yliopistosta toteaa, GPU-pohjaiset LB-LES voivat ratkaista malleja "100-1 000 kertaa nopeammin kuin yleisesti käytetyt äärellisen tilavuuden menetelmän ratkaisijat" [2]. Tämä nopeusetu mahdollistaa insinöörien simuloida massiivisia aluksia tarkkuudella, joka on tarpeen soluvaurioita aiheuttavien pyörteiden havaitsemiseksi.
CFD:n kykyjen käytännön esimerkki tulee Regeneron Ireland DAC ja Thermo Fisher Scientific -tutkijoilta. He onnistuivat skaalaamaan soluviljelyprosessin 2 000 litran bioreaktorista geometrisesti erilaiseen 5 000 litran kertakäyttöiseen bioreaktoriin.Sen sijaan, että he olisivat luottaneet empiirisiin heuristiikkoihin, he käyttivät CFD:tä analysoidakseen parametreja, kuten massansiirtonopeuksia, sekoitusaikoja ja leikkausnopeuksia. Tämä lähestymistapa mahdollisti onnistuneen skaalaamisen ensimmäisellä yrityksellä, välttäen kalliit epäonnistumiset, jotka usein liittyvät teho-tilavuus-suhteeseen perustuvaan skaalaamiseen [5].
CFD:n Asetukset Sekoitetuille Säiliöbioreaktoreille
CFD:n asettamiseksi sekoitetuille säiliöbioreaktoreille aloita määrittelemällä säiliön geometria - tämä sisältää säiliön mitat, juoksupyörän suunnittelun (e.g., Rushton tai kaltevalapainen terä) ja ohjauslevyjen sijoittelun. Oikean turbulenssimallin valinta on ratkaisevaa: realisoitu k-ε-malli toimii hyvin kaasu-nestejärjestelmissä, kun taas LB-LES tarjoaa korkeamman resoluution huippujännitysten tunnistamiseen, jotka voisivat vahingoittaa soluja. Verkkokonvergenssitutkimus varmistaa, että tulokset eivät riipu verkon koosta.
Reunaehtojen on heijastettava todellisia käyttöparametreja, kuten juoksupyörän nopeutta, kaasun syöttönopeuksia, nesteen tiheyttä ja viskositeettia. Viljellyn lihan sovelluksissa käytetään usein konservatiivisia kuplavastuksen malleja leikkausjännityksen arvioimiseksi [8]. Järjestelmän tulisi toimia täysin turbulentissa tilassa, jossa Reynoldsin luvut ylittävät 10 000, jotta teholuku pysyy johdonmukaisena riippumatta juoksupyörän nopeudesta [1].
CFD-ennusteiden hapensiirrosta, sekoitusajoista ja hydrodynaamisesta rasituksesta tulisi olla linjassa kokeellisten tietojen kanssa, jotka on kerätty leikkausherkillä mikroskoettimilla tai nanopartikkelien aggregaateilla [2]. Esimerkiksi matemaattinen massansiirtomalli ohjasi CHO-soluviljelyprosessin suoraa skaalausta 2 litran pöytämalliyksiköstä 1 500 litran teolliseen bioreaktoriin Sartorius.Käyttämällä CFD:tä ennustamaan hapenkulutusta ja CO₂:n poistamista, tiimi säilytti johdonmukaiset tuotteen laatuominaisuudet - kuten N-glykaanit ja varausvariantit - eri mittakaavoissa [6].
CFD muille bioreaktorityypeille
Vaikka sekoitetut säiliöt hallitsevat teollista soluviljelyä, muut bioreaktorisuunnitelmat vaativat räätälöityjä CFD-lähestymistapoja. Esimerkiksi keinuvat tai aaltobioreaktorit käyttävät Volume of Fluid (VOF) -menetelmää simuloimaan kaasu-neste rajapintaa, sillä aaltoliike aiheuttaa leikkausjännitystä näissä järjestelmissä. Nämä suunnitelmat luovat paljon lempeämpiä leikkausympäristöjä - maksimijännitys on noin 0,01 Pa verrattuna sekoitettuihin säiliöihin - mutta niiden skaalautuvuus on rajallinen suurimittakaavaisessa viljellyn lihan tuotannossa [4].
Ontelokuitubioreaktorit puolestaan käyttävät huokoisten aineiden malleja, jotka perustuvat Brinkmanin yhtälöihin simuloimaan ravinteiden diffuusiota ja virtausvastusta kalvojen läpi.Fluidisoidut petijärjestelmät vaativat Euler-Lagrange-malleja hiukkas-nestevuorovaikutusten ja petilaajenemisen mallintamiseen, kun taas ilmankiertobioreaktorit käyttävät Euler-Euler-menetelmiä kuplien aiheuttaman turbulenssin ja kaasun pidätyksen analysointiin [4]. Jokaisella suunnittelulla on omat haasteensa: fluidisoiduissa petijärjestelmissä on tasapainotettava mikrokantajien jakautuminen leikkausaltistuksen kanssa, kun taas ilmankiertojärjestelmissä on hallittava kuplien puhkeamisesta aiheutuvia jännityksiä, jotka ovat johtava solukuoleman syy ilmastetuissa bioreaktoreissa [1] [7] .
Näiden CFD-lähestymistapojen ymmärtäminen on olennaista leikkausjännityksen hallitsemiseksi eri bioreaktorisuunnitelmissa, joita käytetään viljellyn lihan tuotannossa.
| Bioreaktorin tyyppi | CFD-lähestymistapa | Keskeinen huomioitava asia |
|---|---|---|
| Sekoitetun säiliön | RANS (SST), LES, LB-LES | Energian dissipaatio juoksupyörän alueella (εMax) |
| Aalto/Keinunta | Nesteen tilavuus (VOF) | Kaasu-neste rajapinnan seuranta |
| Ontto kuitu | Huokoinen media (Brinkman) | Ravinteiden virtaus ja kalvon vastus |
| Nestevuode | Euler-Lagrange | Hiukkasten ja nesteen välinen vuorovaikutus, vuoteen laajeneminen |
| Ilmanostin | Euler-Euler | Kaasukuplien aiheuttama turbulenssi ja kaasun pidättyminen |
Nämä erilaiset CFD-menetelmät korostavat räätälöityjen strategioiden tarvetta, jotka ovat keskeisessä asemassa laitteiden valinnassa ja leikkausjännityksen hallinnassa.
Pienennetyt mallit ja kokeellinen validointi
Vaikka laskennallinen virtausdynamiikka (CFD) tarjoaa arvokkaita ennusteita, se ei voi korvata todellisen maailman testauksen tarvetta prosessien skaalaamisessa. Kokeellinen validointi on ratkaisevan tärkeää varmistettaessa, että laskennalliset mallit edustavat tarkasti todellisia leikkausjännitysolosuhteita. Tässä pienennetyt mallit astuvat kuvaan, jäljitellen suurten tuotantobioreaktoreiden hydrodynaamista ympäristöä pienemmissä, helpommin hallittavissa järjestelmissä. Näin tekemällä ne vähentävät kalliiden virheiden riskiä siirryttäessä pienimuotoisista teollisen mittakaavan toimintoihin. Tämä vaihe ei ainoastaan vahvista CFD-ennusteita, vaan myös varmistaa luotettavamman ja tehokkaamman skaalausprosessin.
Pienennettyjen mallien luominen
Pienennetyn mallin suunnittelu alkaa geometrisen samankaltaisuuden ylläpitämisellä.Tämä tarkoittaa, että avainkomponenttien, kuten säiliön korkeuden ja halkaisijan sekä juoksupyörän halkaisijan ja säiliön halkaisijan, välinen suhde säilytetään samana [11]. Kun geometria on kohdallaan, insinöörit valitsevat skaalauskriteerin. Yleisiä valintoja ovat teho tilavuusyksikköä kohti (P/V), juoksupyörän kärjen nopeus tai energian hajontanopeus (EDR). Kuitenkin keskittyminen paikalliseen EDR:ään keskimääräisen P/V:n sijaan antaa paremman käsityksen leikkausheterogeenisuudesta, mikä on kriittistä tarkan mallinnuksen kannalta.
Edistyneempi lähestymistapa sisältää moniosastoiset simulaattorit. Esimerkiksi helmikuussa 2021 Emmanuel Anane ja hänen tiiminsä kehittivät kaksiosastoisen skaalausalasimulaattorin, joka yhdistää sekoitetun säiliöreaktorin (STR) ja tulppavirtausreaktorin (PFR). Tätä mallia käytettiin tutkimaan, miten CHO-solut reagoivat liuenneen hapen gradientteihin. Heidän tutkimuksensa paljasti kriittisen viipymäaikakynnyksen, joka on 90 sekuntia.Tämän pisteen jälkeen CHO-solut osoittivat 15% elinkelpoisten solujen tiheyden laskua ja laktaatin kertymisen lisääntymistä [10]. Tämä havainto tarjoaa selkeän vertailukohdan teollisten bioreaktoreiden suunnittelulle, jotka ylläpitävät solujen elinkelpoisuutta.
Solukasvun turvaamiseksi insinöörit pyrkivät usein pitämään juoksupyörän kärjen nopeudet alle 1,5 m/s [1]. Lisäksi Kolmogorovin mikrokiertopituuden - turbulenssin mitta - tulisi ylittää solujen koko, tyypillisesti 20 μm tai enemmän nisäkässoluille, jotta vältetään hydrodynaaminen vaurio [1][3]. Esimerkiksi, kun energiansyöttö on 0,1 W/kg eläinsoluviljelmissä, pienimmät pyörteet ovat noin 60 μm, tarjoten turvallisen puskurin [3].
Kokeellisten CFD-ennusteiden validointi
Kun pienoismalli on käytössä, kokeelliset menetelmät ovat olennaisia CFD:stä johdettujen parametrien validoinnissa. Partikkelikuvanopeusmittaus (PIV) on laajalti käytetty tekniikka tähän tarkoitukseen. Seuraamalla hiukkasia nesteessä, PIV auttaa vahvistamaan, vastaavatko pienoismallin virtauskuviot ja nopeuskentät CFD-ennusteita [12][4].
Jälkivärjäys- ja värinpoistomenetelmiä käytetään myös sekoitusaikojen validointiin. Tässä prosessissa jälkivärjäysaineita, kuten happoja, emäksiä tai suolaliuoksia, lisätään lähelle juoksupyörää, ja niiden jakautumista seurataan, kunnes 95% homogeenisuus saavutetaan [12][3] .Suurikokoisissa nisäkässolubioreaktoreissa (5 000 L - 20 000 L) sekoitusajat vaihtelevat tyypillisesti 80 - 180 sekunnin välillä [10].
Maaliskuussa 2020 James Scully ja hänen tiiminsä Regeneron Ireland DAC:ssä onnistuivat skaalaamaan soluviljelyprosessin 2 000 L bioreaktorista 5 000 L kertakäyttöiseen bioreaktoriin, jolla oli erilainen geometria. He luottivat CFD:hen ennustaakseen keskeisiä parametreja, kuten massansiirtonopeuksia, sekoitusaikoja ja leikkausnopeuksia. Nämä ennusteet validoitiin sitten yksivaiheisilla ja monivaiheisilla kokeilla, mikä mahdollisti onnistuneen ensimmäisen yrityksen skaalata ilman suurikokoisia pilottikokeita [5].
"CFD-simulaatioita käytetään yhä enemmän täydentämään klassisia prosessitekniikan tutkimuksia laboratoriossa tilallisesti ja ajallisesti ratkaistuilla tuloksilla tai jopa korvaamaan ne, kun laboratoriotutkimukset eivät ole mahdollisia." - Stefan Seidel, School of Life Sciences, ZHAW [12]
Lisävalidointitekniikoihin kuuluu vääntömomentin mittaus tietyn tehon syötön (P/V) ja ulottuvuudettomien teholukujen vahvistamiseksi tietyillä sekoitusnopeuksilla [12][3]. Happensiirtonopeudet varmistetaan menetelmillä, kuten kaasunpoisto- tai sulfiittitekniikoilla, jotka määrittävät tilavuuskohtaisen hapen massansiirtokertoimen (kLa) [12][7]. Mikrokantajia käyttävissä järjestelmissä käytetään valon vaimenemista tai kameraperusteisia menetelmiä, jotta löydetään vähimmäisnopeus, joka tarvitaan kaikkien partikkelien suspendoimiseksi, varmistaen, että CFD-ennusteet kiinteän faasin jakautumisesta ovat tarkkoja [12][4].
sbb-itb-ffee270
Tekijät, jotka vaikuttavat leikkausjännitykseen bioreaktoreissa
Solujen elinkelpoisuuden suojelemiseksi skaalausprosessin aikana on tärkeää ymmärtää leikkausjännitystä ohjaavat fyysiset tekijät. Laskennallisen virtausdynamiikan (CFD) ennusteet ja skaalausalennusvalidaatiot paljastavat, että energian hajoamisnopeudella (EDR) on keskeinen rooli. EDR mittaa, kuinka juoksupyörän kineettinen energia muuttuu lämmöksi, mikä johtaa epätasaiseen energian jakautumiseen. Esimerkiksi kaltevan terän juoksupyörissä energia keskittyy yleensä juoksupyörän ympärille, luoden korkean leikkauksen alueita, jotka voivat vahingoittaa soluja, ellei niitä hallita asianmukaisesti.
Juoksupyörän suunnittelu ja tehonsyöttö
Juoksupyörän tyyppi vaikuttaa merkittävästi virtauskuvioihin ja leikkausintensiteettiin. Esimerkiksi Rushton-turbiinit tuottavat säteittäistä virtausta ja korkeaa leikkausta, mikä tekee niistä ihanteellisia mikrobikäymiseen, mutta vähemmän sopivia leikkausherkille nisäkässoluille.Toisaalta, kaltevat siipipyörät luovat aksiaalivirtausta alhaisemmalla leikkausvoimalla ja paremmalla pumppaustehokkuudella samalla tehonsyötöllä. Tämä tekee niistä suositun valinnan sovelluksille, kuten viljellyn lihan tuotannolle, jossa solujen elinkelpoisuus on etusijalla.
| Siipipyörän tyyppi | Virtauskuvio | Teholuku (Nₚ) | Leikkaustaso | Pääasiallinen sovellus |
|---|---|---|---|---|
| Rushton-turbiini | Radiaalinen | ~5.0 | Korkea | Mikrobien fermentointi; kaasun dispergointi[3] |
| Kalteva siipipyörä | Aksiaalinen | ~1.0 | Matala tai kohtalainen | Eläinsoluviljelmä; kiintoaineiden suspensio [3] |
Skaalausstrategiat perustuvat usein vakion tehon syöttöön tilavuutta kohti (P/V). Kuitenkin, kun reaktorin koko kasvaa, tämä voi johtaa korkeampiin juoksupyörän kärjen nopeuksiin. Eläinsoluille kärjen nopeuksien tulisi pysyä alle 1,5 m/s välttääkseen kasvuhäiriöitä [1]. Suurissa reaktoreissa ilmastus voi aiheuttaa vielä enemmän hydrodynaamista rasitusta kuin juoksupyörät, erityisesti astioissa, jotka ylittävät 20 m³ [9] . Nämä tekijät liittyvät läheisesti turbulenssiin, jota käsitellään tarkemmin Kolmogorovin skaalan keskustelussa.
Kolmogorovin skaala ja turbulenssimallinnus
Kolmogorovin skaala (λ) määrittää pienimpien turbulenttien pyörteiden koon, joissa energia häviää lämpönä.Jos nämä pyörteet ovat pienempiä kuin solun halkaisija, mekaaninen vaurio voi olla huolenaihe. Nisäkässoluille, jotka ovat tyypillisesti 15–20 μm kokoisia, pyörteen pituuden on oltava yli 20 μm vaurioiden välttämiseksi [1][3]. Esimerkiksi, kun energiansyöttö on 0,1 W/kg, Kolmogorovin pyörteen halkaisija on noin 60 μm, mikä tarjoaa turvallisen puskurin [3].
"Jos biologiset yksiköt (e.g., nisäkässolut) ovat pienempiä kuin λ [Kolmogorovin mittakaava] bioreaktorissa, niin leikkausvaurioita ei tapahdu." - Muhammad Arshad Chaudhry [3]
Elokuussa 2024, Boehringer Ingelheim Pharma ja Prahan kemian ja teknologian yliopiston tutkijat käyttivät Lattice-Boltzmann Large Eddy Simulations (LB-LES) -simulaatioita validoidakseen CFD-ennusteet 12 500 L teollisessa bioreaktorissa.Käyttämällä leikkausherkkiä nanopartikkelien aggregaatteja, he mittasivat maksimaalisen hydrodynaamisen rasituksen ja osoittivat, että LB-LES voisi ratkaista turbulenttisia mittakaavoja 100–1 000 kertaa nopeammin kuin perinteiset menetelmät [2]. Nämä havainnot ovat keskeisiä strategioiden kehittämisessä leikkausrasituksen minimoimiseksi.
Leikkausrasituksen vähentäminen mallinnustietojen avulla
CFD-mallinnus mahdollistaa insinöörien tunnistaa korkean leikkausrasituksen alueet ja säätää käyttöolosuhteita vastaavasti. Yksi tehokas lähestymistapa on lisätä substraatteja, pH-pohjia tai vaahdonestoaineita lähellä juoksupyörän aluetta sen sijaan, että ne lisättäisiin nesteen pinnalle. Tämä varmistaa nopean jakautumisen ja minimoi paikalliset pitoisuusgradientit [3]. Viljellyn lihan tuotannossa liiallinen leikkaus voi irrottaa soluja mikrokantajista, kun taas riittämätön sekoitus johtaa mikrokantajien laskeutumiseen ja ravinne-epätasapainoon [9].
Suojaavat lisäaineet, kuten Pluronic F-68 (Poloxamer 188), ovat yleisesti käytössä suojaamaan soluja leikkausvoimilta, erityisesti kuplien puhkeamisesta nesteen pinnalla aiheutuvilta - merkittävä solukuoleman aiheuttaja bioreaktoreissa [1]. Näiden pinta-aktiivisten aineiden avulla on raportoitu jopa 100 000 W/m³ energiansyöttöjä ilman tappavia vaikutuksia [1]. Lisäksi kaasun sisääntulonopeuden pitäminen alle 30 m/s spargerin aukossa auttaa vähentämään tuottavuuden menetyksiä ja solukuolleisuutta [1].
Laitteiden löytäminen bioreaktorin skaalaamiseen
Kuinka Cellbase tukee bioreaktorien hankintaa
Bioreaktoreiden skaalaaminen viljellyn lihan tuotantoon tuo mukanaan omat haasteensa. Tässä
Käyttäessään
Bioreaktoreiden onnistunut skaalaus biolääkealalla vaikuttaa merkittävästi näiden tuotteiden laatuun ja markkinoille pääsyn nopeuteen [5].
Hyödyntämällä CFD-pohjaista dataa, tiimit voivat tehostaa laitteiden valintaa ja minimoida toistuvien kokeilujen tarpeen [5]. Nämä oivallukset ovat ratkaisevia valittaessa bioreaktoreita, jotka on suunniteltu optimaalinen leikkausjännityksen hallinta mielessä.
Laitteiden valinta leikkausjännityksen hallintaan
Leikkausjännityksen tehokkaaseen hallintaan tietyt laitteiden tekniset tiedot ovat erityisen tärkeitä. Juoksupyörän geometria on keskeinen tekijä. Esimerkiksi kaltevat siipipyörät tuottavat aksiaalivirtausta tehonumerolla (Np) noin 1,0, kun taas Rushton-turbiineilla on huomattavasti korkeampi Np, noin 5,0.Tämä tarkoittaa, että kaltevat teräsuunnitelmat tuottavat merkittävästi vähemmän tehoa ja siten vähemmän leikkausta samalla pyörimisnopeudella [3]. Sovelluksissa, jotka koskevat nisäkässoluja viljellyssä lihassa, on tärkeää pitää juoksupyörän kärjen nopeus alle 1,5 m/s soluvaurioiden välttämiseksi [1].
Spargerin konfiguraatio on toinen kriittinen huomioitava seikka. Liiallisen leikkauksen estämiseksi laitteiden tulisi varmistaa, että kaasun sisääntulonopeus spargerin aukossa pysyy alle 30 m/s ja aukon Reynoldsin luku alle 2 000. Näiden kynnysten ylittäminen voi johtaa "suihkujärjestelmään", jossa kuplat hajaantuvat epätasaisesti ja luovat paikallisia leikkausalueita [1]. Pora-aukkoiset tai avoimet putkispargerit sopivat paremmin leikkausherkille soluille verrattuna mikrospargereihin. Lisäksi laitteiden tulisi tukea skaalautuvuutta alaspäin. Toimittajat, jotka tarjoavat penkkimallisia malleja (e.g., 3 L järjestelmät), jotka ovat geometrisesti samanlaisia kuin laajamittaiset järjestelmät (2 000 L tai enemmän), mahdollistavat tiimien validoida CFD-ennusteet pienemmässä mittakaavassa ennen siirtymistä täysimittaiseen tuotantoon [1][2].
Päätelmä
Bioreaktoreiden skaalaaminen viljellyn lihan tuotantoon vaatii siirtymistä perinteisistä yritys-ja-erehdysmenetelmistä mallipohjaisiin strategioihin paikallisten leikkauserojen käsittelemiseksi. Laskennallinen virtausdynamiikka (CFD) on tullut keskeiseksi työkaluksi tässä prosessissa, mikä mahdollistaa insinöörien ennustaa hydrodynaamisia ympäristöjä ja visualisoida leikkausalueita yksinkertaisten teho-tilavuus-suhteiden ulkopuolella [1]. Noudattamalla kriittisiä parametreja - kuten pitämällä Kolmogorovin pyörteiden pituudet yli 20 μm ja juoksupyörän kärjen nopeudet alle 1,5 m/s - insinöörit voivat suojata nisäkässoluja leikkausvaurioilta samalla varmistaen asianmukaisen sekoituksen ja hapensiirron [1].
Kehittyneet laskentamenetelmät, kuten Large Eddy Simulation (LES) ja Lattice-Boltzmann -tekniikat, ovat osoittaneet tehokkuutensa prosessien skaalaamisessa. Esimerkiksi maaliskuussa 2020 Regeneron Ireland DAC onnistui skaalaamaan soluviljelyprosessin 2 000 litran bioreaktorista geometrisesti erilaiseen 5 000 litran kertakäyttöjärjestelmään ensimmäisellä yrityksellä. Tämä saavutettiin käyttämällä moniparametrisia CFD-ennusteita, mikä poisti laajojen fyysisten kokeiden tarpeen [5]. Tämä "ensimmäisellä kerralla oikein" -strategia ei ainoastaan vähennä kontaminaatioriskejä, vaan myös lyhentää markkinoille pääsyä - mikä on kriittistä viljellyn lihan sektorille.
Kokeelliset validointimenetelmät, kuten hiukkaskuvanopeusmittaus (PIV), vahvistavat edelleen CFD-mallien tarkkuuden [2]. Nämä validoidut mallit ovat nyt keskeisessä roolissa hankintapäätöksissä.Yritykset, kuten
Usein kysytyt kysymykset
Miten laskennallinen virtausdynamiikka (CFD) tukee bioreaktorien skaalausta viljellyn lihan tuotannossa?
Laskennallinen virtausdynamiikka (CFD) on mullistava tekijä, kun on kyse bioreaktorien skaalaamisesta viljellyn lihan tuotantoon. Se tarjoaa syvällisen ymmärryksen virtausdynamiikasta, leikkausjännityksestä, sekoitustehokkuudesta ja massansiirtonopeuksista - kaikki kriittisiä tekijöitä solujen kasvulle ihanteellisen ympäristön luomiseksi.
CFD:n avulla insinöörit voivat optimoida olennaisia elementtejä, kuten juoksupyörän suunnittelua, sekoitusnopeutta ja kaasun syöttöä. Tämä varmistaa, että bioreaktorit toimivat parhaissa mahdollisissa olosuhteissa, suojaten sekä solujen terveyttä että tuottavuutta.
Lisäksi CFD mahdollistaa siirtymisen pienistä laboratoriokokoonpanoista suuriin teollisen mittakaavan bioreaktoreihin ilman tehokkuuden tai johdonmukaisuuden heikkenemistä. Tämä tarkoittaa, että viljellyn lihan tuotanto voi laajentua sujuvasti säilyttäen korkeat standardit.
Mikä tekee Large Eddy Simulations (LES) -menetelmistä parempia kuin perinteiset menetelmät bioreaktorimallinnuksessa?
Large Eddy Simulations (LES) tarjoaa syvemmän ja tarkemman näkemyksen turbulentista virtauksesta bioreaktoreissa verrattuna perinteisiin menetelmiin, kuten Reynolds-averaged Navier-Stokes (RANS).Keskittymällä suurikokoisiin pyörteisiin ja mallintamalla vain pienimmät dissipatiiviset liikkeet, LES voi tunnistaa kriittiset leikkausjännityksen hotspotit, kuten pyörteiden aiheuttamat korkean leikkauksen alueet, jotka muuten saattaisivat jäädä huomaamatta. Tämä yksityiskohtaisuuden taso on keskeisessä roolissa soluvaurioiden vähentämisessä ja luotettavuuden varmistamisessa kasvatetun lihan tuotannon laajentamisessa.
Toisin kuin menetelmät, jotka ovat voimakkaasti riippuvaisia empiirisistä korrelaatioista, LES tarjoaa vahvempia ennustekykyjä siirryttäessä laboratoriomittakaavasta teollisuusmittakaavan bioreaktoreihin. Laskentatekniikoiden edistysaskeleet ovat myös tehneet LES:stä helpommin saatavilla, mahdollistaen yksityiskohtaiset simulaatiot ilman kohtuuttomia laskentaresursseja. Yrityksille, jotka pyrkivät integroimaan LES-pohjaisia suunnitelmia,
Miksi on tärkeää pitää Kolmogorovin pyörteiden pituudet yli 20 µm nisäkässolujen elinkelpoisuuden kannalta?
Kolmogorovin pyörteiden pituuksien ylläpitäminen yli noin 20 µm on ratkaisevan tärkeää nisäkässolujen suojelemiseksi bioreaktoritoimintojen aikana. Kun nämä turbulentit pyörteet kutistuvat solujen kokoa pienemmiksi, ne voivat altistaa solut liialliselle leikkausjännitykselle, mikä voi vahingoittaa niiden kalvoja ja heikentää solujen elinkelpoisuutta.
Pienimpien turbulenttien rakenteiden pitäminen soluja suurempina auttaa vähentämään mekaanisten vaurioiden riskiä. Tämä ei ainoastaan edistä terveempiä soluviljelmiä, vaan myös parantaa bioreaktorin yleistä suorituskykyä. Tämä huomio on vielä tärkeämpi bioreaktorin skaalaamisessa, jossa johdonmukaisten leikkausjännitysolosuhteiden varmistaminen on huomattavasti vaikeampaa.











