Geneettinen stabiilisuus on kriittinen viljellyn lihan tuotannossa. Ilman sitä solulinjat voivat mutatoitua, mikä johtaa epätasaiseen laatuun, turvallisuusriskeihin ja tuotannon epäonnistumisiin. Solujen määrän kasvattaminen tuhansista biljooniin lisää näitä riskejä, mikä tekee vankkojen laadunvalvontajärjestelmien olemassaolon välttämättömäksi. Sääntelyviranomaiset, kuten FDA ja EMA, vaativat todisteita stabiilisuudesta ennen tuotteiden hyväksymistä, sillä jopa pienet geneettiset muutokset voivat aiheuttaa allergisia tai haitallisia seurauksia.
Tärkeimpiä haasteita ovat geneettinen ajautuminen, mutaatioiden kertyminen ja onkogeenien aktivoituminen. Nämä ongelmat johtuvat solujen pitkäaikaisesta passagoinnista, valintapaineista ja ympäristön stressitekijöistä tuotannon aikana. Kehittyneet testausmenetelmät, kuten karyotyypitys, SNP-arrayt ja seuraavan sukupolven sekvensointi (NGS), auttavat havaitsemaan ja käsittelemään näitä riskejä. Ennaltaehkäisevät strategiat, kuten rakenteellinen solupankkitoiminta ja kohdennettu geenitekniikka, suojaavat edelleen epävakaudelta.
Tuottajien on integroitava laadunvalvonta tuotannon jokaiseen vaiheeseen - solupankista suurikokoisiin bioreaktoreihin. Työkalut, kuten STR-profilointi, kontaminaatiotestit ja toiminnalliset analyysit, varmistavat johdonmukaisuuden ja turvallisuuden. Alustat, kuten
Solulinjan kehityksen nopeuttaminen DNA:sta pääsolupankkiin - AGC Biologics
Yleiset haasteet geneettisen vakauden ylläpitämisessä
Geneettisen vakauden varmistaminen viljellyn lihan tuotantosyklin aikana ei ole helppo tehtävä. Tuotannon valtava mittakaava tarjoaa runsaasti mahdollisuuksia geneettisten muutosten kehittymiselle ja leviämiselle. Näiden haasteiden tunnistaminen on avain tehokkaiden laadunvalvontajärjestelmien käyttöönottoon.
Geneettinen ajautuminen ja mutaatioiden kertyminen
Laajennettu solujen passaus on merkittävä genomin epävakauden lähde viljellyn lihan tuotannossa. Kuolemattomat solulinjat ovat luonteeltaan alttiita genomisille muutoksille, mikä voi johtaa spontaaniin mutaatioihin pitkäaikaisen viljelyn aikana [6][5]. Kun solut käyvät läpi useita populaation kaksinkertaistumisia, DNA-replikaation virheet kasaantuvat, mikä johtaa monimuotoisiin solupopulaatioihin ja mahdollisesti toiminnan menetykseen. Christopher Frye ja Luhong He BioPharm International korostavat tätä ongelmaa:
Kloonaalisesti johdetut CHO-solulinjat on usein havaittu eriytyvän, jolloin niistä tulee heterogeeninen populaatio pitkien alaviljelyjaksojen aikana [6].
Teollisuusympäristöissä noin 20% tuotantosolulinjoista osoittaa huomattavaa transgeenien heterogeenisyyttä peräkkäisten sukupolvien aikana [6] . Nämä mutaatiot voivat tapahtua varhain, DNA-replikaation aikana transfektion jälkeen, tai virheiden vuoksi, kun vieraat geenit integroituvat isäntägenomiin [5].
&Selektiiviset paineet lisäävät monimutkaisuutta. Aineet kuten antibiootit ja metaboliset merkkiaineet (e.g. , MTX), joita käytetään solulinjojen stabilointiin, voivat itse asiassa lisätä mutaatiotaajuuksia [6][5]. Joissakin tapauksissa mitä korkeampi näiden aineiden pitoisuus on, sitä korkeampi on mutaatiotaajuus [6]. Ympäristön stressitekijät - kuten ravinnepula, epäoptimaaliset viljelyolosuhteet laajennuksen aikana ja fyysinen stressi laajentumisesta - voivat edelleen horjuttaa geneettistä eheyttä [6][5].Shuai Wang, Solulinjan kehityksen johtaja WuXi Biologics, huomauttaa:
Mutaatioiden tasot voivat muuttua solujen passagoinnin aikana kiinalaisen hamsterin munasarjasolujen (CHO) genomin plastisuuden vuoksi [5].
Epigeneettiset muutokset vaikuttavat myös. Transgeenit voivat osittain tai kokonaan kadota tai hiljentyä viljelyprosessin aikana, mikä vaikuttaa pitkäaikaiseen stabiilisuuteen. Nämä kertyneet mutaatiot eivät ainoastaan vahingoita solujen toimintaa, vaan myös lisäävät onkogeenien aktivoitumisriskiä.
Onkogeenien aktivoinnin riskit
Onkogeenien aktivointi edustaa kriittistä turvallisuushuolta viljellyn lihan tuottajille, koska se voi vaarantaa kokonaisia tuotantoeriä. Geneettinen epävakaus voi johtaa onkogeenien aktivointiin mekanismien, kuten hypermetylaation, kautta, mikä voi johtaa kasvaimen kaltaisiin profiileihin [3][1]. Tuotannon nopea laajentaminen lisää entisestään todennäköisyyttä kerryttää näitä haitallisia mutaatioita [5][6].
Tämä on hyvin tunnustettu haaste. Kansainvälisen innovaatiokonsortion (IQ) mukaan & vastaajista uskoo, että geneettiset mutaatiot ovat suurempi uhka kuin aminohappojen väärä liittäminen tuotannon aikana 67%[5] . Tapaus toukokuulta 2024 havainnollistaa tämän ongelman vakavuutta: WuXi Biologics havaitsi, että 43% klooneista solulinjan kehitysohjelmassa kantoi samaa geneettistä pistemutaatiota. Perimmäinen syy? 2.1%–2.2% varianttitaso plasmidi-DNA:ssa, jota käytettiin transfektiossa, jäi havaitsematta perinteisellä Sanger-sekvensoinnilla.Tämän ratkaisemiseksi yritys otti käyttöön seuraavan sukupolven sekvensoinnin (NGS) laadunvalvontaprosesseihinsa havaitakseen tällaiset variantit varhaisessa vaiheessa [5] .
Geneettisten poikkeavuuksien varhainen havaitseminen on ratkaisevan tärkeää, sillä onkogeeniset muutokset voivat vaarantaa kokonaisia eriä. Vakio G-kaistakaryotyypitys voi tunnistaa epänormaalit alipopulaatiot jopa 14% mosaikismilla kahdessakymmenessä solumetafaasissa [1] . Edistyneemmät tekniikat, kuten NGS, voivat havaita geneettisiä mutaatioita kloonisoluissa herkkyydellä 0.5% [5] .
DNA-metylaatioanalyysi on toinen arvokas työkalu kasvainten potentiaalin arvioimiseksi:
Koska DNA-metylaatiotasot ja tiettyjen geenien hypermetylaatio esiintyvät syövän aloituksessa ja etenemisessä, DNA-metylaatioprofiilien analyysi voi tarjota täydentävää tietoa solujen kasvainten potentiaalista [3].
Todellinen haaste on toteuttaa vankkoja seurantajärjestelmiä, jotka pystyvät tunnistamaan nämä muutokset ennen kuin ne vaarantavat turvallisuuden. Viljellyn lihan tuottajille geneettisen vakauden ylläpitäminen nopean solujen laajenemisen aikana vaatii kehittyneitä laadunvalvontatoimenpiteitä. Erikoistuneet alustat, kuten
Laadunvalvonnan testausmenetelmät
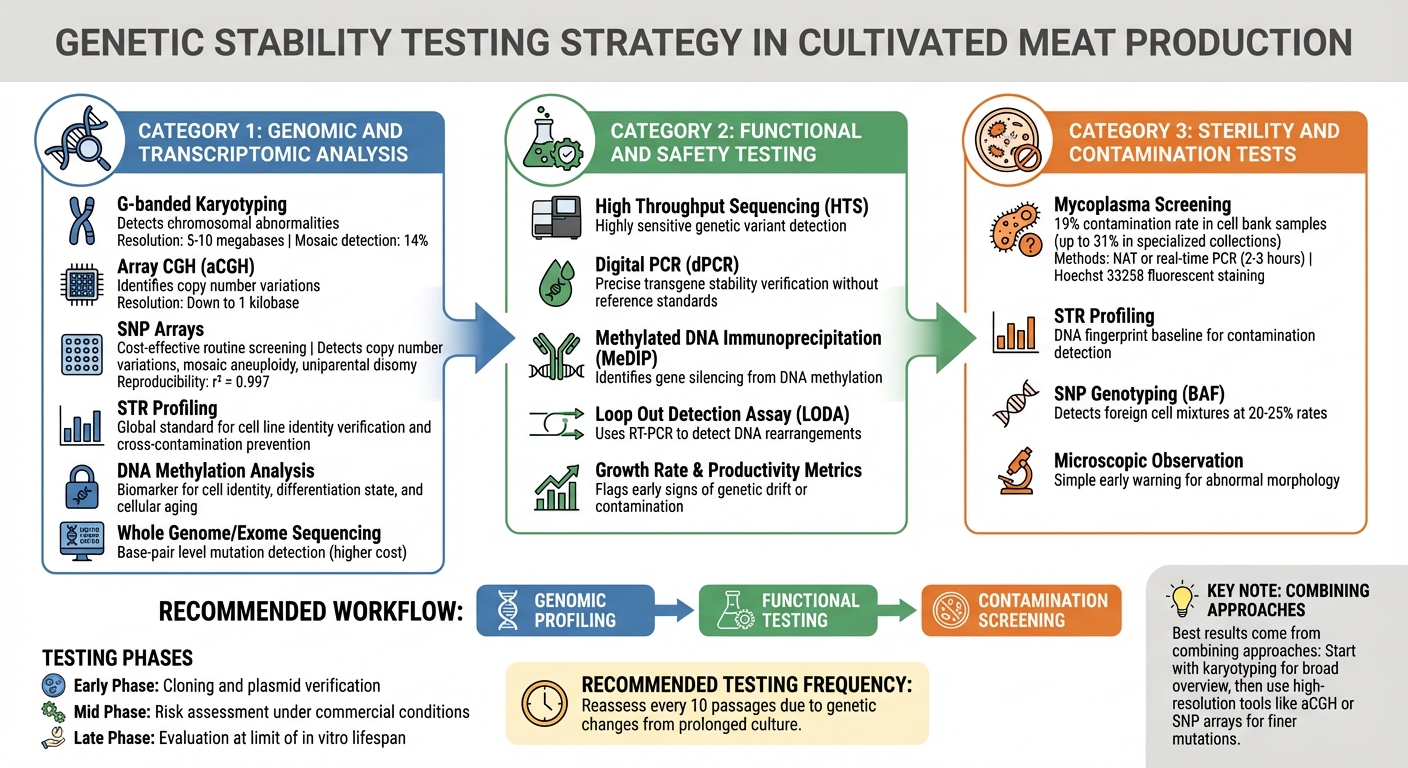
Laadunvalvonnan testausmenetelmät geneettisen stabiilisuuden varmistamiseksi viljellyissä lihasolulinjoissa
Geneettisen epävakauden tunnistaminen ennen kuin se vaikuttaa tuotantoon vaatii monitasoisen testausstrategian. Viljellyn lihan tuottajat luottavat menetelmiin, jotka havaitsevat kaiken suurista kromosomaalisista muutoksista yksittäisiin emäsmutaatioihin. Tekniikoiden valinta riippuu kussakin tuotantovaiheessa esiintyvistä riskeistä. Nämä genomiset työkalut toimivat ensimmäisenä tarkastuspisteenä, jota seuraavat yksityiskohtaiset toiminnalliset ja kontaminaatioarvioinnit.
Genominen ja transkriptominen analyysi
G-raitakaryotyypitys on keskeinen työkalu suurten kromosomaalisten ongelmien, kuten lukumääräisten poikkeavuuksien ja suurten rakenteellisten uudelleenjärjestelyjen, kuten translokaatioiden, tunnistamisessa.Vaikka se voi havaita mosaiikkitasoja noin 14%, sen resoluutio on rajoitettu 5–10 megabasin muutoksiin, mikä tarkoittaa, että pienemmät muutokset voivat jäädä huomaamatta [1] .
Array Comparative Genomic Hybridisation (aCGH) tarjoaa korkeamman resoluution, tunnistaen kopiolukumuutokset jopa 1 kilobaseen asti. Samoin Single Nucleotide Polymorphism (SNP) arrays tarjoavat kustannustehokkaan vaihtoehdon rutiiniseulontaan, havaitsemalla kopiolukumuutokset, mosaiikkianeuploidian ja uniparentaalisen disomian. Validointitutkimukset ovat osoittaneet, että SNP-arrays ovat erittäin toistettavia, B-alleelifrekvenssimittausten (BAF) saavuttaessa vaikuttavan r² = 0.997 [8] [1].
Rocio Aguilar-Quesada Andalusian julkisen terveydenhuollon biopankista korostaa menetelmien yhdistämisen arvoa:
Karyotyypitys on edelleen monipuolinen testi, erityisesti kun sitä täydennetään korkean resoluution testeillä [1] .
Lyhyiden tandemtoistojen (STR) profilointi on maailmanlaajuinen standardi solulinjojen identiteetin varmistamiseksi ja ristikontaminaation estämiseksi [1][9] . Samaan aikaan DNA-metylaatioanalyysi toimii biomarkkerina solujen identiteetille, erilaistumistilalle ja solujen ikääntymiselle [1]. Emäsparitasolla tapahtuvien mutaatioiden havaitsemiseksi koko genomin tai eksomin sekvensointi on vaihtoehto, vaikka se onkin kalliimpaa verrattuna matriisipohjaisiin menetelmiin [1].
Parhaat tulokset saadaan yhdistämällä näitä lähestymistapoja.Aloita karyotyypityksellä saadaksesi laajan yleiskuvan, ja käytä sitten korkean resoluution työkaluja, kuten aCGH tai SNP-mikrosiruja, hienompien mutaatioiden havaitsemiseksi. Säännöllinen uudelleenarviointi - ihanteellisesti joka 10. passagen jälkeen - on kriittistä, sillä pitkäaikainen viljely voi johtaa geneettisiin muutoksiin [10]. Nämä genomiset oivallukset täydennetään sitten toiminnallisilla kokeilla, jotta varmistetaan solujen johdonmukainen käyttäytyminen tuotannon aikana.
Toiminnallinen ja turvallisuustestaus
Pelkkä genominen profilointi ei riitä. Toiminnalliset testit vahvistavat, että solut säilyttävät tarkoitetut ominaisuutensa laajennuksen aikana. Mittarit, kuten kasvunopeudet ja tuottavuus, voivat osoittaa varhaisia merkkejä geneettisestä ajautumisesta tai kontaminaatiosta [9].
Korkean läpimenon sekvensointi (HTS) on erittäin herkkä geneettisten varianttien havaitsemisessa, kun taas digitaalinen PCR (dPCR) tarkasti varmistaa geeninsiirron vakauden ilman vertailustandardeja [11]. Christopher Frye ja Luhong He BioPharm Internationalista korostavat tämän vaiheen tärkeyttä:
Tuotantosolulinja on minkä tahansa bioprosessin perusta, ja siksi tuotantosolulinjan asianmukainen geneettinen karakterisointi on ehdottoman tärkeää prosessikehityksen onnistumiselle [6].
Epigeneettinen vakaus on myös kriittistä. Metyloitu DNA-immunopresipitaatio (MeDIP) auttaa tunnistamaan DNA-metylaation aiheuttaman geenien hiljentymisen, joka on yleinen syy tuottavuuden laskuun [7]. Työkalut, kuten Loop Out Detection Assay (LODA), käyttävät RT-PCR:ää DNA:n uudelleenjärjestelyjen havaitsemiseen, kuten silloin, kun kiinnostava geeni poistetaan, mutta valittava markkeri säilyy [7].
Testauksen tulisi olla linjassa tuotantovaiheen kanssa: varhaisvaiheen testit keskittyvät kloonaukseen ja plasmidien varmistamiseen, keskivaiheen testit arvioivat riskejä kaupallisissa olosuhteissa, ja myöhäisvaiheen testit arvioivat soluja niiden in vitro -eliniän rajoilla [6]. Kokeiden aloittaminen tuoreilla, matalan passagen soluilla pääsolupankista vähentää geneettisen ajautuman riskiä [9].
Steriliteetti- ja kontaminaatiotestit
Kontaminaatiotestaus on olennaista tekijöiden välttämiseksi, jotka voisivat epävakauttaa genetiikkaa. Mykoplasma on erityisen huolestuttava, koska se muuttaa solujen aineenvaihduntaa ja käyttäytymistä aiheuttamatta näkyviä muutoksia viljelmässä [1]. Tutkimukset paljastavat mykoplasmakontaminaation 19% solupankkinäytteistä, ja joissakin erikoiskokoelmissa esiintyy jopa 31% [1].
Säännöllinen mykoplasman seulonta herkkiä nukleiinihappoamplifikaatiotekniikoita (NAT) tai reaaliaikaista PCR:ää käyttäen voi tarjota puolikvantitatiivisia tuloksia 2–3 tunnissa [1]. Hoechst 33258 -fluoresenssivärjäys on toinen menetelmä, joka paljastaa tyypillisiä solunulkoisia fluoresenssikuvioita [9].
STR-profilointi luo DNA-sormenjäljen solulinjoille, toimien vertailukohtana ristikontaminaation havaitsemiseksi [9]. Lisäksi SNP-genotyypitys B-alleelifrekvenssijakaumia (BAF) käyttäen voi tunnistaa kontaminaation muista solulinjoista, havaitsemalla vieraita solusekoituksia 20–25% [8].
Mikroskooppinen tarkastelu on yksinkertainen mutta tehokas varhaisen varoituksen työkalu, sillä epänormaali solumorfologia viittaa usein viljelyongelmiin [9]. Laadunhallintajärjestelmän, kuten ISO 9001:2015, käyttöönotto yhdessä hyvien in vitro -menetelmien käytäntöjen (GIVIMP) kanssa auttaa ylläpitämään standardoituja ja toistettavia viljelyolosuhteita, vähentäen genomin epävakauden riskiä [10].
Viljellyn lihan tuottajille, jotka tarvitsevat pääsyn erikoistuneisiin testauslaitteisiin ja -materiaaleihin, alustat kuten
sbb-itb-ffee270
Ehkäisystrategiat geneettiselle epävakaudelle
Geneettisen epävakauden havaitseminen on yksi asia; sen ehkäiseminen on täysin toinen haaste.Jotta geneettinen vakaus säilyisi, viljellyn lihan tuottajat tarvitsevat hyvin suunniteltuja järjestelmiä, jotka estävät solulinjojen ajautumisen ennen ongelmien syntymistä. Kaksi keskeistä strategiaa johtaa tässä: rakenteellinen solupankkijärjestelmä ja kohdennettu geenitekniikka. Yhdessä nämä lähestymistavat puuttuvat suoraan geneettisen ajautumisen ja onkogeenien aktivoitumisen riskeihin.
Solupankkijärjestelmä ja kryosäilytys
Mutaatioiden kertyminen on todellinen huolenaihe, joten luotettava solupankkijärjestelmä on välttämätön. Alan standardi sisältää kaksitasoisen järjestelmän: Pääsolupankki (MCB) ja Työsolupankki (WCB). Tämä järjestely varmistaa johdonmukaisen lähtökohdan tuotannolle. Passausten määrän rajoittaminen on ratkaisevan tärkeää, sillä jokainen passaus lisää mutaatioiden mahdollisuutta. Säilyttämällä soluja nestemäisessä typessä biologinen aktiivisuus keskeytyy tehokkaasti, mikä vähentää geneettisten muutosten riskiä varastoinnin aikana.
Sen sijaan, että seurattaisiin aikaa, solujen ikä mitataan populaation kaksinkertaistumisilla. Esimerkiksi tyypillinen 5 000 litran tuotantobioreaktori sisältää noin 30 populaation kaksinkertaistumista [6]. Geneettisen yhdenmukaisuuden säilyttämiseksi kaupallinen valmistus rajoittaa tämän määrän 45 ja 60 kaksinkertaistumisen välille[6].
Seulontamenetelmät kuten RT-PCR ja yksittäisen solun qPCR voivat havaita ongelmat varhain, kuten epätavallisen mRNA:n silmukoinnin tai transgeenin vaihtelun. Solulinjat, jotka osoittavat suurta vaihtelua kopiomäärissä, tulisi hylätä tulevien ongelmien välttämiseksi.
Laadunvalvonta on ehdoton. Huolestuttavasti tutkimukset ovat löytäneet, että jopa 31% solulinjoista joissakin pankeissa oli saastunut mykoplasmalla[3] . Tämän estämiseksi STR-profilointia käytetään solulinjojen aitouden varmistamiseen koko pankkiprosessin ajan.Kuten FSA:n tutkimus ja todisteet :
korostavatGeneettinen muuntelu vakauden saavuttamiseksiKoska pankitetut solut ovat lopputuotteen lähtömateriaali, sääntelyviranomaiset saattavat tulevaisuudessa vaatia korkeita standardeja varmistaakseen turvallisen ja korkealaatuisen lihatuotteen[2] .
Geneettinen muuntelu tarjoaa toisen puolustuskerroksen parantamalla suoraan solulinjan vakautta. Tekniikat kuten kohdennettu integraatio (TI), erityisesti Rekombinaasi-välitteinen kasettivaihto (RMCE), mahdollistavat transgeenien tarkan sijoittamisen tiettyihin genomisiin paikkoihin. Tämä lähestymistapa välttää satunnaisen integraation arvaamattomuuden, jossa sijaintivaikutukset ja kopiomäärän epävakaus voivat aiheuttaa ongelmia. Vaikka RMCE:n tehokkuus CHO-soluissa on alle 0.1%[12], tuloksena olevat kloonit ovat ennustettavampia ja vakaampia.
Myös ilmentymisjärjestelmän valinta on tärkeää. Esimerkiksi Glutamiinisyntetaasi (GS)-järjestelmä tuottaa tyypillisesti noin viisi transgeenikopiota solua kohden, kun taas Dihydrofolaatin reduktaasi (DHFR)-järjestelmä voi monistaa kopiomäärät jopa 1 000:een[6]. Vaikka suuremmat kopiomäärät saattavat kuulostaa houkuttelevilta, ne lisäävät DNA-muutosten todennäköisyyttä, mikä tekee GS-pohjaisista järjestelmistä fiksumman valinnan pitkäaikaiseen vakauteen.
Riskien minimoimiseksi edelleen paikkakohtainen mutageneesi ja ennakkotransfektio NGS-seulonta ovat ratkaisevia. Koska Sanger-sekvensoinnilla on korkeampi havaitsemisraja, NGS voi havaita plasmidimutaatiot alle 0.5%, parantaen klooniseulonnan onnistumista yli 90%[5].
Shuai Wang ja kollegat WuXi Biologicsilta korostavat tämän valppauden merkitystä:
Koska prosessin optimointi ei voi korjata geenitason mutaatioita, seuraa mutaatiotasoa vakaissa klooneissa tarkasti[5].
Tuottajille, jotka tarvitsevat erikoistyökaluja - olipa kyseessä sitten kryosäilytys, geenitekniikka tai solulinjojen karakterisointi -
Laadunvalvonnan integrointi tuotantoon
Laadunvalvonnan sisällyttäminen jokaiseen tuotantovaiheeseen on ratkaisevan tärkeää. Ilman jäsenneltyä järjestelmää, jopa hyvin ylläpidetyt solulinjat voivat kokea muutoksia laajennuksen ja skaalaamisen aikana. Laadunvalvonta ei saa olla jälkikäteen ajateltu - sen on oltava keskeinen osa tuotantoa. Tämä alkaa laajennusvaiheessa, jossa tiukat hallintajärjestelmät ja kontrolloidut ympäristöt ovat keskeisessä roolissa.
Laadunvalvonta laajennuksen ja skaalaamisen aikana
Kuten aiemmin keskusteltiin, genomiset ja kontaminaatiotestit ovat elintärkeitä, erityisesti skaalausvaiheessa. Siirtyminen pienistä määristä tuhansiin litroihin tuo mukanaan uusia riskejä, ja jokainen solujen siirto lisää mutaatioiden riskiä. Laadunhallintajärjestelmä (QMS) auttaa hallitsemaan näitä riskejä tehokkaasti. Esimerkiksi vuosina 2017–2022 Josep M. Canals ja hänen tiiminsä Barcelonan yliopistossa ottivat käyttöön ISO 9001:2015 QMS:n standardoidakseen ihmisen pluripotenttien kantasolujen viljelmät. Heidän retrospektiivinen analyysinsä G-banding- ja aCGH-datasta paljasti merkittävän vähennyksen kromosomaalisissa poikkeavuuksissa verrattuna esisovitusolosuhteisiin[10][13]. Kanavat korostivat jatkuvan seurannan merkitystä:
hPSC:iden geneettinen epävakaus viljelyssä tekee genomin eheyden säännöllisestä uudelleenarvioinnista olennaisen vaatimuksen, kun suunnitellaan niiden käyttöä kokeissa [10].
Rutiininomainen genominen seulonta on välttämätöntä. Tekniikat kuten G-raitakaryotyypitys ja aCGH havaitsevat rakenteellisia muutoksia, kun taas Next-Generation Sequencing (NGS) tunnistaa mutaatioita tasoilla alle 0.5%[5]. Kasvukäyrän analyysi voi myös varoittaa ongelmista aikaisin, kuten kontaminaatiosta tai geneettisestä ajautumisesta[9]. Ympäristön seuranta lisää toisen turvakerroksen, käytännöillä kuten laskeutumislevytestaus ja kuuden kuukauden välein tehtävät HEPA-suodattimien tarkastukset varmistavat, että tuotantoympäristö pysyy vakaana ja stressittömänä solulinjoille[4] .
Johdonmukaisuus mediassa ja reagensseissa on yhtä tärkeää. Seerumittomien, määriteltyjen medioiden, kuten mTeSR1, käyttö yhdessä analyysitodistuksen omaavien reagenssien kanssa auttaa vähentämään eräkohtaista vaihtelua ja rajoittaa virustartunnan riskiä[10][4]. Säännölliset morfologiatarkastukset - yksinkertaiset mikroskooppiset havainnot eri viljelmätiheyksillä - voivat havaita erilaistumisen tai stressin varhaisia merkkejä[9]. Erikoislaitteiden tai reagenssien hankintaan, alustat kuten
Toiminnalliset testit tuotteen johdonmukaisuuden varmistamiseksi
Vaikka genominen seuranta turvaa prosessin, toiminnalliset testit varmistavat, että solut toimivat tarkoitetulla tavalla.Geneettinen stabiilisuus ei yksin riitä; solujen on myös säilytettävä kykynsä toimia oikein tuotantoerien välillä. Viljellyssä lihassa tämä tarkoittaa sen varmistamista, että kantasolut, kuten lihassatelliittisolut, voivat edelleen erilaistua kypsäksi lihas- tai rasvakudokseksi laajentumisen jälkeen[2]. Erilaistumiskokeet ovat välttämättömiä tämän varmistamiseksi.
Metabolia-analyysit, kuten MTT, LDH ja Resazuriini, antavat tietoa solujen terveydestä ja elinkelpoisuudesta [4][9]. Nämä, yhdistettynä Short Tandem Repeat (STR) -profiilointiin, auttavat varmistamaan, että solulinjat pysyvät aitoina ja vapaina ristikontaminaatiosta koko tuotantoprosessin ajan[1][9].
Transkriptionaalinen analyysi on toinen kriittinen vaihe.Xiaoyue Chen ja Sam Zhang suosittelevat:
cDNA:ta suositellaan genomi-DNA-sekvensoinnin sijaan mutaatioiden havaitsemiseksi transkriptiotason riskien arvioimiseksi[5].
Tämä menetelmä tarjoaa tarkemman kuvan lopputuotteesta, koska se heijastaa geenien ilmentymistä eikä vain niiden genomisia sijainteja. Yhdistämällä genominen seulonta toiminnallisiin testeihin, tuottajat voivat varmistaa, että jokainen erä täyttää tiukat turvallisuus-, laatu- ja suorituskykystandardit tuotannon jokaisessa vaiheessa.
Päätelmä
Geneettisen vakauden ylläpitäminen on kriittistä viljellyn lihan turvalliselle ja johdonmukaiselle tuotannolle. Francisco J. Molina-Ruiz ja hänen kollegansa Kantasolujen ja regeneratiivisen lääketieteen laboratoriosta korostavat riskejä:
Geneettiset muutokset hPSCs:ssä voivat vaarantaa paitsi hPSC-pohjaisten solutuotteiden turvallisuuden... mutta myös johtaa lähtömateriaalin heterogeeniseen erilaistumistaipumukseen, muuttuneisiin geeniekspressioprofiileihin ja lopullisen solutuotteen tehottomuuteen [10].
Panokset ovat merkittäviä - yli 531 väärin tunnistettua solulinjaa on kirjattu Kansainvälisen solulinjan aitouden varmistuskomitean [1].
Näiden ongelmien ratkaiseminen vaatii vankan laadunvalvontakehyksen. Tämä sisältää menetelmien, kuten STR-profiloinnin, G-bändikaryotyypityksen, aCGH:n ja kehittyneen NGS:n [5], yhdistämisen järjestelmiin, kuten ISO 9001:2015, prosessien standardoimiseksi ja kromosomaalisten poikkeavuuksien minimoimiseksi [13].
Myös taloudelliset tekijät ajavat näiden toimenpiteiden tarvetta.Geneettinen ajautuminen voi johtaa siihen, että mutatoituneet solut saavat kasvuedun, mikä voi pilata kokonaisia tuotantoeriä [10][11]. Kasvavan kiinnostuksen myötä ihmisen pluripotentteihin kantasoluihin, vakaille solulinjoille on suurempi kysyntä kuin koskaan. Kuten professori David L. Kaplan Tuftsin yliopistosta selittää:
Kuolemattomia solulinjoja pidetään yleisesti vaatimuksena suurten syötävien kudosmäärien tuottamiseksi vakaasta, kestävästä bioprosessista [14].
Viljellyn lihan tuottajille laadunvalvonta on sisällytettävä jokaiseen vaiheeseen - plasmidien seulonnasta laajamittaiseen tuotannon seurantaan. Yhdistämällä perusteellisen testauksen ennaltaehkäiseviin strategioihin, tuottajat voivat varmistaa johdonmukaiset ja luotettavat tulokset.
UKK
Kuinka usein geneettisen vakauden testaus tulisi suorittaa skaalausvaiheen aikana?
Geneettisen vakauden testaus on ratkaiseva vaihe skaalausvaiheen aikana ja se tulisi suorittaa säännöllisesti. Kuinka usein tämä testaus tapahtuu, riippuu suurelta osin kyseisestä solulinjasta ja prosessista. Mutaatioiden mahdollisuuden vähentämiseksi ja solujen kantasolumaisuuden säilyttämiseksi on viisasta määrittää geneettiseen analyysiin perustuva passageraja.
Mitkä testit parhaiten havaitsevat pieniä mutaatioita ja suuria kromosomimuutoksia?
Testit kuten SNP-array-analyysi ja genominlaajuinen SNP-genotyypitys ovat e
Mikä on yksinkertaisin tapa estää geneettinen ajautuminen tuotantoerien välillä?
Geneettisen ajautumisen minimoimiseksi on tärkeää suorittaa säännöllisiä geneettisiä ja toiminnallisia analyysejä solulinjoista ja rajoittaa niiden läpikäymien passaasien määrää. Ota käyttöön käytäntöjä, kuten perustaa pääsolupankkeja ja tarkistaa säännöllisesti geneettinen stabiilisuus, kuten laatuvalvontaprotokollissa suositellaan. Nämä toimenpiteet ovat avainasemassa johdonmukaisuuden ylläpitämisessä ja luotettavien tulosten varmistamisessa eri tuotantoerien välillä.











