Kryopræservering er processen med at fryse og opbevare levende celler ved ultralave temperaturer for at bevare deres levedygtighed over tid. Denne metode er afgørende for produktion af dyrket kød, da den sikrer konsistente, stabile cellelinjer og beskytter mod tab fra kontaminering eller udstyrsfejl. Vigtige trin inkluderer:
- Forberedelse: Høst celler under deres vækstfase, kontroller levedygtighed (mål for ≥90%), og forbered dem i frysemedier med kryobeskyttelsesmidler som DMSO eller glycerol.
- Frysning: Brug en kontrolleret kølehastighed (-1°C til -3°C per minut) for at forhindre iskrystaldannelse. Opbevar celler i flydende kvælstofdamp (-135°C til -190°C) for langtidsopbevaring.
- Optøning: Optø celler hurtigt i et 37°C vandbad for at minimere kryobeskyttelsesmiddel toksicitet, og overfør dem derefter til vækstmedier for genopretning.
- Kvalitetskontrol: Mærk hætteglas nøjagtigt, overvåg opbevaringsforholdene, og test levedygtigheden efter optøning for at sikre vellykket konservering.
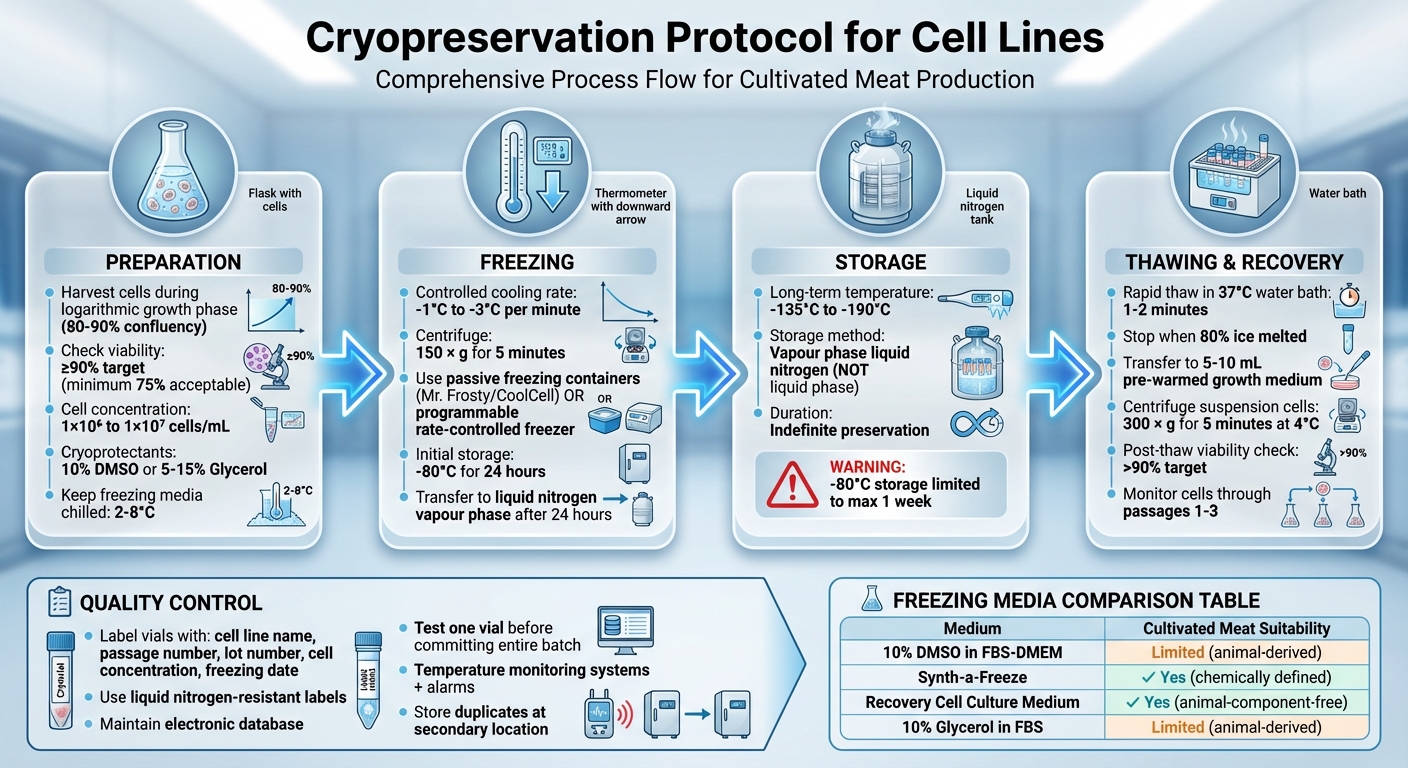
Komplet Kryopræserveringsprotokol for Cellelinjer: 4-trins proces fra forberedelse til opbevaring
Forberedelse af celler til kryopræservering
Høst af celler og levedygtighedskontrol
For at sikre den bedste genopretning efter optøning, høst celler under deres logaritmiske (log) vækstfase. For adherente cellelinjer er dette typisk, når de når 80–90% konfluens [2][3][6].
Kontroller cellernes levedygtighed ved hjælp af Trypan Blue-ekskluderingsmetoden. Bland lige dele (1:1) af 0,4% Trypan Blue med cellesuspensionen, og tæl derefter cellerne ved hjælp af et hæmocytometer.Levedygtige celler vil udelukke farvestoffet og fremstå lyse under mikroskopet, mens ikke-levedygtige celler vil farves blå [4]. Ideelt set skal du sigte efter en levedygtighed på mindst 90% for de bedste genvindingsrater, selvom nogle protokoller kan acceptere et minimum på 75% [1][2][3][5].
Før høst, brug et mikroskop til at kontrollere for bakteriel eller svampeforurening. Sunde suspensionsceller bør fremstå lyse, runde og refraktive under et inverteret fasekontrastmikroskop [2][3].
Når cellerne opfylder de krævede levedygtighedsstandarder, gå videre til de præ-frysnings trin.
Forberedelser før nedfrysning
For adherente celler, brug skånsomme dissociationsmetoder, såsom trypsin eller TrypLE Express, og begræns inkubationstiden for at undgå at beskadige cellemembranerne [5]. Forbered cellerne i en koncentration på 1 × 10⁶ til 1 × 10⁷ celler/mL, afhængigt af cellelinjen [1][6]. Under aliquotering, sørg for at celleophænget blandes hyppigt for at opretholde en ensartet fordeling i kryorørene [5].
Hold frysemediet afkølet mellem 2°C og 8°C under resuspension for at reducere kryobeskyttelsesmidlets toksicitet, før fryseprocessen begynder [5]. Når cellerne er suspenderet i frysemediet, fortsæt hurtigt til fryseprotokollen [1].Kryopræserver altid celler ved det lavest mulige passagenummer for at reducere risikoen for genetisk drift eller morfologiske ændringer [5][7].
Valg af kryobeskyttelsesmidler og frysemedier
Kryobeskyttelsesmuligheder og deres funktioner
Dimethylsulfoxid (DMSO) er bredt anvendt som et kryobeskyttelsesmiddel, typisk i en koncentration på 10% [2]. Det virker ved at trænge ind i cellemembraner og reducere isdannelse under frysning. Dog kan DMSO være toksisk for celler ved stuetemperatur, så hurtig optøning er essentiel for at minimere eksponering og hurtigt fortynde det [1].
Glycerol fungerer som et nyttigt alternativ for cellelinjer, der er følsomme over for DMSO, og anvendes generelt i koncentrationer fra 5% til 15% [8].Det er særligt effektivt for celletyper, hvor DMSO kan forårsage uønsket differentiering [3], og det har tendens til at have lavere toksicitet sammenlignet med DMSO.
I dyrket kød applikationer bruger traditionelle fryseprotokoller ofte en blanding af 90% Fetal Bovine Serum (FBS) og 10% DMSO [1]. Dog begrænser afhængigheden af dyreafledte komponenter disse metoder med hensyn til skalerbarhed og regulatorisk godkendelse [9]. For at løse disse problemer, kemisk definerede medier - som Synth-a-Freeze eller Recovery Cell Culture Medium - giver et alternativ uden dyrekomponenter. Disse medier opretholder høj cellelevedygtighed efter optøning, mens de overvinder udfordringerne forbundet med komponenter af animalsk oprindelse [9].
Sammenligning af frysemedier
Her er en oversigt over fordele og begrænsninger ved forskellige frysemedier, der anvendes i produktion af dyrket kød:
| Medium | Fordele | Ulemper | Egnethed til dyrket kød |
|---|---|---|---|
| 10% DMSO i FBS-DMEM | Etablerede protokoller [1] | Indeholder komponenter af animalsk oprindelse; batchvariabilitet [9] | Begrænset skalerbarhed |
| Synth-a-Freeze | Kemisk defineret; ensartet kvalitet; fri for animalske komponenter [9] | Højere startomkostninger [9] | Ja |
| Recovery Cell Culture Medium | Nem at bruge; designet til hurtig genopretning [9] | Kan have brug for optimering til specifikke cellelinjer | Ja |
| 10% Glycerol i FBS | Alternativ for DMSO-følsomme celler [1] | Afhænger af serum med animalsk oprindelse [9] | Begrænset skalerbarhed |
I februar 2023 demonstrerede forskere ved Tokyo Women's Medical University, ledet af Hironobu Takahashi, vigtigheden af at vælge det rigtige frysemedium.Ved brug af kommercielle muligheder som CELLBANKER 1 og 2, lykkedes det dem at kryopræservere primære bovine myogene celler ved –80°C i op til et år. Bemærkelsesværdigt nok bevarede disse celler deres evne til at proliferere og differentiere til kontraktilt muskelvæv med intakte sarkomerstrukturer efter optøning [10] .
Til produktion af dyrket kød foretrækkes kemisk definerede og GMP-kompatible medier i stigende grad. Som STEMCELL Technologies fremhæver:
Inden for stærkt regulerede områder som celle- og genterapi anbefales det at bruge et GMP-fremstillet, fuldt defineret kryopræserveringsmedium for at sikre, at produkterne konsekvent produceres og kontrolleres i henhold til kvalitetsstandarder [9].
Platforme som
Kryopræserveringsprocedure og kølehastigheder
Trin-for-trin fryseprotokol
Nøglen til vellykket kryopræservering ligger i at opretholde en stabil kølehastighed på -1°C til -3°C per minut[2]. Denne gradvise proces tillader vand at forlade cellerne langsomt, hvilket forhindrer dannelsen af skadelige intracellulære iskrystaller, der kunne sprænge cellemembraner[1].
Begynd med at centrifugere cellerne ved 150 x g i 5 minutter[3]. Når de er centrifugeret, resuspender cellepelleten i et koldt frysemedium indeholdende 10% DMSO ved en koncentration af 2–4×10⁶ celler/mL [3]. For at reducere DMSO-eksponering, gå hurtigt videre til næste trin - nedfrysning.
Fordel cellesuspensionen i forudmærkede kryogene hætteglas. Hvert hætteglas skal tydeligt angive væsentlige detaljer såsom cellelinjens navn, passage nummer, lotnummer, cellekoncentration og datoen for nedfrysning[3]. Med hætteglassene forberedt, er det tid til at vælge og anvende det passende køleudstyr.
Køleudstyr og teknikker
Placer hætteglassene straks i en kontrolleret køleenhed. Passive frysebeholdere, som Nalgene "Mr Frosty" (som bruger isopropanol) eller Corning "CoolCell", er populære valg. Disse værktøjer kan opnå en kølehastighed på cirka 1°C per minut, når de placeres i en -80°C fryser[2] .
For større operationer, hvor konsistens er kritisk, er en programmerbar fryser med kontrolleret hastighed den bedste løsning. Som angivet af Sigma-Aldrich:
ECACC bruger rutinemæssigt en programmerbar fryser med kontrolleret hastighed. Dette er den mest pålidelige og reproducerbare måde at fryse celler på[3].
Efter omkring 24 timer ved -80°C, overfør hætteglassene til dampfasen af flydende nitrogen, hvor temperaturerne ligger mellem -135°C og -190°C, for langtidsopbevaring [4]. Undgå at opbevare celler ved -80°C i længere end en uge, da dette kan kompromittere deres levedygtighed. Temperaturer under -135°C er essentielle for ubegrænset bevaring[2]. Brug af dampfasen i stedet for væskefasen reducerer risikoen for krydskontaminering, mens tilstrækkeligt lave temperaturer opretholdes.
Optønings- og genopretningsprotokoller
Optøningsproces
Hurtig optøning af celler er afgørende for at begrænse toksisk eksponering for kryobeskyttelsesmidler og forhindre, at iskrystaller forårsager skade. Sørg for at bære et ansigtsvisir og isolerede handsker for sikkerhed. Start med at fjerne kryorøret fra flydende nitrogen og løsne låget let for at frigive eventuelt opbygget tryk. Stram derefter låget igen.
Placer røret i et 37°C vandbad, og sørg for, at låget forbliver over vandoverfladen. Lad det tø i 1–2 minutter, eller indtil der kun er få iskrystaller tilbage. Når det er optøet, tør rørets yderside af med 70% alkohol for at opretholde sterilitet.
Overfør indholdet af røret til et rør, der indeholder 5–10 mL forvarmet vækstmedium. Tilsæt mediet langsomt for at hjælpe med at reducere osmotisk chok. Hvis du arbejder med suspensionscellelinjer, centrifuger straks cellesuspensionen ved 300 × g i 5 minutter ved 4°C.Dette trin hjælper med at pelletere cellerne og fjerner kryobeskyttelsesmidlet. Efter centrifugering, resuspender cellerne i frisk medium. For adherente celler er centrifugering normalt unødvendig. I stedet, så cellerne direkte i en passende kulturbeholder og fjern eventuel resterende DMSO under det første medieskift, typisk efter 24 timer.
Vurderinger efter optøning
Lige efter optøning, kontroller cellelevedygtigheden for at sikre, at genopretningen har været vellykket. Brug Trypan Blue-eksklusion metoden til denne vurdering. Ideelt set bør cellelevedygtigheden overstige 90% [11], men et minimum på 75% er acceptabelt. Efter 24 timer, inspicer cellerne under et fasekontrastmikroskop for at bekræfte adhærens, evaluere celletæthed og kontrollere for tegn på kontaminering.
Fortsæt med at overvåge cellerne gennem passager 1–3 for at sikre normal proliferation og at de bevarer deres forventede karakteristika.For cellelinjer, der kommer sig langsommere, kan du forbedre overlevelsen ved at øge den initiale koncentration af føtalt bovint serum til omkring 20% v/v.
sbb-itb-ffee270
Opbevaring og Langtidslevedygtighed
Opbevaringsbetingelser og Varighed
For at opretholde cellelinjens levedygtighed på lang sigt er det essentielt at opbevare dem ved temperaturer under -135°C [7][2]. Dette sikrer, at de forbliver bevaret på ubestemt tid.
Den foretrukne metode til opbevaring af dyrkede kød-cellelinjer er dampfase flydende nitrogen. Denne teknik holder temperaturerne mellem -135°C og -190°C, hvilket gør den ideel til langtidsopbevaring, samtidig med at den tilbyder øget sikkerhed sammenlignet med opbevaring i flydende fase.
Hvis du har brug for at opbevare celler ved -80°C, begræns dette til en periode på 24 timer til en uge. Udover dette kan cellelevedygtigheden falde.For midlertidig opbevaring ved denne temperatur, overfør cellerne til flydende kvælstofopbevaring så hurtigt som muligt.
Brug standard sterile kryogene hætteglas (1–2 mL) med indvendig gevind og en O-ring til sikker opbevaring [4][5]. Placer altid forseglede kryohætteglas i gasfasen frem for væskefasen af kvælstof for at reducere risikoen for hætteglas-eksplosioner under optøning [5]. Derudover skal du sikre, at beholdere med flydende kvælstof er mindst halvt fyldte for at opretholde en sikkerhedsbuffert.
Endelig er strenge kvalitetskontrolforanstaltninger afgørende for at sikre cellernes langsigtede levedygtighed.
Kvalitetskontrolkontroller
For at sikre pålideligheden af opbevarede cellelinjer skal du følge strenge protokoller for kvalitetskontrol. Begynd med at mærke hver hætteglas nøjagtigt med flydende kvælstof-resistente etiketter. Inkluder væsentlige detaljer såsom cellelinjens identitet, lotnummer, passage nummer og frysedato. Oprethold en elektronisk database for at registrere den præcise placering af hver hætteglas, hvilket reducerer den tid, opbevaringsbeholdere skal forblive åbne [7][2].
Før du forpligter hele partier til langtidsopbevaring, test en hætteglas' levedygtighed efter kortvarig gasfaseopbevaring. Dette trin hjælper med at bekræfte, at fryseprocessen var vellykket og identificerer eventuelle potentielle problemer [4][7][2]. For meget værdifulde cellelagre er det klogt at opbevare dubletter på en sekundær placering for at beskytte mod udstyrsfejl eller lokale katastrofer [7][2].
Udstyr alle opbevaringsbeholdere med temperaturovervågningssystemer og alarmer for at opdage lave niveauer af flydende nitrogen [7]. Installér desuden iltalarmer i opbevaringsområder, indstillet til at udløse ved 18% ilt (v/v), for at minimere risikoen for kvælning for personale, der arbejder med flydende nitrogen [7][2].
Cryopreservation of mammalian cell lines video protocol
Konklusion og Vigtige Punkter
Her er en hurtig opsummering af de væsentlige trin og anbefalinger for effektiv kryopræservering i produktion af dyrket kød:
- Cell Harvesting: Saml celler under deres logaritmiske vækstfase, og sørg for, at levedygtigheden overstiger 90%. Brug 10% DMSO som kryobeskyttelsesmiddel, selvom glycerol kan være et alternativ for mere sarte cellelinjer [11][1].
- Køling og Opbevaring: Oprethold en kontrolleret kølehastighed og overfør hurtigt hætteglas til dampfase flydende nitrogenopbevaring for at beskytte celleintegritet [11]
En undersøgelse af Roka Kakehi et al. fremhæver vigtigheden af præcision i kryopræservering [10]:
"At sikre en pålidelig og konsekvent kilde til celler ved brug af kryopræservering vil give os mulighed for at øge den stabile forsyning af lovende celler til produktion af dyrket kød." - Roka Kakehi et al., Tokyo Women's Medical University
- Optøningsproces: Optø celler i et 37°C vandbad i cirka to minutter, og stop når 80% af isen er smeltet. Dette reducerer DMSO-toksicitet og forbedrer cellerecovery [1]. Følg op med levedygtighedstjek efter optøning for at sikre succes og finjustere fremtidige procedurer.
Disse metoder fungerer hånd i hånd med strenge kvalitetskontrolpraksisser. Mærk altid hætteglas nøjagtigt, oprethold organiserede optegnelser, og implementer grundige kontroller før langtidsopbevaring [11]. For specialiserede kryopræserveringsbehov forbinder platforme som
Ofte stillede spørgsmål
Hvad er fordelene ved at bruge kemisk definerede medier til kryopræservering af cellelinjer i produktion af dyrket kød?
Kemisk definerede medier bringer flere fordele, når det kommer til kryopræservering af cellelinjer til produktion af dyrket kød. Ved at fjerne udefinerede komponenter, som serum af animalsk oprindelse, sikrer de konsekvente og forudsigelige resultater - en afgørende faktor for at opretholde cellelinjernes langsigtede pålidelighed.
En anden vigtig fordel er den reducerede risiko for kontaminering og variation. Dette understøtter ikke kun højere kvalitets- og sikkerhedsstandarder, men passer også perfekt til den præcision og skalerbarhed, der kræves for at imødekomme både lovgivningsmæssige krav og forbrugerforventninger i den dyrkede kødindustri.
Hvordan påvirker valget af kryobeskyttelsesmiddel celleoverlevelse under frysning og optøning?
Valget af kryobeskyttelsesmiddel er en nøglefaktor i bevarelsen af cellehelbred under frysning og optøning. To almindeligt anvendte muligheder er dimethyl sulfoxid (DMSO) og glycerol, hver med forskellige egenskaber. DMSO er kendt for sin evne til hurtigt at trænge ind i celler og give stærk beskyttelse. Dog kommer det med en advarsel: ved høje koncentrationer eller ved længerevarende eksponering kan det blive giftigt og potentielt sænke cellelevedygtigheden.
Glycerol, derimod, er mindre giftigt og kan anvendes direkte.Dens ulempe ligger i dens langsommere cellepenetrationshastighed, hvilket kan resultere i mindre øjeblikkelig beskyttelse sammenlignet med DMSO.
At opnå den rette balance er afgørende. Korrekt justering af koncentrationen og eksponeringstiden for kryobeskyttelsesmidlet hjælper med at beskytte celler, samtidig med at risikoen for toksicitet minimeres. Derudover er det vigtigt at overholde bedste praksis for kølehastigheder og opbevaringsforhold for at sikre de højest mulige genvindingsrater efter optøning.
Hvorfor er det vigtigt at kontrollere kølehastigheden under kryopræservering?
At opretholde en stabil kølehastighed, normalt mellem –1°C og –3°C per minut, er nøglen til at holde celler levedygtige. Gradvis nedkøling tillader celler at dehydrere i et kontrolleret tempo, hvilket reducerer chancen for, at skadelige iskrystaller dannes, som kan rive eller beskadige cellemembraner.
Denne målte tilgang beskytter cellernes struktur, hvilket øger deres overlevelse og funktionalitet, når de er optøet.At følge præcise køleprotokoller er afgørende for at sikre vellykket langtidsopbevaring og genopretning af cellelinjer.











