Rengøringsvalidering sikrer, at produktionsudstyr i dyrkede kød faciliteter er grundigt rengjort for at fjerne rester som celledetritus, vækstmedier og mikrober. Det er afgørende for at forhindre krydskontaminering, især i opsætninger med flere produkter.
Vigtige punkter:
- Hvorfor det er vigtigt: Uden ordentlig rengøring kan rester fra en batch forurene den næste. Delt udstyr som bioreaktorer og værktøjer er højrisikoområder.
- Regulatoriske standarder: Overholdelse af retningslinjer som HACCP, GMP og UK-specifikke regler er obligatorisk.
-
Skridt til at validere rengøring:
- Vælg de rigtige rengøringsmidler (e.g. , alkaliske til proteiner, sure til mineraler).
- Test under "værst tænkelige" forhold (e.g. , klæbrige eller højproteinrester).
- Brug svabprøvetagning og sæt målbare grænser (e.g. , 10 ppm for kemiske rester).
- Udfør tre på hinanden følgende rengøringscyklusser for at sikre effektivitet.
- Overvågningsværktøjer: ATP-swabs, TOC-analyse og mikrobiologisk plating hjælper med at verificere renlighed.
Rengøringsvalidering handler ikke kun om sikkerhed - det handler om at sikre konsekvent, pålidelig produktion og opretholde tillid til dyrkede kødprodukter.
Regulatoriske og Biosikkerhedskrav
Relevante Regulatoriske Retningslinjer
I Storbritannien falder dyrket kød under tilsyn af Food Standards Agency (FSA) og Food Standards Scotland (FSS). Disse agenturer vurderer risici og fastsætter krav til sådanne produkter inden for Novel Foods-rammen. Derudover kan visse produkter være nødt til at overholde GMO- eller PBO-regler.
Overholdelse af disse regler afhænger af veletablerede kvalitetssikringssystemer:
- HACCP (Hazard Analysis and Critical Control Points): Fokuserer på at identificere og kontrollere mikrobielle farer.
- GMP (Good Manufacturing Practices): Sikrer ensartet produktion og kvalitetskontrol.
- GCCP (Good Cell Culture Practices): Omhandler håndtering af cellelinjer for at minimere kontaminationsrisici.
- GHPs (Good Hygiene Practices): Dækker generelle drifts- og miljøstandarder.
Principperne i Codex Alimentarius danner grundlaget for udformning af specifikke industriretningslinjer og kvalitetskontrolplaner, med inspiration fra sektorer som kliniske og biofarmaceutiske industrier.
"Principperne i Codex og HACCP giver et solidt grundlag for at opbygge specifikke retningslinjer og kvalitetskontrolplaner for denne sektor, og der kan drages læring fra den kliniske/biopharma-industri og tilpasses til nye fødevarekrav."
– FSA Research and Evidence [1]
For at sikre pålidelighed bør mikrobiologi og rengøringsvalideringer være i overensstemmelse med UKAS standarder. Lærdomme fra kliniske og biopharma-praksisser kan tilpasses til fødevareproduktion og adressere de unikke udfordringer, som faciliteter for dyrket kød står overfor.
Biosikkerhedsrisici i multi-produkt anlæg
Faciliteter, der producerer flere dyrkede kødprodukter, står over for biosikkerhedsproblemer, der går ud over de typiske risici ved fødevareproduktion. Disse inkluderer:
- Traditionelle fødevarebårne patogener: Såsom enterobakterier og dyrevirusser.
- Skjulte forurenende stoffer: Som mycoplasma og mykobakterier, der undgår detektion i kulturmedier, da de ikke forårsager synlig uklarhed og kræver specialiseret testning.
Disse risici er særligt forhøjede i delte udstyrsopsætninger, hvor visuelle inspektioner alene ikke kan garantere renlighed. Effektiv rengøringsvalidering er afgørende for at eliminere skadelige stoffer som endotoksiner, exotoksiner og mykotoksiner, selv i sporbare mængder.
Avancerede overvågningsteknikker kan hjælpe med at mindske disse risici. For eksempel kan inline-overvågning af pH og opløste iltniveauer tidligt signalere mikrobiel vækst, hvilket indikerer potentielle rengørings- eller steriliseringsfejl. Derudover kan miljøovervågning af luft, overflader og vand inden for faciliteterne identificere forureningstrusler, før de påvirker produktionen.
"Efterhånden som industrien fortsætter med at udvikle og tilpasse udstyr og processer til CCP-produktion, vil rengøring, sterilisering og andre relevante procedurer kræve vurdering og validering, og nationale/internationale standarder bør udvikles."
– FSA Research and Evidence [1]
Disse foranstaltninger fremhæver den kritiske betydning af strenge rengørings- og valideringsprotokoller for at forhindre krydskontaminering og sikre sikkerheden af hver produktionsbatch.
sbb-itb-ffee270
Rengøringsvalidering i 10 trin i Pharma | Komplet vejledning til rengøringsvalidering
Oprettelse af en rengøringsvalideringsprotokol
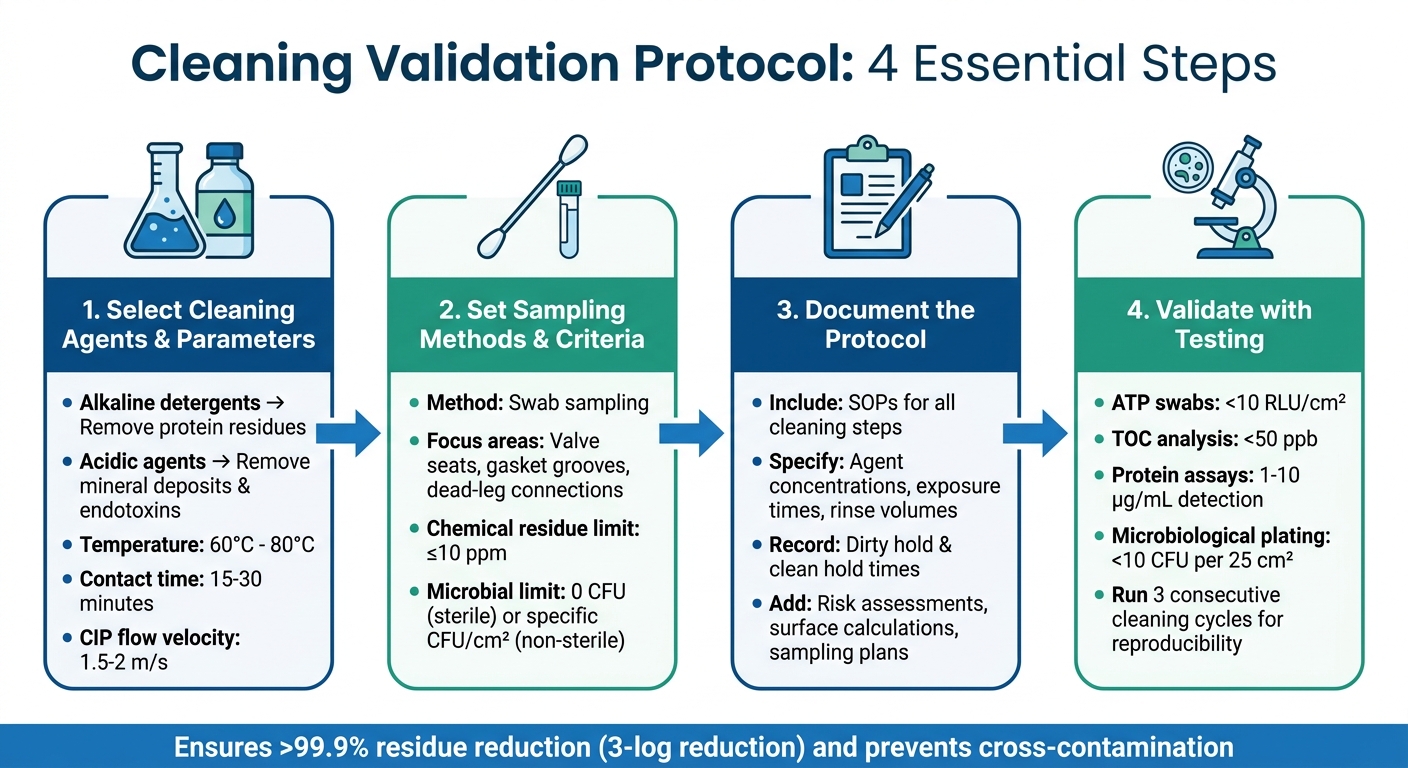
4-trins rengøringsvalideringsprotokol for dyrkede kød faciliteter
Valg af rengøringsmidler og parametre
Valg af de rigtige rengøringsmidler afhænger af typen af rester og de materialer, der anvendes i dit udstyr. For dyrkede kød faciliteter er rustfri stål bioreaktorer (normalt 316L kvalitet) almindelige. Disse kræver alkaliske rengøringsmidler for at fjerne proteinrester, mens sure midler er ideelle til at tackle mineralaflejringer og endotoksiner. For at maksimere effektiviteten af rengøringsmidler uden at skade pakninger eller tætningsringe, skal rengøringstemperaturerne holdes mellem 60°C og 80°C.
Tillad rengøringsmidler at forblive i kontakt i 15–30 minutter, især i vanskelige områder som impellerblade og sensorporte . For clean-in-place (CIP) systemer, sørg for en flowhastighed på 1,5–2 m/s for effektivt at fjerne biofilm. Disse parametre skal dokumenteres omhyggeligt, da de udgør rygraden i din valideringsundersøgelse.
Fastlæggelse af prøvetagningsmetoder og acceptkriterier
Swab-prøvetagning er den foretrukne metode til at detektere rester på udstyrs overflader. Fokuser på områder, der er sværest at rengøre, såsom ventilpladser, pakningsriller og blindforbindelser. Disse steder giver en robust test af, hvor effektiv din rengøringsproces er.
Acceptkriterier skal være baseret på videnskabelig evidens. For kemiske rester er en grænse på 10 ppm bredt anerkendt, hvilket repræsenterer enten 1/1000 af en terapeutisk dosis eller et toksikologisk sikkert niveau.For mikrobiel bioburden kræver sterile produkter en fuldstændig fravær af levedygtige organismer, mens ikke-sterile produkter kan tillade specifikke kolonidannende enheder (CFU) pr. kvadratcentimeter. Når restgrænser fastsættes, skal det samlede overfladeareal af udstyret overvejes, og der skal tages højde for de mest udfordrende produktscenarier.
"En rengøringsvalideringsprotokol er en detaljeret plan, der beskriver alle valideringsaktiviteter. Den omfatter et specifikt valideringsmål og gruppering af produkter og udstyr til validering." – Kazi, GMP Ekspert [3]
Alle prøvetagningsmetoder og acceptkriterier skal være grundigt registreret i protokollen.
Dokumentation af Protokollen
Når rengøringsparametre og prøvetagningsmetoder er fastlagt, skal hele rengøringsprocessen samles i en detaljeret protokol. Denne dokumentation skal overholde både regulatoriske og biosikkerhedsstandarder. Inkluder standardprocedurer (SOP'er), der beskriver hvert trin i rengøringsprocessen, fra den indledende forskylning til den endelige inspektion. Angiv koncentrationer af rengøringsmidler, eksponeringstider, skyllevolumener, verifikationskontroller og varigheder for både "dirty hold" og "clean hold" tider.
Inkluder også risikovurderinger, beregninger af overfladearealer, prøveudtagningsplaner og valideringer af analytiske metoder. Den endelige valideringsrapport, når den er godkendt af ledelsen, vil bekræfte, om din rengøringsproces opfylder alle nødvendige kriterier og overholder reglerne [3] .
Kørsel af valideringsstudier
Valg af værst tænkelige scenarier
Identifikation af de sværeste rengøringsudfordringer er nøglen til at bevise, at din rengøringsproces fungerer effektivt.I dyrkede kød faciliteter er rester som høj-protein vækstmedier eller klæbrige dyrkede kød stilladser, der klæber til bioreaktorvægge, blandt de sværeste at fjerne.
Start med at rangere dine produkter baseret på faktorer som opløselighed, viskositet, proteinindhold og hvor længe de forbliver i kontakt med overflader. For eksempel øger vækstmedier med en 20% proteinkoncentration, der har været i brug i 72 timer, risikoen for denaturering og biofilm dannelse [4][5]. Vær særlig opmærksom på udstyr med indviklede designs - som impellerblade, ventil sæder og sensorporte - da disse områder er notorisk svære at rengøre. Testscenarier som et høj-fedt medium versus et høj-sukker medium kan også hjælpe med at dække spektret af produkter, du håndterer [6][7].
Når du har defineret de værst tænkelige scenarier, skal du fokusere på at validere processen ved at gentage rengøringscyklusser.
Gennemførelse af på hinanden følgende rengøringscyklusser
At udføre tre på hinanden følgende rengøringscyklusser er en effektiv måde at bekræfte både reproducerbarhed og effektivitet. Denne tilgang efterligner faktiske produktionsindstillinger, hvilket sikrer, at der ikke overføres rester mellem partier - især kritisk, når der skiftes fra allergenholdige medier.
For at begynde, tilsmudses udstyret med det identificerede værst tænkelige produkt (e.g. , 10% vækstmedie i en bioreaktor). Kør derefter en fuld rengøringscyklus i henhold til din protokol, og tag prøver både før og efter rengøring. Gentag denne proces to gange mere uden at tilsmudse udstyret igen. Data viser, at ved den tredje cyklus er restniveauerne for proteinrester reduceret med mere end 99,9% (en 3-log reduktion) [4][8]. Pilotanlægforsøg har konsekvent vist, at ATP-niveauer falder til under 10 RLU/cm² efter på hinanden følgende cyklusser [5][9].
Når du bekræfter konsekvente rengøringsresultater, anvend en række metoder til detektion af rester for grundig validering.
Testmetoder til detektion af rester
For at sikre biosikkerhed og opfylde lovgivningsmæssige standarder, kombiner flere metoder til detektion af rester. ATP-swabs er et godt udgangspunkt, der tilbyder hurtig screening for organiske rester og mikrober, med detektionsgrænser så lave som 100 RLU (svarende til færre end 1.000 CFU/cm²). Total organisk kulstof (TOC) analyse er et andet vigtigt værktøj, der måler organiske rester fra vækstmedier med acceptable grænser typisk sat under 50 dele pr. milliard.Til protein-specifik detektion - kritisk i produktionen af dyrket kød - kan assays som Bradford eller BCA identificere rester ved koncentrationer så lave som 1–10 µg/mL [6][7].
Mikrobiologisk plating tilføjer et ekstra lag af præcision ved at identificere levedygtige celler, der forbliver efter rengøring. Brug kontaktplader eller svaberprøver på rengjorte overflader, og inkuber prøverne ved 30–35°C i 48–72 timer på tryptic soy agar. Sterile produkter kræver generelt færre end 10 CFU pr. 25 cm². Forskning udført på rustfri stål overflader har vist færre end 1 CFU efter tre rengøringscyklusser [8][10]. For anvendelser inden for dyrket kød, kombiner ATP-swabs til hurtige kontrol med avancerede metoder som HPLC-MS for at detektere spor af allergener, såsom føtalt bovint serum, ved niveauer så lave som 0,1 ppm [6][7].
For vejledning om GMP-kompatibelt testudstyr, konsulter
Indkøb af rengøringsvalideringsudstyr via Cellbase
Når du har etableret effektive metoder til detektion af rester, er det næste skridt at sikre, at du har det rigtige udstyr til at opretholde dine rengøringsvalideringsprocesser.
GMP-kompatibelt udstyr og forsyninger til validering
Ved indkøb af vatpinde, bed leverandører om genvindingsdata for at bekræfte deres effektivitet. Health Canadas vejledning [2] understreger, at rengøringsprocesser skal overholde principperne for kvalitetsrisikostyring. For at opfylde disse standarder skal du sikre, at dine prøvetagningsværktøjer er blevet valideret gennem genvindingsstudier. Derudover skal du verificere, at følsomheden af dine restdetektionsværktøjer matcher de sundhedsbaserede eksponeringsgrænser (HBEL), du har beregnet.
Fokuser på leverandører på
Løsninger til multi-produkt dyrkede kød faciliteter
Multi-produkt faciliteter står over for unikke udfordringer, især risikoen for krydskontaminering ved skift mellem cellelinjer eller medier, der kan indeholde allergener.
Hvis du er afhængig af automatiserede CIP-systemer, skal du kigge efter udstyr, der sporer kritiske rengøringsparametre såsom temperatur, tryk og flowhastighed. Health Canada fremhæver, at "HBEL, såsom PDE eller TTC, kan derefter bruges i risikobestemmelse og begrundelse af maksimale sikre overførselsgrænser til det næste produkt" [2]. CIP-udstyret tilgængeligt gennem
Konklusion
Rengøringsvalidering spiller en afgørende rolle i at sikre sikkerheden og pålideligheden af multi-produkt dyrket kødproduktion. Det går ud over at opfylde lovkrav - det er en investering i at opretholde sikkerhedsstandarder, operationel effektivitet og forbrugertillid. Ved grundigt at validere, at rengøringsprocesser eliminerer krydsproduktkontaminering og biosikkerhedsrisici, opfylder faciliteter ikke kun overholdelse, men minimerer også chancerne for dyre tilbagekaldelser eller driftsforstyrrelser, samtidig med at de styrker tilliden til dyrkede kødprodukter.
Nøglen til effektiv rengøringsvalidering ligger i at sætte klare, målbare mål, der er i overensstemmelse med lovgivningsmæssige forventninger.For eksempel sikrer udskiftning af vage mål med specifikke mål - som at definere acceptable restfjernelseshastigheder - ansvarlighed og forbedrer produktionsresultater. Denne tilgang opfylder ikke kun lovgivningsmæssige krav, men giver også en solid ramme for de praktiske foranstaltninger, der blev skitseret tidligere.
Konsistens er afgørende. Gennemfør kvartalsvise evalueringer for at vurdere effektiviteten af rengøringsprotokoller og foretag justeringer baseret på præstationsdata. Brug de anbefalede ledende og efterslæbende indikatorer til at spore fremskridt, og opdater dokumentationen regelmæssigt, efterhånden som nye indsigter eller lovgivningsmæssige ændringer opstår [4].
Ofte stillede spørgsmål
Hvordan fastsætter jeg restgrænser for hvert produktomskift?
For at fastsætte restgrænser skal du begynde med en grundig risikovurdering for at identificere kritiske rester, der kan udgøre en bekymring. Brug avancerede analytiske teknikker som HPLC (High-Performance Liquid Chromatography) eller TOC (Total Organic Carbon) analyse under valideringsprocessen for nøjagtigt at måle restniveauer.
Når du har indsamlet data fra rengøringskørsler, anvend statistiske metoder - såsom at beregne gennemsnittet plus 2 eller 3 standardafvigelser - for at bestemme acceptable tærskler. Disse beregninger hjælper med at definere grænser, der både er sikre og i overensstemmelse med industristandarder.
Det er essentielt regelmæssigt at genoverveje og forfine disse grænser. Løbende overvågning og validering sikrer, at resttærsklerne forbliver effektive og i overensstemmelse med sikkerhedskravene i det stadigt udviklende felt af dyrket kødproduktion.
Hvad er den bedste måde at vælge en "worst-case" jord i en multi-produkt fabrik?
Når du vælger en "worst-case" jord i en multi-produkt dyrket kød facilitet, fokuser på det restprodukt, der er sværest at rengøre eller udgør den største risiko for krydskontaminering. Dette kan inkludere visse proteiner, fedtstoffer eller komponenter af mediet. Ved at teste rengøringsmetoder på dette udfordrende restprodukt kan du bekræfte, at processen er grundig nok til at håndtere alle andre restprodukter, hvilket sikrer effektiv dekontaminering i hele fabrikken.
Hvornår skal jeg revalidere rengøring efter en proces- eller opskriftsændring?
Revalidering af rengøring bliver essentielt, når der er ændringer i processer, materialer eller udstyr, der kan påvirke rengøringsprotokollens effektivitet eller bringe nye restprodukter ind. Dette trin sikrer, at restprodukter som proteiner, fedtstoffer eller cellulært affald effektivt fjernes, hvilket reducerer risikoen for kontaminering.Derudover bør regelmæssig revalidering være en del af rutineprocedurerne for at opretholde overholdelse og biosikkerhedsstandarder inden for produktionsfaciliteter for dyrket kød.











