Kasvualustojen validointi on pakollinen vaihe viljellyn lihan yrityksille, jotka hakevat hyväksyntää Ison-Britannian markkinoilla. Tämä prosessi varmistaa tuotteiden turvallisuuden, laadun ja vaatimustenmukaisuuden tiukkojen sääntelykehysten, kuten UK Novel Food Regulations (EU 2015/2283), mukaisesti. Tässä on, mitä sinun tulee tietää:
- Avaintarpeet: Kasvualustojen on täytettävä toksikologian, kontaminaation hallinnan, ravitsemuksellisen laadun ja allergeenisuuden standardit.
- UK:n säädökset: Food Standards Agency (FSA) vaatii HACCP-periaatteiden noudattamista ja luokittelua eläinperäisiksi tuotteiksi (POAO).
- Globaalit standardit: Vaikka Iso-Britannia ja EU jakavat samanlaisia kehyksiä, Yhdysvallat noudattaa CGMP-säädöksiä FD&C Actin mukaisesti.
- Validointiprosessi: Sisältää perusteellisen koostumuksen, puhtauden, toiminnallisuuden ja toimittajan vaatimustenmukaisuuden testauksen sekä kattavan dokumentoinnin.
- Tukialoitteet: Yhdistyneen kuningaskunnan vuonna 2025 käynnistetty sääntelyhiekkalaatikko auttaa yrityksiä täyttämään nämä standardit.
Asianmukainen validointi varmistaa turvallisuuden, rakentaa luottamusta ja noudattaa lakisääteisiä vaatimuksia. Artikkeli syventyy vaiheittaiseen prosessiin, mukaan lukien testausmenetelmät, toimittajien pätevyys ja sääntelyyn liittyvät lähetysvinkit.
Kasvatusalustojen sääntelystandardit
Standardit ja ohjeet
Kasvatusalustat, jotka ovat kriittinen osa viljellyn lihan tuotannossa, on täytettävä tiukat kansainväliset sääntelystandardit. Nämä standardit vaihtelevat alueittain, ja niillä on erityiset vaatimukset koostumukselle, turvallisuudelle ja puhtaudelle.
Yhdistyneessä kuningaskunnassa, kasvatusalustoja säännellään uuden elintarvikkeen asetuksen (yhdistetty asetus (EU) 2015/2283) mukaisesti. Ennen markkinoille hyväksymistä vaaditaan perusteellinen turvallisuusarviointi [1]. Elintarvikestandardivirasto (FSA) luokittelee soluviljellyt tuotteet eläinperäisiksi tuotteiksi (POAO) asetuksen (EY) N:o 853/2004 mukaisesti. Tämä luokitus edellyttää, että tuottajat ottavat käyttöön elintarviketurvallisuuden hallintajärjestelmiä, jotka perustuvat vaarojen arvioinnin ja kriittisten hallintapisteiden (HACCP) periaatteisiin [3]. FSA kehittää myös yksityiskohtaisia teknisiä ohjeita kasvatusalustan koostumuksesta, ja lisäpäivityksiä odotetaan [1]. Nämä puitteet muodostavat perustan tarkemmille sääntelyvaatimuksille.
Yhdysvalloissa, lähestymistapa on erilainen. Kasvatusalustan komponenttien on täytettävä nykyiset hyvät tuotantotavat (CGMP), jotka on esitetty Federal Food, Drug, and Cosmetic Actin (FD&C Act) pykälässä 501(a)(4)(B) [4]. FDA luokittelee alustan komponentit "tarvikkeiksi ja reagensseiksi", joita säätelevät 21 CFR osat 210 ja 211.Nämä komponentit on tarkastettava laadun varmistamiseksi kontaminaation estämiseksi [4] . On mielenkiintoista, että viljellyn lihan kasvatusalustan synteettiset komponentit - kuten aminohapot, vitamiinit ja suolat - luokitellaan usein luokan I lääkinnällisiksi laitteiksi 21 CFR 864.2220:n mukaan, mikä vapauttaa ne ennakkoilmoitusvaatimuksista [6][7].
Euroopan unionissa, sääntelykehys on läheisesti yhdenmukainen Yhdistyneen kuningaskunnan kanssa, sillä se noudattaa myös asetusta (EU) 2015/2283. &Euroopan elintarviketurvallisuusviranomainen (EFSA) valvoo hyväksyntäprosessia [1]. ICH Q6B -ohjeiden mukaan kasvatusalustan komponentit, mukaan lukien antibiootit, indusoijat ja muut ainesosat, käsitellään prosessiin liittyvinä epäpuhtauksina. Näitä epäpuhtauksia on valvottava ja vähennettävä hyväksyttäville tasoille [5]. Missä mahdollista, apuaineiden ja reagenssien tulisi noudattaa farmakopean standardeja [5].
| Toimivalta-alue | Ensisijainen sääntely | Luokittelu | Turvajärjestelmä | Median valvonta |
|---|---|---|---|---|
| Yhdistynyt kuningaskunta (GB) | Assimiloitu sääntely (EU) 2015/2283 [1] | Eläinperäinen tuote (POAO) [3] | HACCP (Asetus 852/2004) [3] | FSA/FSS Sandbox-ohjeistus [1] |
| Euroopan unioni / NI | Asetus (EU) 2015/2283 [1] | Eläinperäinen tuote (POAO) [3] | HACCP (Asetus 852/2004) [3] | EFSA:n hyväksyntäprosessi [1] |
| Yhdysvallat | FD&C Act Section 501(a)(4)(B) [4] | New Animal Drug / Food [4] | CGMP (21 CFR 210/211) [4] | FDA CVM / USDA-FSIS [4] |
Viljellyn lihan sääntelyvaatimukset
Viljellyn lihan tuottajien on varmistettava, että jokainen kasvatusalustan erä noudattaa tiukkoja turvallisuus- ja laatustandardeja.Kasvualustan validointi on keskeinen osa näiden tuotteiden laajempaa sääntelykehystä. HACCP-periaatteiden (asetus (EY) 852/2004) mukaisesti kasvualusta tunnistetaan ensisijaiseksi syötteeksi ja mahdolliseksi kontaminaation lähteeksi - kemiallinen, mikrobiologinen tai muu [3] . FSA korostaa tätä huolta:
"Soluviljeltyjen tuotteiden tuotannon pääasialliset vaarat liittyvät solulinjan identiteettiin (ja johdonmukaisuuteen), tuotantoprosessin aikana aiheutuneisiin vaaroihin (mikrobiologinen kontaminaatio, kasvualusta ja jäännöskomponentit lopputuotteessa) ja allergeeneihin." [3]
Jos kasvualustan koostumukseen tehdään muutoksia, vaaditaan välitön HACCP-katsaus [3]. Yhdistyneessä kuningaskunnassa validointi on suoritettava ennen käyttöönottoa, jotta voidaan varmistaa virtauskaavioiden tarkkuus ja ohjaustoimenpiteiden tehokkuus [3].
Yhdysvalloissa FDA vaatii, että kaikki reagenssit ja väliainekomponentit täyttävät tiukat laatuvaatimukset haitallisten aineiden välttämiseksi [4]. Toimittajien ja sopimuslaboratorioiden on noudatettava CGMP-säädöksiä, ja mikä tahansa toimittaja, joka ei noudata niitä, on poistettava, jotta tuotteita ei luokitella "väärennetyiksi" [4]. FDA korostaa tämän tärkeyttä:
"Kaikki uudet eläinlääkkeet, mukaan lukien ACTP:t, on valmistettava CGMP:n mukaisesti, jotta varmistetaan, että nämä lääkkeet täyttävät Federal Food, Drug, and Cosmetic Act (FD&C Act) -lain turvallisuusvaatimukset." [4]
Tällä hetkellä useat yritykset, jotka osallistuvat Ison-Britannian sääntelyhiekkalaatikkoon - kuten BlueNalu, Gourmey, Hoxton Farms, Mosa Meat,
Kasvatusalustan validointivaiheet
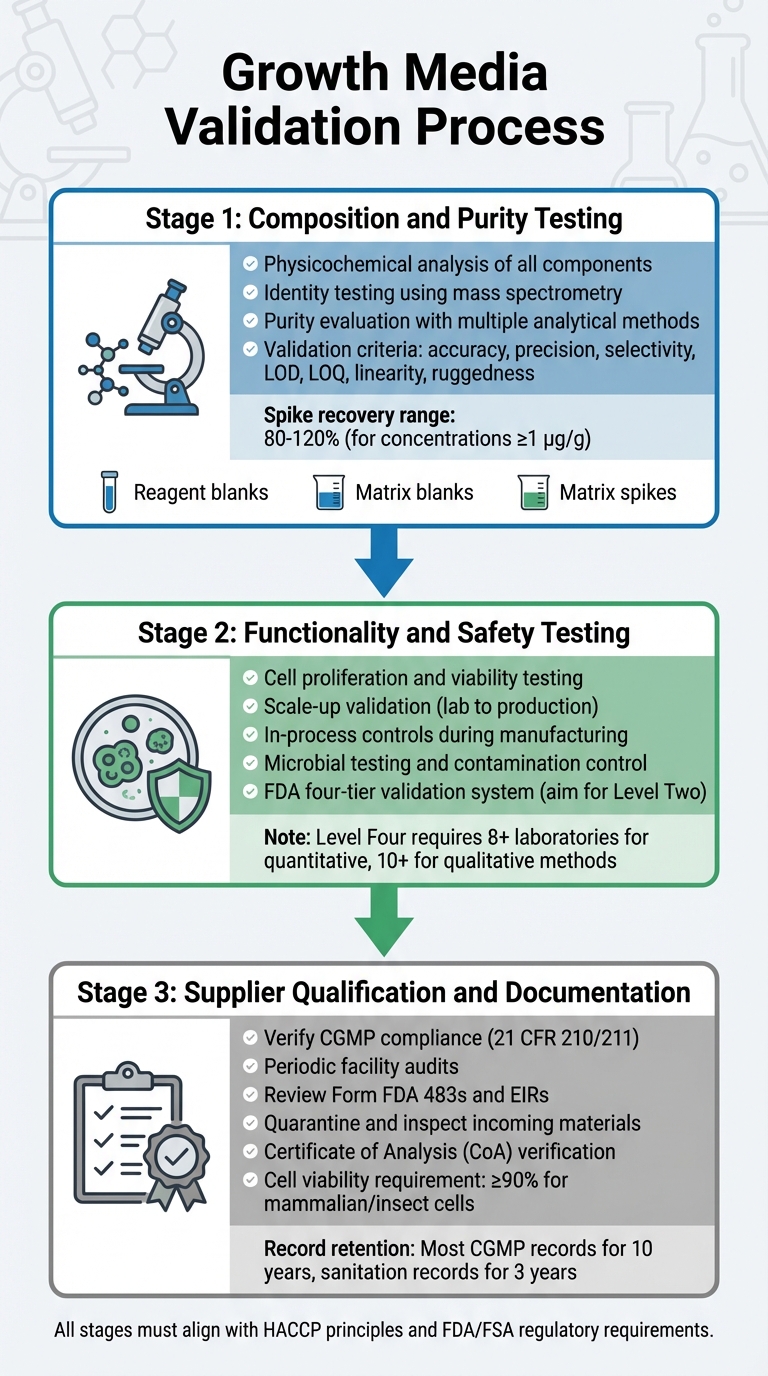
Kasvatusalustan validointiprosessi viljellyn lihan sääntelyhyväksyntää varten
Kasvatusalustan validointi sisältää yksityiskohtaisen prosessin, joka tutkii sen koostumusta, toimivuutta, turvallisuutta ja toimittajan vaatimustenmukaisuutta.Jokainen vaihe rakentuu edellisen päälle, varmistaen vankan validointiprosessin, joka on linjassa sääntelyvaatimusten kanssa. Tämä sisältää koostumuksen, toiminnallisuuden ja bioprosessiväliaineiden toimittajien vaatimustenmukaisuuden testauksen.
Koostumus- ja puhtausanalyysi
Ensimmäinen vaihe keskittyy perusteelliseen fysikaalis-kemialliseen analyysiin jokaisesta komponentista. Tämä sisältää ainesosien, kuten aminohappojen, vitamiinien ja epäorgaanisten suolojen, tarkan koostumuksen, fysikaalisten ominaisuuksien ja molekyylirakenteen tunnistamisen [5]. Molekyylirakenteiden vahvistamiseksi identiteettitestaus käyttää erittäin spesifisiä menetelmiä, mukaan lukien fysikaalis-kemialliset, biologiset ja immunokemialliset tekniikat. Työkaluja, kuten massaspektrometriaa, käytetään molekyyli-identiteettien varmistamiseen niiden fragmentaatiokuvioiden kautta [8].
Puhtausarviointi vaatii useita analyyttisiä menetelmiä haluttujen komponenttien erottamiseksi epäpuhtauksista.Nämä testit on käsiteltävä sekä prosessiin liittyviä että tuotteeseen liittyviä epäpuhtauksia [5]. Analyyttisten tekniikoiden on täytettävä tiukat validointikriteerit, mukaan lukien tarkkuus, toistettavuus, valikoivuus, havaitsemisrajat (LOD), määritysrajat (LOQ), lineaarisuus ja kestävyys [8]. Validointiprotokollien tulisi myös sisältää:
- Reagenssiblankit varmistaakseen, että reagenssit ovat vapaita analyyteistä.
- Matriksiblankit varmistaakseen, että näyteympäristö ei häiritse.
- Matriksipiikit palautumisen ja tarkkuuden arvioimiseksi.
Kvantitatiivisille menetelmille pitoisuuksilla 1 µg/g (ppm), hyväksyttävät piikkipalautukset ovat tyypillisesti välillä 80% ja 120% [8].
Jotta johdonmukaisuus säilyisi, valmistajien tulisi luoda tuotantoon edustavista eristä johdettuja ensisijaisia viitemateriaaleja. Nämä toimivat jäljitettävinä standardeina työviitemateriaalien kalibroinnissa [5]. Kun puhtauskoe on valmis, median on osoitettava kykynsä tukea tehokasta solukasvua ja täyttää turvallisuusstandardit.
Toiminnallisuus- ja turvallisuustestaus
Kun koostumus on vahvistettu, median on osoitettava tehokkuutensa viljellyn lihan tuotannon tukemisessa. Tämä sisältää sen osoittamisen, että solut voivat lisääntyä, säilyttää elinkelpoisuutensa ja laajentua laboratoriotiloista tuotantomääriin. Tämä siirtymä vaatii usein pilottimittakaavan järjestelmiä tarvittavien sääntelytietojen tuottamiseksi.FDA vaatii valmistuksen aikana prosessinhallintaa, alkaen varhaisista vaiheista, kuten solujen passagointi ja sadonkorjuu, varmistaakseen tuotteen yhdenmukaisuuden ja turvallisuuden [4].
Turvallisuuden validointi sisältää tiukan mikrobien testauksen ja kontaminaation hallinnan, kuten FDA:n ennakkomarkkina-arvioinneissa on esitetty [9].
FDA käyttää nelitasoista järjestelmää kemiallisten menetelmien validointiin, alkaen tasosta yksi (hätä- tai rajoitettu käyttö) tasoon neljä (täydet yhteistyötutkimukset, jotka täyttävät AOAC/ISO-standardit) [8]. Rutiininomaista sääntelytestausta varten pyri tason kaksi yhden laboratorion validointiin, joka sisältää kattavan suorituskyvyn arvioinnin [8]. Täydet yhteistyötutkimukset kvantitatiivisille menetelmille vaativat vähintään kahdeksan laboratorion osallistumisen, kun taas kvalitatiiviset menetelmät tarvitsevat kymmenen [8]. Kun median suorituskyky on vahvistettu, on tärkeää varmistaa, että kaikki raaka-aineet tulevat vaatimustenmukaisilta toimittajilta.
Toimittajan pätevyys ja dokumentointi
Valmistajien on työskenneltävä varmennettujen, CGMP-vaatimusten mukaisten toimittajien kanssa. Toimittajien tulisi täyttää 21 CFR 210/211 -standardit [4]. Varmennus sisältää toimittajien tilojen säännölliset auditoinnit, joilla arvioidaan laadunhallintaohjelmien, menettelyjen ja yleisen CGMP-vaatimustenmukaisuuden noudattamista [4].
Ennen sopimusten tekemistä tarkista toimittajan vaatimustenmukaisuushistoria, mukaan lukien FDA:n lomake 483 ja laitoksen tarkastusraportit (EIR) [4]. FDA korostaa tätä velvollisuutta:
"Ennen kuin teet sopimuksen, sopimuksen tai muun järjestelyn toisen laitoksen kanssa suorittaaksesi minkä tahansa valmistusvaiheen puolestasi, sinun tulisi varmistaa, että laitos noudattaa sovellettavia sääntelyyn liittyviä CGMP-vaatimuksia." [4]
Kaikki saapuvat materiaalit on asetettava karanteeniin ja tarkastettava ennen vapauttamista, jotta ne täyttävät päämääritykset [10]. Toimittajien on toimitettava analyysitodistus (CoA) tai jäljitettävät, CGMP/GLP-vaatimusten mukaiset testitulokset [10]. Vakaille solulinjoille dokumentoinnin on sisällettävä jäljitettävä kloonaushistoria [10]. Imettäväiset tai hyönteissolut vaativat tyypillisesti vähintään 90% elinkelpoisuuden hyväksymiseksi CGMP-projekteissa [10]. Asiakirjat on säilytettävä sääntelyohjeiden mukaisesti [4] .
Sopimuksissa on selkeästi määriteltävä CGMP-vastuut ja vaadittava toimittajia ilmoittamaan valmistajille kaikista ehdotetuista muutoksista testisarjoihin tai -menetelmiin [4]. Jos testaus ulkoistetaan, varmista, että sopimuslaboratoriot käyttävät validoituja analyyttisiä menetelmiä ja ovat FDA-rekisteröityjä [4].
Sääntelyyn liittyvien asiakirjojen valmistelu
Kun kasvatusalustasi on validoitu, seuraava vaihe on koota asiakirja, joka osoittaa FDA:n ja USDA-FSIS:n edellyttämien kaikkien turvallisuus- ja laatustandardien noudattamisen. Tämä asiakirja toimii kriittisenä linkkinä validoinnin ja sääntelyn noudattamisen välillä, antaen viranomaisille selkeän kuvan kasvatusalustasi turvallisuudesta ja tuotantoprosesseista.
Hakemuskansion vaaditut osat
Kansiosi tulisi sisältää yksityiskohtainen erittely kasvatusalustan koostumuksesta, luetellen kaikki aminohapot, vitamiinit, epäorgaaniset suolat ja kasvutekijät. FDA:n ohjeet korostavat, että tarkastusprosessi arvioi paitsi itse kasvatusalustan myös koko tuotantoprosessin. Tämä sisältää primaaristen ja kuolemattomien solulinjojen ja pankkien perustamisen, valmistusvalvonnan toteuttamisen sekä kaikkien komponenttien ja syötteiden varmistamisen [11].
Lisäksi kansion on sisällettävä perusteellinen turvallisuus- ja toksikologinen arviointi, joka todistaa viljellyn materiaalin ja kaikkien sen syötteiden elintarviketurvallisuuden. Sisällytä valmistusvalvontatiedot, prosessin validointitiedot ja laatuohjelman dokumentaatio osoittaaksesi, että tuotantosi on johdonmukaista ja saasteetonta.
Sinun tulisi myös toimittaa toimitus- ja reagenssien tarkistusasiakirjat, jotka osoittavat validoinnin kaikille mediassa käytetyille materiaaleille, mukaan lukien itse valmistetut. USDA-FSIS:n säätelemiin tuotteisiin sisällytä HACCP-suunnitelmat ja hygieniakäytännöt. FDA suosittelee säilyttämään suurimman osan CGMP-asiakirjoista vähintään 10 vuotta, kun taas laitoksen puhdistus- ja hygienia-asiakirjat tulisi säilyttää vähintään 3 vuotta [4]. Tämä on linjassa toimittajan pätevöintipyrkimysten kanssa, varmistaen, että kaikki syötteet täyttävät CGMP- ja sääntelyvaatimukset.
Laitoksen vaatimustenmukaisuuden dokumentointi
Ennen viljellyn lihan tuottamista, käsittelyä tai varastointia ihmisravinnoksi, laitosten on rekisteröidyttävä FDA:lle [12]. Dokumentaatiosi tulisi sisältää kattavan elintarviketurvallisuussuunnitelman, joka käsittelee vaarojen analysointia (biologiset, kemialliset ja fysikaaliset), ennaltaehkäiseviä toimenpiteitä (kuten puhtaanapito, allergeenien hallinta ja toimitusketjun toimenpiteet) sekä valvontamenettelyjä [12].
Myös mediantäyttösimulaatiot ovat keskeinen vaatimus. Näihin kuuluu 14 päivän inkubointi ja kasvunedistämistestit aseptisten käytäntöjen vahvistamiseksi. Kuten FDA selittää:
"Mediantäytön tulisi arvioida kriittisten (steriilien) laitteiden aseptista kokoonpanoa ja toimintaa, pätevöittää operaattorit ja arvioida heidän tekniikkaansa sekä osoittaa, että ympäristön hallinta on riittävää" [2].
Varmista, että tietueesi sisältävät toimittajan pätevöintitiedot, kuten testit, jotka on tehty toimittajan ensimmäisille kolmelle erälle varmistaaksesi, että ne vastaavat analyysitodistusta.Muut olennaiset asiakirjat sisältävät ympäristönvalvontalokit, laitteiden kalibrointiaikataulut ja lämpötilan seurantatiedot. USDA:n säätelemille prosesseille valmistele HACCP-suunnitelmat, kirjalliset puhtaanapidon standarditoimintamenettelyt (SSOP:t) ja takaisinvetomenettelyt [12][13].
sbb-itb-ffee270
Regulaationmukainen kasvatusalustojen hankinta Cellbase
Varmennetut toimittajat viljellylle lihalle
Kun olet varmistanut kasvatusalustasi koostumuksen, seuraava askel on hankkia komponentit, jotka täyttävät sääntelyvaatimukset. Tämä ei ole yhtä yksinkertaista kuin tilata geneerisiltä toimittajilta. Soluviljellyille tuotteille sovelletaan tiukkoja hygieniavaatimuksia, ja jokaisella kasvatusalustan komponentilla on oltava erityinen dokumentaatio sääntelyhyväksyntää varten [3]. Siinä vaiheessa
Hankinnan ominaisuudet
Alusta tarjoaa myös läpinäkyvän hinnoittelun ja suoran viestintäominaisuuden, jonka avulla tiimit voivat nopeasti pyytää tarjouksia, analyysitodistuksia ja muita sääntelyasiakirjoja. Yhdistämällä nämä kriittiset hankintatoiminnot yhteen järjestelmään, joka on räätälöity viljellyn lihan tuotantoon,
Päätelmä
Kasvatusalustan validointi sääntelyhyväksyntää varten ei ole vain muodollisuus - se on laillinen vaatimus viljellyn lihan tuotteiden tuomiseksi Ison-Britannian markkinoille. Tämä sisältää perusteellisen koostumuksen ja puhtauden testauksen, vahvan HACCP-suunnitelman toteuttamisen ja yksityiskohtaisen dokumentoinnin ylläpitämisen jokaisessa vaiheessa.
"Elintarvikkeita ei saa saattaa markkinoille, jos ne ovat turvattomia. Tämä tarkoittaa, että ne eivät saa olla terveydelle haitallisia tai ihmisravinnoksi kelpaamattomia." - Food Standards Agency [3]
Yhdistyneen kuningaskunnan elintarvikestandardiviraston sääntelyhiekkalaatikko korostaa sen sitoutumista työskentelemään teollisuuden toimijoiden kanssa selkeän teknisen ohjeistuksen luomiseksi kasvatusalustojen koostumuksesta [1]. Yritykset, jotka asettavat oikean validoinnin etusijalle nyt, ovat vahvemmassa asemassa, kun nämä ohjeet on täysin määritelty.
Vaatimustenmukaisuuden täyttäminen ei ole pelkästään sääntelyvaatimusten täyttämistä - se on kuluttajien luottamuksen ansaitsemista ja tuoteturvallisuuden varmistamista. Tiukka laadunvalvonta on sekä sääntelyhyväksynnän että markkinoille pääsyn ytimessä. Jotta hyväksyntäprosessi sujuisi, keskity vahvojen validointiprotokollien rakentamiseen, tarkkojen tietojen ylläpitämiseen ja yhteistyöhön luotettavien toimittajien. nämä toimenpiteet eivät ainoastaan yksinkertaista hyväksyntää, vaan myös luovat pohjan suuremmalle kuluttajien luottamukselle.
UKK
Mitkä ovat tärkeimmät vaiheet kasvatusalustojen validoinnissa sääntelyhyväksyntää varten?
Kasvatusalustojen validointi sääntelyhyväksyntää varten tarkoittaa sen todistamista, että koostumus on turvallinen, luotettava ja soveltuu viljellyn lihan tuottamiseen. Prosessi näyttää yleensä tältä:
- Riskinarviointi: Aloita määrittelemällä käyttämäsi solulinja, tuotteen tavoitteet ja sen kriittiset laatuominaisuudet (kuten pH tai ravintoainekoostumus). Tunnista mahdolliset vaarat, kuten mikrobikontaminaatio, ja laadi toimenpiteet näiden riskien hallitsemiseksi.
- Testaus ja spesifikaatiot: Aseta selkeät hyväksymiskriteerit tekijöille, kuten steriiliys, puhtaus ja teho. Käytä vakiintuneita testausmenetelmiä varmistaaksesi, että nämä standardit täyttyvät johdonmukaisesti.
- Validointitutkimukset: Suorita perusteellinen prosessivalidointi, mukaan lukien laitteiden kvalifiointi ja useiden erien testaus, varmistaaksesi, että tulokset ovat toistettavissa ja johdonmukaisia.
- Stabiilisuustestaus: Tarkista, kuinka media säilyy ajan myötä arvioimalla sen laatua koko suunnitellun säilyvyysajan asianmukaisissa säilytysolosuhteissa (tyypillisesti 2–8 °C).
- Dokumentointi: Kokoa kaikki yhteen kattavaksi validointiasiakirjaksi. Tämän tulisi sisältää kaikki testitulokset ja analyysit sääntelyvaatimusten täyttämiseksi.
Käsittelemällä huolellisesti jokaisen näistä vaiheista, keräät todisteet, jotka osoittavat, että media täyttää viljellyn lihan tuotannon turvallisuus- ja laatuvaatimukset.
Mitkä ovat tärkeimmät erot Ison-Britannian ja Yhdysvaltojen säädöksissä viljellyn lihan kasvatusalustoille?
Yhdistyneessä kuningaskunnassa viljellyn lihan kasvatusalustojen sääntely kuuluu uusien elintarvikkeiden asetuksen (EU-asetus 2015/2283), piiriin, joka on säilytetty Ison-Britannian lainsäädännössä. Kaikki kasvatusalustat, joita käytetään tuotteissa, joita ei ole yleisesti kulutettu ennen 15. toukokuuta 1997, on käytävä läpi virallinen uusien elintarvikkeiden arviointi Elintarvikestandardiviraston (FSA) toimesta. Tämä prosessi vaatii yksityiskohtaisten asiakirjojen toimittamista, mukaan lukien tietoja alustan koostumuksesta, alkuperästä ja puhtaudesta. Lisäksi tarvitaan HACCP-pohjainen riskinarviointi osoittamaan, miten epäpuhtaudet hallitaan soluviljelyprosessin aikana.
Joulukuusta 2025 lähtien FSA on ottanut käyttöön soluviljeltyjen tuotteiden hiekkalaatikon. Tämä aloite tarjoaa ohjeistusta ja tukee nopeampaa tiedonkeruuta uusien elintarvikkeiden hakemuksille.Yritysten on toimitettava kattava asiakirja, joka käsittelee median turvallisuutta, johdonmukaisuutta ja valmistuksen validointia saadakseen lopullisen hyväksynnän. Vasta tämän hyväksynnän jälkeen tuotetta voidaan myydä Isossa-Britanniassa.
Sen sijaan Yhdysvalloilla ei ole erityistä uuselintarvikekehystä, joka olisi räätälöity kasvatusmedioille, mikä tekee suorista sääntelyvertailuista haastavia. Isossa-Britanniassa toimiville yrityksille sellaisten mediakomponenttien hankkiminen, jotka jo täyttävät nämä tiukat standardit, voi yksinkertaistaa hyväksyntäprosessia.
Miten Ison-Britannian sääntelyhiekkalaatikko tukee kasvatusmedioiden validointia?
Ison-Britannian sääntelyhiekkalaatikko viljellyille tuotteille tarjoaa hyvin järjestetyn ympäristön, jossa yritykset voivat testata ja hienosäätää kasvatusmediakoostumuksiaan.Ohjattuna Food Standards Agency (FSA) ja Food Standards Scotland (FSS), tämä ohjelma toimii kuuden kuukauden jaksoissa. Tänä aikana yritykset voivat suorittaa turvallisuustestejä, tehdä riskinarviointeja ja tarkistaa dokumentaatiota samalla kun saavat arvokasta palautetta sääntelyviranomaisilta.
Tämä käytännönläheinen lähestymistapa mahdollistaa käytännön kokeilut ja vaiheittaiset parannukset, nopeuttaen turvallisuustietojen keräämistä ja auttaen yrityksiä mukautumaan sääntelyvaatimuksiin. Viljellyn lihan parissa työskenteleville, ennakkoon hyväksytyn kasvatusalustan hankkiminen











