Histonimuokkaukset ovat proteiinien kemiallisia muutoksia, jotka vaikuttavat geenien aktiivisuuteen muuttamatta DNA:ta. Nämä muokkaukset ovat elintärkeitä solulinjojen kehittämisessä viljellyn lihan tuotannossa, auttaen soluja kasvamaan, säilyttämään identiteettinsä ja erilaistumaan lihaskudokseksi. Artikkeli tutkii, kuinka tietyt histonimerkit, kuten H3K4me3 (geenien aktivointi), H3K27ac (tehostajan aktiivisuus) ja H3K27me3 (geenien tukahduttaminen), säätelevät solukäyttäytymistä.
Käsitellyt keskeiset kohdat:
- H3K4me3 tukee aktiivisia geenejä ja nopeaa erilaistumista.
- H3K27ac hallitsee tehostajia geeniekspression aikana kasvuvaiheissa.
- H3K27me3 varmistaa, että ei-toivotut geeniohjelmat pysyvät inaktiivisina.
- Kromatiinitilat, joita nämä merkit muokkaavat, vaihtelevat lajien ja solutyyppien välillä, vaikuttaen tuotannon laatuun.
Artikkeli korostaa myös viimeaikaista tutkimusta, mukaan lukien kuinka sikojen solujen positionaalinen geeniekspressio vaikuttaa lihan laatuun ja kuinka kohdennettu epigeneettinen editointi voi parantaa solulinjojen suorituskykyä. Tulevaisuuden suuntiin kuuluu epigeneettisten työkalujen hienosäätö ja kromatiinitilojen tutkiminen tuotannon tehokkuuden ja mittakaavan.
optimoimiseksi.Histonimuutokset selitetty | Asetylaatio, metylointi & Geenien säätely
sbb-itb-ffee270
Histonimuutosten tyypit ja niiden toiminnot
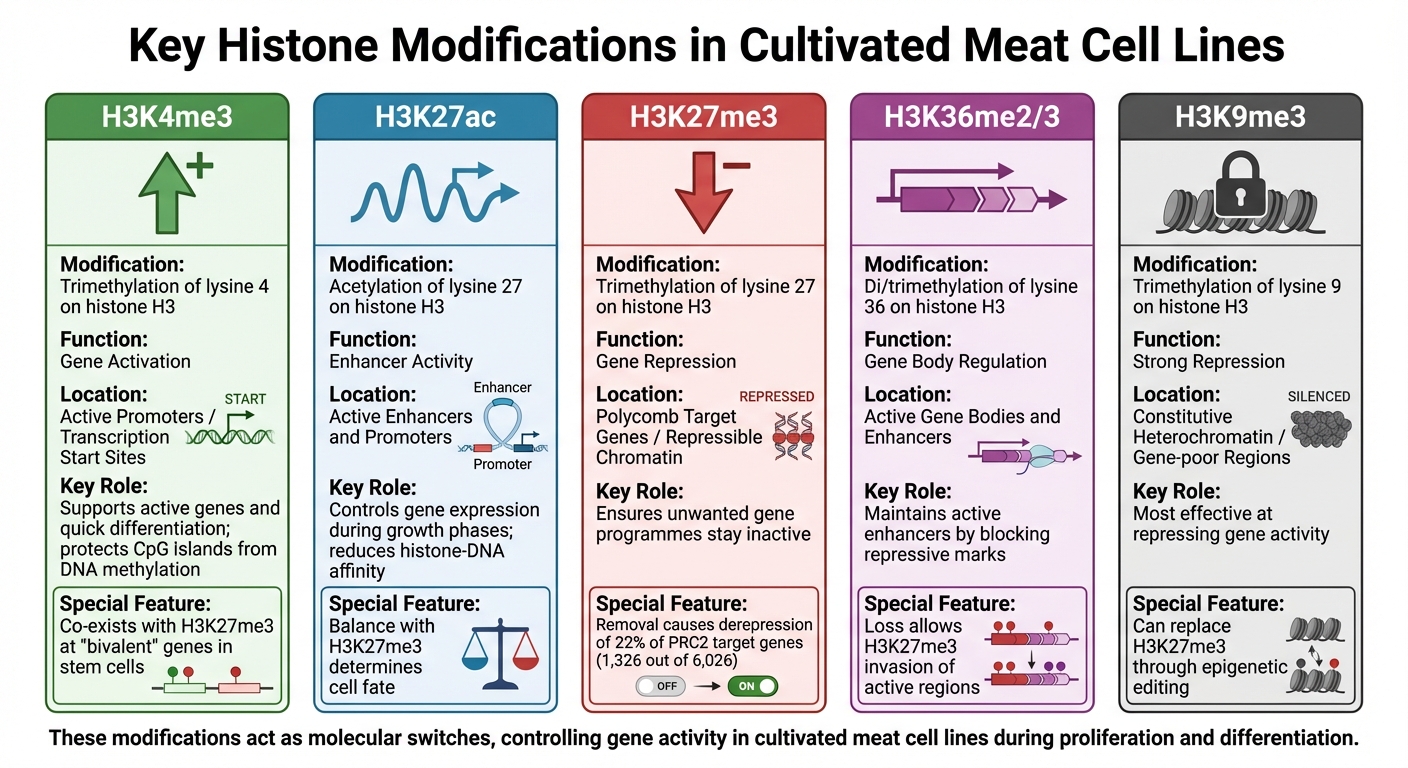
Keskeiset histonimuutokset viljellyissä lihasolulinjoissa: Toiminnot ja genomiset kontekstit
Histonimuutoksilla on keskeinen rooli geenien aktiivisuuden säätelyssä, toimien kuin molekyylikytkimet, jotka kontrolloivat, ovatko geenit päällä vai pois päältä viljellyissä lihasolulinjoissa.Nämä kemialliset merkit - pääasiassa metylointi ja asetylointi - kiinnittyvät histonien tiettyihin jäännöksiin, luoden erillisiä genomisia kuvioita. Jokaisella modifikaatiolla on erityinen tehtävä, ja ymmärtämällä näitä rooleja tutkijat voivat paremmin ennustaa ja vaikuttaa solujen käyttäytymiseen tuotannon aikana. Tämä tieto on olennaista prosessien optimoinnissa viljellyn lihan bioprosessoinnissa.
Tässä on erittely tärkeimmistä histonimuutoksista, jotka vaikuttavat geenien säätelyyn viljellyn lihan solulinjoissa.
H3K4me3 ja geenien aktivointi
H3K4me3 (lysiini 4:n trimetylointi histoni H3:ssa) liittyy aktiivisiin geenien promoottoreihin ja helpottaa transkriptiota geenien aloituskohdissa, erityisesti solu- ja aineenvaihduntaan liittyvissä geeneissä. Tämä modifikaatio suojaa myös CpG-saarten promoottoreita uudelta DNA-metyloinnilta, varmistaen, että olennaiset geenit pysyvät saatavilla transkriptiota varten [4].
Ensisijaisissa tai kuolemattomissa solulinjoissa, joita käytetään viljellyssä lihassa, H3K4me3 esiintyy usein yhdessä repressiivisten merkkien, kuten H3K27me3:n kanssa "bivalent" geeneissä. Nämä geenit pysyvät valmiina aktivoitumaan, mikä mahdollistaa nopean erilaistumisen lihaskudokseksi tarvittaessa [4] .
Mielenkiintoista on, että H3K4me3 vuorovaikuttaa muiden modifikaatioiden kanssa. Esimerkiksi H3K36me3:n asettuminen voi estää H3K4-metyylitransferaasien toimintaa, vähentäen H3K4me3-tasoja promoottoreissa ja muuttaen geeniekspressiokuvioita [4].
H3K27ac ja tehostajan aktiivisuus
H3K27ac (histoni H3:n lysiini 27:n asetylaatio) on aktiivisten tehostajien ja promoottoreiden merkki. Vähentämällä histonien ja DNA:n välistä affiniteettia, H3K27ac luo ympäristön, joka edistää transkriptiota [5] . Viljellyissä lihasolulinjoissa H3K27ac-tasojen muutokset eri kasvuvaiheissa määrittävät, mitkä geenit ilmentyvät solujen siirtyessä lisääntymisestä erilaistumiseen.
Tasapaino H3K27ac:n ja repressiivisten modifikaatioiden, kuten H3K27me3:n, välillä on avainasemassa solun kohtalon määrittämisessä. Esimerkiksi H3K36me2:n menetys, joka tukee tehostajatoimintaa, voi sallia H3K27me3:n tunkeutua aiemmin aktiivisiin alueisiin, vähentäen H3K27ac-tasoja ja hiljentäen kohdegeenit [5].
H3K27me3 ja geenien repressio
H3K27me3 (lysiini 27:n trimetylaatio histoni H3:ssa) on repressiivinen merkki, joka edistää suljettuja kromatiinirakenteita, tehokkaasti hiljentäen geenejä. Tämä modifikaatio, jonka katalysoi Polycomb Repressive Complex 2 (PRC2), on kriittinen tuhansien kehityksellisten geenien repressioiden ylläpitämisessä [4] .
Viljellyissä lihasolulinjoissa H3K27me3 varmistaa, että ei-toivotut geeniohjelmat pysyvät inaktiivisina tiettyjen kasvuvaiheiden aikana, säilyttäen solujen tarkoitetun identiteetin.
"H3K27me3 yhdessä H2AK119ub1:n kanssa on välttämätön useiden tuhansien Polycomb-kohdegeenien transkriptionaalisen repressioinnin ylläpitämiseksi." - Nature Communications [4]
Tutkimukset ovat osoittaneet, että H3K27me3:n poistaminen hiiren alkion kantasoluista johtaa noin 22% (1,326:sta 6,026:sta) PRC2-kohdegeenin derepressioon [4] . Viljellyn lihan osalta tämän modifikaation hallinta voi auttaa tukahduttamaan vaihtoehtoisia solukohtaloita, kuten rasva- tai sidekudoksen muodostumista, keskittyen samalla lihaksen kehitykseen.
| Histonimuokkaus | Säätelytoiminto | Genominen konteksti |
|---|---|---|
| H3K4me3 | Geenien aktivointi | Aktiiviset promoottorit / Transkription aloituskohdat |
| H3K27ac | Tehostajatoiminta | Aktiiviset tehostajat ja promoottorit |
| H3K27me3 | Geenien repressio | Polycomb-kohdegeenit / Repressiokelpoinen kromatiini |
| H3K36me2/3 | Geenirungon säätely | Aktiiviset geenirungot ja tehostajat |
| H3K9me3 | Vahva repressio | Konstitutiivinen heterokromatiini / Geeniköyhät alueet |
Kromatiinitilat viljellyissä lihassolulinjoissa
Histonimuokkaukset eivät toimi yksin - ne yhdistyvät muodostamaan kromatiinitiloja, , jotka ovat ainutlaatuisia genomisia ympäristöjä, jotka säätelevät geenien saatavuutta.Nämä tilat ovat ratkaisevassa asemassa viljellyn lihan solulinjojen käyttäytymisen muokkaamisessa sekä laajentumisen että erilaistumisen aikana, mikä tekee niistä keskeisiä bioprosessoinnin optimoinnissa.
Kromatiinitilojen tunnistaminen histonimerkkien avulla
Tutkijat kartoittavat kromatiinitiloja tutkimalla histonimerkkien, kuten H3K4me3, H3K27ac ja H3K27me3, yhdistelmiä. Esimerkiksi porsaan sikiön fibroblasteissa (PFF) ja trofektodermisoluissa (PTr2) on tunnistettu 10 erilaista kromatiinitilaa, mukaan lukien aktiiviset transkription aloituskohdat, kaksitoimiset promoottorit ja oletetut tehostajat [6]. Nämä tilat auttavat ennustamaan geenien aktiivisuutta.
Tehostajatilat, jotka ovat pääasiassa merkitty H3K27ac:lla intergeenisten ja intronisten alueiden kohdalla, ovat usein rikastettu yhdessä kromatiinin uudelleenmuokkausproteiinin BRG1 kanssa [6].
Erityisen huomionarvoinen piirre on laajojen H3K4me3-alueiden läsnäolo, jotka kattavat alueita, jotka ovat 4 kb tai enemmän. Nämä alueet edustavat vain 1.7% - 1.8% kaikista ennustetuista transkription aloituskohdista sian solulinjoissa, mutta ovat kriittisiä kehitys- ja kudosspesifisten geenien merkitsemisessä [6] . Mielenkiintoista on, että sian sikiön fibroblasteissa 52% geeneistä , jotka on merkitty näillä laajoilla alueilla, ovat kudosspesifisiä, verrattuna vain 25% PTr2-soluissa [6] .
"Nämä havainnot parantavat ymmärrystämme epigeneettisestä maisemasta, joka on läsnä sian varhaisessa kehityksessä, ja tarjoavat näkemyksiä siitä, miten kromatiinitilan vaihtelut liittyvät solun identiteettiin." - BMC Epigenetiikka & Kromatiini [6]
Nämä kromatiinitilaprofiilit eivät ainoastaan eroa yksittäisen lajin sisällä, vaan vaihtelevat myös eri eläinsolulinjojen välillä, joita käytetään viljellyn lihan tuotannossa.
Kromatiinin erot eläinsolulinjojen välillä
Kromatiinitilamallit muuttuvat merkittävästi riippuen viljellyn lihan tuotannossa käytetystä lajista ja solutyypistä. Esimerkiksi kanan solulinjoissa H3K4me3 kattaa 30% - 55% sen genomisesta esiintymisestä geenien promoottoreissa [7]. Kuitenkin kanan primordiaalisissa sukusoluissa (PGC), H3K4me3-tasot laskevat huomattavasti verrattuna pluripotentteihin soluihin. Tämä vähennys tukee bivalenttien tilojen siirtymistä repressiivisiin tiloihin sukusolujen spesifikaation aikana [7] .
Sikojen trofektodermin (PTr2) solut osoittavat korkeampia H3K27ac-tasoja promoottorialueilla (57.36%) verrattuna sikiön fibroblasteihin (41.58%), kun taas H3K27me3-rikastuminen on alhaisempaa PTr2-soluissa (7.77%) kuin PFF-soluissa (22%) [6]. Nämä vaihtelut heijastavat kunkin kehitysvaiheen erityisiä epigeneettisiä tarpeita ja vaikuttavat siihen, miten nämä solut reagoivat viljelyolosuhteisiin.
Naudan satelliittisolujen, differentoituminen "reservisolun" kohtaloon (Pax7+/Ki-67-) ohjautuu hiljaisilla kromatiinitiloilla, joita säätelevät NOTCH- ja MAPK/ERK-signaalit. Tämä prosessi kuitenkin vähentää proteiinituottoa [3]. Tällainen vaihtelu korostaa, kuinka kromatiinitilat vaikuttavat suoraan tuotannon tehokkuuteen. Näiden erojen syvällisempi ymmärtäminen on ratkaisevan tärkeää solulinjojen suorituskyvyn hienosäätämiseksi viljellyn lihan tuotannossa.
Histonimuutosten käyttö solulinjojen parantamiseksi
Rakentaen kromatiinitiloista tiedetyn päälle, syvennymme siihen, miten kohdennetut histonimuutokset voivat suoraan parantaa viljellyn lihan solulinjojen suorituskykyä.
Proliferaation ja suspensiokasvuun sopeutumisen tehostaminen
Histonimerkkien säätäminen voi merkittävästi lisätä solujen proliferaatiota ja auttaa soluja siirtymään kiinnittyneestä kasvusta suspensiokasvuun. Tämä muutos on ratkaiseva viljellyn lihan bioreaktorijärjestelmille. Esimerkiksi, H3K36-metylaation vähentäminen tekee fibroblasteista vähemmän reagoivia TGFβ:lle, mikä johtaa joustavampaan solutilaan [1].
Joulukuussa 2022, Believer Meats -tutkijat saavuttivat läpimurron kanan fibroblasteilla (HUN-CF-2 ja HUN-CF-4).He osoittivat spontaania kuolemattomuutta seerumittomissa suspensioviljelmissä, saavuttaen 100 miljoonaa solua per ml (10⁸ solua/ml) ja saavuttaen saantoja 36% w/v . Tiimi, jota johti Yaakov Nahmias, käytti lesitiiniä - elintarviketurvallista pientä molekyyliä - aktivoidakseen PPARγ-reitin ja edistääkseen rasvan muodostumista ilman geneettistä muuntelua. Heidän viljelty kanan prototyyppinsä sai aistinvaraisen arvion 4,5 viidestä [2] .
"Kuolemattomuus ilman geneettistä muuntelua ja korkean tuoton valmistus ovat kriittisiä viljellyn lihan markkinoille saattamiseksi." - Yaakov Nahmias, Chief Scientific Officer, Believer Meats [2]
Nämä havainnot korostavat tarkkojen epigeneettisten työkalujen potentiaalia solulinjojen kehittämisen edelleen hienosäätämiseksi.
Tarkkuus epigeneettisessä editoinnissa
Näiden solumuutosten täydentämiseksi tarkat epigeneettiset editointimenetelmät mahdollistavat histonimerkkien kohdennetun manipuloinnin. Vuoden 2025 tutkimus hiiren alkion kantasoluista osoitti, että kimeerinen rekrytoija (S12N), joka on fuusioitu SUV39H2:n tai SETD2:n katalyyttisiin domeeneihin, voi korvata H3K27me3:n H3K9me3:lla tai H3K36me3:lla tuhansissa geeneissä. Näistä H3K9me3 osoittautui tehokkaammaksi geenitoiminnan tukahduttamisessa [8].
Kuitenkin näiden muutosten onnistuminen riippuu suuresti olemassa olevasta kromatiiniympäristöstä. Esimerkiksi jäännös H3K4me3 geenien promoottoreissa voi estää DNA-metylaatiokoneiston, mikä vaikeuttaa halutun geenin hiljentämisen saavuttamista [8]. Tämä viittaa siihen, että solun suorituskyvyn optimointi vaatii usein useiden histonimerkkien säätämistä samanaikaisesti sen sijaan, että keskityttäisiin yhteen muutokseen.
Päätelmät ja tulevaisuuden suuntaviivat
Keskeiset havainnot
Histonimuokkaukset ovat kriittisessä roolissa molekyylikytkiminä , ohjaamassa geenien aktiivisuutta viljellyissä lihasolulinjoissa. Erityisesti H3K36me2 ja H3K36me3 auttavat ylläpitämään aktiivisia tehostajia estämällä repressiivisiä merkkejä, kuten H3K27me2/3, tunkeutumasta geenirunkoihin [9][10]. Kun H3K36-metylaatio menetetään, kromatiinirakenne häiriintyy, mikä sallii repressiivisten merkkien, kuten H3K9me3, tunkeutua aktiivisiin alueisiin [9]."H3K36-metylaatio [on] keskeinen kromatiinitilan ja genomirakenteen säätelijä." - Nature Communications [9]
Histonimerkkien välinen vuorovaikutus on olennaista solulinjojen suorituskyvyn parantamiseksi.Tutkimukset viittaavat siihen, että useiden histonimuutosten kohdentaminen yhdessä saavuttaa usein parempia tuloksia kuin keskittyminen vain yhteen [4].
Näiden havaintojen perusteella tulevien tutkimusten on hyödynnettävä tarkkoja epigeneettisiä työkaluja varmistaakseen jatkuvat parannukset viljellyn lihan solulinjojen suorituskyvyssä.
Tulevaisuuden tutkimusmahdollisuudet
Solulinjojen suorituskyvyn parantaminen vaatii innovatiivisia lähestymistapoja, kuten yksisolutason RNA-sekvensointi, epigeneettisen maiseman kartoittamiseksi eri solualapopulaatioissa. Tämä on erityisen tärkeää tunnistettaessa ja ymmärrettäessä hiljaisia "varastosoluja", jotka vastustavat erilaistumista. Nämä solut, jotka ilmentävät markkereita kuten PAX7 ja NOTCH2 sen sijaan, että sitoutuisivat myogeeniseen fuusioon, muodostavat merkittävän haasteen viljellyn lihan tuotannossa [3].
Toinen lupaava suuntaus sisältää kimeeristen epigeneettisten kompleksien kehittämisen tarkkaan, ei-geneettiseen hallintaan. Esimerkiksi vuonna 2025 tutkijat osoittivat, että yhdistämällä SUZ12:n N-terminaali SUV39H2:n tai SETD2:n katalyyttisiin domeeneihin voidaan tehokkaasti korvata H3K27me3 H3K9me3:lla tai H3K36me3:lla useissa geeneissä [4]. Lisäksi H3K36me2:n seuranta tehostajissa voisi toimia laadunvalvontamerkkinä solulinjan vakauden varmistamiseksi [9].
Tulevien ponnistelujen tulisi keskittyä H3K36-metylaation ylläpitämiseen solusukupolvien yli. Tämä auttaisi estämään epigeneettistä ajautumista, mahdollistaen tutkijoille ja yrityksille, kuten
UKK
Kuinka histonimerkit vaikuttavat lihasten erilaistumiseen viljellyissä lihasolulinjoissa?
Histonimerkit ovat keskeisiä tekijöitä lihasten erilaistumisessa, erityisesti viljellyissä lihasolulinjoissa. Esimerkiksi H3K27me3-merkin väheneminen erilaistumisen aikana käynnistää myogeeniset transkriptio-ohjelmat, mikä mahdollistaa lihasten kehitykseen tarvittavien geenien aktivoitumisen. Histonimuutosten, kuten H3K27me3, hienosäätö tukee solulinjojen siirtymistä proliferaatiosta lihaskudoksen muodostamiseen tietyillä ominaisuuksilla. Nämä epigeneettiset säädöt ovat olennaisia viljellyn lihan tuotannon edistämiseksi.
Mitkä histonimuutokset ennustavat parhaiten vakaata, korkean tuoton solukasvua bioreaktoreissa?
H3K36-metylaatio erottuu luotettavana merkkinä vakaalle, korkean tuoton solukasvulle bioreaktoreissa.Tämä muutos on keskeisessä roolissa solujen identiteetin säilyttämisessä ja linjausohjelmien hallinnassa - molemmat ovat olennaisia solujen tasaisen lisääntymisen varmistamiseksi, erityisesti viljellyn lihan tuotannossa.
Voiko epigeneettinen editointi parantaa solulinjoja muuttamatta niiden DNA-sekvenssiä?
Epigeneettinen editointi tarjoaa keinon parantaa solulinjoja muuttamatta niiden DNA-sekvenssiä. Säätämällä histonimerkkejä ja kromatiinirakennetta se hallitsee geeniekspressiota. Tutkimukset histonimuutoksista korostavat, kuinka nämä muutokset voivat vaikuttaa solujen identiteettiin ja toimintaan. Tämä lähestymistapa tarjoaa erityistä lupausta viljellyn lihan solulinjojen hienosäätöön.











