Testy na jałowość są kluczowe dla produkcji mięsa hodowlanego, gdzie nawet drobne zanieczyszczenie może prowadzić do kosztownych niepowodzeń partii. Proces ten zapewnia, że żadne szkodliwe mikroorganizmy nie zakłócają pracy bioreaktora, chroniąc zarówno jakość produktu, jak i rentowność finansową. Przy średnich wskaźnikach zanieczyszczeń wynoszących 11,2% - i wzrastających do 19,5% w przypadku produkcji na dużą skalę - producenci stają przed znacznymi wyzwaniami w utrzymaniu sterylnych środowisk.
Kluczowe punkty obejmują:
- Główne źródła zanieczyszczeń: Personel, surowce i operacje bioreaktora są powszechnymi punktami wejścia dla drobnoustrojów.
- Metody testowania: Filtracja membranowa dla dużych objętości, bezpośrednia inokulacja dla mniejszych próbek oraz testy obciążenia biologicznego podczas produkcji są powszechnie stosowane.
- Monitorowanie w czasie rzeczywistym: Narzędzia takie jak czujniki tlenu rozpuszczonego i analiza gazów wylotowych umożliwiają wczesne wykrywanie aktywności drobnoustrojów.
- Nowe Technologie: Monitorowanie oparte na AI, sterylizacja zimną plazmą i zautomatyzowane systemy obrazowania oferują szybsze i bardziej precyzyjne zarządzanie zanieczyszczeniami.
Dla producentów mięsa hodowlanego, połączenie tradycyjnych testów sterylności z zaawansowanymi rozwiązaniami monitorującymi jest niezbędne do zmniejszenia ryzyka i poprawy efektywności produkcji.
Rocker Discover - Jak przeprowadzić test sterylności?
sbb-itb-ffee270
Źródła zanieczyszczeń w systemach bioreaktorów
Aby zapobiec awariom partii w systemach bioreaktorów, kluczowe jest zidentyfikowanie, skąd pochodzi zanieczyszczenie. Zanieczyszczenia zazwyczaj dzielą się na trzy główne kategorie: mikrobiologiczne, cząsteczkowe i endotoksyny. Każdy typ stwarza unikalne wyzwania dla produkcji mięsa hodowlanego, co sprawia, że opracowanie specyficznych strategii zapobiegawczych jest niezbędne.
Personel jest głównym źródłem zanieczyszczeń, często wprowadzając zanieczyszczenia poprzez złuszczanie skóry, niewłaściwe ubieranie się lub słabą higienę rąk [4][7]. Nawet przy rygorystycznych protokołach, proste ruchy mogą zakłócać przepływ powietrza, prowadząc do turbulencji lub obszarów stagnacji, gdzie mogą gromadzić się zanieczyszczenia [4][9]. U.S. Food and Drug Administration podkreśla związane z tym ryzyko, stwierdzając, że "jakakolwiek ręczna lub mechaniczna manipulacja sterylizowanym lekiem, komponentami, pojemnikami lub zamknięciami przed lub podczas aseptycznego montażu stwarza ryzyko zanieczyszczenia i dlatego wymaga starannej kontroli" [4].
Czynniki środowiskowe również odgrywają znaczącą rolę.Na przykład, brak utrzymania dodatniego ciśnienia w zakresie 10–15 Pascalów może pozwolić na przedostanie się niefiltrowanego powietrza do stref sterylnych [3][4]. Dodatkowo, problemy takie jak nieskuteczność filtrów HEPA - gdzie retencja cząstek spada poniżej 99,97% - lub uszkodzone filtry gazów sprężonych mogą szybko zagrozić sterylności [4].
Zanieczyszczenie surowców i linii komórkowych
Surowce wchodzące do systemu bioreaktora stanowią duże ryzyko zanieczyszczenia. Nieweryfikowane składniki, komponenty pożywek wzrostowych i linie komórkowe (dostępne poprzez wyspecjalizowane rynki B2B) mogą wprowadzać patogeny oportunistyczne [2]. Środowisko bogate w składniki odżywcze w pożywkach do hodowli komórkowych jest szczególnie podatne na zanieczyszczenia, co sprawia, że procesy produkcji mięsa hodowlanego są bardziej narażone w porównaniu do bioprocesów mikrobiologicznych [8].
Składniki wrażliwe na ciepło, które nie mogą być poddane autoklawowaniu, są szczególnie ryzykowne, ponieważ wymagają alternatywnych metod sterylizacji, takich jak filtracja [1][8]. Ponadto, sam proces inokulacji niesie ze sobą wrodzone ryzyko. Nawet gdy membrany są dezynfekowane alkoholem lub procedury są wykonywane w pobliżu otwartego płomienia, nie ma absolutnej gwarancji przeciwko zanieczyszczeniu podczas wprowadzania linii komórkowych [8]. Te ryzyka podkreślają znaczenie dokładnej weryfikacji surowców przed ich wprowadzeniem do systemu.
Ryzyka operacyjne bioreaktorów
Codzienne operacje w bioreaktorach stwarzają liczne możliwości zanieczyszczenia. Pobieranie próbek ręczne jest szczególnie wysokiego ryzyka, ponieważ każdy punkt dostępu zwiększa szansę wprowadzenia zanieczyszczeń [1].Problemy takie jak uszkodzone uszczelki, uszkodzone pierścienie O-ring lub niesterylizowane zamknięcia dodatkowo zwiększają ryzyko [4][8]. Dodatkowo, przenoszenie materiałów z obszarów o niższej klasyfikacji do stref o wyższej klasyfikacji bez odpowiedniej dekontaminacji stanowi kolejną krytyczną podatność [7].
Utrzymanie ścisłej kontroli środowiskowej jest niepodważalne. Różnice ciśnień między obszarami czystymi powinny być monitorowane na bieżąco, a wszelkie nietypowe zmiany muszą być natychmiast zbadane [4]. W krytycznych obszarach klasy 100 (ISO 5) liczba cząstek o rozmiarach ≥0,5 μm musi pozostawać poniżej 3 520 cząstek na metr sześcienny podczas operacji [4].Ponadto, rozpylanie środków dezynfekujących lub 70% alkoholu izopropylowego w pobliżu próbnika powietrza może zwiększać odczyty cząsteczek, podczas gdy kondensat na filtrach gazowych może powodować blokady lub sprzyjać wzrostowi drobnoustrojów [4][7].
Te operacyjne ryzyka podkreślają znaczenie wdrożenia rygorystycznych metod testowania jałowości w celu ochrony procesów bioreaktorów.
Metody Testowania Jałowości dla Bioreaktorów
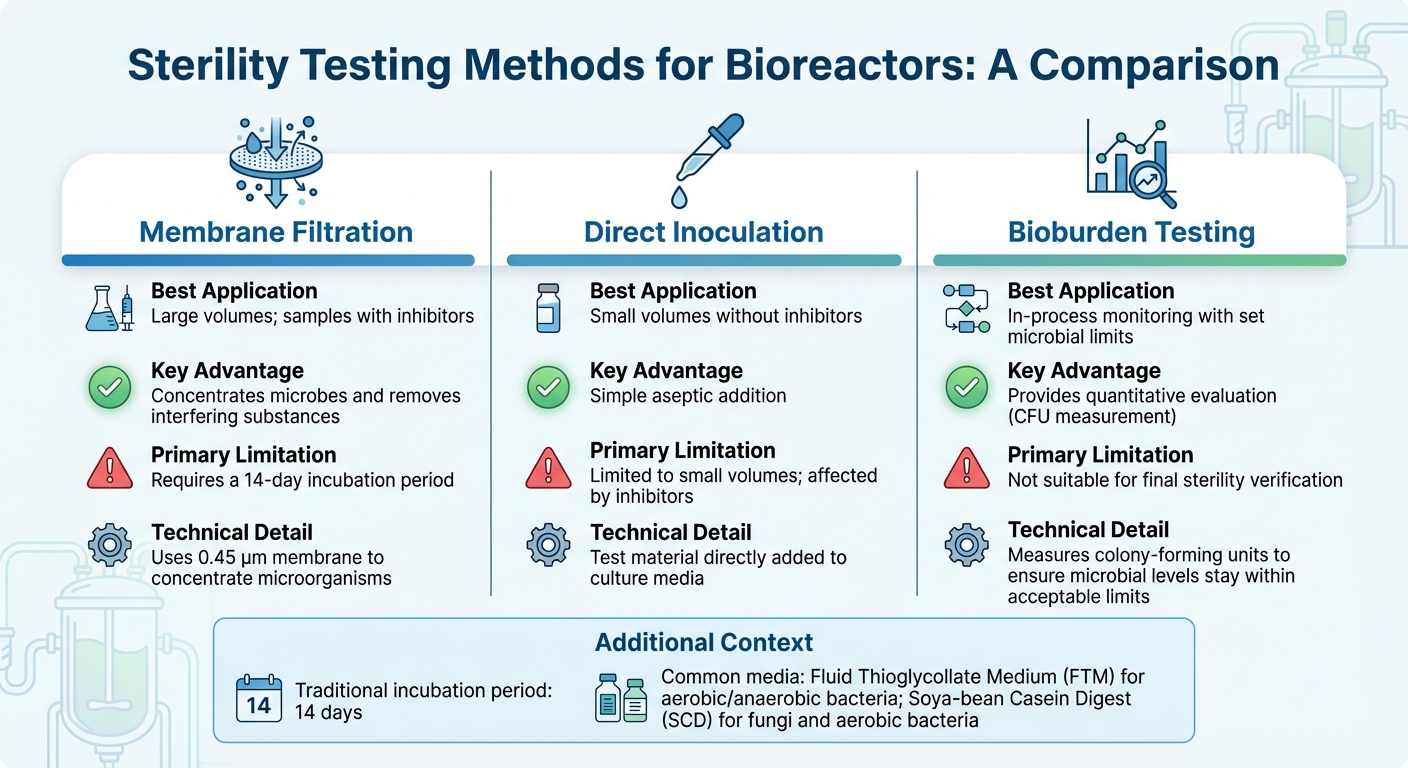
Porównanie Metod Testowania Jałowości dla Bioreaktorów
Wybór odpowiedniego testu jałowości dla bioreaktorów zależy od takich czynników jak rozmiar bioreaktora, etap produkcji i wyzwania związane ze skalowaniem, oraz skład próbki - szczególnie gdy obecne są inhibitory. Dla większości zastosowań przemysłowych, filtracja membranowa jest preferowaną metodą [3].Tymczasem techniki molekularne, takie jak PCR, oferują szybsze wykrywanie specyficznych zanieczyszczeń. Poniżej omówimy metody dostosowane do produkcji mięsa hodowlanego, uwzględniając unikalne wyzwania związane z testowaniem zarówno dużych, jak i małych próbek.
Dla próbek o dużej objętości, powszechnych w bioreaktorach przemysłowych, filtracja membranowa wykorzystuje membranę o średnicy 0,45 µm do koncentracji mikroorganizmów, poprawiając czułość wykrywania [10]. Ta metoda jest szczególnie skuteczna dla próbek zawierających antybiotyki, ponieważ płukanie może wyeliminować inhibitory przed inkubacją. Z drugiej strony, bezpośrednia inokulacja, gdzie materiał testowy jest bezpośrednio dodawany do pożywki, działa lepiej dla mniejszych objętości próbek, ale ma trudności z obsługą substancji hamujących. Po skoncentrowaniu próbek i usunięciu inhibitorów, inkubacja i walidacja zapewniają dokładność wyników.
Tradycyjne testy jałowości opierają się na 14-dniowym okresie inkubacji w celu wizualnego potwierdzenia wzrostu drobnoustrojów [3]. Powszechnie stosowane pożywki to Fluid Thioglycollate Medium (FTM) dla bakterii tlenowych i beztlenowych oraz Soya-bean Casein Digest (SCD) dla grzybów i bakterii tlenowych. Przed przeprowadzeniem jakiegokolwiek testu jałowości, kluczowe jest potwierdzenie, że produkt nie hamuje wzrostu drobnoustrojów poprzez testy bakteriostazy i fungistazy.
Do bieżącego monitorowania procesów, ilościowe testy obciążenia biologicznego oferują bardziej praktyczne rozwiązanie niż binarne testy jałowości, szczególnie w produkcji mięsa hodowlanego. W przeciwieństwie do testów jałowości, które dają prosty wynik zaliczenia/niezaliczenia, testy obciążenia biologicznego mierzą jednostki tworzące kolonie (CFU), aby zapewnić, że poziomy drobnoustrojów pozostają w dopuszczalnych granicach.Ta metoda jest zgodna z nowymi standardami jakości spożywczej, łącząc rygorystyczne kontrole farmaceutyczne z ekonomicznymi realiami produkcji żywności na dużą skalę.
W przypadku dostaw do testów jałowości i rozwiązań bioreaktorowych, profesjonaliści zajmujący się mięsem hodowlanym mogą zwrócić się do zaufanych dostawców, takich jak
| Metoda | Najlepsze Zastosowanie | Kluczowa Zaleta | Główne Ograniczenie |
|---|---|---|---|
| Filtracja Membranowa | Duże objętości; próbki z inhibitorami | Koncentruje mikroby i usuwa substancje zakłócające[3] | Wymaga 14-dniowego okresu inkubacji[3] |
| Bezpośrednia Inokulacja | Małe objętości bez inhibitorów | Proste aseptyczne dodanie | Ograniczone do małych objętości; wpływ inhibitorów[3] |
| Testowanie Obciążenia Biologicznego | Monitorowanie w procesie z ustalonymi limitami mikrobiologicznymi | Zapewnia ilościową ocenę | Nieodpowiednie do ostatecznej weryfikacji jałowości [3] |
Monitorowanie w czasie rzeczywistym i zapewnienie jałowości
Poleganie na tradycyjnych 14-dniowych testach jałowości wiąże się z ryzykiem utraty całych partii, jeśli zanieczyszczenie zostanie wykryte zbyt późno.Monitorowanie w czasie rzeczywistym oferuje proaktywne rozwiązanie poprzez obserwację kluczowych parametrów procesowych w momencie ich występowania. Pozwala to na natychmiastowe działanie, jeśli coś pójdzie nie tak. W produkcji mięsa hodowlanego, gdzie cykle bioreaktorów trwają tygodniami i wykorzystują kosztowne pożywki wzrostowe, wczesne wykrycie zanieczyszczenia może zaoszczędzić tysiące funtów i uniknąć opóźnień w produkcji. Łącząc dane w czasie rzeczywistym z konwencjonalnymi testami jałowości, producenci mogą zniwelować lukę między opóźnionym potwierdzeniem a szybką interwencją.
Monitorowanie oparte na czujnikach
Kluczowe wskaźniki, takie jak poziom tlenu rozpuszczonego (DO) i poziomy pH, mogą wcześnie sygnalizować zanieczyszczenie. Gdy bakterie lub grzyby przenikają do bioreaktora, szybko zużywają tlen - powodując spadek poziomu DO - i uwalniają kwasy metaboliczne, które znacznie obniżają pH [12]. Te zmiany można wykryć na kilka godzin przed tym, jak zanieczyszczenie stanie się widoczne.Podczas gdy tradycyjne testy jałowości potwierdzają wyniki po zakończeniu procesu, monitorowanie w czasie rzeczywistym działa jako zabezpieczenie, zapewniając, że proces przebiega zgodnie z planem i wcześniej adresując ryzyko zanieczyszczenia.
Analiza gazów wylotowych, wykorzystująca spektrometrię masową z sektorem magnetycznym, nieustannie mierzy poziomy tlenu i dwutlenku węgla w gazach wylotowych bioreaktora. W kontrolowanych badaniach zanieczyszczeń ta metoda zidentyfikowała wzrost mikroorganizmów w ciągu 22,4 godzin poprzez zmiany w poziomie tlenu, podczas gdy wykrywanie oparte na pH opóźniało się do 25,8 godzin [13]. Systemy z sektorem magnetycznym dostarczają precyzyjnych pomiarów tlenu z dokładnością do 0,003% (v/v) przez siedem dni, przewyższając tradycyjne detektory paramagnetyczne, które są dokładne jedynie do ±0,2% (v/v) [13].
Sensory spektroskopowe zapewniają nieinwazyjne monitorowanie przez ściany jednorazowych bioreaktorów, co jest kluczowe dla utrzymania jałowości.Spektroskopia UV-vis może wykrywać uszkodzenia błony poprzez pomiar absorpcji światła w zakresie 350–400 nm, podczas gdy wyciekające materiały wewnątrzkomórkowe pojawiają się w zakresie 800–900 nm [14]. Sondy pojemnościowe, jedyne dostępne komercyjnie czujniki zaprojektowane do pomiaru gęstości żywych komórek, osiągają to poprzez wykrywanie zmian w polaryzacji błony [14]. Dla zakładów zarządzających wieloma bioreaktorami, narzędzia takie jak Rapid Multi-Stream Sampler mogą monitorować jednocześnie do 16 strumieni gazu [13].
Te systemy oparte na czujnikach, w połączeniu z kontrolą środowiskową, taką jak zapobieganie zanieczyszczeniom HVAC, tworzą solidną obronę przed zanieczyszczeniami.
Kontrola Środowiskowa i Ciśnieniowa
Utrzymanie dodatniego ciśnienia między strefami czystego pomieszczenia jest kluczowe dla zapobiegania przedostawaniu się zanieczyszczeń [3].Systemy nadciśnieniowe, w połączeniu z filtracją HEPA, działają jako fizyczne bariery przed wnikaniem drobnoustrojów. Słyszalne lub wizualne alarmy na filtrach HEPA mogą natychmiast powiadomić personel, jeśli ciśnienie spadnie poniżej akceptowalnych poziomów [3].
Liczenie cząstek nieożywionych to kolejna warstwa obrony. Liczniki cząstek laserowych nieustannie weryfikują, czy środowisko spełnia normy czystości powietrza ISO podczas pracy. Monitorując zarówno cząstki 0,5 µm, jak i 5,0 µm, te urządzenia zapewniają, że jakość powietrza pozostaje w wymaganych granicach [7]. Jeśli wystąpią nieoczekiwane odchylenia - takie jak nagły spadek DO lub wahania pH - natychmiastowa izolacja dotkniętego bioreaktora i wstrzymanie dodawania pożywki mogą zapobiec rozprzestrzenianiu się zanieczyszczeń [12].
W celu pozyskiwania specjalistycznych czujników i sprzętu dostosowanego do operacji związanych z mięsem hodowlanym, firmy takie jak
Nowe technologie w testowaniu jałowości
Tradycyjne metody testowania jałowości często zawodzą z powodu długich, 14-dniowych okresów inkubacji i polegania na ręcznym pobieraniu próbek, co może pozostawiać luki w wykrywaniu. Nowe technologie wkraczają, aby sprostać tym wyzwaniom, oferując szybsze i bardziej precyzyjne wykrywanie zanieczyszczeń. Jest to szczególnie istotne w produkcji mięsa hodowlanego, gdzie wysoki koszt pożywek wzrostowych i długie czasy hodowli sprawiają, że zanieczyszczenie w późnym etapie jest finansowym koszmarem.
Systemy monitorowania oparte na AI
Sztuczna inteligencja przekształca wykrywanie zanieczyszczeń poprzez analizę danych w czasie rzeczywistym w celu identyfikacji intruzji mikrobiologicznych.Kiedy bakterie atakują bioreaktor, zużywają tlen i produkują kwasy metaboliczne, co prowadzi do zauważalnych spadków poziomów tlenu rozpuszczonego i pH. Systemy AI mogą wykrywać te odchylenia w zużyciu tlenu i składników odżywczych, sygnalizując potencjalne zanieczyszczenie znacznie wcześniej niż tradycyjne testy obciążenia biologicznego i protokoły sterylności mogą dostarczyć wyniki [12].
Te platformy AI również włączają modele matematyczne, aby określić dokładny czas wystąpienia zanieczyszczenia i symulować, jak populacje drobnoustrojów rosną w czasie. Pomaga to operatorom śledzić zanieczyszczenie do jego źródła, niezależnie od tego, czy jest to wadliwe źródło zasilania, błąd operacyjny, czy problem z wyposażeniem. Techniki takie jak analiza prawdopodobieństwa Poissona dodatkowo zwiększają dokładność testów obciążenia biologicznego, zmniejszając prawdopodobieństwo fałszywych negatywów [12].
"Modele matematyczne pomagają w szacowaniu czasu wprowadzenia zanieczyszczeń i dynamiki wzrostu drobnoustrojów, poprawiając śledzenie zanieczyszczeń." - Naveenganesh Muralidharan, Starszy Menedżer, MSAT, AGC Biologics [12]
Gdy wykrywane są anomalie, natychmiastowe działania - takie jak izolowanie bioreaktora i wstrzymanie wszystkich dodatków paszowych - mogą zapobiec rozprzestrzenianiu się problemu [12]. Systematyczne podejście obejmujące testy obciążenia biologicznego, identyfikację molekularną i analizę szybkości wzrostu jest niezbędne do zidentyfikowania przyczyny źródłowej i wdrożenia środków naprawczych. Te narzędzia AI wypełniają lukę między tradycyjnymi metodami a proaktywnym zarządzaniem zanieczyszczeniami.
Sterylizacja zimną plazmą
Technologia zimnej plazmy oferuje nietermiczną opcję sterylizacji, która jest szczególnie dobrze dostosowana do produkcji mięsa hodowlanego.Działając w temperaturze pokojowej lub w jej pobliżu, jest idealny do sterylizacji wrażliwych komponentów, takich jak części bioreaktorów, czujniki i tworzywa sztuczne, które nie mogą wytrzymać ciepła tradycyjnej autoklawizacji [15][16][17]. Ta metoda wykorzystuje reaktywne formy tlenu i azotu oraz światło UV do zakłócania błon mikroorganizmów i DNA. Jest skuteczna przeciwko szerokiemu zakresowi zanieczyszczeń, w tym przetrwalnikom bakteryjnym (Bacillus, Clostridium), grzybom, wirusom, a nawet prionom [15][17].
Jedną z wyróżniających cech zimnej plazmy jest to, że nie pozostawia toksycznych pozostałości. Po wyłączeniu zasilania, reaktywne formy szybko przekształcają się w tlen, eliminując potrzebę fazy desorpcji [16][18].Jest również energooszczędny, wymagając jedynie standardowego gniazdka elektrycznego zamiast źródeł ciepła opartych na paliwach kopalnych [15][16]. Na przykład badania pokazują, że zimna plazma może osiągnąć >5 log redukcji w Bacillus cereus zarodnikach w ciągu 25 minut przy mocy 300W [15].
Jednak technologia ta nie jest pozbawiona ograniczeń. Jej efekty sterylizacji są głównie powierzchniowe, co oznacza, że ma trudności z penetracją złożonych geometrii, gdzie mikroby mogą ukrywać się w szczelinach lub rowkach [15][16]. Wysoka zawartość białka lub tłuszczu w środowiskach bioreaktorów może również chronić mikroby poprzez wychwytywanie reaktywnych gatunków, zmniejszając efektywność sterylizacji [15][18].
| Funkcja | Zimna plazma |
|---|---|
| Zalety | Nietermiczna, nietoksyczna, energooszczędna, bez pozostałości, szybka[16] |
| Ograniczenia | Ograniczona penetracja, zmniejszona skuteczność w złożonych geometriach[15][16] |
Zautomatyzowane systemy wykrywania oparte na obrazach
Dodając do zestawu, zautomatyzowane systemy obrazowania stanowią potężne narzędzie do wykrywania zanieczyszczeń w czasie rzeczywistym. Te systemy oferują szczegółowe wglądy morfologiczne w rozwój komórek, co jest kluczowe dla wykrywania wzorców zanieczyszczeń w miarę ich występowania[19].W przeciwieństwie do tradycyjnej mikroskopii offline - która wymaga ręcznego pobierania próbek i barwienia - zautomatyzowane obrazowanie integruje się bezproblemowo z monitorowaniem online lub at-line. Pozwala to operatorom monitorować biomasę i zdrowie komórek bez kompromisów w zakresie sterylności [19].
Poprzez redukcję interwencji manualnych, systemy te zmniejszają błędy ludzkie i poprawiają powtarzalność w procesach hodowli [19]. Zaawansowane algorytmy przetwarzania obrazu mogą śledzić postęp fermentacji, optymalizować produkcję metabolitów i zapewniać spójność - kluczowy czynnik przy skalowaniu procesów biotechnologicznych [19].
"Dostępność zaawansowanych technik pobierania próbek w połączeniu z zautomatyzowanymi narzędziami pomiarowymi...może znacznie skrócić czas potrzebny na wybór szczepu, rozwój procesu i kontrolę procesu poprzez zmniejszenie liczby kroków w procesie produkcji/uprawy, zwłaszcza kroków manualnych, oraz ograniczenie propagacji błędów." - A.C. Veloso i E.C. Ferreira, Uniwersytet Minho [19]
Pomimo swoich zalet, integracja tych systemów nie zawsze jest prosta. Kultury komórkowe są złożone, surowce różnią się, a czujniki muszą wytrzymać surowe metody sterylizacji, takie jak para lub napromieniowanie gamma [19]. Dla firm chcących wdrożyć te technologie, platformy takie jak
Wniosek
Zapewnienie sterylności bioreaktora w produkcji mięsa hodowlanego nie jest łatwym zadaniem, ale zintegrowana strategia testowania sterylności może to uczynić osiągalnym.Ta strategia łączy tradycyjne metody, takie jak filtracja membranowa dla większych objętości próbek i bezpośrednie zaszczepianie dla mniejszych, z nowoczesnymi narzędziami molekularnymi, takimi jak PCR i qPCR, do szybkiego badania patogenów. Dodatkowo, monitorowanie środowiska - poprzez pobieranie próbek powietrza i wymazywanie powierzchni - dodaje dodatkowe zabezpieczenie, adresując ryzyko zanieczyszczenia w systemach HVAC, wychwytując potencjalne zanieczyszczenia zanim wpłyną na naczynia produkcyjne [11].
Wybór podejścia do testowania zależy od czynników takich jak wielkość próbki, obecność substancji, które mogą zakłócać wyniki, oraz czy skupiamy się na pełnej walidacji sterylności, czy tylko monitorowaniu obciążenia biologicznego. Pobieranie próbek z wielu punktów w bioreaktorze - góra, środek i dół - pomaga stworzyć dokładny profil mikrobiologiczny i zmniejsza szansę na przeoczenie lokalnych zanieczyszczeń [1].Jest to szczególnie istotne, biorąc pod uwagę, że ryzyko zanieczyszczenia w produkcji mięsa hodowlanego jest znacznie wyższe niż w produkcji biofarmaceutycznej, co podkreśla potrzebę rygorystycznych protokołów sterylności [6].
Kluczowe dla utrzymania sterylności pożywki w bioreaktorach jest pozyskiwanie odpowiedniego sprzętu. Narzędzia takie jak systemy do pobierania próbek aseptycznych z wstępnie sterylizowanymi septami i filtry HEPA zdolne do wychwytywania 99,97% cząstek większych niż 0,3 μm są niezbędne [4]. Platformy takie jak
W miarę rozwoju branży, hybrydowe podejścia do sterylności stają się coraz ważniejsze.Stosowanie kontroli na poziomie farmaceutycznym podczas wczesnych etapów hodowli nasion, przy jednoczesnym przyjęciu standardów spożywczych dla produkcji na dużą skalę, stanowi równowagę między bezpieczeństwem a opłacalnością [5][6]. Te zintegrowane środki będą kamieniem węgielnym bezpiecznej i efektywnej produkcji mięsa hodowanego w miarę postępu w tej dziedzinie.
FAQ
Jakie są główne przyczyny zanieczyszczeń w systemach bioreaktorów używanych do produkcji mięsa hodowanego?
Zanieczyszczenie w systemach bioreaktorów występuje, gdy sterylne środowisko zostaje zakłócone lub gdy pożywki bogate w składniki odżywcze stwarzają idealne warunki do rozwoju drobnoustrojów. Może to być spowodowane kilkoma czynnikami, takimi jak naruszenia podczas pobierania próbek, konserwacji lub zbioru komórek; uszkodzone lub zablokowane filtry gazowe; zanieczyszczenia już obecne w pożywce wzrostowej; lub tymczasowe otwarcia powstałe podczas instalacji lub serwisowania czujników.Na dodatek, zużyty sprzęt może uwalniać cząstki mikroplastiku, które mogą stanowić siedlisko dla mikroorganizmów.
W produkcji mięsa hodowlanego nawet najmniejsze zanieczyszczenie może zagrozić zarówno bezpieczeństwu, jak i wydajności partii. Aby zredukować te ryzyka, kluczowe jest inwestowanie w wysokiej jakości sprzęt, taki jak sterylne filtry, bioreaktory i zestawy czujników, które spełniają rygorystyczne standardy aseptyczne. Platformy takie jak
W jaki sposób sztuczna inteligencja poprawia testowanie sterylności w bioreaktorach?
Systemy oparte na AI przekształcają testowanie sterylności w bioreaktorach do produkcji mięsa hodowlanego, oferując wgląd w czasie rzeczywistym dzięki ciągłemu monitorowaniu.Korzystając z zaawansowanych biosensorów, te systemy monitorują kluczowe czynniki, takie jak pH, rozpuszczony tlen oraz niezbędne metabolity, takie jak glukoza i aminokwasy. Wszystko to odbywa się bez potrzeby ręcznych kontroli, co znacznie zmniejsza ryzyko zanieczyszczenia.
Co wyróżnia te systemy, to ich zdolność do analizy danych za pomocą algorytmów, które porównują odczyty z ustalonymi standardami jałowości. Oznacza to, że mogą wykrywać nawet najmniejsze oznaki wzrostu drobnoustrojów znacznie wcześniej niż tradycyjne metody. Poza samym wykrywaniem, w grę wchodzi analiza predykcyjna, identyfikująca potencjalne zagrożenia, takie jak problemy podczas instalacji czujników lub wejścia przez porty. Systemy te nawet sugerują środki naprawcze, aby pomóc producentom uniknąć kosztownych strat partii.
Mikroskopia wspomagana AI dodaje kolejny poziom wydajności, natychmiast odróżniając zdrowe komórki od zanieczyszczeń, przyspieszając procesy weryfikacji jałowości.Dla producentów, platformy takie jak
Jakie wyzwania ograniczają stosowanie sterylizacji zimną plazmą w bioreaktorach do produkcji mięsa hodowlanego?
Sterylizacja zimną plazmą jest skuteczna w neutralizowaniu drobnoustrojów, ale wiąże się z pewnymi wyzwaniami, gdy jest stosowana w bioreaktorach do produkcji mięsa hodowlanego. Jednym z głównych problemów jest ograniczona głębokość penetracji reaktywnych gatunków wytwarzanych przez plazmę. Utrudnia to dokładną sterylizację dużych objętości lub gęsto upakowanych mediów. Ponadto, uzyskanie równomiernego pokrycia plazmą w całym reaktorze staje się coraz trudniejsze wraz ze wzrostem rozmiaru systemu.
Skalowanie systemów zimnej plazmy z ustawień laboratoryjnych do bioreaktorów na skalę komercyjną wprowadza dodatkowe przeszkody.Większe reaktory wymagają wyższych stosunków mocy do objętości, co może skutkować czasami sterylizacji, które są dalekie od praktycznych. Wiele systemów zimnej plazmy działa również w warunkach próżniowych lub opiera się na gazach reaktywnych, co dodaje warstw złożoności w zakresie bezpieczeństwa, zgodności z przepisami i projektowania sprzętu. Czynniki te sprawiają, że metoda jest mniej idealna dla dużych bioreaktorów typowo wymaganych w komercyjnej produkcji mięsa hodowanego. Innym problemem jest potencjalne uszkodzenie spowodowane przez reaktywne formy tlenu i azotu (RONS), które są kluczowe dla inaktywacji drobnoustrojów. Te reaktywne formy mogą szkodzić wrażliwym komórkom ssaków lub degradować składniki pożywki, co wymaga starannej optymalizacji w celu utrzymania żywotności komórek. W rezultacie zimna plazma jest często stosowana w połączeniu z innymi technikami sterylizacji, a nie jako samodzielne rozwiązanie.











