- Formål: Sikrer, at bioreaktorer opfylder regulatoriske og produktionsstandarder, opretholder sterilitet, præcis miljøkontrol og fødevaresikkerhed.
- Nøglefunktioner: Omrørte tankbioreaktorer blev valgt for deres egnethed til bovine muskelceller, hvilket tilbyder kontrollerede skærekræfter og skalerbarhed.
- Udfordringer: Opskalering af bioreaktorer til høje celletætheder og reduktion af omkostninger krævede nytænkning af materialer, steriliseringsmetoder og procesdesign.
- Løsninger: Overgang til fødevaregodkendte materialer, brug af omkostningseffektive steriliseringsmetoder og integration af maskinlæring til procesoptimering reducerede omkostningerne betydeligt.
- Resultater: Produktionsomkostningerne faldt fra £437,000/kg til £1.95/kg, med en 15-dobling i produktivitet og op til 92% reduktion i drivhusgasemissioner, når der anvendes vedvarende energi.
Denne undersøgelse beskriver, hvordan valideringsprotokoller og smarte designvalg bringer dyrket kød tættere på prisparitet med konventionelt kød.
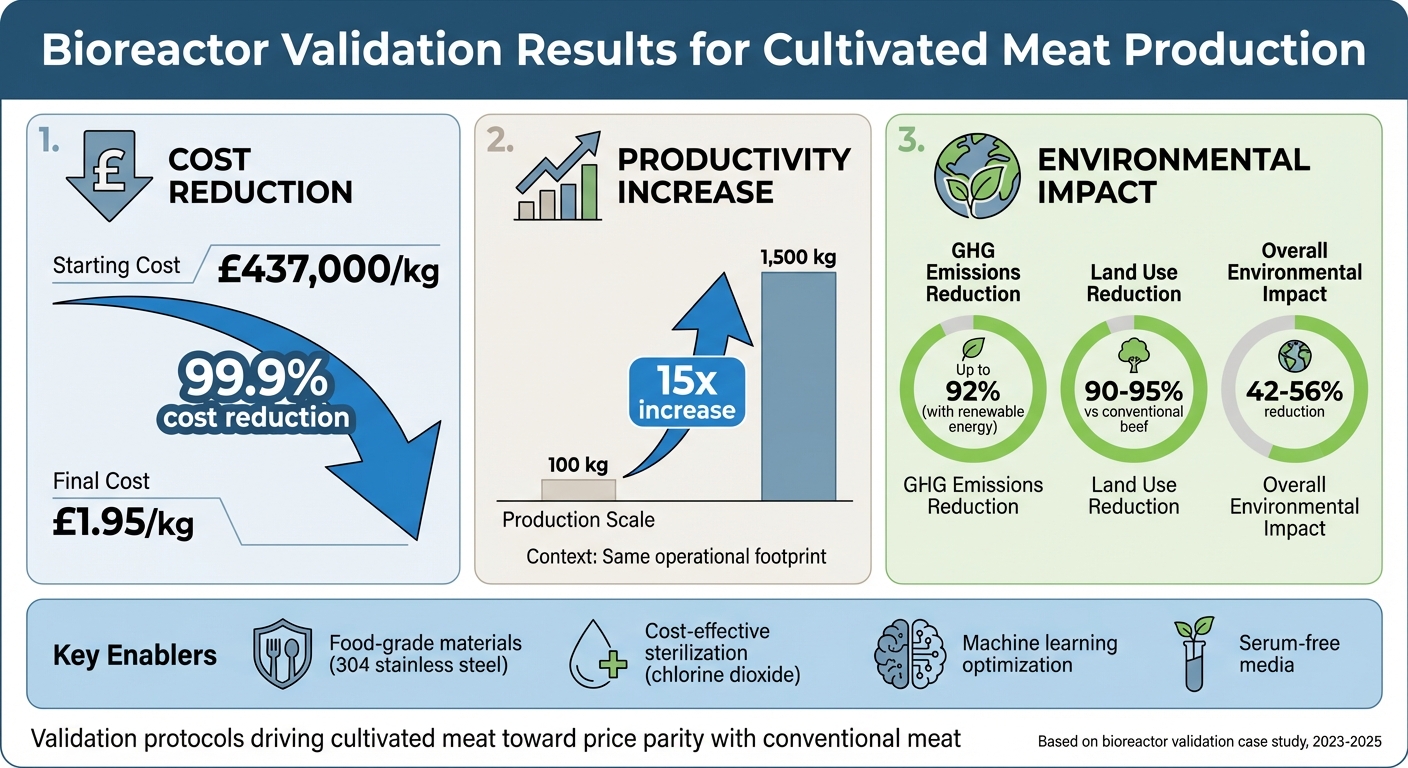
Bioreaktorvalideringens indvirkning: Omkostningsreduktion og miljømæssige fordele i produktionen af dyrket kød
Regulatoriske krav til bioreaktorvalidering
Anvendelige regulatoriske standarder
I industrien for dyrket kød er opfyldelse af strenge regulatoriske standarder en kritisk del af bioreaktorvalideringsprocessen. I Storbritannien kategoriserer Food Standards Agency (FSA) og Food Standards Scotland (FSS) dyrket kød under "produkter af animalsk oprindelse" (POAO). Denne klassificering sikrer, at fødevaresikkerheds- og hygiejneregler gælder for alle produktionsstadier, inklusive bioreaktoroperationer.Men ifølge britisk vejledning (december 2025), mens disse produkter falder ind under POAO-kategorien, kvalificerer de sig ikke juridisk som "kød". Denne sondring betyder, at visse konventionelle dyrevelfærds- og mikrobiologiske krav er udelukket, hvilket former de specifikke valideringsprotokoller, der er nødvendige i Storbritannien.
Globalt varierer sikkerhedsvurderinger i varighed. Singapore og USA afslutter typisk anmeldelser inden for 12 måneder, mens EU gennemsnitligt tager omkring 18 måneder. Storbritannien har kortlagt sin egen vej med CCP Sandbox-programmet, finansieret indtil februar 2027. Dette initiativ gør det muligt for regulatorer at samarbejde direkte med virksomheder som Gourmey, Hoxton Farms, og Mosa Meat, for at strømline data krav og fremskynde sikkerhedsvurderinger.
"Sandbox-programmet giver os mulighed for at fremskynde regulatorisk viden for at reducere barrierer for nye fødevareteknologier uden at gå på kompromis med sikkerhedsstandarder."
– Dr. Thomas Vincent, Vicedirektør for Innovation, FSA [3]
Uanset jurisdiktion skal virksomheder indsende detaljerede sikkerhedsdossierer, før de går ind på markedet. Disse dossierer beskriver produktionsprocesser, produktets sammensætning og sikkerhedsdata. De skal også bekræfte, at dyrket kød er ernæringsmæssigt sammenligneligt med konventionelt kød, herunder analyser af makro- og mikronæringsstoffer samt aminosyre- og fedtsyreprofiler.
Valideringsprotokolkrav
Regulatoriske standarder kræver strenge valideringsprotokoller for bioreaktorer for at sikre sikre og kontrollerede operationer. En vigtig komponent er implementeringen af en Hazard Analysis and Critical Control Point (HACCP) plan. Dette framework identificerer og afbøder risici på hvert trin af produktionen, fra den indledende cellebiopsi til den endelige høst af cellemassen. I betragtning af nyheden ved dyrket kødproduktion skal sikkerhedsvurderinger adressere potentielle farer gennem hele processen.
Valideringsprotokoller skal bevise, at bioreaktorsystemer opretholder sterile forhold under produktionscyklusser, hvilket effektivt forhindrer mikrobiel forurening. Derudover skal disse protokoller vurdere, om proteiner i dyrket kød kan udløse allergiske reaktioner hos forbrugerne.
"Vores nye vejledning giver klarhed for virksomheder, hvilket hjælper dem med at forstå og korrekt demonstrere over for britiske fødevaremyndigheder, hvordan deres produkter er sikre. Specifikt sikrer denne vejledning, at virksomheder har vurderet potentielle allergirisici, og at de er ernæringsmæssigt passende, før de kan godkendes til salg."
– Dr. Thomas Vincent, vicedirektør for innovation, FSA [2]
I Storbritannien fokuserer validering på at give tilstrækkelige data til en videnskabelig risikovurdering snarere end at give markedsautorisation. Nicolas Morin-Forest, medstifter & CEO for GOURMEY, fremhævede denne forskel:
"Storbritanniens validering markerer et kritisk skridt i vores reguleringsrejse for nye fødevarer og bekræfter, at vi nu skrider frem til en fuld risikovurdering, hvilket bringer os et skridt tættere på at gøre vores produkter tilgængelige for forbrugerne." [4]
Bioreaktorvalg og systemspecifikationer
Valgt bioreaktorteknologi
Anlægget valgte en omrørt-tank bioreaktor, et valg drevet af dens pålidelige ydeevne med bovint muskelprogenitorceller. Nøglefaktorer, der påvirkede denne beslutning, omfattede cellernes specifikke behov, den ønskede produktionsskala og overordnede omkostningsovervejelser.
Bovin muskelceller, der er afhængige af forankring, kræver lave skærekræfter - under 0,1 N/m² - for at undgå skader under dyrkning. Det omrørte tankdesign opfyldte dette krav, mens det viste sig at være tilpasningsdygtigt til både pilot-skala eksperimenter og kommerciel produktion. Omkostninger var en anden vigtig faktor, med pilot-skala enheder prissat mellem £50,000 og £100,000, hvilket gør dem tilgængelige for budgetter typiske i den dyrkede kødsektor snarere end i den farmaceutiske industri[5][7].
Produktionsskalaen målrettede volumener mellem 100 og 1.000 liter for at sikre kommerciel gennemførlighed. Modulære omrørte tank-systemer blev valgt frem for pakkebed-alternativer på grund af deres evne til at skalere op med en faktor 10 uden at overskride masseoverførselsgrænserne, idet de opretholder kLa-værdier over 50 h⁻¹. Disse systemer sigter mod at producere 1–10 kg dyrket kød pr. batch, hvilket balancerer kapitalinvesteringen til cirka £200 pr. liter kapacitet [7][8].
Systemdesignfunktioner
Da den omrørte tank-bioreaktor blev valgt, blev dens design inkorporeret med avancerede funktioner for at fremme optimal cellevækst. Gasutvekslingssystemet anvender mikro-sparger teknologi, der leverer bobler mellem 20–100 µm. Denne opsætning opnår kLa-værdier på 100–200 h⁻¹ ved 37°C, idet opløst iltniveauer opretholdes ved 30–50% mætning. For at håndtere CO₂-stripping kombineres hovedrumsbeluftning med membrankontaktorer og antiskumsensorer[5][6].
For effektiv blanding bruger bioreaktoren dobbelte Rushton-impellere, der opererer ved hastigheder på 50–150 rpm. Dette sikrer ensartet blanding med skærehastigheder under 5.000 s⁻¹, der beskytter cellerne mod skader, mens næringsstofgradienter holdes under 10%. Omrøring er PID-kontrolleret med realtidsfeedback på pH og opløst iltniveauer, hvilket understøtter perfusionshastigheder på 1–5 beholdervolumener per dag[5][7].
Skalerbarhed var et centralt fokus i designet. Bioreaktoren opretholder geometrisk lighed på tværs af forskellige skalaer, i overensstemmelse med et højde-til-diameter-forhold på 2:1. CFD-optimerede impellere sikrer lineær opskalering, og pilotforsøg viste en 95% fastholdelse i cellelevedygtighed ved opskalering fra 10 liter til 200 liter.Den modulære design muliggør integration i større produktionssystemer, samtidig med at GxP-overensstemmelsesstandarder overholdes[7] [8].
Procesanalytisk teknologi er også integreret, med Raman-spektroskopi til realtidsmonitorering af kritiske parametre som pH (6,8–7,2) og laktat (holdes under 2 g/L). Prædiktive modeller, tilpasset fra monoklonal antistofproduktion, sporer glukoseniveauer med R²-værdier over 0,95, hvilket sikrer præcis proceskontrol[5] [6][7].
Disse funktioner forbedrer ikke kun cellekultivering, men opfylder også de strenge valideringsstandarder, der kræves af britiske tilsynsmyndigheder.
Valideringsprotokol Udførelse
Kernevalideringsprocedurer
For at sikre operationel integritet blev en grundig valideringsprotokol udført, der inkorporerede avancerede designfunktioner. Realtidsovervågning spillede en nøglerolle, med procesanalytisk teknologi (PAT) sensorer, der kontinuerligt sporede kritiske parametre som opløst ilt, pH og CO₂-niveauer under hver dyrkningskørsel[6] . Processen begyndte med celler sået ved en tæthed på 1×10⁵ celler/mL, dyrket i en uge i et medium indeholdende 3 g/L glukose. Raman-spektroskopi blev anvendt til at overvåge laktat- og glukoseniveauer gennem hele processen[5].
Skærestressanalyse bekræftede, at omrøringskræfterne forblev under 0,1 Pa, hvilket er den kritiske grænse for bovine muskelceller. Efter stress-testning viste cellelevedygtigheden sig at forblive over 90%[6].
Sterilitetstestning udvidet til alle råmaterialer, med særlig opmærksomhed på vækstmedier. Leverandører blev pålagt at levere analysecertifikater, verificeret gennem tredjepartstestning, i overensstemmelse med britiske anlægsstandarder. Protokollen omfattede ELISA immunoassays til at detektere endotoksiner fra gramnegative bakterier, sammen med flowcytometri til at identificere forurenende stoffer baseret på cellestørrelse, form og fluorescensegenskaber[9] .
Procesoptimeringsmetoder
Når systemstabilitet var bekræftet, skiftede indsatsen til at forfine processen ved hjælp af avanceret analyse. Maskinlæringsalgoritmer justerede dynamisk mediestrømningshastigheder og omrøringshastigheder baseret på kontinuerlige PAT-data.Disse modeller, trænet på design af eksperimenter (DoE) datasæt, identificerede omkostningseffektive fodringsstrategier ved at korrelere permittivitetsmålinger med biomassekvalitet[6] . Denne tilgang var særligt effektiv under proliferationsfasen, hvor konsistente vækstrater er afgørende for kommerciel produktion.
Raman-spektroskopi, oprindeligt udviklet til produktion af monoklonale antistoffer, blev med succes tilpasset til anvendelser inden for dyrket kød. Dens analytspecificitet gjorde det muligt for anlægget at anvende etablerede valideringsprotokoller, mens den nødvendige præcision for realtidsmonitorering gennem hele dyrkningscyklussen blev opretholdt[5].
Tekniske udfordringer og løsninger
Opskalering og produktivitetsproblemer
Opskalering af bioreaktorer fra laboratorieindstillinger til kommerciel produktion var ingen lille bedrift.Faciliteten havde til formål at producere 10–100 kg dyrket kød, hvilket krævede enorme 10¹²–10¹³ celler for at nå dette mål [11]. Men at nå høje celletætheder viste sig at være en betydelig udfordring. Mens hul-fiber bioreaktorer teoretisk kan opnå tætheder på 10⁸ til 10⁹ celler/mL [13], faldt konventionelle bioreaktordesigns kort for produktion af dyrket kød.
Matt McNulty, en GFI Research Fellow, forklarede roden til problemet: "Bioreaktorerne, der bruges i dyrket kød, er stadig i høj grad tilpasset fra konventionelle fødevare- og farmaceutiske designs. Disse designs er ikke specifikt skræddersyet til behovene for produktion af dyrket kød og driver derfor højere omkostninger gennem ineffektivitet i denne manglende tilpasning" [12]. Denne uoverensstemmelse mellem design og formål nødvendiggjorde en fuldstændig nytænkning af udstyr og processer.
Implementerede løsninger og præstationsdata
For at tackle disse udfordringer omarbejdede faciliteten sit udstyr og sine protokoller for at tilpasse sig mere præcist til de specifikke krav til produktion af dyrket kød. En af de vigtigste ændringer involverede overgangen fra farmaceutiske standarder til fødevarestandarder. For eksempel erstattede teamet 316 rustfri stålfartøjer med 304 rustfri stålalternativer, som opfyldte fødevaresikkerhedskravene, samtidig med at kapitalomkostningerne blev reduceret betydeligt [12]. Derudover blev den traditionelle damp-på-stedet steriliseringsproces udskiftet med klordioxidgasbehandling. Denne justering tillod brugen af tyndere væggede beholdere lavet af alternative materialer, hvilket yderligere reducerede omkostningerne [12].
En anden omkostningsbesparende foranstaltning involverede skift fra farmaceutisk vand til fødevaregodkendt vand klassificeret som "Generelt Anset som Sikkert" (GRAS) til medieforberedelse [12]. Teamet introducerede også spiselige mikrobærere og stilladser, som ikke kun løste problemer med cellefrigørelse, men også overholdt fødevaresikkerhedsregler [11].
For yderligere at optimere driften implementerede anlægget multiplexede sensorsystemer. Disse sensorer leverede realtidsdata om ydeevne, som kunne anvendes i maskinlæringsapplikationer til at finjustere processer [12]. Samlet set havde disse ændringer en dramatisk indvirkning på produktionsomkostningerne, idet de reducerede dem fra £437,000/kg til kun £1.95/kg [10]. Denne bemærkelsesværdige omkostningsreduktion fremhæver, hvordan tilpasning af produktionsprotokoller til reguleringsstandarder kan opnå kommerciel skalerbarhed uden at gå på kompromis med sikkerhed eller kvalitet.
sbb-itb-ffee270
Valideringsresultater og Industriens Indvirkning
Målte Ydelsesresultater
Gennem grundige tests demonstrerede systemet et imponerende spring i produktivitet. Ved brug af boblefri kontinuerlig bioreaktorteknologi steg cellevækstproduktiviteten 15 gange, og øgede produktionen fra 100 kg til 1.500 kg - alt inden for samme operationelle ramme[16]. Under differentieringsfasen førte justeringer til optimering af cellebiomasse til en 128% stigning, hvilket markant reducerede den samlede miljøpåvirkning med 42–56%. Overgangen fra C2C12 til CHO-cellemetabolisme spillede også en stor rolle i at reducere miljøpåvirkningerne, og opnåede reduktioner på op til 67% når drevet af vedvarende energikilder[14]. Endnu mere bemærkelsesværdigt reducerede brugen af vedvarende energi drivhusgasemissionerne med op til 92% og reducerede arealanvendelsen med 90–95% sammenlignet med traditionelle oksekødsproduktionsmetoder[15] [16]. Disse resultater baner vejen for bredere adoption i hele industrien.
Bidrag til Industriens Praksis
Valideringsresultaterne har omdefineret standarder for bioreaktordesign og regulatorisk overholdelse i produktionen af dyrket kød. Ved at vise, at fødevarekvalitetsstandarder effektivt kan erstatte farmaceutiske standarder uden at gå på kompromis med sikkerheden, har processen introduceret en omkostningsbesparende køreplan for industrien.For eksempel, skift fra 316 til 304 rustfrit stål, kombineret med klordioxidsterilisering og brugen af GRAS-klassificeret vand, reducerede kapitalomkostningerne betydeligt, mens overholdelsen blev opretholdt.
Ud over at bevise teknisk gennemførlighed ændrer disse fremskridt branchens benchmarks. Økonomiske modeller antyder, at integreret kontinuerlig behandling kunne levere 55% besparelser på kapital- og driftsomkostninger over et årti[1]. For indkøbsteams giver platforme som
Konklusion
Hovedresultater
Denne analyse fremhæver, hvordan produktion af dyrket kød kan bevæge sig mod kommerciel succes ved at træffe smarte valg af udstyr og forfine driftsprotokoller. Valg af fødevaregodkendte materialer som 304 rustfrit stål i stedet for det dyrere 316 rustfrit stål sikrer sikkerhed og overholdelse, samtidig med at omkostningerne reduceres. Overgangen til serumfrit medie, som bekræftet af Singapore Food Agency's godkendelse af GOOD Meat's formuleringer i begyndelsen af 2023, eliminerer de etiske og økonomiske udfordringer forbundet med dyreafledte input[15].
Opskalering af produktionen med airlift-reaktorer, især ved 260.000 L, har vist potentiale til at reducere omkostningerne til cirka £10,50/kg. Dette er en betydelig forbedring sammenlignet med omkostningen på £24,50/kg forbundet med mindre 42.000 L omrørte tankreaktorer[17]. Men at opnå høje celletætheder - op til 2 × 10⁸ celler/mL - kræver avancerede perfusionssystemer til at håndtere metabolisk affald som ammoniak og laktat. Procesoptimering har vist sig at være afgørende for at imødegå disse udfordringer[11]. For indkøbsteams giver platforme som
Fremtidige Udviklinger
Med omkostningseffektivitet og proceskontrol valideret, skifter fokus nu til mega-skala bioreaktorer, som lover at omdefinere produktionsøkonomien.GOOD Meats meddelelse i maj 2022 om en facilitet med ti 250.000 L bioreaktorer - i stand til at producere 13.700 metriske ton dyrket kylling og oksekød årligt - markerer et betydeligt skridt fra pilotprojekter til industriel skala produktion [11][15]. Dette er i overensstemmelse med den økonomiske benchmark fastsat af Patrick G. Negulescu et al. fra University of California, Davis:
"For at være direkte konkurrencedygtig med oksekød, skal CM-produkter, eller i det mindste produktionsomkostningerne, falde til et niveau under $9/kg kød"[17]
Prognoser indikerer, at dette mål er inden for rækkevidde, især da medieomkostningerne fortsætter med at falde, med mål sat til mindre end £0,20 pr. liter.
Innovationer som spiselige mikrobærere og hybridsystemer, der kombinerer celleudvidelse og differentiering i et enkelt kar, forventes at forenkle valideringsprocesser og reducere risikoen for kontaminering. De protokoller, der er beskrevet i denne case study, tilbyder en replikerbar model for virksomheder, der skalerer deres operationer op, hvilket beviser, at grundig testning kan sameksistere med omkostningsreduktion. Efterhånden som flere faciliteter adopterer disse validerede metoder, nærmer den dyrkede kødindustri sig prisparitet med traditionelt kød. Samtidig leverer sektoren bemærkelsesværdige miljømæssige fordele, herunder op til 92% reduktion i drivhusgasemissioner, når de drives af vedvarende energikilder[15].
Bioreaktorer opsummering: sensorer, modellering, opskalering og alternativ reaktordesign
Ofte stillede spørgsmål
Hvilke beviser forventer regulatorer i et bioreaktor valideringsdossier for dyrket kød?
Reguleringsorganer kræver bioreaktor valideringsdossierer for at bekræfte, at systemer fungerer inden for definerede parametre. Dette indebærer at sikre konsekvent procesydelse og realtidsmonitorering af nøglefaktorer som pH-niveauer, opløst ilt , og temperatur . Derudover spiller sterilitetstest en afgørende rolle i at forhindre kontaminering. Overholdelse af standarder som ISO 14644-1 og EU GMP Annex 1 er obligatorisk for at opretholde mikrobiel kontrol og opretholde sterile fremstillingspraksis.
Hvordan kan en omrørt-tank bioreaktor opskaleres uden at skade bovine muskelceller?
Opskalering af en omrørt-tank bioreaktor til produktion af dyrket kød indebærer håndtering af skærestress , som kan skade bovine muskelceller. For at tackle dette anvendes værktøjer som computational fluid dynamics (CFD) og skaleringsmodeller til at forudsige strømningsmønstre. Disse indsigter vejleder justeringer af impellerdesign og omrøringshastigheder, hvilket hjælper med at reducere celledamage.
Lige så vigtigt er det at sikre en ensartet fordeling af næringsstoffer og ilt. Avancerede overvågningssystemer, kombineret med effektive blandingsteknikker, er nøglen til at skabe konsistente betingelser. Denne tilgang hjælper med at minimere lokaliseret stress og understøtter cellehelbred gennem storskala produktion.
Hvilke ændringer i omkostningsreduktion har den største indvirkning på £/kg?
Adoption af engangsbioreaktorer har en mærkbar effekt på at reducere omkostninger målt i £/kg. Mens disse systemer reducerer de indledende kapitalinvesteringer og arbejdsomkostninger, medfører de højere forbrugsomkostninger. Derudover øger introduktionen af realtidsmonitorering og mediegenbrugsteknologier den operationelle effektivitet. Disse fremskridt strømliner ikke kun processerne, men fører også til langsigtede omkostningsbesparelser.











