Valget mellem bovine og porcine cellelinjer er en kritisk beslutning for produktion af dyrket kød. Hver celletype tilbyder forskellige fordele og udfordringer, der påvirker skalerbarhed, mediekrav og evnen til at skabe strukturerede kødprodukter. Her er en hurtig oversigt:
- Bovine cellelinjer er velegnede til produktion af muskelvæv, især til produkter som bøffer. De udmærker sig i marmorering, men står over for udfordringer med langvarig differentiering og kræver genetiske modifikationer for skalerbarhed.
- Porcine cellelinjer er ideelle til fedtproduktion, med spontan immortalisation og stabil vækst over hundrede fordoblinger. De er omkostningseffektive til storskalaproduktion, men kan kræve præcis timing for co-differentiering med muskelceller.
Hurtig Sammenligning
| Attribute | Bovine Cellelinjer | Porcine Cellelinjer |
|---|---|---|
| Fordoblingstid | ~39 timer (tidlige passager) | 20–24 timer (tidlige passager) |
| Immortalisering | Kræver genetisk modifikation | Spontan |
| Differentiation | Stærk tidligt, falder efter ~25 fordoblinger | Stabil adipogen effektivitet (>200 fordoblinger) |
| Medieomkostninger | Højere på grund af rekombinante vækstfaktorer | Lavere med heme-suppleret medie |
| Struktureret Kød Egnethed | Egnet til marmorering og muskel-fedt adskillelse | Effektiv til fedt-muskel co-differentiering |
Begge cellelinjer har unikke styrker og begrænsninger, hvilket gør valget afhængigt af produktmål og produktionsstrategier.
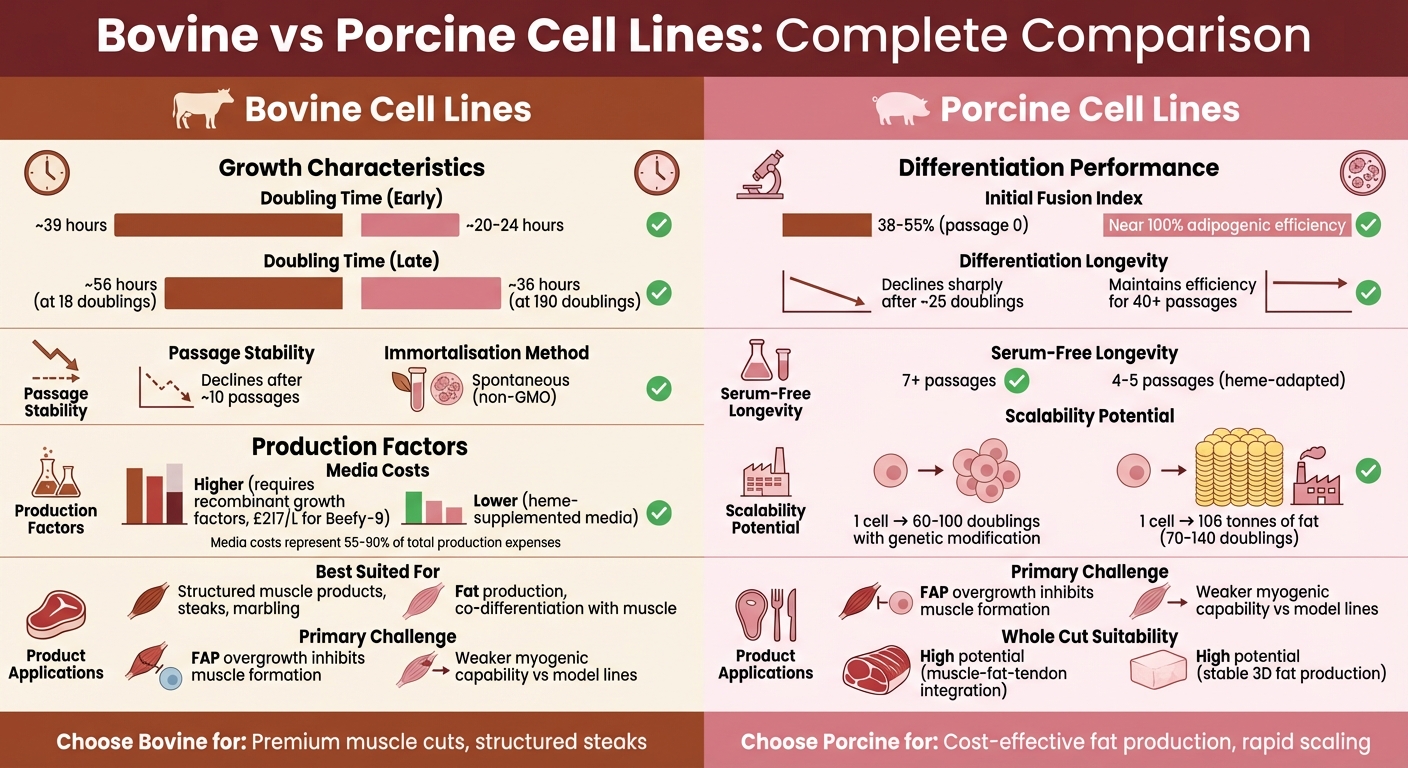
Sammenligning af bovine vs porcine cellelinjer til produktion af dyrket kød
Bovine cellelinjer
Anvendelser i dyrket kød
Bovine cellelinjer er særligt velegnede til at producere strukturerede kødprodukter som bøffer og andre premium udskæringer. En af deres fremtrædende egenskaber er deres evne til at udvikle autentisk marmorering - det intramuskulære fedt, der er ansvarligt for oksekøds karakteristiske smag og tekstur. Denne marmorering opnås gennem rollen af bovine satellitceller (BSCs), som danner muskelkomponenten, og fibro-adipogene progenitorer (FAPs), som genererer fedt med en fedtsyreprofil næsten identisk med naturligt bovint subkutant fedt [2].
At skabe korrekt marmorering kræver omhyggelig koordinering under differentiering.I modsætning til svinesystemer, som samtidig kan differentiere muskel og fedt, håndterer bovine systemer typisk differentieringen af myogene (muskel-dannende) og adipogene (fedt-dannende) celler separat. Disse komponenter kombineres derefter for at opnå præcis kontrol over forholdet mellem fedt og muskel. Mens denne metode tillader større tilpasning, introducerer den også yderligere kompleksitet i produktionsprocessen [2].
Vækstkarakteristika
Selvom bovine celler er effektive til at generere både muskel og fedt, præsenterer deres vækstdynamik udfordringer for storskalaproduktion. Et nøgleproblem opstår med bovine satellitceller, som mister deres evne til at differentiere, når de fortsætter med at proliferere. For eksempel kan primære bovine myoblaster gennemgå mellem 60 og 100 population fordoblinger, mens de opretholder en normal karyotype.Men deres evne til at fusionere til myotuber - et essentielt trin for dannelse af muskelvæv - falder betydeligt efter omkring 25 fordoblinger. Denne begrænsning skaber en flaskehals for opskalering af produktionen, som kræver cirka 2,9×10¹¹ celler per kilogram våd masse [7].
I maj 2023 tacklede forskere ved Tufts University Centre for Cellular Agriculture dette problem ved at udvikle genetisk immortaliserede bovine satellitceller (iBSCs). Ved at introducere bovin Telomerase reverse transkriptase (TERT) og Cyclin-afhængig kinase 4 (CDK4) var disse celler i stand til at overstige 120 fordoblinger, mens de stadig dannede multinukleære myotuber. Andrew J.Stout fra Tufts University understregede vigtigheden af dette gennembrud:
"For at kultiveret kød skal lykkes i stor skala, skal muskelceller fra fødevare-relevante arter udvides in vitro på en hurtig og pålidelig måde for at producere millioner af metriske ton biomasse årligt." [5]
Vækstpræstationen er også stærkt påvirket af faktorer som såningstæthed og medieformulering. For eksempel viste bovine adipose-afledte stamceller (bASCs) optimal vækst ved en såningstæthed på 1.500 celler/cm², og opnåede en 28-dobbelt ekspansion i spinnerflasker ved brug af en 80% medieudvekslingsstrategi [1]. Derudover har kemisk definerede serumfrie medier vist sig at understøtte den eksponentielle vækst af bovine myoblaster med hastigheder, der når 97% af dem, der opnås med traditionelle serumholdige medier [6] . Dette reducerer ikke kun omkostningerne, men stemmer også overens med etiske overvejelser, hvilket gør det til en lovende tilgang til fremtidig produktion.
Disse kvæg-specifikke væksttræk giver et solidt grundlag for at sammenligne dem med svinecellelinjer i forbindelse med produktion af dyrket kød.
sbb-itb-ffee270
Svinecellelinjer
Anvendelser i dyrket kød
Svinecellelinjer er afgørende for at producere modne unilokulære adipocytter, der tæt ligner naturligt svinefedt[9].
Et fremtrædende eksempel er FaTTy cellelinjen, skabt gennem spontan immortalisation. Denne cellelinje viser en imponerende ~100% adipogen effektivitet over 200 fordoblinger, og producerer fedtsyreprofiler, der ligger tæt på dem, der findes i naturligt svinefedt. Dyrkede adipocytter afledt fra denne linje kan opnå lipidvolumener så høje som 96.670 μm³.Som FaTTy Research Team forklarer:
"FaTTy er en unik husdyrcellelinje med en distinkt adipogen fænotype, kendetegnet ved evnen til pålideligt at differentiere med høj effektivitet under forskellige kulturforhold og til at generere modne adipocytter, der viser fedtsyreprofiler sammenlignelige med naturligt fedt." [9]
En anden bemærkelsesværdig cellelinje, PK15H, trives i høje hæmmediekoncentrationer på op til 40 mM. Denne egenskab hjælper med at replikere den rige farve og jernholdige smag, der er typisk for traditionelt svinekød[3]. Desuden kan dyrket svinefedt finjusteres for sundere lipidkompositioner, hvilket opnår monoumættede-til-mættede fedtsyreforhold på 3,2, sammenlignet med det 1,4 forhold, der almindeligvis findes i naturligt væv[9].
Vækstkarakteristika
Porcine cellelinjer er ikke kun dygtige til fedtproduktion, men udmærker sig også i vækst og skalerbarhed. De udviser stabil og hurtig ekspansion, hvilket gør dem særligt velegnede til storskalaproduktion. For eksempel starter FaTTy-linjen med en population fordoblingstid på 20–24 timer, som kun aftager lidt til 22–36 timer mellem den 140. og 190. fordobling. Denne konsistens er en game-changer, da en enkelt FaTTy-celle udvidet fra 70 til 140 population fordoblinger teoretisk kunne producere 106 tons fedt inden for en 11-dages differentieringsperiode[9] .
En stor fordel ved disse cellelinjer er deres spontane immortalisation, hvilket muliggør langsigtet ekspansion uden behov for genetisk modifikation. Denne ikke-GMO-status er en regulatorisk sejr.Fremhævende dette bemærkede University of Ulsan College of Medicine:
"Vores undersøgelse rapporterer en svinecelle, der kan dyrkes i høj-heme medier og kan opretholdes under serumfrie betingelser." [3]
Derudover viser svinemuskelstamceller bemærkelsesværdig skalerbarhed med ekspansionsrater på 10⁶ til 10⁷ gange, i stand til at producere mellem 100 g og 1 kg dyrket kød[10]. Fremskridt inden for cellesorteringsteknikker, ved brug af markører som CD31, CD45, JAM1, ITGA5 og ITGA7, har betydeligt forbedret isoleringen af højrenhedsmuskelstamceller. Disse metoder leverer en 20% stigning i PAX7 positivitet sammenlignet med ældre teknikker[11]. Denne forbedring sikrer, at den myogene potentiale bevares på tværs af flere passager, hvilket adresserer det almindelige problem med nedsat differentieringskapacitet under forlænget ekspansion.
Disse vækst- og differentieringsfordele gør svineceller til et fremtrædende valg frem for kvægceller til produktion af dyrket kød.
ICAN Webinar om cellelinjer og kulturmedier til anvendelser inden for dyrket kød
Vækstrater og proliferation sammenlignet
Lad os dykke ned i, hvordan svine- og kvægcellelinjer klarer sig, når det kommer til vækst og proliferation. svinecellelinjer, som den spontant immortaliserede FaTTy-linje, er bemærkelsesværdigt hurtigere. Deres initiale population fordoblingstid er kun 20–24 timer [9]. I modsætning hertil tager kvægsatellitceller, selv når de dyrkes i optimeret serumfrit medie som Beefy-9, omkring 39 timer per fordobling [12].
Forskellene bliver endnu tydeligere over flere passager.Primære bovine satellitceller har tendens til at miste både deres proliferation og differentieringsevner efter omkring 10 passager [2]. På den anden side har FaTTy svinelinjen opretholdt næsten 100% adipogen effektivitet gennem mere end 200 populationfordoblinger. Selv i senere stadier øges deres fordoblingstid kun beskedent til 22–36 timer [9]. En undersøgelse fra maj 2022 fra Tufts University fremhævede, at bovine celler i Beefy-9 opnåede 18,2 populationfordoblinger over syv passager (28 dage) samtidig med at bevare over 96% Pax7⁺ stamcelleegenskaber [12]. I mellemtiden bekræftede en rapport fra januar 2025 fra University of Edinburgh, at FaTTy-linjen oversteg 200 fordoblinger uden at miste sit differentieringspotentiale [9].
Der er også en markant kontrast i, hvordan disse celler opnår immortalisation.Bovintceller har typisk brug for genetisk manipulation - almindeligvis gennem TERT og CDK4 overekspression - for at opretholde langvarig ekspansion ud over 120 fordoblinger [5]. Sammenlignet hermed opnår svineceller som FaTTy-linjen spontan immortalisation uden genetisk modifikation. Dette giver en klar regulatorisk fordel, især på markeder, der er forsigtige med GMO'er [9].
Sammenligningstabel
| Funktion | Bovine Satellitceller | Porcine MSCs (FaTTy Line) |
|---|---|---|
| Gennemsnitlig fordoblingstid | ~39 timer (optimeret serumfri) [12] | 20–24 timer (tidlige passager) [9] |
| Sen-passage fordoblingstid | ~56 timer (ved 18 fordoblinger) [12] | ~36 timer (ved 190 fordoblinger) [9] |
| Passagestabilitet | Aftager efter ~10 passager [2] | Stabil for >200 fordoblinger [9] |
| Immortalisationsmetode | Engineered (TERT/CDK4) [2] | Spontan [9] |
| Stamcelleegenskaber/Differentiering | >96% Pax7⁺ (op til passage 6) [12] | Næsten 100% adipogen effektivitet [9] |
Det er værd at bemærke, at in vivo satellitceller fordobles på cirka 17 timer, hvilket fremhæver vanskeligheden ved at matche naturlige vækstrater in vitro [12].
Mediekrav og differentieringseffektivitet
Medieafhængighed sammenlignet
Medieomkostninger kan dominere produktionen af dyrket kød, ofte udgør de 55% til 90% af udgifterne, og i nogle systemer overstiger de endda 99% [3][12].
For bovine celler er et almindeligt krav 20% føtalt bovint serum, hvilket kan være en betydelig medieudgift [12]. Et serumfrit alternativ, Beefy-9, bruger et B8 basismedium kombineret med rekombinant humant albumin. Omkostningerne varierer afhængigt af kilde og ordremængde, så det er bedst at tjekke leverandøren eller produktsiden for aktuelle prisoplysninger [12]. Dog kan høje albuminniveauer i serumfrit medium hæmme celleadhæsion, så rekombinant albumin tilsættes typisk 24 timer efter passering [12].
Porcine cellelinjer tager en anden tilgang til serumfri tilpasning. PK15-celler bruger for eksempel bakterielle hæm-ekstrakter fra Corynebacterium [3]. Hæm reducerer ikke kun serumafhængighed, men forbedrer også smag og farve. Når det er sagt, kan koncentrationer over 10 mM blive toksiske, selvom porcine celler kan tolerere op til 40 mM på grund af opregulering af afgiftningsgener [3] . På trods af denne tolerance forbliver porcine celler dyrket i hæm-suppleret medium generelt kun levedygtige i 4-5 passager, mens bovine celler dyrket i Beefy-9 kan opretholde vækst i syv eller flere passager [3][12].
Begge celletyper er stærkt afhængige af fibroblast vækstfaktor-2 (FGF-2).Bovintceller kan for eksempel opretholde kortvarig vækst, selv når FGF-2-niveauerne reduceres fra 40 ng/mL til 5 ng/mL [12]. Derudover hjælper brugen af lav-glukose medier (1 g/L) med at bevare stamcellemarkører i bovintceller [13].
Disse specifikke mediekrav er kritiske, når produktionen skal skaleres, og de påvirker direkte differentieringseffektiviteten.
Differentiation Efficiency
Mens medieomkostninger er en væsentlig faktor, spiller differentieringseffektiviteten også en stor rolle i at bestemme skalerbarheden af dyrket kød.
Bovintceller står over for udfordringer med differentieringseffektivitet, når de udvides. For eksempel opnår bovine myoblaster fra Belgisk Blå kvæg oprindeligt en fusionsindeks på omkring 55% ved 14 population fordoblinger, men dette falder kraftigt til mindre end 10% ved 25 fordoblinger [7]. På samme måde starter føtalt-afledte bovine celler med højere fusionsindekser (omkring 54,6%) sammenlignet med voksen-afledte celler (ca. 38,0%), men begge oplever et fald i differentieringskapacitet på omkring 6,81% pr. passage [7].
Porcine celler, derimod, viser mere stabil ydeevne. Den immortaliserede ISP-4 porcine preadipocytstamme bevarer høj adipogen differentieringseffektivitet i over 40 passager, og opnår en 100-dobling i lipidakkumulering under en 8-dages differentieringsprotokol [8]. Dette gør porcine celler særligt attraktive til fedtproduktion, mens bovine celler er bedre egnet til muskel-differentiering i de tidlige passager, men har svært ved langvarig vedligeholdelse.
| Funktion | Bovine Satellitceller | Porcine Cellelinjer |
|---|---|---|
| Initial Fusion Index | 38–55% (passage 0) [7] | Ikke specificeret for muskel |
| Differentiation Longevity | Faldt kraftigt efter ~25 fordoblinger [7] | Opretholder effektivitet i over 40 passager (ISP-4 adipogen) [8] |
| Serumfri Langlevetid | Opretholder vækst i 7+ passager [12] | Levedygtig i 4–5 passager (heme-tilpasset) [3] |
| Vigtige Tilskud | Rekombinant albumin, FGF-2 [12] | Heme-ekstrakt, insulin, dexamethason [3][8] |
| Lipidproduktion | Minimal (muskel fokus) | 100-dobbelt stigning (ISP-4) [8] |
Egnethed til strukturerede kødprodukter
Valget af cellelinjer spiller en afgørende rolle i at forme ikke kun vækst- og mediebetingelserne, men også strukturen af dyrkede kødprodukter.Når man sigter mod at replikere teksturen og udseendet af en bøf eller svinekotelet, er det essentielt at balancere fedt- og muskelceller i de rette proportioner.
Fedt-Muskel Co-Differentiering
Bovine og porcine cellelinjer opfører sig forskelligt, når det kommer til co-differentiering. Bovine cellekulturer står ofte over for udfordringer som FAP (fibro-adipogene progenitor) overvækst, hvilket forstyrrer muskeludviklingen ved at sænke fusionsindekset. Derudover frigiver adipocytter i disse kulturer signaler, såsom myostatin og IL-6, der blokerer myogenin-ekspression, hvilket effektivt stopper dannelsen af muskelfibre[16].
For at imødegå dette skabte forskere hos Mosa Meat et optimeret serumfrit vækstmedium (i-SFGM). Dette medium inkluderer triiodothyronin (T3) og øget HGF, mens PDGF-BB udelukkes for at kontrollere FAP overvækst.De bruger også modulære adiposfærer (200–400 µm) til at holde fedt- og muskelceller fysisk adskilt under de tidlige vækststadier[4][14].
Porcine cellelinjer viser derimod en mere koordineret tilgang til co-differentiering. ISP-4 præadipocytstammen fungerer for eksempel godt med porcine muskel satellitceller, hvilket producerer marmorering, der ligner konventionelt kød. Denne proces involverer en 48-timers adipogen induktionsfase, efterfulgt af 96 timer i 2% hesteserum for at udløse myogenese. Dette resulterer i modne muskelfibre vævet sammen med adipocytter[8]. Dog har porcine muskel satellitceller en tendens til at have svagere myogene kapaciteter sammenlignet med standardmodellinjer som C2C12, hvilket kræver præcis timing for at sikre, at adipocytter ikke dominerer kulturen[8].
Disse forskelle i differentiering fremhæver de unikke udfordringer og muligheder, som hver celletype præsenterer for opskalering af produktion.
Skalerbarhed og Produktionsudfordringer
Opskalering af struktureret dyrket kødproduktion kræver konsekvent celleydelse. Svinecellelinjer har en tendens til at være mere skalerbare. For eksempel opretholder den spontant immortaliserede FaTTy-linje næsten 100% adipogen effektivitet over 200 populationer fordoblinger[9]. Udvidelse af en svinecellelinje fra 70 til 140 fordoblinger kunne teoretisk producere op til 106 tons fedt[9]. Desuden har ISP-4-stammen vist en 40-dobling i celletæthed inden for seks dage, når den dyrkes på mikrobærere i et spinnerkolbesystem[8].
"FaTTy er en unik husdyrcellelinje med en distinkt adipogen fænotype...disse funktioner, sammen med dens ikke-GMO-natur, gør FaTTy til et meget lovende grundlæggende værktøj." – Nature Food, 2025[9]
Bovint cellelinjer står over for flere forhindringer. FAP-forurening reducerer deres evne til effektivt at differentiere til muskelvæv[4]. Derudover gør de høje omkostninger ved vækstfaktorer som FGF-2 og TGF-β - som ofte udgør over 90% af medieudgifterne - skalering af bovine cellelinjer dyrere[17]. Disse celler kræver også specialiserede belægninger, såsom Laminin-521, for at fremme satellitcelleadhæsion og minimere FAP-interferens[4].
Produktion af et ton dyrket kød involverer omkring 10¹³ celler, og strukturerede produkter som hele udskæringer kræver avancerede produktionssystemer, såsom perfusion eller packed-bed reaktorer, for at understøtte de 3D stilladser og biomaterialer, der er nødvendige for deres udvikling[15].
Sammenligningstabel
| Attribute | Bovine Cell Lines | Porcine Cell Lines |
|---|---|---|
| Primær skalerbarhedsudfordring | FAP-overvækst i muskelkulturer[4] | Tilpasning til suspension/serumfri kultur[9] |
| Differentiationsstabilitet | Aftager efter ~10 passager[2] | Stammer som FaTTy stabile i >200 fordoblinger[9] |
| Co-Differentiering | Adipocytter hæmmer myogenese[16] | Succesfulde marmorering-prototyper opnået[2][8] |
| Strukturel Styrke | Høj; i stand til at integrere muskel-fedt-sene[14] | Moderat; fokus på justeret fiber vækst[14] |
| Hel Skæring Egnethed | Højt potentiale, begrænset af FAP interferens[4] | Højt potentiale på grund af stabil 3D fedtproduktion[9] |
| Tekstur Udfordring | Reduceret sammenhængskraft efter tilberedning[14] | Tendens til at være blødere end kommercielt svinekød[14] |
Konklusion
At beslutte mellem bovine og porcine cellelinjer indebærer at balancere deres forskellige fordele og udfordringer i produktionen af dyrket kød.Bovinesatellitceller er en direkte vej til at skabe skeletmuskelvæv og drager fordel af eksisterende serumfrie medieformuleringer som Beefy-9 [2]. På den anden side er svinecellelinjer allerede blevet brugt til at udvikle dyrkede svineprototyper og viser potentiale i at co-differentiere med satellitceller for at skabe marmorerede kødstrukturer [2].
Skalerbarhed forbliver en stor udfordring. Medieomkostninger og bioreaktorskalerbarhed udgør 55%–90% af de samlede produktionsudgifter, og tilgængeligheden af optimerede cellelinjer er stadig begrænset, hvilket forsinker kommerciel fremgang [3][2].
"De cellelinjer, der anvendes i produktionen af dyrket kød, bestemmer i sidste ende mange af de nedstrøms variabler, der skal overvejes." – GFI [2]
FAQs
Hvilken cellelinje er bedst til hele skåret produkter som bøffer eller koteletter?
Cellelinjer afledt fra muskel-residente progenitorceller, som satellitceller, er ofte ideelle til at producere hele skåret produkter som bøffer eller koteletter. Disse celler har evnen til at udvikle sig til modent muskelvæv, hvilket skaber den strukturerede tekstur og form, der er nødvendig for disse typer produkter.
Hvordan vælger jeg mellem genetisk immortalisation og spontan immortalisation?
Valget af, hvordan man immortaliserer celler til dyrket kødproduktion, afhænger af dine prioriteter, herunder sikkerhed, skalerbarhed og regulatoriske overvejelser.
Genetisk immortalisation involverer introduktion af specifikke gener, såsom telomerase, for at opnå præcis kontrol over cellernes evne til at dele sig uendeligt.Mens denne metode tilbyder forudsigelighed og konsistens, kan den rejse bekymringer om genetisk modifikation og potentielle risici, såsom tumorigenicitet.
På den anden side, spontan immortalisation forekommer naturligt over tid i langtids cellekulturer. Denne tilgang undgår genetisk manipulation, hvilket kunne gøre reguleringsgodkendelse lettere og øge accepten blandt forbrugere, der er skeptiske over for genetisk modifikation.
Begge metoder har deres styrker og udfordringer, og tilbyder forskellige veje mod skalerbar produktion af dyrket kød. Valget afhænger i sidste ende af at balancere kontrol, reguleringsmæssige forhindringer og forbrugertillid.
Hvad er den største omkostningsdriver i medier for bovine vs porcine celler?
Den største udgift ved produktion af medier til bovine og porcine celler kommer ned til omkostningerne og kompleksiteten af dets komponenter.Udvikling og finjustering af medieformuleringer er en stor udfordring, især da medier udgør mindst 50% af de variable driftsomkostninger. Oven i det tilføjer tilpasninger skræddersyet til hver art et ekstra lag af kompleksitet. Disse aspekter spiller en stor rolle i at forme de samlede produktionsomkostninger for dyrket kød.











