Overgangen fra føtalt bovint serum (FBS) til serumfri medier (SFM) er afgørende for at skalere produktionen af dyrket kød. Afhængighed af FBS skaber udfordringer som høje omkostninger, begrænset forsyning og inkonsekvent kvalitet. SFM tilbyder et sikrere, mere kontrolleret alternativ, men det kommer med forhindringer:
- Problemer med celleadhæsion: Myoblaster har svært ved at hæfte uden serum, hvilket ofte kræver dyre belægninger som laminin eller Matrigel. Konditioneret medie eller specifikke tilskud kan forbedre adhæsionen.
- Langsommere vækstrater: Serumfri systemer mangler vigtige næringsstoffer, hvilket fører til reduceret proliferation og ammoniakophobning. Tilføjelse af vækstfaktorer og erstatning af glutamin med alternativer kan hjælpe.
- Inkonsistent mediepræstation: Mange kommercielle SFM'er, optimeret til humane celler, understøtter ikke effektivt væksten af husdyrmyoblaster. Test på tværs af arter og over længere perioder med et medieoptimeringsopdagelsessæt er afgørende.
Løsninger inkluderer skræddersyede formuleringer, delvis mediumudskiftning og co-kultursystemer for at efterligne serum-lignende forhold. Mens SFM kan nærme sig ydeevnen af FBS-systemer, introducerer skalering til 3D-bioreaktorer kompleksiteter som adhæsion og affaldshåndtering. Omhyggelig overvågning af cellekvalitet sikrer succes i storskala produktion.
Overgangen til SFM handler ikke kun om bedre videnskab - det bliver en nødvendighed, da FBS-priserne fortsætter med at stige. Forskere og producenter skal fokusere på at optimere medier og finde pålidelige materialer for at gøre produktionen af dyrket kød levedygtig og omkostningseffektiv.
Plantebaserede stilladser, der inducerer serumfri celleadhæsion til dyrket kød - Indi Geurs - ISCCM9
sbb-itb-ffee270
Almindelige problemer i serumfrit medium til myoblaster
Overgangen fra serum-baserede til serumfri formuleringer kan præsentere flere tekniske udfordringer, der forstyrrer arbejdsgange og øger omkostningerne. Disse problemer viser sig ofte på specifikke måder, startende med celleadhæsion.
Reduceret celleadhæsion og overlevelse
En af de største udfordringer er, at myoblaster ikke hæfter godt i serumfrit medium. Serum giver naturligt en blanding af proteiner, vækstfaktorer og lipider, der hjælper celler med at klæbe til overflader. Uden disse komponenter har myoblaster svært ved at hæfte, hvilket ofte fører til tidlig celledød.
For at løse dette, er mange serumfri systemer afhængige af dyre belægningsmidler som laminin 511 eller Matrigel. Men selv med disse belægninger falder tilhæftningsniveauerne ofte under det, der ses i serum-baserede kulturer. For eksempel fandt en undersøgelse fra 2024, at standard serumfrit medium kun understøttede 2.210 ± 319 celler/cm² på ubelagte skåle. Til sammenligning tredoblede et konditioneret serumfrit medium - suppleret med secernerede faktorer fra andre cellelinjer - næsten dette tal til 5.985 ± 1.558 celler/cm² [2].
Et andet problem er øget følsomhed over for antibiotika. I serumfrie opsætninger kan antibiotika som Penicillin, Streptomycin og Amphotericin B reducere proliferation med op til 62%, sammenlignet med en reduktion på 20–26% i serum-baserede systemer [1]. Uden serums beskyttende elementer er celler mere sårbare over for stress, hvilket yderligere hæmmer deres overlevelse og vækst.
Langsommere cellevækst
Selv hvis celler formår at hæfte sig, halter vækstraterne ofte bagefter.Serum leverer essentielle næringsstoffer som vækstfaktorer, cytokiner, kolesterol og fedtsyrer - mange af disse mangler eller er utilstrækkelige i de fleste kommercielle serumfrie formuleringer. Dette ernæringsmæssige hul resulterer i lavere celleudbytter og længere produktionstider.
En anden komplikation er ammoniakopbygning fra glutaminmetabolisme. Ammoniak hæmmer væksten, og i serumfrie forhold, hvor celler allerede er under metabolisk stress, kan denne toksicitet alvorligt hindre ekspansion. Mange kommercielle medier blev oprindeligt designet til humane celler, så de opfylder muligvis ikke de specifikke ernæringsbehov for bovine eller porcine myoblaster [1][3].
Delvis medieudskiftning, såsom at udskifte 75% af mediet under fodring, kan hjælpe med at bevare nogle endogene vækstfaktorer.Mens dette beskedent forbedrer vækstraterne, lukker det ikke helt hullet mellem serumfrie og serumbaserede systemer [1].
Variabel ydeevne på tværs af kommercielle produkter
Ikke alle kommercielle serumfrie medier yder ens. I en undersøgelse, der sammenlignede syv formuleringer, understøttede kun tre - FBM™, Essential 8™ og TeSR™-E8™ - konsekvent vækst af bovine myoblaster over seks dage. Andre, som StemPro™ og mTeSR1™, understøttede vækst i kun fire dage, før de gik i stå, mens STEMmacs™ slet ikke kunne opretholde proliferation [1].
Problemet ligger i, at de fleste kommercielle medier er optimeret til humane stamceller eller fibroblaster, ikke husdyrmyoblaster. Det, der fungerer godt i biomedicinsk forskning, er ofte utilstrækkeligt til produktion af dyrket kød. Denne inkonsistens fremhæver behovet for formuleringer, der er skræddersyet specifikt til husdyrmyoblaster. Producentdata for humane celler kan ikke pålideligt forudsige, hvor godt et medium vil fungere med bovine eller porcine celler.
For at finde det rigtige serumfrie medium er det afgørende at udføre udvidede tests - ideelt set over seks til ti dage - for at sikre, at det understøtter vedvarende celleudvidelse frem for blot kortsigtet vækst.
Sammenligning af kommercielle serumfrie mediemuligheder
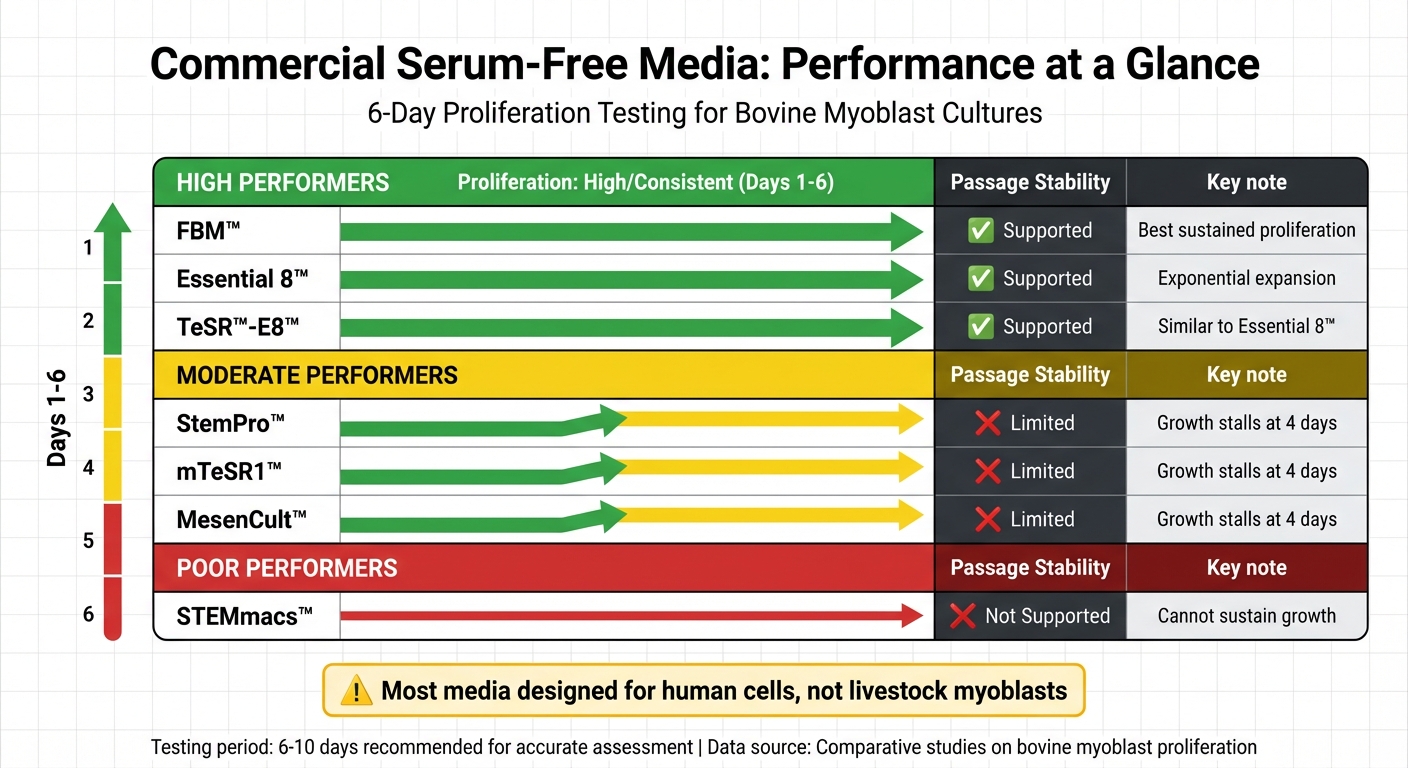
Ydelsessammenligning af kommercielle serumfrie medier til bovine myoblastkulturer
Ydelsesdata for almindelige medier
Når det kommer til serumfrie medier til myoblastkulturer, kan ydeevnen variere meget. Nogle produkter, som FBM™, Essential 8™, og TeSR™-E8™, understøtter konsekvent bovin myoblastproliferation over seks dage. I modsætning hertil har andre, såsom StemPro™, mTeSR1™, og MesenCult™, tendens til at stoppe efter blot fire dage.I mellemtiden STEMmacs™ undlader at opretholde vækst helt [1].
Her er en hurtig sammenligning af præstationsmålinger for disse medier:
| Medium | Proliferation (Dage 1–6) | Passagestabilitet | Vigtige observationer |
|---|---|---|---|
| FBM™ | Høj/Konsistent | Understøttet | Tilbyder det bedste potentiale for vedvarende proliferation [1] |
| Essential 8™ | Høj/Konsistent | Understøttet | Understøtter eksponentiel ekspansion, dog mindre end serum-baseret [1] |
| TeSR™-E8™ | Høj/Konsistent | Understøttet | Ligner Essential 8™ for bovine myoblaster [1] |
| StemPro™ | Moderat | Begrænset | Vækst stopper efter fire dage [1] |
| mTeSR1™ | Moderat | Begrænset | Vækst stopper efter fire dage [1] |
| MesenCult™ | Moderat | Begrænset | Vækst stopper efter fire dage [1] |
| STEMmacs™ | Lav/Ingen | Ikke understøttet | Kan ikke opretholde vækst af bovine myoblaster [1] |
Interessant nok viser de fleste medier - undtagen FBM™ - betydeligt lavere celleantal inden for 24 timer efter såning sammenlignet med serum-baserede kontroller. Dette fremhæver vigtigheden af at evaluere disse metrikker, når man vælger et medium, især i betragtning af regulatoriske tendenser i vækstmedier for fødevaresikkerhed.
Sådan vælger du det rigtige serumfrie medium
Valg af det bedste serumfrie medium handler ikke kun om vækstrater; det kræver en balance af flere faktorer som proliferation, vedhæftning og omkostningseffektivitet. Test af medier over en seks-dages periode er afgørende, da kortere assays kan give misvisende resultater [1].
Artspecifikitet er en anden vigtig overvejelse. Mange serumfrie muligheder er designet med menneskelige celler i tankerne, hvilket betyder, at de måske ikke opfylder de ernæringsmæssige krav fra husdyrmyoblaster som bovine eller porcine celler. De ernæringsmæssige behov for forskellige arter og celletilstande kan variere betydeligt, så testning er essentiel [3] .
Belægningskrav spiller også en stor rolle. Nogle medier kræver dyre belægninger som laminin eller Matrigel for at sikre celleadhæsion. Hvis din proces involverer ubelagte overflader eller fødevaregodkendte materialer, er det værd at teste, om mediet kan understøtte vedhæftning uden disse tilsætningsstoffer. Konditioneret medie eller formuleringer skræddersyet til ubelagte skåle kan være et omkostningseffektivt alternativ [2] .
En anden kritisk faktor er brug af antibiotika. Standard antibiotikacocktails, såsom Penicillin/Streptomycin, kan reducere myoblastproliferation med 20–26% i serumholdige medier og med så meget som 62% i serumfrie systemer. Eliminering af antibiotika kan føre til betydeligt højere celleudbytter [1].
Endelig må du ikke overse håndtering af metabolisk affald. Ammoniakophobning kan være giftig for kulturer, så det er en god idé at supplere medier med ikke-ammoniageniske forbindelser som α-ketoglutarat eller pyruvat. Disse tilsætningsstoffer hjælper med at reducere ammoniakgiftighed og forlænge kulturernes levetid [3].
Metoder til at Forbedre Serumfri Myoblastkulturer
At imødegå udfordringerne ved serumfri myoblastkulturer kræver målrettede strategier. Her er nogle praktiske metoder til at forbedre deres ydeevne.
Tilføjelse af Nøgletilskud
Inkorporering af specifikke tilskud kan markant forbedre myoblastvækst. En blanding af FGF-2 (10 ng/ml), EGF (5 ng/ml), IGF (5 ng/ml), og insulin (10 μg/ml) har vist sig at forbedre celleekspansion i basale medier som FBM [1] . Disse vækstfaktorer arbejder sammen for at fremme celleproliferation, samtidig med at de opretholder den udifferentierede tilstand, der er nødvendig for produktion.
Aminosyrer og vitaminer er også afgørende. Forbindelser som pyridoxamin (Vitamin B6), asparagin, og glutaminsyre spiller en nøglerolle i at fremme celleadhæsion og proliferation, især på ubelagte overflader [2] . Disse kosttilskud hjælper med at erstatte den metaboliske støtte, der typisk leveres af serum, og adresserer adhæsionsrelaterede udfordringer.
"Komponentanalyse og valideringseksperimenter foreslog, at pyridoxamin, asparagin og glutaminsyre bidrog til erhvervelsen af kulturfunktionen af det udviklede medium." - npj Science of Food [2]
Dog er forsigtighed nødvendig med lipidbaserede kosttilskud som LipoGro. Mens de kan stimulere vækst, kan de også inducere adipogen differentiering, hvilket får myoblaster til at udvikle fedtvakuoler og miste deres muskelcelleidentitet [1].
Skræddersyede Medieformuleringer
Tilpasning af medieformuleringer kan optimere serumfrie kulturer ved hjælp af et vækstfaktor-opdagelsessæt. En effektiv tilgang involverer brug af konditioneret medie. Medie konditioneret ved co-kulturering af HepG2 (human hepatom) og NIH/3T3 (mus fibroblast) celler replikerer det metaboliske profil af den føtale lever. Denne metode opnår en celletæthed på 5.985 ± 1.558 celler/cm² på ubelagte skåle, sammenlignelig med de 6.722 ± 1.500 celler/cm² opnået med serumholdige medier [2] . Interaktionen mellem disse celletyper fremmer sekretionen af serumlignende komponenter, der forbedrer væksten.
En anden omkostningseffektiv strategi er delvis medieudskiftning. Ved kun at udskifte 75% af mediet i stedet for en fuld udskiftning bevares endogene vækstfaktorer produceret af cellerne, hvilket forbedrer vækstraterne uden behov for yderligere tilskud [1].
Forebyggelse af tidlig differentiering med inhibitorer
At opretholde en proliferativ tilstand kræver omhyggelig kontrol af differentieringssignaler. For eksempel kan konditioneret medie fra HepG2-celler undertrykke ekspressionen af det myogene differentieringsmarkør Desmin, og holde cellerne udifferentierede og klar til ekspansion [2].
Derudover hjælper sporing af markører som CD29 (integrin beta-1) og Ki67 med at sikre, at formuleringen er effektiv til at opretholde celleproliferation, hvilket reducerer risikoen for for tidlig differentiering.Disse markører giver en pålidelig måde at overvåge og justere kulturforholdene for optimale resultater.
Skalering af serumfri myoblastkulturer til produktion
Overgang til 3D-kultursystemer
Overgangen fra serumfri myoblastkulturer fra flade 2D-skåle til 3D-bioreaktorsystemer kommer med sine egne udfordringer, især når det kommer til celleadhæsion. At belægge bioreaktorkomponenter med dyre midler som laminin er ikke praktisk til storskalaproduktion. Dog har brugen af konditioneret medie fra HepG2 og NIH/3T3 co-kulturer eller berigelse af basalmedie med forbindelser som pyridoxamin, asparagin og glutaminsyre vist sig effektivt. Disse metoder tillader myoblaster at binde sig til ubelagte 3D-stilladser og mikrocarriers, at tackle adhæsionsproblemerne uden at ty til dyre belægninger [2].
En anden kritisk faktor i skalering er håndtering af metabolisk affald.Tætte bioreaktorkulturer kan opleve en opbygning af giftig ammoniak, hvilket kan undgås ved at erstatte glutamin med ikke-ammoniageniske alternativer såsom α-ketoglutarat, glutamat eller pyruvat [3]. Disse justeringer er essentielle, når man bevæger sig ud over småskala-systemer og kræver omhyggelig kvalitetskontrol og sensormonitorering for at opretholde integriteten af myoblaster under produktionen.
Bekræftelse af Cellekvalitet i Tilpassede Kulturer
Efterhånden som kulturer tilpasses til produktion i større skala, er det afgørende at sikre cellernes kvalitet. Teknikker som transkriptomik, metabolomik og funktionelle assays bruges til at verificere, at cellerne opretholder høje niveauer af CD29 og Ki67, mens de undertrykker Desmin-ekspression. Disse markører indikerer, at cellerne forbliver i en proliferativ, udifferentieret tilstand under skaleringsprocessen [2]. Overvågning af disse indikatorer er særligt vigtigt, når omkostningsbesparende foranstaltninger, såsom skift til fødevaregodkendte komponenter eller brug af delvise medieændringer, indføres. Dette trin sikrer, at overgangen fra forskningskvalitet til produktionskvalitetssystemer ikke kompromitterer cellekvaliteten. Finjustering af disse parametre er et kritisk skridt mod at gøre produktionen af dyrket kød skalerbar og omkostningseffektiv.
Serumfri vs Serum-baseret Kulturpræstation
Når de er optimeret, kan serumfri systemer opnå resultater, der er tæt på traditionelle serum-baserede kulturer. Tabellen nedenfor fremhæver nøglemetrikker fra bovine myoblastkulturer dyrket på ubelagte overflader:
| Metrik | Serumbaseret (20% FBS + 10% HS) | Betinget serumfri |
|---|---|---|
| Celleadhæsion (24t) | ~6.722 celler/cm² | ~5.985 celler/cm² |
| Celleproliferation (72t) | ~10.050 celler/cm² | ~8.998 celler/cm² |
| CD29 Ekspression | Høj | Høj |
| Ki67 Ekspression | Høj | Høj |
| Desmin Ekspression | Undertrykt | Undertrykt |
Data hentet fra npj Science of Food [2]
Mens serum-baserede systemer stadig har en lille fordel i celletæthed, leverer serumfrit medium sammenlignelige resultater i adhæsionsmarkørudtryk og holder celler udifferentierede - nøglefaktorer for produktion.Forskellen mindskes yderligere, når specifikke kosttilskud tilføjes for at optimere formuleringer, hvilket gør serumfrie systemer til en stadig mere praktisk mulighed for storskalaproduktion af dyrket kød.
Konklusion
Overgangen af myoblastkulturer til serumfrit medium kommer med sine udfordringer: tidlige vedhæftningsproblemer, langsommere cellevækst og inkonsekvente resultater fra kommercielle produkter. Dog kan enkle ændringer - som at fjerne antibiotika og vælge delvise medieudskiftninger - markant forbedre proliferationsraterne [1]. Ved omhyggeligt at vælge medier og tilføje specifikke vækstfaktorer kan forskere lukke hullet mellem serumfrie og serumbaserede systemer med hensyn til ydeevne. Disse fremskridt baner vejen for opskalering af produktionen.
Opskalering af serumfrie kulturer introducerer dog nye lag af kompleksitet.Overgang af celler til 3D-bioreaktorsystemer samtidig med at de opretholder deres fænotype kræver streng kvalitetskontrol. Alligevel viser beviser, at veloptimerede serumfrie systemer kan opnå celletætheder, der er sammenlignelige med dem, der dyrkes i serumbaserede medier. Dette gør serumfrie metoder stadig mere praktiske til kommerciel produktion af dyrket kød.
Det økonomiske argument for serumfrie medier er svært at ignorere. Med FBS-priser, der fortsætter med at stige, bliver serumbaserede metoder økonomisk uholdbare [1] . Dette skift handler ikke kun om tekniske forbedringer - det handler om økonomisk overlevelse for den dyrkede kødindustri.
For forskere og produktionsteams, der foretager denne overgang, er det afgørende at skaffe de rigtige materialer. Fra kemisk definerede medier til rekombinante vækstfaktorer, er adgang til pålidelige forsyninger nøglen. Dette er hvor
Ofte stillede spørgsmål
Hvordan kan jeg forbedre myoblast-tilhæftning i serumfrit medium uden laminin eller Matrigel?
For at forbedre myoblast-tilhæftning i serumfrit medium uden at bruge laminin eller Matrigel, overvej at bruge betinget serumfrit medium. Denne tilgang kan fremme adhæsion og proliferation selv på ubelagte skåle. En anden mulighed er at optimere mediet ved at tilføje komponenter som FGF2, fetuin, og BSA. Disse justeringer kan gøre en mærkbar forskel i at forbedre cellehæftning og vækst, hvilket eliminerer behovet for ekstracellulære matrixbelægninger.
Hvad er den hurtigste måde at reducere ammoniakophobning i serumfri myoblastkulturer?
For at reducere ammoniakophobning i serumfri myoblastkulturer, bør du fokusere på at forbedre medieformuleringen. En tilgang er at bruge konditioneret medie, der fremmer både celleadhæsion og proliferation, samtidig med at ammoniakniveauerne holdes lave. Derudover kan forfining af kulturforholdene hjælpe med at minimere ammoniakproduktionen. Dette kan involvere justering af faktorer som pH, temperatur eller næringsstofkoncentrationer for bedre at tilpasse sig cellernes metaboliske behov.
Hvordan validerer jeg, at myoblaster forbliver udifferentierede efter skift til serumfrit medie?
For at sikre, at myoblaster forbliver i deres udifferentierede tilstand, når de dyrkes i serumfrit medie, er det afgørende at spore specifikke markører.Pax7 er en pålidelig indikator for udifferentierede myoblaster, mens fraværet af differentieringsmarkører som myosin heavy chain (MHC) bekræfter, at de ikke er begyndt at differentiere.
Du kan bruge teknikker som:
- Immunocytokemi: Til at visualisere proteinudtryk i celler.
- Flowcytometri: Til at analysere markørudtryk i en stor cellepopulation.
- qPCR: Til at måle mRNA-niveauer af nøglemarkører.
Derudover er det essentielt at observere cellerne under et mikroskop. Myoblaster bør bevare deres karakteristiske udseende og undgå dannelsen af multinukleære myotuber, som er et klart tegn på differentiering. Ved at kombinere disse metoder og overvåge regelmæssigt kan du sikre, at cellerne forbliver udifferentierede.











