Skalering af produktion af dyrket kød kræver præcis kontrol over bioreaktorforhold. Mindre udsving i pH, iltniveauer eller temperatur kan betydeligt påvirke udbyttet, når man går fra laboratorie- til kommerciel skala. Traditionelle manuelle overvågningsmetoder fejler ofte i at opdage disse problemer tidligt, hvilket risikerer kontaminering, ineffektivitet og højere omkostninger.
Denne case study undersøger, hvordan en produktionsfacilitet implementerede real-time overvågningssystemer, opnåede:
- Forbedret effektivitet: Automatiserede sensorer overvågede kontinuerligt kritiske parametre som pH, ilt og celletæthed, hvilket reducerede celleskader og sikrede konsistente udbytter.
- Bedre overholdelse: Automatiseret datalogning skabte GMP-kompatible batchregistre, hvilket forenklede reguleringsinspektioner.
- Lavere omkostninger: Automatisering reducerede arbejdskraftbehov og muliggjorde brugen af mere overkommelige næringsstoffer.
Anlægget integrerede avancerede sensorer, flowkontrollere og mikrofluidiske enheder i bioreaktorer, hvilket sikrede sterilitet og kontinuerlig overvågning. Implementeringen tog 18–24 måneder, med målbare forbedringer i produktionseffektivitet og omkostningsstyring.
Realtidsovervågning er blevet en nøgleløsning til opskalering af dyrket kødproduktion, hvilket tilbyder præcis kontrol, reducerede risici og strømlinet overholdelse.
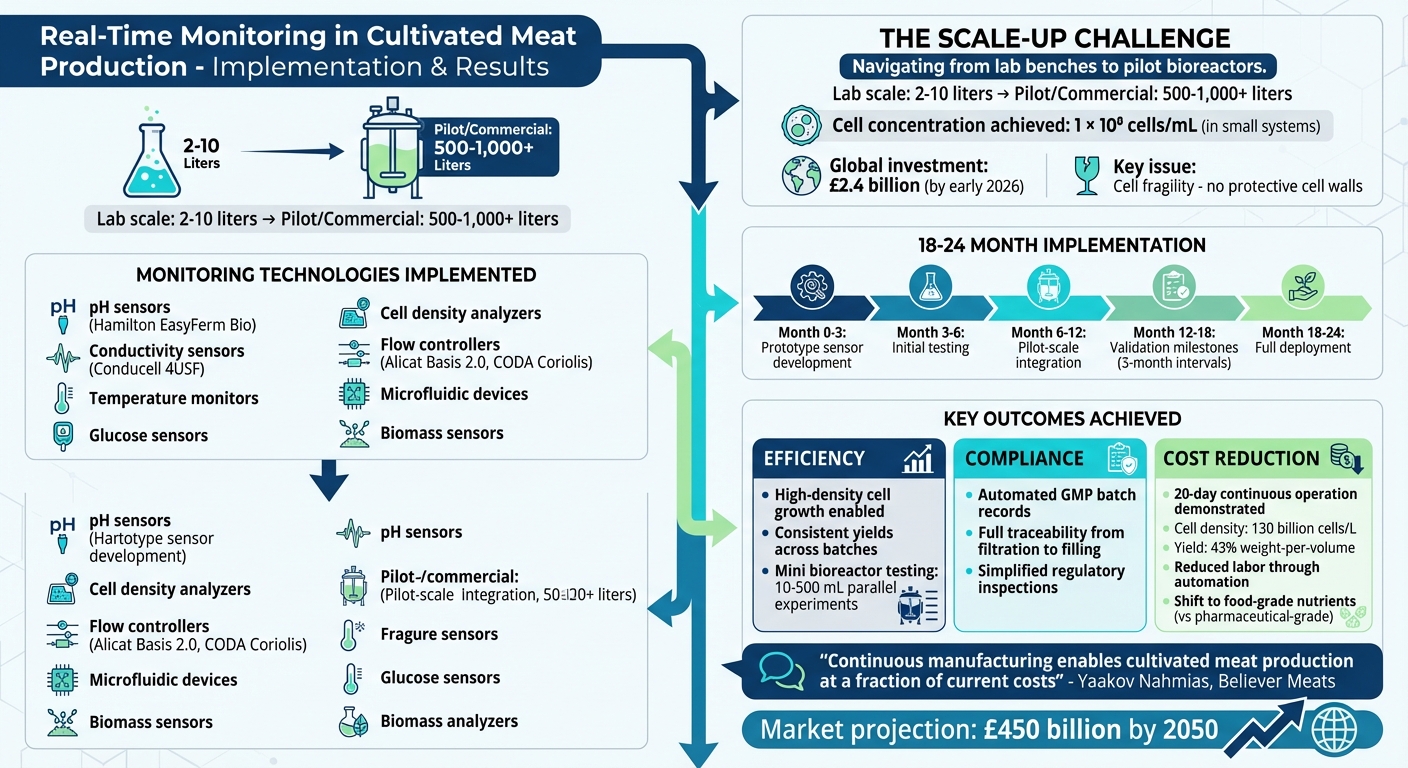
Implementeringstidslinje for realtidsovervågning og nøgleresultater i dyrket kødproduktion
Udfordringen: Begrænset synlighed under opskalering
Fra laboratorie- til pilot- og kommerciel produktion
Opskalering af dyrket kødproduktion fra små 2–10 liters laboratoriebioreaktorer til systemer, der overstiger 1.000 liter, medfører en række udfordringer, som manuel overvågning simpelthen ikke kan håndtere.For eksempel, mens små perfusionsbioreaktorer har opnået høje cellekoncentrationer på over 1 × 10⁸ celler per milliliter, har det været inkonsekvent at replikere disse resultater i større omrørte tanksystemer med simplere medier[7]. Denne casestudie fremhæver en facilitet, der står over for netop dette problem - hvad der fungerede problemfrit i et forskningslaboratorium, faldt fra hinanden, da det blev skaleret til et 500-liters pilotsystem.
Rodårsagen til problemet ligger i celle skrøbelighed. I modsætning til de robuste mikrobielle celler, der anvendes i traditionel fermentering, mangler dyrkede kød celler beskyttende cellevægge, hvilket gør dem meget modtagelige for skader fra væskekræfter i større bioreaktorer[1]. Selv mindre turbulens på disse skalaer kan forårsage betydelig celledestruktion. Traditionelle skaleringsregler, såsom 4× seed train faktoren, viste sig utilstrækkelige givet de stramme økonomiske begrænsninger ved produktion af dyrket kød[7].
Disse udfordringer gjorde det klart, at et mere pålideligt og kontinuerligt overvågningssystem var essentielt.
Problemer med traditionelle overvågningsmetoder
I større skalaer svigtede traditionelle overvågningsmetoder. Manuel prøvetagning, for eksempel, udgjorde en risiko for kontaminering og skabte ineffektivitet. Hver gang en prøve blev taget fra bioreaktoren, blev det aseptiske miljø kompromitteret - et kritisk problem for de storskala operationer, der kræves til kommerciel produktion[7]. At opretholde sterilitet under dataindsamling blev en topprioritet for produktionsteamet.
"Systemet ville kræve aseptisk drift (inklusive viral eksklusion) i meget stor skala ud over den nuværende praksis for at undgå kontaminering og potentielt batchtab."
- ACS Fødevarevidenskab & Teknologi [7]
Manuelle processer øgede også arbejdskraftomkostningerne og gjorde det sværere at opretholde nøjagtige GMP-batchoptegnelser, som er afgørende for overholdelse af lovgivningen. Uden realtidsdata om vigtige parametre som pH, iltniveauer og skærespændingstærskler blev problemer ofte overset, indtil produktionsudbyttet allerede havde lidt.
De økonomiske indsatser var enorme. I begyndelsen af 2026 var der investeret over £2,4 milliarder globalt i dyrket kødteknologi [7], hvilket skabte et enormt pres for at opnå konsekvent, skalerbar produktion. For at bygge bro mellem laboratorie succes og kommerciel levedygtighed havde anlægget brug for en overvågningsløsning, der kunne levere realtidsindsigt uden at gå på kompromis med sterilitet eller effektivitet.
sbb-itb-ffee270
Hvordan realtids overvågningssystemer blev implementeret
Overvågningsteknologier anvendt
Anlægget introducerede sensorer til at overvåge kritiske bioreaktorparametre kontinuerligt, mens sterilitet blev opretholdt. Systemets rygrad omfattede temperaturovervågning, glukosesensorer og celletæthedsanalyseapparater . For pH-niveauer blev
For at styre præcis gas- og væsketilførsel anvendte teamet Alicat Basis 2.0 og CODA Coriolis Mass Flow Controllers, som var essentielle for at opretholde stabile kulturmiljøer. Alicat L-Series Liquid Flow Meters overvågede medie- og næringsstoftilførselsrater.Derudover blev biomassesensorer og lab-on-a-chip mikrofluidiske enheder integreret til realtidsmonitorering. Dette skift fra manuelle kontrol til automatiseret dataindsamling gjorde det muligt for teamet at overvåge alt fra næringsstofniveauer til metabolitophobning på en struktureret og effektiv måde.
Disse avancerede sensorkapaciteter skabte et fundament for en gnidningsfri integration med facilitets bioprocesseringssystemer.
Forbindelse til eksisterende bioprocesseringssystemer
Integrationsindsatsen prioriterede kompatibilitet med facilitets eksisterende bioreaktor- og inkubationsopsætninger. Sensorer blev omhyggeligt placeret i turbulente bioreaktorer for at beskytte de sarte dyrkede kød celler[6]. Overvågningssystemerne var direkte forbundet til automatiserede bioproceskontrolsystemer, for at sikre overholdelsesovervågning og udsende advarsler, når parametre faldt uden for det ønskede område[2][3].
Glukosesensorer gav kontinuerlige opdateringer om næringsstofniveauer og udløste advarsler, når justeringer var nødvendige. Celletæthedsanalyseapparater, der bruger levende cellebilleddannelse, sporede befolkningsvækst, hvilket muliggjorde præcise indgreb under opskaleringsfaser[2][5]. En nedskaleret testtilgang blev brugt til at identificere potentielle udfordringer tidligt, mens dråbebaserede integrationsmetoder minimerede cellestress under sensorinstallation[2][5]. Denne integration forbedrede proceskontrol og sikrede sporbare, reguleringskompatible data.Resultatet var en problemfri dataflow fra bioreaktorsensorer til kontrolsystemer, hvilket eliminerede behovet for hyppig manuel prøvetagning.
Med integrationen fuldført, skiftede fokus til at implementere systemet på en struktureret tidslinje.
Implementeringstidslinje og milepæle
Implementeringsprocessen strakte sig over 18–24 måneder, startende med udvikling og test af prototypesensorer til in-situ målinger. Ved den tredje måned var den indledende prototypefase afsluttet. Integration i pilot-skala bioreaktorer fulgte, med valideringsmilepæle sat med tre måneders intervaller[2].
Tendenser inden for opskalering af dyrket kød og bioprocessering
Resultater: Målte forbedringer i produktionen
Efter implementeringen af systemet oplevede anlægget klare fremskridt inden for effektivitet, sporbarhed og omkostningsstyring.Ved at adressere udfordringerne ved opskalering af dyrket kød, forbedrede det nye overvågningssystem produktionens resultater betydeligt.
Forbedret processeffektivitet og udbytte
Introduktionen af realtidsmonitorering medførte mærkbare gevinster i produktionen ved kontinuerligt at spore essentielle kulturparametre. Dette sikrede, at optimale betingelser blev opretholdt gennem hver batchcyklus. Ved at overvåge tærskelværdier for skærekraft under opskalering beskyttede anlægget de sarte dyrkede kødceller mod skader forårsaget af væskekræfter, hvilket resulterede i mere konsistente celletætheder og bedre udbytter.
Mini-bioreaktorer, der spænder fra 10 til 500 mL, spillede en afgørende rolle under medieoptimerings fasen. Deres evne til at køre parallelle eksperimenter fremskyndede identifikationen af ideelle vækstbetingelser før opskalering. Denne høj-gennemløbsmetode reducerede sandsynligheden for fejl i den kommercielle produktionsfase.
Forbedret Dataadgang og Sporbarhed
Omfattende datalogning skabte robuste GMP-batchjournaler og sikrede overholdelse af lovgivningen. Dette system sporede hvert trin, fra filtrering til aseptisk fyldning, opretholdt konsistens på tværs af batches og muliggjorde hurtig fejlfinding, når der opstod afvigelser. Med industrielle bioreaktorer, der overstiger 1.000 L, blev stærke proceskontroller og let tilgængelige data endnu mere essentielle[7]. Udover overholdelse hjalp disse systemer også med at reducere driftsomkostninger.
Reducerede Arbejds- og Driftsomkostninger
Automatisering spillede en nøglerolle i at reducere behovet for konstant manuel overvågning. AI-drevne perfusionssystemer kontrollerede aktivt pH, iltniveauer og skærestress, hvilket muliggjorde høj tæthed af cellevækst, mens personalet kunne fokusere på mere kritiske opgaver[8]. I august 2024 demonstrerede forskere fra Hebrew University of Jerusalem og Believer Meats effektiviteten af kontinuerlig produktion med tangential flow-filtrering. Deres proces fungerede i 20 dage med daglige høstninger, opnåede en celletæthed på 130 milliarder celler pr. liter og et vægt-til-volumen udbytte på 43% [9] .
"Vores resultater viser, at kontinuerlig produktion muliggør produktion af dyrket kød til en brøkdel af de nuværende omkostninger, uden at ty til genetisk modifikation eller mega-fabrikker." – Yaakov Nahmias, Grundlægger, Believer Meats[9]
Realtidsmonitorering understøttede også overgangen fra farmaceutisk kvalitet til mere overkommelige fødevarekvalitetsnæringsstoffer. Ved at vælge cellelinjer, der kan trives i mere magre vækstmedier, reducerede faciliteterne deres afhængighed af dyre rekombinante proteiner. Denne overgang, kombineret med automatiserede samlebåndsmodeller inspireret af bilindustrien, forenklede driften og reducerede arbejdskraften, der kræves for at overvåge individuelle partier[9][10].
Lærte Lektier og Fremtidige Overvejelser
Løsning af Tekniske og Organisatoriske Problemer
Implementeringen af realtids-overvågningssystemer afslørede nogle uventede forhindringer. Et stort problem var at bestemme den bedste sensorplacering i turbulente bioreaktorer under opskaleringsfasen[6]. Sensore placeret forkert producerede ofte upålidelige data, hvilket fik teams til at skabe standardiserede protokoller for sensorplacering, før de gik videre til fuldskala operationer.
Automatisering af sensorintegration viste sig at være en game-changer, hvilket betydeligt reducerede kontaminationsrisici forbundet med manuel prøvetagning[1] . Som tidligere diskuteret bevarer automatiseret overvågning ikke kun aseptiske forhold, men minimerer også behovet for manuel indgriben. Overgangen til automatiserede dataplatforme krævede dog tæt samarbejde mellem bioprocesingeniører, dataforskere og produktionsledere. Klare protokoller blev essentielle for at reagere på afvigelser i procesparametre[11].
Et andet kritisk skridt var omfattende medarbejdertræning. At sikre, at teammedlemmer forstod datafortolkning og systemkalibrering, var afgørende for en gnidningsfri overgang til kontinuerlig overvågning. Standard operating procedures (SOPs) for sensor maintenance and data validation replaced outdated manual workflows, creating a more integrated system that allowed for quicker and more informed decision-making.
Disse erfaringer fremhæver vigtigheden af at planlægge skalerbare overvågningsarkitekturer til fremtidige operationer.
Skalering af overvågningssystemer på tværs af flere faciliteter
Udvidelse af overvågningssystemer på tværs af flere faciliteter kræver modulære designs, der kan håndtere stigende produktionsvolumener[2]. Faciliteter, der omhyggeligt dokumenterer tidslinjer for sensordeployment, integrationsskridt og fejlfinding, kan opbygge en vidensbase for at forenkle fremtidige installationer.En nedskaleringsmetode - test af overvågningssystemer på mindre bioreaktorer (10 til 500 mL) før fuldskala implementering - har vist sig effektiv til at identificere potentielle tekniske problemer, før de påvirker kommerciel produktion[2].
Konsistens er en anden nøglefaktor. Standardisering af dataformater og sensorspecifikationer på tværs af faciliteter sikrer generering af reproducerbare datasæt. Denne konsistens muliggør også AI-drevne analyser til at identificere præstationstendenser og informere om bedste praksis[5]. Etablering af baseline-metrikker er afgørende for nøjagtigt at måle effektivitetsforbedringer under opskalering.
Hvordan Cellbase Understøtter Adoptering af Overvågningsteknologi
Efterhånden som faciliteter udvider deres overvågningssystemer, bliver det stadig vigtigere at have en pålidelig indkøbspartner.Indkøb af specialiserede sensorer, mikrofluidiske enheder og AI-drevne analyser skræddersyet til produktion af dyrket kød kan være en kompleks opgave.
Derudover spiller teknisk support en afgørende rolle i en vellykket implementering.
Konklusion
Realtids overvågningssystemer spiller en nøglerolle i opskaleringen af dyrket kødproduktion fra laboratorieforsøg til fuldskala kommercielle operationer. Ved kontinuerligt at indsamle data om kritiske kulturparametre, tillader disse systemer præcis kontrol over processer, hvilket sikrer ensartet produktkvalitet og overholdelse af lovgivningsmæssige standarder[1].
Integrationen af automatiseret overvågning tilføjer et ekstra lag af effektivitet ved at reducere behovet for manuelle indgreb. Dette er særligt vigtigt for at spore forskydningsspænding, hvilket hjælper med at beskytte de sarte dyrkede kød celler mod skader forårsaget af væskekræfter[1]. Med dette niveau af synlighed kan produktionsteams hurtigt adressere ineffektivitet og opretholde detaljerede batchoptegnelser, der kræves for GMP-standarder og biosikkerhedsinspektioner[1].
Fra et regulatorisk perspektiv forenkler disse systemer overholdelse ved automatisk at generere omfattende produktionsoptegnelser til rutineinspektioner, hvilket sikrer materialernes sikkerhed og integritet[13]. For kontinuerlige bioprocesseringsoperationer - nogle gange strækkende sig over 60 dage eller mere - er realtidsopsporing af celletæthed, metabolitter og potentielle kontaminanter afgørende for at holde kulturer stabile og produktive[12].
Skalerbarheden af disse overvågningssystemer er måske deres mest værdifulde funktion.Modulære designs, der integrerer problemfrit med standard bioreaktorer og inkubationsudstyr, giver faciliteter mulighed for at udvide overvågningskapaciteter, efterhånden som produktionen vokser, uden behov for større infrastrukturændringer[1] . Med markedet for dyrket kød forventet at nå £450 milliarder i 2050[12], vil efterspørgslen efter skalerbare overvågningsløsninger kun vokse. At imødekomme disse udfordringer direkte med robuste systemer er ikke længere valgfrit - det er essentielt.
For teams, der ønsker at opgradere deres overvågningsinfrastruktur, er sourcing af pålidelige sensorer, flowkontrollere og datalogger værktøjer et kritisk første skridt.
Ofte stillede spørgsmål
Hvilke bioreaktorparametre er vigtigst under opskalering af dyrket kød?
Vigtige faktorer at overvåge i bioreaktorer til opskalering af dyrket kød inkluderer metabolitter som laktat og ammoniak, biomassetæthed, kuldioxid (CO₂) niveauer, glukose, pH-niveauer , og opløst ilt. Disse parametre er essentielle, fordi de har en direkte indvirkning på cellernes sundhed, vækstrater og den overordnede gennemførlighed af opskalering af produktionsprocesser.
Hvordan reducerer realtidsmonitorering risikoen for kontaminering uden manuel prøvetagning?
Realtidsmonitorering hjælper med at holde kontamineringsrisici i skak ved at opdage luftbårne kontaminanter, så snart de opstår. Dette muliggør hurtig handling for at løse problemet og opretholde sterile forhold uden at være afhængig af manuel prøvetagning.Som et resultat fremskynder det ikke kun processen, men reducerer også risikoen for menneskelige fejl.
Hvad er den hurtigste måde at skaffe kompatible sensorer og flowkontrollere til dyrkede kød-bioreaktorer?
Den hurtigste måde at skaffe kompatible sensorer og flowkontrollere til dyrkede kød-bioreaktorer er ved at bruge











