Kryosäilytys on prosessi, jossa elävät solut jäädytetään ja säilytetään erittäin alhaisissa lämpötiloissa niiden elinkelpoisuuden säilyttämiseksi ajan mittaan. Tämä menetelmä on kriittinen viljellyn lihan tuotannossa, varmistaen johdonmukaiset, vakaat solulinjat ja suojaten kontaminaatiolta tai laitteistovioilta aiheutuvilta menetyksiltä. Tärkeät vaiheet sisältävät:
- Valmistelu: Kerää solut niiden kasvuvaiheessa, tarkista elinkelpoisuus (tavoitteena ≥90%), ja valmistele ne jäädytysliuoksessa, joka sisältää kryoprotektantteja kuten DMSO tai glyseroli.
- Jäädytys: Käytä hallittua jäähdytysnopeutta (-1°C - -3°C minuutissa) estääksesi jääkidevaurioita. Säilytä solut nestemäisen typen höyryssä (-135°C - -190°C) pitkäaikaista säilytystä varten.
- Sulatus: Sulata solut nopeasti 37°C vesihauteessa minimoidaksesi kryoprotektantin toksisuuden, ja siirrä ne sitten kasvatusliuokseen toipumista varten.
- Laadunvalvonta: Merkitse injektiopullot tarkasti, seuraa säilytysolosuhteita ja testaa elinkelpoisuus sulatuksen jälkeen onnistuneen säilytyksen varmistamiseksi.
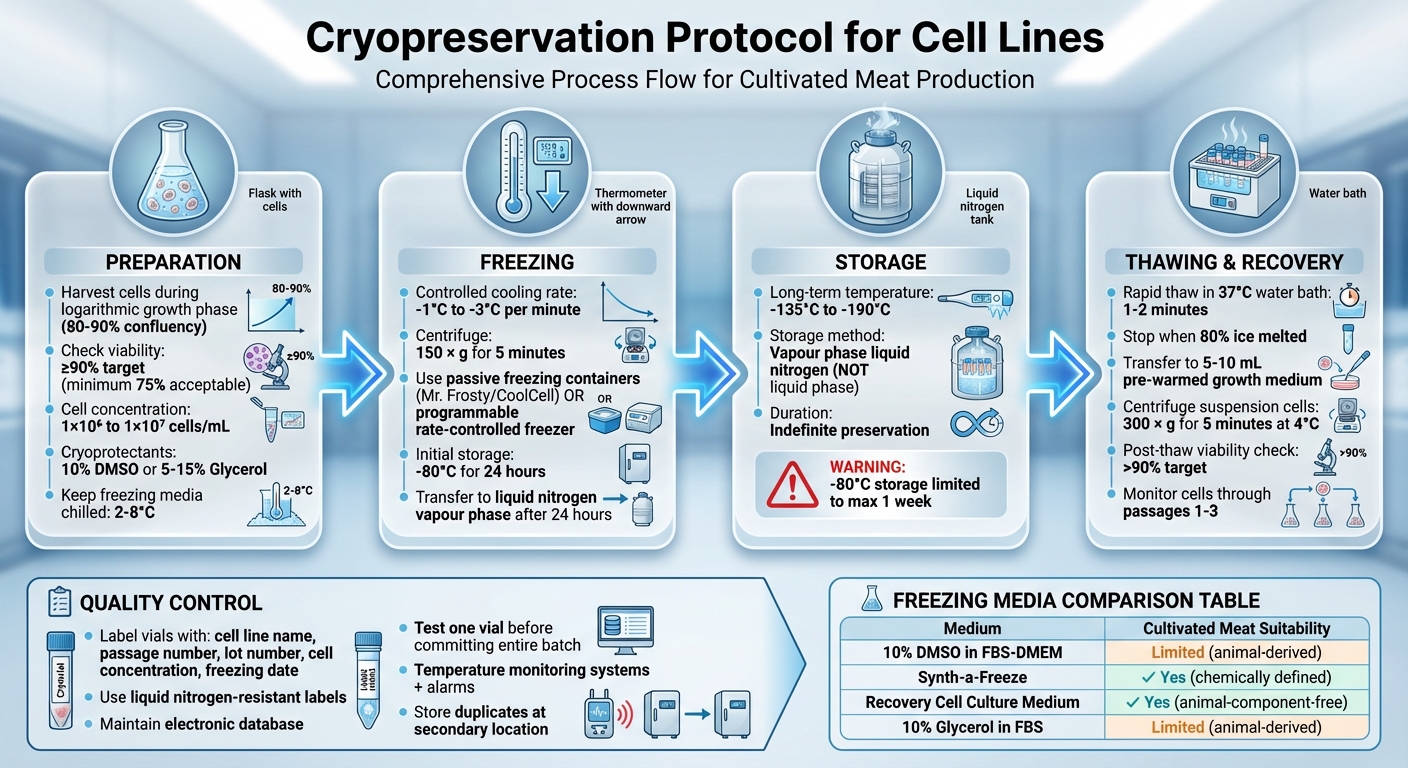
Täydellinen kryosäilytysprotokolla solulinjoille: 4-vaiheinen prosessi valmistelusta säilytykseen
Solujen valmistelu kryosäilytykseen
Solujen keräys ja elinkelpoisuuden tarkistus
Parhaan toipumisen varmistamiseksi sulatuksen jälkeen, kerää solut niiden logaritmisessa (log) kasvuvaiheessa. Adherenttien solulinjojen kohdalla tämä on tyypillisesti, kun ne saavuttavat 80–90% konfluenssin [2][3][6].
Tarkista solujen elinkelpoisuus Trypan Blue -poissulkemismenetelmällä. Sekoita yhtä suuret osat (1:1) 0.4% Trypan Bluea solususpension kanssa ja laske sitten solut hemocytometrillä.Elinkelpoiset solut eivät ota väriainetta ja näyttävät kirkkailta mikroskoopin alla, kun taas elinkelvottomat solut värjäytyvät sinisiksi [4]. Ihannetapauksessa pyri vähintään 90% elinkelpoisuuteen parhaan palautumisprosentin saavuttamiseksi, vaikka jotkut protokollat saattavat hyväksyä vähintään 75% [1][2][3][5].
Ennen sadonkorjuuta käytä mikroskooppia bakteeri- tai sienikontaminaation tarkistamiseen. Terveiden suspensiosolujen tulisi näyttää kirkkailta, pyöreiltä ja valoa taittavilta käänteisessä vaihekontrastimikroskoopissa [2][3].
Kun solut täyttävät vaaditut elinkelpoisuusstandardit, siirry esijäädytysvaiheisiin.
Ennen pakastusta tehtävät valmistelut
Adherenttien solujen osalta käytä hellävaraisia irrotusmenetelmiä, kuten trypsiiniä tai TrypLE Express, ja rajoita inkubointiaikaa solukalvojen vaurioitumisen välttämiseksi [5]. Valmistele solut pitoisuuteen 1 × 10⁶ - 1 × 10⁷ solua/ml solulinjasta riippuen [1][6]. Aliquotoinnin aikana varmista, että solususpensio sekoitetaan usein tasaisen jakautumisen ylläpitämiseksi kryovialeissa [5].
Pidä pakastusväliaine viileänä 2°C - 8°C välillä resuspension aikana vähentääksesi kryoprotektantin toksisuutta ennen pakastusprosessin alkamista [5]. Kun solut on suspendoitu pakastusväliaineeseen, siirry nopeasti pakastusprotokollaan [1].Säilytä solut aina mahdollisimman alhaisella passagenumerolla vähentääksesi geneettisen ajautumisen tai morfologisten muutosten riskiä [5][7].
Kryoprotektanttien ja jäädytysmedioiden valinta
Kryoprotektanttivaihtoehdot ja niiden toiminnot
Dimetyylisulfoksidi (DMSO) on laajalti käytetty kryoprotektantti, tyypillisesti 10% [2] pitoisuudella. Se toimii tunkeutumalla solukalvoihin ja vähentämällä jään muodostumista jäädytyksen aikana. Kuitenkin, DMSO voi olla myrkyllistä soluille huoneenlämmössä, joten nopea sulatus on välttämätöntä altistuksen minimoimiseksi ja sen nopeaksi laimentamiseksi [1].
Glyseroli toimii hyödyllisenä vaihtoehtona solulinjoille, jotka ovat herkkiä DMSO:lle, ja sitä käytetään yleensä pitoisuuksina 5% - 15% [8].Se on erityisen tehokas solutyypeille, joissa DMSO saattaa aiheuttaa ei-toivottua erilaistumista [3], ja sillä on taipumus olla vähemmän myrkyllinen verrattuna DMSO:hon.
Viljellyn lihan sovelluksissa perinteiset pakastusprotokollat käyttävät usein seosta 90% sikiönaudan seerumia (FBS) ja 10% DMSO [1]. Kuitenkin eläinperäisiin komponentteihin tukeutuminen rajoittaa näitä menetelmiä skaalautuvuuden ja sääntelyhyväksynnän osalta [9]. Näiden ongelmien ratkaisemiseksi kemiallisesti määritellyt väliaineet - kuten Synth-a-Freeze tai Recovery Cell Culture Medium - tarjoavat eläinkomponentittoman vaihtoehdon. Nämä väliaineet ylläpitävät korkeaa solujen elinkelpoisuutta sulatuksen jälkeen samalla kun ne voittavat eläinperäisiin komponentteihin liittyvät haasteet [9].
htmlPakastusväliaineiden vertailu
Tässä on erittely viljellyn lihan tuotannossa käytettyjen erilaisten pakastusväliaineiden eduista ja rajoituksista:
| Väline | Edut | Haitat | Soveltuvuus viljellylle lihalle |
|---|---|---|---|
| 10% DMSO FBS-DMEM:ssä | Vakiintuneet protokollat [1] | Sisältää eläinperäisiä komponentteja; eräkohtainen vaihtelu [9] | Rajoitettu skaalautuvuus |
| Synth-a-Freeze | Kemiallisesti määritelty; tasainen laatu; ei eläinperäisiä komponentteja [9] | Korkeammat alkuperäiskustannukset [9] | Kyllä |
| Recovery Cell Culture Medium | Helppokäyttöinen; suunniteltu nopeaan palautumiseen [9] | Voi vaatia optimointia tietyille solulinjoille | Kyllä |
| 10% Glyseroli FBS:ssä | Vaihtoehto DMSO-herkille soluille [1] | Perustuu eläinperäiseen seerumiin [9] | Rajoitettu skaalautuvuus |
Helmikuussa 2023, Tokyo Women's Medical University:n tutkijat, Hironobu Takahashin johdolla, osoittivat oikean jäädytysmedian valinnan tärkeyden.Kaupallisia vaihtoehtoja, kuten CELLBANKER 1 ja 2, käyttämällä he onnistuivat kryosäilyttämään primaarisia naudan myogeenisiä soluja –80°C:ssa jopa vuoden ajan. Huomattavasti, nämä solut säilyttivät kykynsä lisääntyä ja erilaistua supistuvaksi lihaskudokseksi, jossa oli ehjät sarkomeerirakenteet sulatuksen jälkeen [10].
Viljellyn lihan tuotannossa kemiallisesti määritellyt ja GMP-yhteensopivat väliaineet ovat yhä suositumpia. Kuten STEMCELL Technologies korostaa:
Tiukasti säännellyillä aloilla, kuten solu- ja geeniterapiassa, suositellaan käyttämään GMP-valmistettua, täysin määriteltyä kryosäilytysväliainetta, jotta varmistetaan, että tuotteet valmistetaan ja valvotaan johdonmukaisesti laatustandardien mukaisesti [9].
Alustat kuten
Kryosäilytysmenetelmä ja jäähdytysnopeudet
Vaiheittainen pakastusprotokolla
Onnistuneen kryosäilytyksen avain on ylläpitää tasainen jäähdytysnopeus -1°C - -3°C minuutissa[2]. Tämä asteittainen prosessi mahdollistaa veden poistumisen soluista hitaasti, estäen vahingollisten solunsisäisten jääkiteiden muodostumisen, jotka voisivat rikkoa solukalvoja[1].
Aloita sentrifugoimalla solut 150 x g 5 minuutin ajan[3]. Sentrifugoinnin jälkeen resuspendoi solupelletti kylmässä pakastusväliaineessa, joka sisältää 10% DMSO:tä pitoisuudella 2–4×10⁶ solua/mL [3].Vähentääksesi DMSO-altistusta, siirry nopeasti seuraavaan vaiheeseen - pakastamiseen.
Jaa solususpensio ennalta merkittyihin kryogeenisiin putkiin. Jokaisessa putkessa tulisi selvästi ilmoittaa olennaiset tiedot, kuten solulinjan nimi, passagenumero, eränumero, solupitoisuus ja pakastuspäivämäärä[3]. Kun putket ovat valmiina, on aika valita ja käyttää sopivaa jäähdytyslaitteistoa.
Jäähdytyslaitteet ja -tekniikat
Aseta putket välittömästi hallitun jäähdytyslaitteen sisään. Passiiviset pakastusastiat, kuten Nalgene "Mr Frosty" (joka käyttää isopropanolia) tai Corning "CoolCell" , ovat suosittuja valintoja. Nämä työkalut voivat saavuttaa jäähdytysnopeuden noin 1°C minuutissa, kun ne asetetaan -80°C pakastimeen[2] .
Suurempiin operaatioihin, joissa johdonmukaisuus on kriittistä, ohjelmoitava nopeudensäädöllä varustettu pakastin on paras vaihtoehto. Kuten Sigma-Aldrich toteaa:
ECACC käyttää säännöllisesti ohjelmoitavaa nopeudensäädöllä varustettua pakastinta. Tämä on luotettavin ja toistettavin tapa pakastaa soluja[3] .
Noin 24 tunnin jälkeen -80°C:ssa, siirrä pullot nestemäisen typen höyryvaiheeseen, jossa lämpötilat vaihtelevat -135°C:n ja -190°C:n välillä, pitkäaikaista säilytystä varten [4]. Vältä solujen säilyttämistä -80°C:ssa yli viikon ajan, sillä tämä voi heikentää niiden elinkelpoisuutta. Lämpötilat alle -135°C ovat välttämättömiä määräämättömän pitkäaikaiseen säilytykseen[2]. Höyryvaiheen käyttäminen nestemäisen vaiheen sijasta vähentää ristikontaminaation riskiä samalla kun ylläpidetään riittävän alhaisia lämpötiloja.
Sulatus- ja palautusprotokollat
Sulatusprosessi
Solujen nopea sulatus on tärkeää, jotta voidaan rajoittaa myrkyllisen kryoprotektantin altistumista ja estää jääkiteiden aiheuttamat vauriot. Varmista, että käytät kokokasvosuojusta ja eristettyjä käsineitä turvallisuuden takaamiseksi. Aloita poistamalla kryoviaalin nestetypestä ja löysäämällä korkkia hieman paineen vapauttamiseksi. Kiristä sitten korkki uudelleen.
Aseta putki 37°C vesihauteeseen varmistaen, että korkki pysyy vedenpinnan yläpuolella. Anna sen sulaa 1–2 minuuttia tai kunnes vain muutama jääkide on jäljellä. Kun se on sulanut, pyyhi putken ulkopinta 70% alkoholilla steriiliyden ylläpitämiseksi.
Siirrä putken sisältö putkeen, joka sisältää 5–10 ml esilämmitettyä kasvatusväliaineita. Lisää väliaine hitaasti auttaaksesi vähentämään osmoottista shokkia. Jos työskentelet suspensiosolulinjojen kanssa, sentrifugoi solususpensio välittömästi 300 × g 5 minuutin ajan 4°C:ssa.Tämä vaihe auttaa pelletoimaan solut ja poistamaan kryoprotektantin. Sentrifugoinnin jälkeen resuspendoi solut tuoreessa väliaineessa. Adherenttien solujen kohdalla sentrifugointi on yleensä tarpeetonta. Sen sijaan kylvä solut suoraan sopivaan viljelyastiaan ja poista mahdollinen jäännös-DMSO ensimmäisen väliaineen vaihdon yhteydessä, yleensä 24 tunnin kuluttua.
Sulattamisen jälkeiset arvioinnit
Heti sulattamisen jälkeen tarkista solujen elinkyky varmistaaksesi, että toipuminen on onnistunut. Käytä Trypan Blue -poissulkemismenetelmää tähän arviointiin. Ihannetapauksessa solujen elinkyvyn tulisi ylittää 90% [11] , mutta vähintään 75% on hyväksyttävää. 24 tunnin kuluttua tarkista solut faasikontrastimikroskoopilla varmistaaksesi kiinnittymisen, arvioi solutiheys ja tarkista mahdolliset kontaminaation merkit.
Jatka solujen seurantaa läpikulkujen 1–3 aikana varmistaaksesi normaalin lisääntymisen ja että ne säilyttävät odotetut ominaisuutensa.Solulinjoille, jotka toipuvat hitaammin, voit parantaa selviytymistä lisäämällä alkuperäistä sikiönaudan seerumin pitoisuutta noin 20% v/v.
sbb-itb-ffee270
Säilytys ja pitkäaikainen elinkelpoisuus
Säilytysolosuhteet ja kesto
Solulinjojen elinkelpoisuuden säilyttämiseksi pitkällä aikavälillä on tärkeää säilyttää ne alle -135°C lämpötiloissa [7][2]. Tämä varmistaa, että ne pysyvät säilyneinä määräämättömän ajan.
Viljellyn lihan solulinjojen säilyttämiseen suositeltu menetelmä on höyryfaasinen nestemäinen typpi. Tämä tekniikka pitää lämpötilat -135°C ja -190°C välillä, mikä tekee siitä ihanteellisen pitkäaikaiseen säilytykseen ja tarjoaa paremman turvallisuuden verrattuna nestefaasisäilytykseen.
Jos sinun täytyy säilyttää soluja -80°C lämpötilassa, rajoita tämä 24 tunnista yhteen viikkoon. Tämän jälkeen solujen elinkelpoisuus saattaa heikentyä.Tilapäistä säilytystä varten tässä lämpötilassa siirrä solut nestemäiseen typpeen mahdollisimman pian.
Käytä standardeja steriilejä kryogeenisiä putkiloita (1–2 ml), joissa on sisäkierre ja O-rengas turvallista säilytystä varten [4][5]. Aseta aina suljetut kryoputkilot kaasufaasiin mieluummin kuin nestefaasiin typen räjähdysriskin vähentämiseksi sulatuksen aikana [5]. Lisäksi varmista, että nestemäisen typen säiliöt pidetään vähintään puoliksi täynnä turvamarginaalin ylläpitämiseksi.
Lopuksi, tiukat laadunvalvontatoimenpiteet ovat kriittisiä solujen pitkäaikaisen elinkelpoisuuden varmistamiseksi.
Laadunvalvontatarkastukset
Varmistaaksesi varastoitujen solulinjojen luotettavuuden, noudata tiukkoja laadunvalvontaprotokollia. Aloita merkitsemällä jokainen putkilo tarkasti nestemäistä typpeä kestävillä etiketeillä.Sisällytä olennaiset tiedot, kuten solulinjan tunniste, eränumero, passagenumero ja pakastuspäivämäärä. Pidä sähköistä tietokantaa, johon merkitään kunkin ampullin tarkka sijainti, mikä vähentää aikaa, jonka varastointiastiat tarvitsevat olla auki [7][2].
Ennen kuin sitoudut koko erien pitkäaikaiseen varastointiin, testaa yhden ampullin elinkelpoisuus lyhytaikaisen kaasuvaihevarastoinnin jälkeen. Tämä vaihe auttaa varmistamaan, että pakastusprosessi onnistui ja tunnistaa mahdolliset ongelmat [4][7][2]. Erittäin arvokkaiden solukantojen osalta on viisasta säilyttää kopioita toissijaisessa paikassa suojautuakseen laitteistovioilta tai paikallisilta katastrofeilta [7][2].
Varusta kaikki säilytysastiat lämpötilanvalvontajärjestelmillä ja hälyttimillä, jotka havaitsevat alhaiset nestemäisen typen tasot [7]. Lisäksi asenna happihälyttimet säilytystiloihin, jotka laukeavat 18% hapen (v/v) kohdalla, vähentääksesi tukehtumisriskejä nestemäisen typen kanssa työskentelevälle henkilöstölle [7] [2].
Imettävien solulinjojen kryosäilytyksen video-ohjeet
Johtopäätökset ja keskeiset havainnot
Tässä on nopea yhteenveto olennaisista vaiheista ja suosituksista tehokkaaseen kryosäilytykseen viljellyn lihan tuotannossa:
- Solujen kerääminen: Kerää solut niiden logaritmisessa kasvuvaiheessa varmistaen, että elinkelpoisuus ylittää 90%. Käytä 10% DMSO:ta kryosuoja-aineena, vaikka glyseroli voi olla vaihtoehto herkemmille solulinjoille [11] [1]
- Jäähdytys ja varastointi: Säilytä hallittu jäähdytysnopeus ja siirrä ampullit nopeasti höyryvaiheen nestetypen varastointiin solujen eheyden turvaamiseksi [11]
Roka Kakehi et al.:n tutkimus korostaa tarkkuuden merkitystä kryosäilytyksessä [10]:
"Luotettavan ja johdonmukaisen solulähteen varmistaminen kryosäilytyksen avulla mahdollistaa lupaavien solujen vakaan tarjonnan lisäämisen viljellyn lihan tuotantoon." - Roka Kakehi et al., Tokion naisten lääketieteellinen yliopisto
- Sulatusprosessi: Sulata solut 37°C vesihauteessa noin kahden minuutin ajan, lopettaen kun 80% jäästä on sulanut.Tämä vähentää DMSO:n toksisuutta ja parantaa solujen palautumista [1]. Seuraa sulatuksen jälkeisiä elinkelpoisuustarkastuksia varmistaaksesi onnistumisen ja hienosäätääksesi tulevia menettelyjä.
Nämä menetelmät toimivat käsi kädessä tiukkojen laadunvalvontakäytäntöjen kanssa. Merkitse aina pullot tarkasti, pidä järjestelmälliset tiedot ja suorita perusteelliset tarkastukset ennen pitkäaikaista varastointia [11]. Erikoistuneisiin kryosäilytystarpeisiin, alustat kuten
Usein kysytyt kysymykset
Mitkä ovat kemiallisesti määritellyn median käytön edut solulinjojen kryosäilytyksessä viljellyn lihan tuotannossa?
Kemiallisesti määritelty media tuo useita etuja, kun kyseessä on solulinjojen kryosäilytys viljellyn lihan tuotantoa varten.Poistamalla määrittelemättömät komponentit, kuten eläinperäisen seerumin, he varmistavat johdonmukaiset ja ennustettavat tulokset - mikä on ratkaisevan tärkeää solulinjojen pitkäaikaisen luotettavuuden ylläpitämiseksi.
Toinen keskeinen etu on pienentynyt kontaminaation ja vaihtelun riski. Tämä ei ainoastaan tue korkeampia laatu- ja turvallisuusstandardeja, vaan myös sopii täydellisesti yhteen tarkkuuden ja skaalautuvuuden kanssa, joita tarvitaan sekä sääntelyvaatimusten että kuluttajien odotusten täyttämiseksi viljellyn lihan teollisuudessa.
Miten kryoprotektantin valinta vaikuttaa solujen selviytymiseen jäädytyksen ja sulatuksen aikana?
Kryoprotektantin valinta on keskeinen tekijä solujen terveyden säilyttämisessä jäädytyksen ja sulatuksen aikana. Kaksi laajalti käytettyä vaihtoehtoa ovat dimetyylisulfoksidi (DMSO) ja glyseroli, joilla on kummallakin omat erityispiirteensä. DMSO tunnetaan kyvystään tunkeutua soluihin nopeasti ja tarjota vahvaa suojaa.Kuitenkin, siihen liittyy varoitus: korkeissa pitoisuuksissa tai pitkäaikaisessa altistuksessa se voi muuttua myrkylliseksi, mahdollisesti heikentäen solujen elinkykyä.
Glyseroli, toisaalta, on vähemmän myrkyllistä ja sitä voidaan käyttää suoraan. Sen haittapuoli on solujen hitaampi läpäisykyky, mikä voi johtaa vähemmän välittömään suojaan verrattuna DMSO:hon.
Oikean tasapainon saavuttaminen on ratkaisevaa. Kryoprotektantin pitoisuuden ja altistusajan asianmukainen säätäminen auttaa suojaamaan soluja samalla kun minimoidaan myrkyllisyyden riski. Lisäksi parhaiden käytäntöjen noudattaminen jäähdytysnopeuksien ja säilytysolosuhteiden suhteen on olennaista, jotta varmistetaan mahdollisimman korkeat toipumisasteet sulatuksen jälkeen.
Miksi on tärkeää hallita jäähdytysnopeutta kryosäilytyksen aikana?
Vakaan jäähdytysnopeuden ylläpitäminen, yleensä välillä –1°C ja –3°C minuutissa, on avain solujen elinkelpoisuuden säilyttämiseen.Jäähdytys vähitellen mahdollistaa solujen kuivumisen hallitulla tahdilla, mikä vähentää haitallisten jääkiteiden muodostumisen riskiä, jotka voivat repiä tai vahingoittaa solukalvoja.
Tämä mitattu lähestymistapa suojaa solujen rakennetta, parantaen niiden selviytymistä ja toimivuutta sulatuksen jälkeen. Tarkkojen jäähdytysprotokollien noudattaminen on olennaista solulinjojen onnistuneen pitkäaikaisen varastoinnin ja palautumisen varmistamiseksi.











