Stabilność genetyczna jest kluczowa dla produkcji mięsa hodowlanego. Bez niej linie komórkowe mogą mutować, co prowadzi do niespójnej jakości, zagrożeń dla bezpieczeństwa i niepowodzeń produkcyjnych. Skalowanie od tysięcy do bilionów komórek potęguje te ryzyka, co sprawia, że solidne systemy kontroli jakości są niezbędne. Organy regulacyjne, takie jak FDA i EMA, wymagają dowodów stabilności przed zatwierdzeniem produktów, ponieważ nawet drobne zmiany genetyczne mogą wywołać reakcje alergiczne lub szkodliwe skutki.
Kluczowe wyzwania obejmują dryf genetyczny, akumulację mutacji i aktywację onkogenów. Problemy te wynikają z przedłużonego pasażowania komórek, presji selekcyjnej i stresorów środowiskowych podczas produkcji. Zaawansowane metody testowania, takie jak kariotypowanie, macierze SNP i sekwencjonowanie nowej generacji (NGS), pomagają wykrywać i rozwiązywać te zagrożenia. Strategie zapobiegawcze, takie jak strukturalne bankowanie komórek i ukierunkowana inżynieria genetyczna, dodatkowo chronią przed niestabilnością.
Producenci muszą integrować kontrolę jakości na każdym etapie produkcji - od bankowania komórek po bioreaktory na dużą skalę. Narzędzia takie jak profilowanie STR, testy na zanieczyszczenia i testy funkcjonalne zapewniają spójność i bezpieczeństwo. Platformy takie jak
Przyspieszenie rozwoju linii komórkowych od DNA do głównego banku komórek - AGC Biologics
Typowe wyzwania w utrzymaniu stabilności genetycznej
Zapewnienie stabilności genetycznej w całym cyklu produkcyjnym mięsa hodowlanego to nie lada wyzwanie. Sama skala produkcji stwarza wiele możliwości rozwoju i rozprzestrzeniania się zmian genetycznych. Rozpoznanie tych wyzwań jest kluczem do wdrożenia skutecznych systemów kontroli jakości.
Dryf genetyczny i akumulacja mutacji
Przedłużone pasażowanie komórek jest głównym źródłem niestabilności genomowej w produkcji mięsa hodowlanego. Linia komórkowa o nieograniczonej zdolności do podziału, z natury, jest podatna na zmiany genomowe, co może prowadzić do spontanicznych mutacji podczas długoterminowej hodowli [6][5]. W miarę jak komórki przechodzą przez wiele podwojeń populacji, błędy w replikacji DNA narastają, co skutkuje zróżnicowanymi populacjami komórek i potencjalnie utratą funkcji. Christopher Frye i Luhong He z BioPharm International podkreślają ten problem:
Linie komórkowe CHO pochodzące z klonów często obserwowano, że się różnicują, stając się heterogenną populacją w długich okresach subkultury [6].
W warunkach przemysłowych około 20% linii komórkowych wykazuje znaczną heterogeniczność transgenu w kolejnych pokoleniach [6]. Te mutacje mogą wystąpić na wczesnym etapie, podczas replikacji DNA po transfekcji, lub z powodu błędów podczas integracji obcych genów z genomem gospodarza [5].
Presje selekcyjne dodają kolejny poziom złożoności. Czynniki takie jak antybiotyki i markery metaboliczne (e.g. , MTX) używane do stabilizacji linii komórkowych mogą faktycznie zwiększać wskaźniki mutacji [6][5]. W niektórych przypadkach, im wyższe stężenie tych czynników, tym wyższy wskaźnik mutacji [6]. Stresory środowiskowe - takie jak niedobory składników odżywczych, nieoptymalne warunki hodowli podczas skalowania i stres fizyczny związany z ekspansją - mogą dodatkowo destabilizować integralność genetyczną [6][5].
Shuai Wang, Dyrektor ds. Rozwoju Linii Komórkowych w WuXi Biologics, zauważa:
Poziomy mutacji mogą się zmieniać podczas pasażowania komórek z powodu plastyczności genomowej komórek jajnika chomika chińskiego (CHO) [5].
Zmiany epigenetyczne również odgrywają rolę. Transgeny mogą być częściowo lub całkowicie tracone lub wyciszane podczas procesu hodowli, co wpływa na długoterminową stabilność. Te nagromadzone mutacje nie tylko szkodzą funkcji komórek, ale także zwiększają ryzyko aktywacji onkogenów.
Ryzyko Aktywacji Onkogenów
Aktywacja onkogenów stanowi istotne zagrożenie dla bezpieczeństwa producentów mięsa hodowlanego, ponieważ może zagrozić całym partiom produkcyjnym. Niestabilność genetyczna może prowadzić do aktywacji onkogenów poprzez mechanizmy takie jak hipermetylacja, co może skutkować profilami przypominającymi nowotwory [3][1]. Szybka ekspansja wymagana w produkcji dodatkowo zwiększa prawdopodobieństwo nagromadzenia się tych szkodliwych mutacji [5][6].
Jest to dobrze rozpoznane wyzwanie. Według Międzynarodowego Konsorcjum ds. Innowacji & Jakości w Rozwoju Farmaceutycznym (IQ), 67% respondentów uważa, że mutacje genetyczne stanowią większe zagrożenie niż błędne włączenie aminokwasów podczas produkcji [5] . Przypadek z maja 2024 roku ilustruje powagę tego problemu: WuXi Biologics odkryło, że 43% klonów z programu rozwoju linii komórkowej miało tę samą punktową mutację genetyczną. Przyczyna? Poziom wariantu 2,1%–2,2% w plazmidowym DNA używanym podczas transfekcji, który nie został wykryty przez tradycyjne sekwencjonowanie Sanger. Aby temu zaradzić, firma włączyła sekwencjonowanie nowej generacji (NGS) do swoich procesów kontroli jakości, aby wcześnie wykrywać takie warianty [5].
Wczesne wykrywanie nieprawidłowości genetycznych jest kluczowe, ponieważ zmiany onkogenne mogą zagrozić całym partiom. Standardowe kariotypowanie metodą G-pasmową może zidentyfikować nieprawidłowe subpopulacje przy mozaikowości na poziomie zaledwie 14% w dwudziestu metafazach komórkowych [1]. Bardziej zaawansowane techniki, takie jak NGS, mogą wykrywać mutacje genetyczne w komórkach klonalnych z czułością 0,5% [5].
Analiza metylacji DNA to kolejne cenne narzędzie do oceny potencjału nowotworowego:
Ponieważ poziomy metylacji DNA i hipermetylacja niektórych genów występują w inicjacji i progresji raka, analiza profili metylacji DNA może dostarczyć uzupełniających informacji o potencjale nowotworowym komórek [3].
Prawdziwym wyzwaniem jest wdrożenie solidnych systemów monitorowania zdolnych do identyfikacji tych zmian, zanim zagrożą one bezpieczeństwu.Dla producentów mięsa hodowlanego utrzymanie stabilności genetycznej podczas szybkiej ekspansji komórek wymaga zaawansowanych środków kontroli jakości. Specjalistyczne platformy, takie jak
Metody Testowania Kontroli Jakości
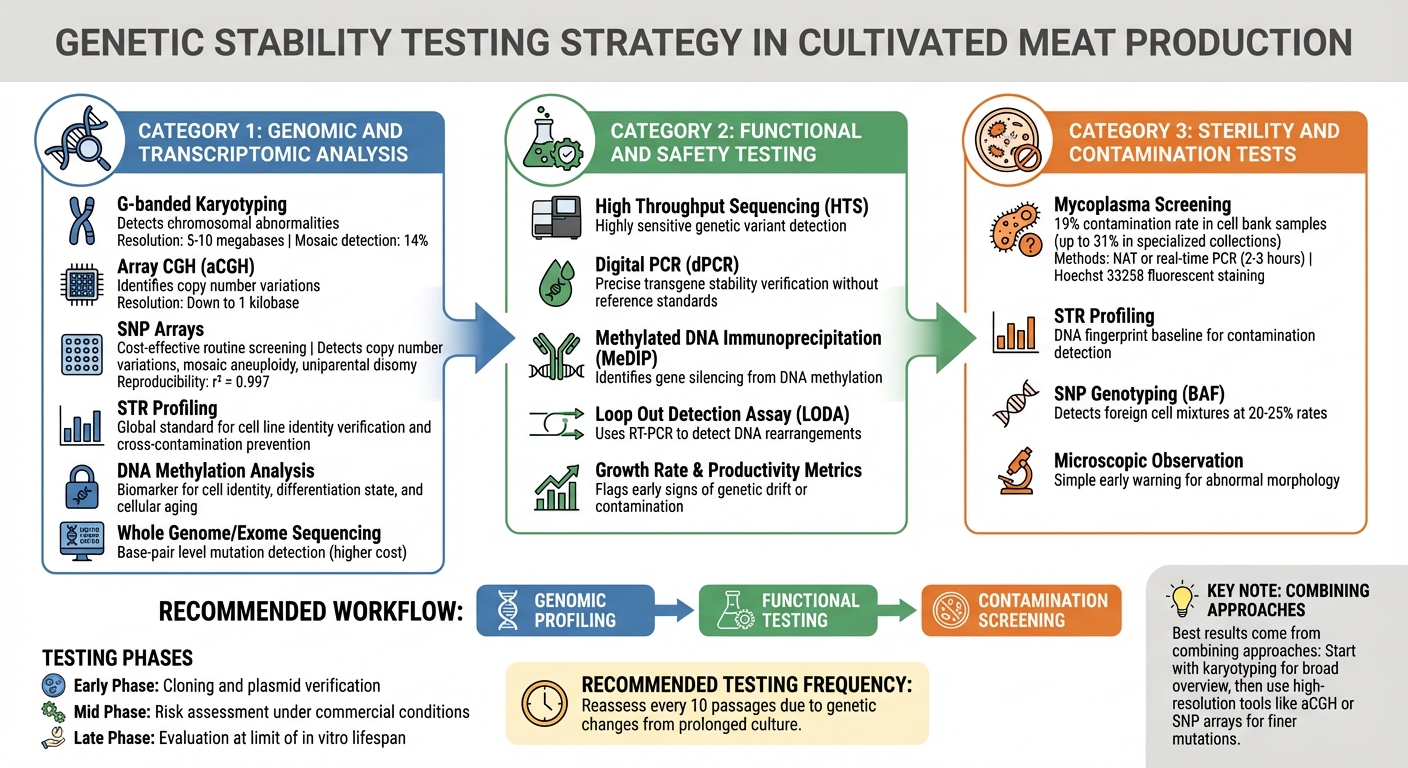
Metody Testowania Kontroli Jakości Stabilności Genetycznej w Liniach Komórkowych Mięsa Hodowlanego
Identyfikacja niestabilności genetycznej zanim wpłynie na produkcję wymaga wielowarstwowej strategii testowania. Producenci mięsa hodowlanego polegają na metodach, które wykrywają wszystko, od dużych zmian chromosomalnych po mutacje pojedynczych zasad. Wybór technik zależy od ryzyk obecnych na każdym etapie produkcji. Te narzędzia genomowe działają jako pierwszy punkt kontrolny, po którym następują szczegółowe oceny funkcjonalne i oceny zanieczyszczeń.
Analiza Genomiczna i Transkryptomiczna
Kariotypowanie z prążkami G jest kluczowym narzędziem do identyfikacji głównych problemów chromosomowych, takich jak nieprawidłowości liczebne i duże rearanżacje strukturalne, takie jak translokacje. Chociaż może wykrywać poziomy mozaikowe na poziomie około 14%, jego rozdzielczość jest ograniczona do zmian o wielkości 5–10 megabaz, co oznacza, że mniejsze zmiany mogą pozostać niezauważone [1].
Porównawcza hybrydyzacja genomowa na mikromacierzach (aCGH) oferuje wyższą rozdzielczość, identyfikując zmiany liczby kopii do 1 kilobazy. Podobnie, mikromacierze polimorfizmu pojedynczego nukleotydu (SNP) stanowią opłacalną opcję do rutynowego badania przesiewowego, wykrywając zmiany liczby kopii, mozaikową aneuploidię i disomię uniparentalną. Badania walidacyjne wykazały, że mikromacierze SNP są wysoce powtarzalne, a pomiary częstotliwości alleli B (BAF) osiągają imponujące r² = 0.997 [8] [1].
Rocio Aguilar-Quesada z Andaluzyjskiego Banku Biobanków Systemu Zdrowia Publicznego podkreśla wartość łączenia metod:
Kariotypowanie pozostaje wszechstronnym testem, zwłaszcza gdy jest uzupełnione testami o wysokiej rozdzielczości [1].
Profilowanie krótkich powtórzeń tandemowych (STR) jest globalnym standardem weryfikacji tożsamości linii komórkowych i zapobiegania krzyżowemu zanieczyszczeniu [1] [9]. W międzyczasie, analiza metylacji DNA służy jako biomarker tożsamości komórkowej, stanu różnicowania i starzenia się komórek [1]. Do wykrywania mutacji na poziomie par zasad, sekwencjonowanie całego genomu lub egzomu jest opcją, choć wiąże się z wyższymi kosztami w porównaniu z metodami opartymi na macierzach [1].
Najlepsze wyniki osiąga się poprzez łączenie tych podejść. Rozpocznij od kariotypowania, aby uzyskać ogólny przegląd, a następnie użyj narzędzi o wysokiej rozdzielczości, takich jak aCGH lub macierze SNP, aby uchwycić drobniejsze mutacje. Regularna ponowna ocena - najlepiej co 10 pasaży - jest kluczowa, ponieważ długotrwała hodowla może prowadzić do zmian genetycznych [10]. Te informacje genomowe są następnie uzupełniane testami funkcjonalnymi, aby zapewnić spójne zachowanie komórek w całym procesie produkcji.
Testowanie funkcjonalne i bezpieczeństwa
Profilowanie genomowe samo w sobie nie wystarcza. Testy funkcjonalne potwierdzają, że komórki zachowują swoje zamierzone cechy podczas ekspansji. Takie wskaźniki jak tempo wzrostu i produktywność mogą wskazywać na wczesne oznaki dryfu genetycznego lub zanieczyszczenia [9].
Wysokoprzepustowe sekwencjonowanie (HTS) jest bardzo czułe na wykrywanie wariantów genetycznych, podczas gdy cyfrowa PCR (dPCR) precyzyjnie weryfikuje stabilność transgenu bez potrzeby stosowania standardów odniesienia [11] . Christopher Frye i Luhong He z BioPharm International podkreślają znaczenie tego kroku:
Linia komórkowa produkcji jest fundamentem każdego bioprocesu, a zatem odpowiednia charakterystyka genetyczna linii komórkowej produkcji jest absolutnie kluczowa dla sukcesu rozwoju procesu [6].
Stabilność epigenetyczna jest również krytyczna. Immunoprecypitacja metylowanego DNA (MeDIP) pomaga zidentyfikować wyciszanie genów spowodowane metylacją DNA, co jest częstą przyczyną spadku produktywności [7]. Narzędzia takie jak Loop Out Detection Assay (LODA) wykorzystują RT-PCR do wykrywania przemieszczeń DNA, na przykład gdy gen zainteresowania jest usuwany, a marker selekcyjny pozostaje [7].
Testowanie powinno być zgodne z fazą produkcji: testy wczesnej fazy koncentrują się na klonowaniu i weryfikacji plazmidów, testy w fazie środkowej oceniają ryzyko w warunkach komercyjnych, a testy w późnej fazie oceniają komórki na granicy ich żywotności in vitro [6]. Rozpoczęcie eksperymentów ze świeżymi, niskoprzepustowymi komórkami z głównego banku komórek zmniejsza ryzyko dryfu genetycznego [9].
Testy na jałowość i zanieczyszczenia
Testowanie na zanieczyszczenia jest niezbędne, aby uniknąć czynników, które mogą destabilizować genetykę. Mykoplazma jest szczególnie niepokojąca, ponieważ zmienia metabolizm i zachowanie komórek bez powodowania widocznych zmian w kulturze [1]. Badania wykazują zanieczyszczenie mykoplazmą w 19% próbek banku komórek, przy czym niektóre specjalistyczne kolekcje wykazują wskaźniki sięgające nawet 31% [1].
Regularne badania przesiewowe na obecność mykoplazmy z wykorzystaniem czułych technik amplifikacji kwasów nukleinowych (NAT) lub PCR w czasie rzeczywistym mogą dostarczyć półilościowe wyniki w ciągu 2–3 godzin [1]. Barwienie fluorescencyjne Hoechst 33258 to inna metoda, ujawniająca charakterystyczne wzory fluorescencji zewnątrzkomórkowej [9].
Profilowanie STR ustala odcisk palca DNA dla linii komórkowych, działając jako punkt odniesienia do wykrywania zanieczyszczeń krzyżowych [9]. Dodatkowo, genotypowanie SNP z wykorzystaniem rozkładów częstotliwości alleli B (BAF) może identyfikować zanieczyszczenia z innych linii komórkowych, wykrywając mieszanki obcych komórek w tempie 20–25% [8].
Mikroskopowa obserwacja jest prostym, ale skutecznym narzędziem wczesnego ostrzegania, ponieważ nieprawidłowa morfologia komórek często sygnalizuje problemy z hodowlą [9]. Wdrożenie Systemu Zarządzania Jakością, takiego jak ISO 9001:2015, wraz z Dobrymi Praktykami Metod In Vitro (GIVIMP), pomaga utrzymać znormalizowane i powtarzalne warunki hodowli, zmniejszając ryzyko niestabilności genomowej [10].
Dla producentów mięsa hodowlanego potrzebujących dostępu do specjalistycznego sprzętu testowego i materiałów, platformy takie jak
sbb-itb-ffee270
Strategie Zapobiegania Niestabilności Genetycznej
Wykrycie niestabilności genetycznej to jedno; jej zapobieganie to zupełnie inne wyzwanie.Aby utrzymać stabilność genetyczną, producenci mięsa hodowlanego potrzebują dobrze przemyślanych systemów, które zapobiegają dryfowi linii komórkowych zanim pojawią się problemy. Dwie kluczowe strategie prowadzą tutaj: ustrukturyzowane bankowanie komórek i celowana inżynieria genetyczna. Razem te podejścia bezpośrednio rozwiązują ryzyko dryfu genetycznego i aktywacji onkogenów.
Bankowanie komórek i krioprezerwacja
Akumulacja mutacji jest realnym zagrożeniem, dlatego niezawodny system bankowania komórek jest koniecznością. Standard branżowy obejmuje system dwupoziomowy: Główny Bank Komórek (MCB) i Roboczy Bank Komórek (WCB). To rozwiązanie zapewnia spójny punkt wyjścia do produkcji. Ograniczenie liczby pasaży jest kluczowe, ponieważ każdy pasaż zwiększa szansę na mutacje. Przechowując komórki w ciekłym azocie, aktywność biologiczna jest skutecznie wstrzymywana, co zmniejsza ryzyko zmian genetycznych podczas przechowywania.
Zamiast śledzenia czasu, wiek komórek mierzony jest przez podwojenia populacji . Na przykład typowy bioreaktor produkcyjny o pojemności 5000 litrów obejmuje około 30 podwojeń populacji[6]. Aby utrzymać spójność genetyczną, produkcja komercyjna ogranicza tę liczbę do 45-60 podwojeń[6].
Metody przesiewowe, takie jak RT-PCR i qPCR pojedynczej komórki, mogą wcześnie wykrywać problemy, takie jak nietypowe składanie mRNA lub zmienność transgenu. Linie komórkowe wykazujące dużą zmienność w liczbie kopii powinny być odrzucane, aby uniknąć przyszłych problemów.
Kontrola jakości jest niepodważalna. Alarmująco, badania wykazały, że do 31% linii komórkowych w niektórych bankach było zanieczyszczonych mykoplazmą [3]. Aby temu zapobiec, profilowanie STR jest używane do potwierdzenia autentyczności linii komórkowych w całym procesie bankowania.Jak podkreślono przez FSA Research and Evidence:
Ponieważ bankowane komórki są materiałem wyjściowym dla produktu końcowego, w przyszłości mogą być wymagane wysokie standardy przez organy regulacyjne, aby zapewnić bezpieczny produkt mięsny o wysokiej jakości [2].
Inżynieria genetyczna dla stabilności
Inżynieria genetyczna zapewnia dodatkową warstwę obrony poprzez bezpośrednie zwiększenie stabilności linii komórkowych. Techniki takie jak celowana integracja (TI), szczególnie Rekombinaza-Mediowana Wymiana Kaset (RMCE), pozwalają na precyzyjne wstawienie transgenów w określone lokalizacje genomowe. To podejście unika nieprzewidywalności losowej integracji, gdzie efekty pozycyjne i niestabilność liczby kopii mogą powodować problemy. Chociaż RMCE w komórkach CHO ma wskaźniki wydajności poniżej 0,1%[12], powstałe klony są bardziej przewidywalne i stabilne.
Wybór systemu ekspresji również ma znaczenie. Na przykład, system syntetazy glutaminowej (GS) zazwyczaj skutkuje około pięcioma kopiami transgenu na komórkę, podczas gdy system reduktazy dihydrofolianowej (DHFR) może amplifikować liczby kopii do 1 000[6]. Chociaż wyższe liczby kopii mogą wydawać się atrakcyjne, zwiększają one prawdopodobieństwo zmian DNA, co sprawia, że systemy oparte na GS są mądrzejszym wyborem dla długoterminowej stabilności.
Aby dodatkowo zminimalizować ryzyko, mutageneza specyficzna dla miejsca i przesiewanie NGS przed transfekcją są kluczowe. Ponieważ sekwencjonowanie Sangera ma wyższy limit detekcji, NGS może wykrywać mutacje plazmidów poniżej 0,5%, poprawiając skuteczność przesiewania klonów do ponad 90%[5].
Shuai Wang i współpracownicy z WuXi Biologics podkreślają znaczenie tej czujności:
Ponieważ optymalizacja procesu nie może naprawić mutacji na poziomie genów, monitoruj poziomy mutacji w stabilnych klonach rygorystycznie[5].
Dla producentów potrzebujących specjalistycznych narzędzi - czy to do krioprezerwacji, inżynierii genetycznej, czy charakteryzacji linii komórkowych -
Integracja kontroli jakości w produkcji
Włączenie kontroli jakości w każdą fazę produkcji jest kluczowe. Bez ustrukturyzowanego systemu, nawet dobrze utrzymane linie komórkowe mogą doświadczać zmian podczas ekspansji i zwiększania skali. Kontrola jakości nie powinna być przemyślana później - musi być centralną częścią produkcji. To zaczyna się na etapie skalowania, gdzie kluczową rolę odgrywają ścisłe systemy zarządzania i kontrolowane środowiska.
Kontrola jakości podczas ekspansji i skalowania
Jak omówiono wcześniej, testy genomowe i kontaminacyjne są kluczowe, zwłaszcza podczas skalowania. Przejście z małych objętości do tysięcy litrów wprowadza nowe ryzyka, a każde przejście komórek zwiększa szansę na mutacje. System Zarządzania Jakością (QMS) pomaga skutecznie zarządzać tymi ryzykami. Na przykład, w latach 2017-2022, Josep M. Canals i jego zespół na Uniwersytecie w Barcelonie wdrożyli ISO 9001:2015 QMS, aby ustandaryzować kultury ludzkich pluripotencjalnych komórek macierzystych. Ich retrospektywna analiza danych G-banding i aCGH wykazała znaczną redukcję aberracji chromosomowych w porównaniu do warunków przed adaptacją[10][13] . Kanały podkreśliły znaczenie ciągłego monitorowania:
Niestabilność genetyczna wykazywana przez hPSC w kulturze sprawia, że częsta ocena integralności genomu jest niezbędnym wymogiem przy planowaniu ich użycia do eksperymentów[10].
Rutynowe badania genomowe są koniecznością. Techniki takie jak kariotypowanie metodą G-pasmowania i aCGH wykrywają zmiany strukturalne, podczas gdy sekwencjonowanie nowej generacji (NGS) identyfikuje mutacje na poziomach poniżej 0,5%[5]. Analiza krzywej wzrostu może również wcześnie sygnalizować problemy, takie jak zanieczyszczenie lub dryf genetyczny[9]. Monitorowanie środowiska dodaje kolejny poziom bezpieczeństwa, a praktyki takie jak testowanie osiadania płyt i półroczne kontrole filtrów HEPA zapewniają, że środowisko produkcyjne pozostaje stabilne i wolne od stresu dla linii komórkowych [4].
Spójność w mediach i odczynnikach jest równie ważna. Używanie zdefiniowanych mediów bez surowicy, takich jak mTeSR1, wraz z odczynnikami posiadającymi Certyfikat Analizy, pomaga zmniejszyć zmienność między partiami i ogranicza ryzyko zanieczyszczenia wirusowego[10][4]. Regularne kontrole morfologii - proste obserwacje mikroskopowe przy różnych gęstościach hodowli - mogą wykryć wczesne oznaki różnicowania lub stresu[9]. Do pozyskiwania specjalistycznego sprzętu lub odczynników, platformy takie jak
Funkcjonalne testy dla spójności produktu
Podczas gdy monitorowanie genomowe zabezpiecza proces, funkcjonalne testy zapewniają, że komórki działają zgodnie z przeznaczeniem.Stabilność genetyczna sama w sobie nie wystarcza; komórki muszą również zachować zdolność do prawidłowego funkcjonowania w różnych partiach produkcyjnych. W przypadku mięsa hodowanego oznacza to potwierdzenie, że komórki macierzyste, takie jak satelitarne komórki mięśniowe, mogą nadal różnicować się w dojrzałą tkankę mięśniową lub tłuszczową po ekspansji[2] . Testy różnicowania są niezbędne do weryfikacji tego.
Testy metaboliczne, takie jak MTT, LDH i Resazuryna, dostarczają informacji o zdrowiu i żywotności komórek[4][9]. Te, w połączeniu z profilowaniem krótkich powtórzeń tandemowych (STR), pomagają potwierdzić, że linie komórkowe pozostają autentyczne i wolne od zanieczyszczeń krzyżowych w całym procesie produkcji[1][9].
Analiza transkrypcyjna to kolejny kluczowy krok.Xiaoyue Chen i Sam Zhang zalecają:
cDNA zamiast sekwencjonowania DNA genomowego jest zalecane do wykrywania mutacji w celu oceny ryzyka na poziomie transkrypcji[5].
Ta metoda oferuje dokładniejszy obraz końcowego produktu, ponieważ odzwierciedla, jak geny są wyrażane, a nie tylko ich lokalizacje genomowe. Poprzez połączenie przesiewania genomowego z funkcjonalnymi testami, producenci mogą zapewnić, że każda partia spełnia rygorystyczne standardy bezpieczeństwa, jakości i wydajności na każdym etapie produkcji.
Wniosek
Utrzymanie stabilności genetycznej jest kluczowe dla bezpiecznej i konsekwentnej produkcji mięsa hodowlanego. Francisco J. Molina-Ruiz i jego koledzy z Laboratorium Komórek Macierzystych i Medycyny Regeneracyjnej podkreślają ryzyka:
Zmiany genetyczne w hPSC mogą zagrozić nie tylko bezpieczeństwu produktów komórkowych opartych na hPSC...ale także prowadzą do heterogenicznej skłonności do różnicowania materiału wyjściowego, zmienionych profili ekspresji genów i nieefektywności końcowego produktu komórkowego [10].
Stawki są znaczące - ponad 531 błędnie zidentyfikowanych linii komórkowych zostało zarejestrowanych przez Międzynarodowy Komitet ds. Autentykacji Linii Komórkowych [1].
Rozwiązanie tych problemów wymaga solidnych ram kontroli jakości. Obejmuje to łączenie metod takich jak profilowanie STR, kariotypowanie G-pasmowe, aCGH i zaawansowane NGS [5] , obok systemów takich jak ISO 9001:2015 w celu standaryzacji procesów i minimalizacji nieprawidłowości chromosomalnych [13].
Czynniki ekonomiczne również napędzają potrzebę tych działań.Dryf genetyczny może prowadzić do uzyskania przez zmutowane komórki przewagi wzrostowej, co potencjalnie może zepsuć całe partie produkcyjne [10][11]. Wraz z rosnącym zainteresowaniem ludzkimi pluripotencjalnymi komórkami macierzystymi, zapotrzebowanie na stabilne linie komórkowe nigdy nie było większe. Jak wyjaśnia profesor David L. Kaplan z Uniwersytetu Tufts:
Nieśmiertelne linie komórkowe są ogólnie uważane za wymóg do generowania ogromnych ilości jadalnej tkanki w stabilnym, solidnym bioprocesie [14].
Dla producentów mięsa hodowlanego kontrola jakości musi być wbudowana w każdy etap - od przeszukiwania plazmidów po monitorowanie produkcji na dużą skalę. Poprzez połączenie dokładnych testów z strategiami zapobiegawczymi, producenci mogą zapewnić spójne i niezawodne wyniki.
FAQ
Jak często należy przeprowadzać testy stabilności genetycznej podczas skalowania?
Testy stabilności genetycznej są kluczowym krokiem podczas skalowania i powinny być przeprowadzane regularnie. Częstotliwość tych testów w dużej mierze zależy od konkretnej linii komórkowej i procesu. Aby zmniejszyć ryzyko mutacji i utrzymać zdolność komórek do różnicowania, warto ustalić limit pasaży na podstawie analizy genetycznej.
Jakie testy najlepiej wykrywają małe mutacje i duże zmiany chromosomowe?
Testy takie jak analiza SNP array i genotypowanie SNP na całym genomie są e
Jaki jest najprostszy sposób zapobiegania dryfowi genetycznemu w partiach produkcyjnych?
Aby zminimalizować dryf genetyczny, kluczowe jest regularne przeprowadzanie analiz genetycznych i funkcjonalnych linii komórkowych oraz ograniczenie liczby ich pasaży. Wdrożenie praktyk takich jak ustanawianie głównych banków komórek i rutynowe sprawdzanie stabilności genetycznej, zgodnie z zaleceniami protokołów kontroli jakości. Te środki są kluczowe dla utrzymania spójności i zapewnienia niezawodnych wyników w różnych partiach produkcyjnych.











