Korkean läpimenon CRISPR-seulonta muuttaa viljellyn lihan alaa mahdollistamalla tarkat geneettiset muutokset solulinjojen suorituskyvyn parantamiseksi. Tässä on mitä sinun tarvitsee tietää:
- Keskeinen haaste: Viljellyn lihan tuotanto vaatii solulinjoja, jotka kasvavat tehokkaasti, vastustavat ikääntymistä ja erilaistuvat lihas- ja rasvakudokseksi.
- CRISPR:n rooli: Kohdistamalla tuhansia geenejä samanaikaisesti, nämä alustat tunnistavat geneettisiä muokkauksia, jotka parantavat kasvua, viivästyttävät vanhenemista ja tukevat erilaistumista.
- Merkittäviä havaintoja: Tutkimukset ovat osoittaneet, että geenien kuten TP53 ja PTEN poistaminen naudan mesenkymaalisista kantasoluista voi lisätä lisääntymistä jopa 1 000-kertaiseksi 30 päivässä ja pidentää niiden elinikää 100:sta 200 päivään.
- Sovellukset: CRISPR-työkaluja, kuten knockout-seulontoja, CRISPRi:tä ja CRISPRa:ta, käytetään solujen kasvun optimoimiseen, geeniekspression säätelyyn ja lisääntymisen tasapainottamiseen erilaistumisen kanssa.
- Teollisuuden työkalut: Kehittyneet tekniikat, kuten RMCE, RNA-seq ja yksittäisten solujen alustat, yhdistävät CRISPR-tulokset multi-omics-datan kanssa, varmistaen tarkat ja skaalautuvat parannukset.
Bioprosessien insinööreille ja T&K-ammattilaisille nämä innovaatiot ratkaisevat kriittisiä pullonkauloja viljellyn lihan prosessien skaalaamisessa samalla kun ne säilyttävät solujen laadun ja toiminnallisuuden. CRISPR:n integrointi automatisoituihin järjestelmiin ja räätälöityihin resursseihin, kuten
CRISPR-Cas9:n perusteet koko genomin laajuisille knockout-seulonnoille
Kuinka CRISPR-Cas9 toimii laajamittaisessa geenieditoinnissa
CRISPR-Cas9-järjestelmä perustuu Cas9-nukleaasin ja yksittäisohjaus-RNA:n (sgRNA) yhdistelmään, joka kohdistuu tiettyihin DNA-sekvensseihin. Kun sgRNA ohjaa Cas9:n haluttuun genomin kohtaan, entsyymi luo kaksoisjuosteen katkoksen DNA:han. Tämä katkos korjataan pääasiassa ei-homologisella päiden yhdistämisellä (NHEJ), joka on virhealtis prosessi ja usein aiheuttaa pieniä insertioita tai deleetioita (indelit). Nämä indelit voivat aiheuttaa kehysvaihdosmutaatioita, jotka tehokkaasti häiritsevät kohdegeenin toimintaa [1]. Tämä tarkka mekanismi on perusta koko genomin laajuisille knockout-seulonnoille, jotka ovat keskeisiä solukäyttäytymisen kriittisten säätelijöiden tunnistamisessa.
Suurimittakaavaiseen seulontaan tutkijat käyttävät monipuolista sgRNA-kirjastoa, joka toimitetaan yleensä sekasolu-populaatioon lentivirus-transduktiolla. Varmistaakseen, että jokainen solu saa vain yhden geneettisen muutoksen, pidetään alhainen infektiomäärä (MOI noin 0,3) [1]. Ajan myötä solut, joilla on edullisia mutaatioita, lisääntyvät yleensä menestyksekkäämmin kuin muut, ilmiö, joka on havaittu monenlaisissa solutyypeissä ja kokeellisissa olosuhteissa.
Vaihtoehtoiset toimitusmenetelmät, kuten rekombinaasi-välitteinen kasettivaihto (RMCE), tarjoavat lisätarkkuutta kohdistamalla tiettyihin genomisiin "laskeutumisalustoihin" vähentääkseen integraatiokohtien vaihtelua. Esimerkiksi tutkimuksessa, jossa käytettiin CHO-K1-soluja, käytettiin viruksetonta RMCE-menetelmää seulomaan 111 651 ainutlaatuista gRNA:ta 21 585 geenin yli. Tämä lähestymistapa tunnisti geenit, jotka ovat välttämättömiä solujen kunnon kannalta 16- ja 37-päivän jaksojen aikana [7].
Genominlaajuisen seulonnan hyödyt
Genominlaajuiset knockout-seulonnat hyödyntävät CRISPR-Cas9:n tarkkuutta tutkiakseen systemaattisesti tuhansia geenejä. Tämä mahdollistaa tutkijoiden löytää geenejä, jotka vaikuttavat solujen selviytymiseen, kasvuun ja stressivasteisiin. Geneettisten tekijöiden lisäksi pintafunktionalisoinnin optimointi on kriittistä solujen kiinnittymisen ja kasvun parantamiseksi näissä järjestelmissä. Tällainen puolueeton tutkimus on erityisen merkityksellistä viljellyn lihan tuotannossa, missä mesenkymaaliset kantasolut (jotka muodostavat noin 25% solulähteistä) kohtaavat usein haasteita, kuten rajallista lisääntymistä ja varhaista vanhenemista [1] .
sbb-itb-ffee270
Yhdistetyt CRISPR-kirjastojen seulontamenetelmät
Yhdistettyjen CRISPR-kirjastojen rakentaminen
Yhdistetyt CRISPR-kirjastot alkavat huolellisesti valitusta kokoelmasta yksittäisopas-RNA:ita (sgRNA).Kultivoidun lihan tutkimuksen yhteydessä kohdennetut kirjastot suunnitellaan usein keskittymään tiettyihin geeniperheisiin, kuten transkriptiotekijöihin tai solujen lisääntymisen säätelijöihin. Tämä lähestymistapa auttaa tasapainottamaan kustannuksia ja laajennettavuutta samalla kun keskitytään haluttuun fenotyyppiin liittyviin ominaisuuksiin [1].
Prosessi alkaa oligonukleotidien synteesillä poolina, niiden monistamisella PCR:n avulla ja kloonaamisella kuljetusvektoriin. Esimerkiksi vuonna 2025 rakennetussa naudalle spesifisessä kirjastossa oli 3 000 sgRNA:ta, jotka kohdistuivat 603 geeniin tunnistamaan kantasolujen laajenemiseen vaikuttavia tekijöitä [1]. Suuremmassa mittakaavassa koko genomin laajuiset seulonnat voivat saavuttaa paljon suuremman monimutkaisuuden. Yksi esimerkki on kiinalaisen hamsterin munasarjasolujen (CHO) seulonta, jossa käytettiin 111 651 ainutlaatuista gRNA:ta kohdistamaan 21 585 geeniä [7].
Lentivirusvälitteistä transfektiota käytetään yleisesti näiden kirjastojen toimittamiseen alhaisella infektiomäärällä (noin 0,3), mikä varmistaa, että jokainen solu käy läpi vain yhden geneettisen muutoksen [1]. Vaihtoehtoisesti viruksettomat menetelmät, kuten rekombinaasi-välitteinen kasettivaihto (RMCE), integroivat gRNA-kirjaston ennalta määrättyihin genomin "laskeutumisalustoihin" pääsolulinjassa. Tämä tekniikka saavuttaa 99.9% gRNA-kattavuuden minimaalisella vääristymällä [7] .
Tilastollisen luotettavuuden ylläpitämiseksi tutkijat varmistavat korkean kattavuuden - tyypillisesti 500-600 solua per sgRNA [1] [7] . Jotkut alustat käyttävät indusoitavia Cas9 (iCas9) -järjestelmiä, jotka mahdollistavat tarkan hallinnan siitä, milloin geenieditointi tapahtuu. Esimerkiksi editointi voidaan käynnistää sen jälkeen, kun solut saavuttavat tietyn tilan, kuten korkean tiheyden tai vanhenemisen alkamisen.Tämä ajallinen hallinta on erityisen hyödyllinen ei-proliferatiivisten vaiheiden tutkimisessa, jotka ovat ratkaisevia vanhenemisesteiden voittamiseksi valitsemalla primaariset vs. kuolemattomat solulinjat viljellyn lihan tuotannon skaalaamiseksi [4] .
Kun kirjasto on rakennettu, tutkijat siirtyvät kohdennettuihin seulontakokeisiin geenitoiminnan arvioimiseksi.
Seulontamenetelmät viljellyn lihan solulinjoille
Kirjaston rakentamisen jälkeen tutkijat arvioivat solujen suorituskykyä kilpailukokeiden ja toiminnallisten lajittelutekniikoiden avulla. Laajalti käytetty menetelmä on kilpailuun perustuva proliferaatiokoe, joka tunnistaa geneettiset muutokset, jotka antavat kasvun tai vanhenemisen vastustuskyvyn - keskeiset ominaisuudet solulinjojen optimoinnissa viljellylle lihalle.
Lyhytaikaiset seulonnat (kestävät noin 30 päivää) tunnistavat geenit, jotka vaikuttavat välittömästi solusykliin, kun taas pitkäaikaiset seulonnat (jopa 200 päivää) keskittyvät geeneihin, jotka auttavat soluja voittamaan replikaation aiheuttaman vanhenemisen. Tämä on kriittinen haaste viljellyn lihan tuotannon laajentamisessa [1]. Monimutkaisempien ominaisuuksien, kuten parannetun proteiinierityksen tai tiettyjen merkkiaineiden ilmentymisen osalta käytetään fluoresenssiaktivoitua solujen lajittelua (FACS). Yksi esimerkki on "kylmäkaappauserityskoe", joka eristää tuottavat solupopulaatiot keräämällä eritetyt proteiinit solupinnalle ennen lajittelua [7] [5].
Validointi on ratkaiseva vaihe seulontatulosten vahvistamisessa. Cellular Fitness (CelFi) -koe esimerkiksi seuraa ajan myötä kehysten ulkopuolisten ja kehysten sisäisten mutaatioiden suhdetta.Jos solut, joilla on kehysten ulkopuolisia mutaatioita, katoavat populaatiosta, se viittaa siihen, että kohdegeeni on olennainen solujen elinkelpoisuudelle [2].
Kesäkuussa 2025 Shijie Dingin johtamat tutkijat Nanjingin maatalousyliopistossa käyttivät CRISPR/Cas9:ää luodakseen CDKN2A–/– sian satelliittisolulinjoja . Nämä muokatut solut säilyttivät vakaan lisääntymisen vähintään 15 passagen ajan seerumittomissa olosuhteissa säilyttäen kantasolumerkit. Kun ne kylvettiin kasvipohjaiselle 3D-syötävälle alustalle, ne muodostivat lihamaisia rakenteita, joiden rakenne oli parantunut, mukaan lukien parantunut pureskeltavuus ja sitkoisuus [8].
"Nämä havainnot osoittavat CRISPR-seulonnan hyödyllisyyden nautaeläinten kantasolujen ominaisuuksien optimoimiseksi ja tarjoavat polun kohti laajamittaisempaa viljellyn lihan tuotantoa tulevaisuudessa." – Communications Biology [1]
Pooled CRISPR-Genetic Screens in Mammalian Cells | Protocol Preview
CRISPRi ja CRISPRa käänteisen geenisäätelyn seulontoihin
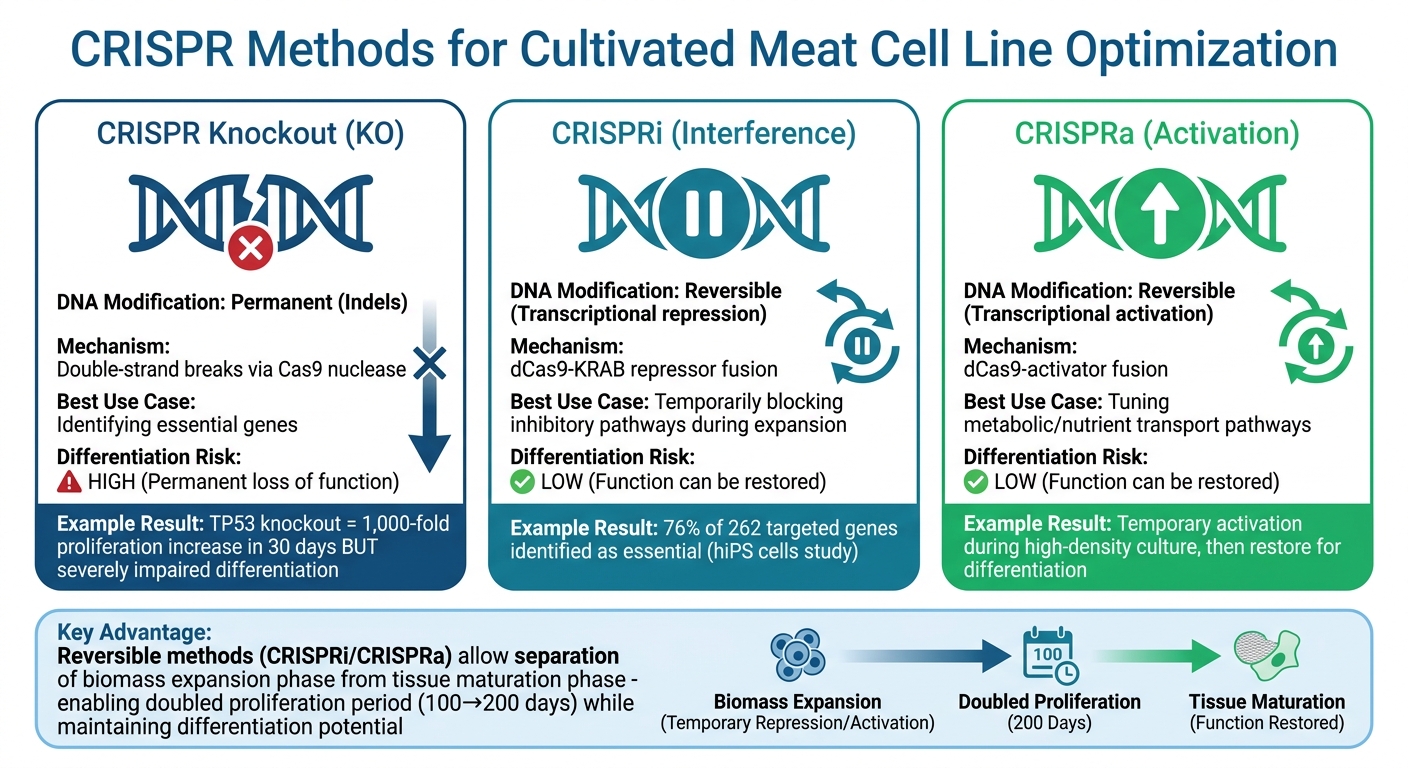
CRISPR-geenieditointimenetelmät viljellylle lihalle: Knockout vs CRISPRi/CRISPRa vertailu
CRISPRi:n ja CRISPRa:n käyttö funktionaalisessa genomikassa
Viljellyn lihan tuotannon parantamisessa CRISPR-interferenssi (CRISPRi) ja CRISPR-aktivaatio (CRISPRa) tarjoavat tehokkaita työkaluja. Nämä tekniikat käyttävät inaktiivista Cas9-proteiinia yhdessä repressoreiden tai aktivaattoreiden kanssa, mikä mahdollistaa tutkijoiden säätää geeniekspressiota tilapäisesti tekemättä pysyviä muutoksia DNA:han [10].
Tämä käänteisyys on erityisen tärkeää suuren haasteen ratkaisemiseksi: geenit, jotka edistävät nopeaa solukasvua, häiritsevät usein erilaistumisen myöhempiä vaiheita lihas- tai rasvakudokseksi. Esimerkiksi TP53-geenin pysyvä poisto naudan mesenkymaalisista kantasoluista voi lisätä lisääntymistä yli 1 000-kertaiseksi vain 30 päivässä, mutta heikentää vakavasti niiden kykyä erilaistua [1]. CRISPRi tarjoaa joustavamman ratkaisun estämällä väliaikaisesti erilaistumista estäviä reittejä biomassan laajentumisen aikana viljellyn lihan bioreaktoreissa. Kun solut ovat valmiita kudoksen kypsymiseen, normaali geenitoiminta voidaan palauttaa.
Lokakuussa 2025 tutkijat, kuten Gabriele Casagrande Raffi ja Roderick L. Beijersbergen Netherlands Cancer Institute:sta, kehittivät indusoitavan CRISPR-järjestelmän.Tämä lähestymistapa viivästyttää geenieditointia, kunnes solut saavuttavat tiettyjä tiloja - kuten korkean tiheyden tai ei-proliferatiivisen vaiheen - auttaen säilyttämään solujen elinkelpoisuuden [4].
CRISPRi erottuu myös tarkkuudellaan verrattuna perinteiseen RNA-interferenssiin (RNAi). RNAi johtaa usein epäjohdonmukaisiin tuloksiin ja kohteen ulkopuolisiin vaikutuksiin, kun taas CRISPRi tarjoaa luotettavampaa ja tarkempaa geenin tukahduttamista [2]. Toinen etu on, että CRISPRi välttää p53:een liittyvän toksisuuden laukaisemisen, joka johtuu usein DNA-vauriovasteista. Vuonna 2025 Liqin Wangin johtamassa tutkimuksessa Sun Yat-sen University Cancer Centre, tutkijat käyttivät doksisykliini-indusoitavaa KRAB–dCas9-järjestelmää seulomaan 262 geeniä ihmisen indusoiduissa pluripotenttisissa kantasoluissa (hiPS-solut). He havaitsivat, että 76% kohdennetuista käännökseen liittyvistä geeneistä (200:sta 262:sta) oli välttämättömiä kasvulle, mikä osoittaa järjestelmän tehokkuuden [10].
Tämä kyky hienosäätää geeniekspressiota tekee CRISPRi:stä ja CRISPRa:sta arvokkaita työkaluja solujen lisääntymisen ja erilaistumisen tasapainottamiseen toiminnallisen genomiikan tutkimuksessa.
Reversiibelien näyttöjen soveltaminen viljellyn lihan sovelluksiin
Reversiibeli geenisäätely tarjoaa ratkaisuja viljellyn lihan tuotannon keskeisiin haasteisiin. Esimerkiksi CRISPRa voi tilapäisesti aktivoida geenejä, jotka liittyvät ravinteiden kuljetukseen tai aineenvaihduntareitteihin korkean tiheyden viljelyssä. Kun solut saavuttavat halutun tiheyden, järjestelmä voi palauttaa geeniekspression normaalille tasolle, tukien asianmukaista erilaistumista lihas- tai rasvakudokseksi.
Indusoitavat järjestelmät mahdollistavat myös biomassan laajentumisvaiheen erottamisen kudoksen kypsymisestä. CRISPRi voi tukahduttaa vanhenemiseen liittyviä geenejä laajennusprosessin aikana, mikä käytännössä kaksinkertaistaa naudansolujen lisääntymisjakson noin 100 päivästä yli 200 päivään [1]. Kun riittävä biomassa on saavutettu, tutkijat voivat palauttaa normaalin geeniekspression mahdollistamaan erilaistumisen. Tämä lähestymistapa on erityisen hyödyllinen mesenkymaalisille kantasoluille, jotka pyrkivät siirtymään ennenaikaiseen vanhenemiseen viljelyssä [1].
"Näiden kahden prosessin kohdennettu geneettinen muokkaus voisi optimoida MSC:n laajentumistehokkuuden samalla säilyttäen niiden olennaisen monikykyisyyden ja erilaistumispotentiaalin, mikä lopulta edistää skaalautuvia viljeltyjä lihajärjestelmiä." – Communications Biology [1]
Alla oleva taulukko korostaa eroja palautuvien ja pysyvien geenisäätelymenetelmien välillä:
| Ominaisuus | CRISPR Knockout (KO) | CRISPRi / CRISPRa |
|---|---|---|
| DNA-muokkaus | Pysyvä (Indels) | Palautuva (Transkriptionaalinen) |
| Mekanismi | Kaksijuosteiset katkokset | dCas9-efuusio |
| Paras käyttötapaus | Välttämättömien geenien tunnistaminen | Metabolisten/kasvureittien säätely |
| Differentiation Risk | Korkea (Pysyvä toiminnan menetys) | Matala (Toiminto voidaan palauttaa) |
Tämä vertailu havainnollistaa, kuinka käänteiset geenisäätelymenetelmät voidaan räätälöidä vastaamaan viljellyn lihan tuotantoon tarkoitettujen solulinjojen kehittämisen erityisiä haasteita.
CRISPR-seulontojen yhdistäminen solupaneeli- ja genotyypitysteknologioihin
CRISPR-seulontojen yhdistäminen multi-omiksianalyysiin
Multi-omiksin ja automatisoidun genotyypityksen integrointi CRISPR-seulontoihin parantaa niiden hyödyllisyyttä, erityisesti viljellyn lihan solulinjojen kehittämisessä.
CRISPR-seulontojen yhdistäminen multi-omiksiin, kuten RNA-sekvensointiin, mahdollistaa tutkijoille tiettyjen geenien poiston vaikutusten kartoittamisen soluprosesseihin. Tämä on erityisen tärkeää viljellyn lihan kannalta, jossa solujen lisääntymisen ja erilaistumisen tasapainon ymmärtäminen on kriittistä.
Esimerkiksi yhdistetty CRISPR-poistoseulonta, joka kohdistuu 600 geeniin naudan rasvaperäisissä mesenkymaalisissa kantasoluissa, yhdistettynä RNA-seq:iin, paljasti, että TP53 ja PTEN poistaminen viivästytti solujen vanhenemista.Nämä solut säilyttivät nuorekkaan geeniekspressioprofiilin, jossa solusyklin geenit olivat ylireguloituja, mikä johti 50% kaksinkertaistumisnopeuden kasvuun 50 päivää transduktion jälkeen [1] .
Yksittäissolualustat, kuten CROP-seq, vievät tämän pidemmälle havaitsemalla samanaikaisesti sekä sgRNA:n että transkriptiomuutokset yksittäisissä soluissa [6]. Tämä tarkkuuden taso on korvaamaton geneettisten muutosten tunnistamisessa, jotka parantavat lihasten erilaistumista tai proteiinisynteesiä - kriittisiä tekijöitä halutun tekstuurin ja ravitsemuksellisten ominaisuuksien saavuttamiseksi viljellyssä lihassa.
Toinen lupaava lähestymistapa sisältää solupaneelin seulonnan, jossa CRISPR-häiriöitä testataan eri luovuttajien, anatomisten paikkojen ja lajien monimuotoisissa solulinjoissa. Esimerkiksi tutkijat validoivat MyoCRISPR-KOLib-kirjaston seitsemän luovuttajan ihmismyoblastilinjoilla.Käyttämällä split-toksiinivalintajärjestelmää he tunnistivat 250 geeniä, jotka ovat välttämättömiä myoblastien fuusiolle. Näistä 41 geeniä vahvistettiin lääketieteellisten tietokantojen kautta vaikuttavan luurankolihasten morfologiaan [6]. Tämä monilinjainen validointi varmistaa, että geneettiset kohteet pysyvät vahvoina biologisten vaihteluiden yli, mikä on keskeinen tekijä viljellyn lihan tuotannon laajentamisessa.
Nämä oivallukset raivaavat tietä automatisoiduille, skaalautuville alustoille, jotka yhdistävät geneettiset seulonnat yksityiskohtaiseen genotyypitykseen teollisiin sovelluksiin.
Automaatio ja Skaalautuvuus Integroituissa Alustoissa
Automaatio on välttämätöntä integroitujen CRISPR- ja genotyypitysalustojen tuottamien laajojen tietoaineistojen ja näytteiden käsittelyssä. RMCE-järjestelmät, jotka mahdollistavat viruksettomat, paikkakohtaiset sgRNA-kirjastojen toimitukset, ovat merkittävä edistysaskel. Nämä alustat varmistavat, että jokainen solu saa yhden, johdonmukaisen sgRNA-kopion, mikä vähentää vaihtelua.RMCE on jo osoittanut korkeaa kirjaston kattavuutta ja minimaalista harhaa kiinalaisen hamsterin munasarja (CHO) soluissa [5].
"Puolueeton korkean läpimenon geneettinen seulonta-alusta on välttämätön seuraavan sukupolven CHO-tehtaiden kehittämiselle." - Kiinalaisen hamsterin munasarjatutkimusryhmä [5]
Skaalautuvuutta parantavat edelleen validointityökalut, kuten Cellular Fitness (CelFi) -määritys. Tämä määritys käyttää kohdennettua syväsekvensointia indel-profiilien seuraamiseen ajan myötä, seuraten kehysten sisäisten ja ulkopuolisten mutaatioiden suhdetta. Yhdistämällä nämä mutaatiot kasvuetuihin tai -haittoihin, tutkijat voivat tehokkaasti varmistaa geneettiset kohteet viljellyissä lihasolulinjoissa [2].
| Teknologia | Integraatiomenetelmä | Pääasiallinen hyöty viljellylle lihalle |
|---|---|---|
| RNA-seq / Multi-omics | CRISPR-osumien yhdistäminen transkriptomiikkaan | Ymmärtäminen, miten geenit säätelevät kasvua ja erilaistumista[1][6] |
| Split-Toxin-järjestelmät | Solufuusion yhdistäminen elinkelpoisuuden valintaan | Fuusiokykyisten tai viallisten solujen kvantitatiivinen valinta[6] |
| RMCE-alustat | Paikkakohtainen gRNA-kirjastojen integrointi | Korkean läpimenon, virukseton seulonta johdonmukaisilla geenikopiomäärillä[5] |
| CROP-seq | Yksisolutason CRISPR + RNA-seq | sgRNA:n ja transkriptiomuutosten samanaikainen havaitseminen [6] |
| CelFi Assay | Indelien kohdennettu syväsekvensointi | Nopea geneettisten kohteiden validointi seuraamalla alleelifrekvenssien muutoksia [2] |
Nämä edistyneet alustat tehostavat prosessia geneettisten kohteiden tunnistamisesta niiden vaikutuksen validointiin solujen elinkelpoisuuteen.Tämä tehokkuus tukee solulinjojen kehittämistä, jotka ovat riittävän kestäviä laajamittaiseen viljellyn lihan tuotantoon.
CRISPR-seulontojen käyttö solulinjan kasvun ja lisääntymisen parantamiseksi
CRISPR-seulontamenetelmistä on tullut tehokas työkalu solulinjan suorituskyvyn parantamiseen, tarjoten suoria etuja viljellyn lihan tuotannolle.
Esimerkkejä CRISPR-pohjaisista solulinjan parannuksista
CRISPR-seulonnat ovat onnistuneesti parantaneet solulinjan suorituskykyä viljellyn lihan tutkimuksessa. Esimerkiksi yhdistetty knockout-seulonta, joka kohdistui 600 geeniin naudan rasvaperäisissä mesenkymaalisissa kantasoluissa, tunnisti TP53 ja PTEN kasvun keskeisiksi estäjiksi. TP53-geenin poisto lisäsi merkittävästi solujen määrää 30 päivän kuluessa[1] . Lisäksi muokatut naudan mesenkymaaliset kantasolut osoittivat 12% keskimäärin suurempaa kaksinkertaistumisnopeutta [1] .
Kohdistamalla tuumorin suppressorigeenejä, tutkijat pidentivät solujen proliferaatiokykyä noin 100 päivästä yli 200 päivään, ohittaen tehokkaasti Hayflickin rajan. Tämä vanhenemisen viivästyminen mahdollistaa biomassan laajenemisen teollisesti merkittävien aikajaksojen aikana[1] .
Toisessa esimerkissä Nanjingin maatalousyliopiston tutkijat, joita johtivat Shijie Ding, Chunbao Li ja Guanghong Zhou, käyttivät CRISPR/Cas9-tekniikkaa kehittääkseen CDKN2A−/− sian satelliittisolulinjoja. Nämä muokatut solut säilyttivät vakaan proliferaation vähintään 18 passagen ajan räätälöidyssä 19-komponenttisessa seerumittomassa väliaineessa (A19). Ne myös kylvettiin onnistuneesti syötäville tukirakenteille, luoden lihamaisia rakenteita, joilla on parantunut pureskeltavuus ja sitkoisuus[8]. Solut säilyttivät yli 90% elinkelpoisuuden useiden passagien ajan seerumittomissa olosuhteissa[8].
"CRISPR-pohjaiset CDKN2A knockout -solut tarjoavat uusiutuvan lähteen lihasprogenitoreille, mikä vähentää riippuvuutta toistuvista eläinbiopsioista."
Nämä esimerkit korostavat, kuinka CRISPR-seulonnat voivat tunnistaa geneettisiä muutoksia, jotka parantavat kasvunopeuksia, hidastavat solujen ikääntymistä ja mahdollistavat seerumittoman viljelyn - kolme olennaista tekijää viljellyn lihan tuotannon skaalaamiseksi.
CRISPR-optimoitujen solulinjojen skaalaushaasteet
Vaikka CRISPR-optimoidut solulinjat osoittavat selviä etuja, niiden skaalaaminen teolliseen käyttöön tuo mukanaan haasteita. Parannettu proliferaatio tapahtuu usein erilaistumisen kustannuksella.Esimerkiksi TP53 knockoutit naudan mesenkymaalisissa kantasoluissa on yhdistetty lihasdifferentiaatiogeeneiden ilmentymisen vähenemiseen, mikä voi estää niiden kykyä kypsyä syötäväksi kudokseksi[1]. Tämän ratkaisemiseksi saatetaan tarvita lisästrategioita, kuten lisäravinteiden lisäämistä kasvatusalustaan tai tiettyjen transkriptiotekijöiden aktivoimista, jotta differentiaatio voidaan palauttaa laajentamisen jälkeen[1].
Toinen kriittinen kysymys on geneettisen vakauden ylläpitäminen. Geenikopioiden määrän vaihtelut (aneuploidia) ja kohdistamattomat vaikutukset CRISPR-muokkauksen aikana voivat johtaa epäjohdonmukaisiin tuloksiin tai vääriin positiivisiin tuloksiin seulontatutkimuksissa[2]. Työkalut, kuten Cellular Fitness (CelFi) -testi, auttavat lieventämään näitä riskejä seuraamalla kehysten ulkopuolisten indelien suhdetta ajan myötä, varmistaen, että havaitut kasvuedut liittyvät suoraan aiottuihin muokkauksiin[2].
Taloudelliset ja tekniset esteet ovat edelleen olemassa. Mesenkymaaliset kantasolut, jotka muodostavat noin 25% solulähteistä viljellyn lihan teollisuudessa, kohtaavat haasteita, kuten kasvutekijöiden korkeat kustannukset, tarve optimoidulle seerumittomalle väliaineelle, ja suurten bioreaktoreiden (10 000–50 000 L kapasiteetit) kehittäminen[1][9] [11]. Lisäksi halutun tekstuurin varmistaminen, kun soluja kylvetään 3D-rakenteisiin, on edelleen monimutkainen tehtävä[11].
"Viljellyn lihan nykytila kohtaa merkittäviä haasteita, mukaan lukien korkeat kustannukset, skaalautuvuusongelmat ja tarve lisäteknologisille edistysaskeleille."
- Communications Biology [1]
Näiden haasteiden voittaminen vaatii kattavaa lähestymistapaa, joka yhdistää geneettisen optimoinnin edistysaskeliin mediakoostumuksessa, bioreaktoriteknologiassa ja erilaistamisprotokollissa. Vaikka CRISPR-seulonnat tarjoavat kriittisiä geneettisiä oivalluksia, näiden löydösten muuttaminen skaalautuviksi ratkaisuiksi vaatii integroituneita järjestelmiä ja tiukkoja validointiprosesseja. Nämä ponnistelut ovat elintärkeitä, jotta viljellyn lihan tuotanto saadaan siirrettyä laboratoriosta kaupalliseen käyttöön.
Kuinka Cellbase Tukee CRISPR-tutkimusta viljellyssä lihassa
CRISPR-seulonta on jo osoittanut potentiaalinsa, mutta sen skaalaaminen teolliseen käyttöön vaatii pääsyä erikoistyökaluihin ja -resursseihin. Tässä
CRISPR-resurssien saatavuus Cellbase kautta
Toisin kuin laajakirjoiset lääkealan toimittajat,
Marraskuussa 2025
"Jokainen viljellyn lihan yritys, jonka kanssa puhuimme, tuhlasi aikaa samaan hankintaongelmaan. Kriittisten komponenttien toimittajien löytäminen tarkoitti farmasian toimittajien selaamista, jotka eivät ymmärtäneet elintarvikesovelluksia."
- David Bell, Cultigen Groupin perustaja [15]
Keskittämällä nämä resurssit,
Yhteistyön mahdollistaminen viljellyn lihan kehittämisessä
Alusta on suunniteltu käsittelemään suurten kaupallisten projektien vaatimuksia, kuten Believer Meats ja Aleph Farms. Nämä hankkeet vaativat infrastruktuuria 50 000 litran bioreaktoreille ja optimoiduille tuotantoketjuille, joita
Päätelmä
Korkean läpimenon CRISPR-seulonta on siirtynyt lupaavasta konseptista kriittiseksi työkaluksi viljellyn lihan kehittämisessä. Tämän teknologian vaikutus solulinjojen optimointiin on kiistaton. Esimerkiksi viimeaikaiset läpimurrot ovat osoittaneet, että geneettiset muutokset voivat kaksinkertaistaa naudan kantasolujen lisääntymisiän 100 päivästä 200 päivään, vähentää vanhenevien solujen populaatiot 60% vain 10%, ja saavuttaa huikean 1 000-kertaisen solumäärän kasvun yhden kuukauden aikana [1] . Nämä edistysaskeleet merkitsevät selvää siirtymää kokeellisesta tutkimuksesta käytännön teollisiin sovelluksiin.
Kompaktit alustat ja kohdennetut kirjastot vastaavat alan kiireellisimpiin haasteisiin.Digitaaliset mikrofluidijärjestelmät mahdollistavat nyt seulonnan vain 3 000 solulla per ehto, mikä tekee mahdolliseksi työskennellä rajoitettujen primaaristen eläinsolujen kanssa, joita ei ole kaupallisesti saatavilla. Samaan aikaan keskittyneet kirjastot, kuten MyoCRISPR-KOLib, kohdistavat tehokkaasti 90% olennaisiin transkripteihin samalla kun ne kattavat vain kolmanneksen genomista [3][6]. Tämä tarkkuuden ja tehokkuuden taso on kriittinen resurssirajoitteiden voittamiseksi ja tuotannon skaalaamiseksi.
"Nämä havainnot osoittavat CRISPR-seulonnan hyödyllisyyden nautaeläinten kantasolujen ominaisuuksien optimoimiseksi ja tarjoavat polun kohti skaalautuvampaa viljellyn lihan tuotantoa tulevaisuudessa." [1]
Huolimatta näistä edistysaskeleista, menestys riippuu oikean infrastruktuurin saatavuudesta.Tutkijat tarvitsevat laji-spesifisiä gRNA-kirjastoja, elintarvikekäyttöön suunniteltuja kasvatusalustoja, yhteensopivia bioreaktoreita ja analyysityökaluja, jotka on räätälöity viljellyn lihan tuotantoon lääketeollisuuden sijaan. Näihin tarpeisiin vastaten
Tiimeille, jotka työskentelevät seuraavan viljellyn lihan solulinjojen aallon kehittämiseksi, työkalut ja teknologiat ovat valmiina. Haasteena on nyt CRISPR-seulonnan nopea ja tehokas käyttöönotto sen täyden potentiaalin saavuttamiseksi.
UKK
Kuinka valitset CRISPR knockoutin, CRISPRi:n ja CRISPRa:n välillä seulontaa varten?
Valinta näiden järjestelmien välillä riippuu erityisestä biologisesta kysymyksestäsi ja tavoittelemastasi lopputuloksesta:
- CRISPR knockout: Tämä menetelmä häiritsee geenin toimintaa kokonaan, mikä tekee siitä ihanteellisen geenin menetyksen tai inaktivaation vaikutusten tutkimiseen.
- CRISPRi: Reprimoimalla geeniekspressiota ilman DNA:n leikkaamista, tämä lähestymistapa sopii hyvin välttämättömien geenien tutkimiseen tai kun tarvitaan palautuvaa suppressiota.
- CRISPRa: Jos sinun täytyy lisätä geeniekspressiota, tämä järjestelmä on paras valinta. Se on erityisen hyödyllinen yliekspression vaikutusten tutkimiseen, kuten solujen lisääntymisen tai erilaistumisen edistämiseen.
Kun teet päätöksiä, ota huomioon solumallisi, kohdegeenisi ja kokeesi yleiset tavoitteet.
Kuinka voit lisätä proliferaatiota vahingoittamatta lihas- tai rasvadifferentiaatiota?
Lihas- tai rasvasolujen proliferaation lisääminen samalla, kun niiden kyky erilaistua säilyy, on keskeinen haaste viljellyn lihan tuotannossa. Yksi lupaava lähestymistapa sisältää CRISPR-pohjaisen geenieditoinnin, joka mahdollistaa geenien tarkan manipuloinnin kasvun parantamiseksi tai solujen eliniän pidentämiseksi. Esimerkiksi kohdistaminen myostatiiniin (MSTN) voi edistää solujen kasvua, kun taas CDKN2A editointi auttaa soluja ohittamaan vanhenemisen.
Siitä huolimatta, tasapainon saavuttaminen proliferaation ja erilaistumisen välillä on kriittistä. Tiettyjen kohteiden, kuten P53 (TP53), väärä hallinta voi heikentää erilaistumista, mikä voi vaarantaa kudoksen laadun.Navigoidakseen näitä monimutkaisuuksia, korkean läpimenon CRISPR-seulonta on keskeinen. Tämä tekniikka tunnistaa tehokkaimmat geenisäätelijät, mikä avaa tien skaalautuvalle ja terveelle kudoskehitykselle viljellyn lihan tuotannossa.
Mitä tarvitaan CRISPR-seulonnan osumien validointiin ennen solulinjan skaalaamista?
CRISPR-seulonnan osumien validointi viljellyn lihan tuotantoa varten vaatii menetelmällisen lähestymistavan. Ensin geenitoiminto on vahvistettava itsenäisten kokeiden, kuten geenin poisto, avulla varmistaakseen, että havaitut vaikutukset ovat toistettavissa. Seuraavaksi on tärkeää arvioida näiden geenien biologinen merkitys tutkimalla niiden vaikutusta tekijöihin, kuten solujen lisääntymiseen, elinkelpoisuuteen ja pitkäikäisyyteen.
Turvallisuusarvioinnit ovat yhtä tärkeitä, jotta voidaan sulkea pois ei-toivotut vaikutukset tai geneettinen epävakaus, jotka voisivat vaarantaa prosessin.Toiminnallinen validointi teollisuusolosuhteita jäljittelevissä olosuhteissa, kuten bioreaktoreissa, on toinen kriittinen vaihe. Tämä varmistaa, että geneettiset muokkaukset toimivat odotetusti suurimittaisissa tuotantoympäristöissä. Perusteellinen testaus jokaisessa vaiheessa on ehdoton edellytys ennen kuin harkitaan laajentamista.











