Agitacja jest kluczowa w produkcji mięsa hodowlanego, zapewniając komórkom dostęp do tlenu i składników odżywczych, jednocześnie unikając nagromadzenia odpadów. Jednak nadmierna agitacja powoduje problemy, takie jak odrywanie się komórek, uszkodzenia błon i zmniejszony wzrost. Znalezienie odpowiedniej równowagi jest niezbędne, szczególnie w dużych bioreaktorach, gdzie nawet drobne korekty mogą wpłynąć na produkcję.
Kluczowe wnioski:
- Optymalna agitacja: Badania pokazują, że 60 obr./min w reaktorach z mieszadłem jest idealne dla równoważenia dostarczania składników odżywczych i naprężeń ścinających.
-
Typy bioreaktorów:
- Reaktory z mieszadłem: Skuteczne mieszanie, ale ryzyko wysokiego naprężenia ścinającego.
- Reaktory falowe: Delikatne mieszanie, ograniczone przez transfer tlenu.
- Systemy airlift: Jednolite mieszanie z niskim naprężeniem, ale wymagają precyzyjnej kontroli.
- Środki Ochronne: Dodatki takie jak Poloxamer 188 i natlenianie bez pęcherzyków zmniejszają uszkodzenia komórek.
- Wyzwania Skalowania: Większe systemy zwiększają ryzyko ścinania, wymagając precyzyjnego monitorowania i modelowania CFD.
Utrzymanie precyzyjnej kontroli mieszania jest kluczowe dla skalowania produkcji mięsa hodowanego przy jednoczesnej ochronie integralności komórek.
Jak Mieszanie Wpływa na Wzrost i Przeżywalność Komórek
Co Pokazują Ostatnie Badania
Ostatnie badania określiły konkretne progi mieszania, które wpływają na wzrost i przeżywalność komórek. Na przykład, badanie ABM-CFD z użyciem komórek FS-4 na mikronośnikach w 100 ml bioreaktorze z mieszadłem wykazało, że 60 obr./min to optymalna prędkość mieszania. Przy tej prędkości składniki odżywcze i tlen są równomiernie rozprowadzane, a naprężenie ścinające pozostaje w zakresie 0–80 mPa. Jednak przekroczenie 60 obr./min prowadzi do uszkodzeń i odłączenia komórek z powodu zwiększonych sił.Przy 220 obr./min liczba Reynoldsa wirnika gwałtownie wzrasta z 1,444 do 5,294.7, co oznacza przejście do przepływu turbulentnego. Ta turbulencja generuje wiry mniejsze niż mikronośniki, które mogą uszkodzić komórki i ich błony [2].
Inne badanie koncentrujące się na mezenchymalnych komórkach macierzystych pochodzących z ludzkiej pępowiny podkreśliło, jak nawet niewielkie zwiększenie intensywności mieszania znacznie zmniejsza wskaźniki adhezji. To pokazuje wysoką wrażliwość komórek adherentnych na stres mechaniczny [6].
Te odkrycia podkreślają znaczenie precyzyjnego kalibrowania prędkości mieszania, co pozostaje kluczowym obszarem ciągłego doskonalenia.
Znajdowanie Odpowiedniej Intensywności Mieszania
Głównym wyzwaniem jest zrównoważenie minimalnej prędkości mieszania potrzebnej do zawieszenia mikronośników (N<sub>js</sub>) bez przekraczania limitów naprężeń ścinających.Dla komórek mięsa idealne warunki obejmują szybkość rozpraszania energii około 1 mW·kg⁻¹ i czas mieszania poniżej 10 sekund [1].
"Utrzymanie korzystnego mikro- i makro-środowiska dla komórek bez narażania ich na nadmierny stres mechaniczny wynikający z mieszania będzie wymagało innowacji i optymalizacji projektów i procesów bioreaktorów" [2].
Nadmierne mieszanie może mieć dwa szkodliwe skutki: natychmiastową śmierć komórek, gdy stres przekracza krytyczny próg, oraz kumulujący się stres prowadzący do stanu spoczynku. Oba wyniki utrudniają produktywność. To sprawia, że precyzyjna kontrola intensywności mieszania jest kluczowym czynnikiem dla sukcesu komercyjnego, zwłaszcza w produkcji na dużą skalę. W systemach o objętości tak dużej jak 20 m³, nawet minimalne mieszanie może powodować odłączenie komórek, co podkreśla złożoność skalowania przy jednoczesnym utrzymaniu żywotności komórek.
Wprowadzenie do bioreaktorów: Mieszanie, mieszanie & ścinanie
Metody mieszania w bioreaktorach i ich efekty
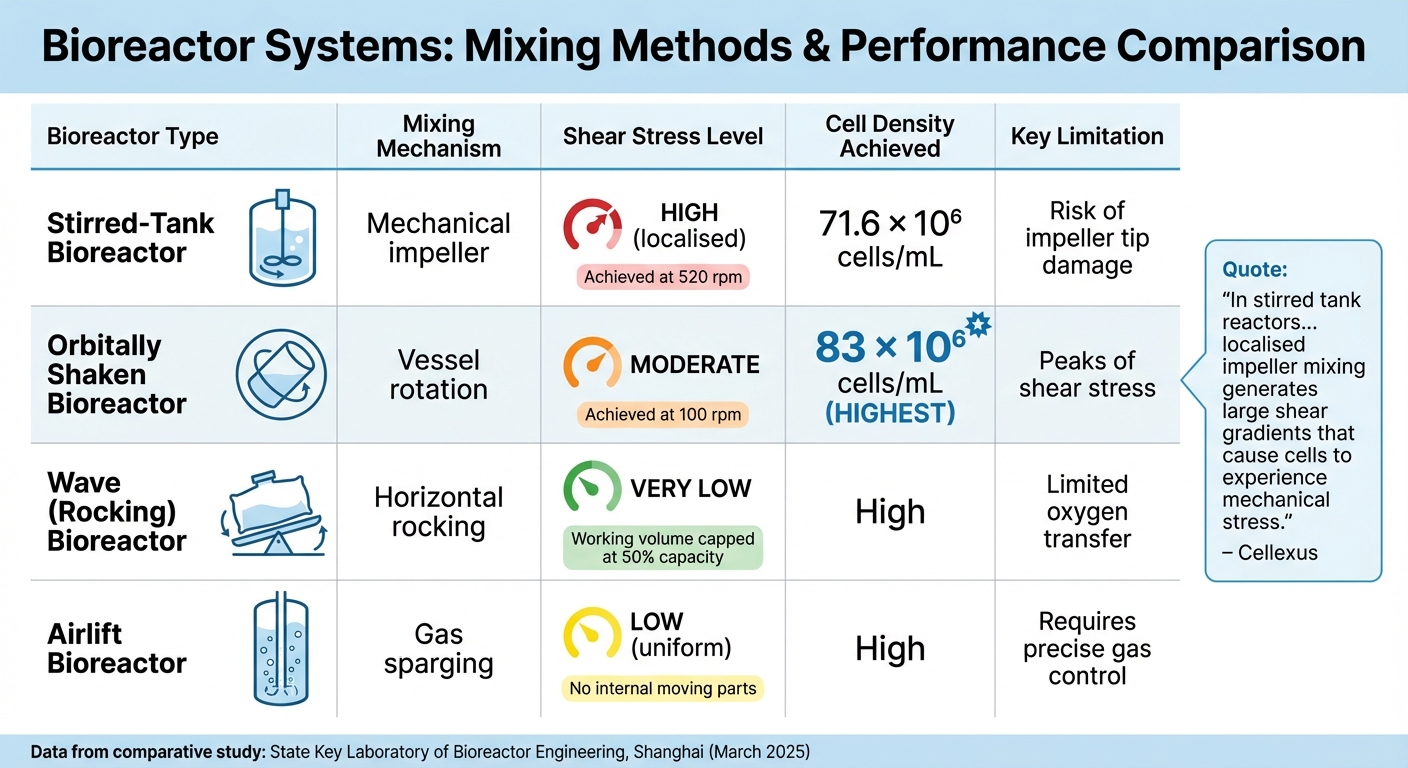
Porównanie typów bioreaktorów do produkcji mięsa hodowlanego
Porównanie różnych systemów bioreaktorów
Projekt bioreaktora odgrywa kluczową rolę w równoważeniu dystrybucji składników odżywczych i zarządzaniu stresem mechanicznym. Każdy typ bioreaktora tworzy odmienne warunki mieszania, które bezpośrednio wpływają na przeżywalność i produktywność komórek. Wybór odpowiedniego systemu oznacza znalezienie równowagi między efektywnym dostarczaniem składników odżywczych a minimalizowaniem sił mechanicznych, które mogą zaszkodzić komórkom.
Bioreaktory z mieszadłem mechanicznym polegają na mechanicznych mieszadłach do mieszania kultury. Mieszadła Rushtona wytwarzają przepływy radialne, prowadząc do lokalnych stref ścinania, zwłaszcza w pobliżu końcówek mieszadła.W przeciwieństwie do tego, mieszadła z łopatkami skośnymi i morskimi tworzą łagodniejsze przepływy, które są lepiej dostosowane do delikatnych komórek ssaków. Badanie przeprowadzone w marcu 2025 roku przez State Key Laboratory of Bioreactor Engineering w Szanghaju porównało wydajność komórek CHO-K1 w bioreaktorach z mieszadłem i wstrząsanych orbitalnie. System z mieszadłem osiągnął 71,6 × 10⁶ komórek/mL przy 520 obr./min, podczas gdy system wstrząsany orbitalnie osiągnął 83 × 10⁶ komórek/mL przy zaledwie 100 obr./min [4].
Bioreaktory falowe (kołyszące) całkowicie eliminują mieszadła, używając jednorazowego worka, który kołysze się na tacy, tworząc łagodne fale do mieszania. To środowisko o niskim ścinaniu jest idealne dla delikatnych linii komórkowych. Jednakże, te systemy polegają na napowietrzaniu powierzchniowym, co może ograniczać transfer tlenu w kulturach o wysokiej gęstości. Aby utrzymać skuteczne formowanie fal, objętość robocza jest ograniczona do 50% całkowitej pojemności worka [7].
htmlBioreaktory airliftowe wykorzystują mieszanie pneumatyczne, gdzie gazowe napowietrzanie cyrkuluje ciecz pomiędzy wznoszącym a opadającym strumieniem. Bez wewnętrznych ruchomych części, systemy airliftowe zapewniają równomierne rozpraszanie energii i niższe siły ścinające w porównaniu do zbiorników z mieszadłem. W przeciwieństwie do bioreaktorów falowych, konstrukcje airliftowe oferują lepszy transfer tlenu dzięki efektywnej cyrkulacji [7].
| Typ bioreaktora | Mechanizm mieszania | Stres ścinający | Osiągnięta gęstość komórek | Kluczowe ograniczenie |
|---|---|---|---|---|
| Zbiornik z mieszadłem | Mechaniczne mieszadło | Wysoki (zlokalizowany) | 71. 6 × 10⁶ komórek/mL | Ryzyko uszkodzenia końcówki mieszadła |
| Orbitralne wstrząsanie | Obrót naczynia | Umiarkowane | 83 × 10⁶ komórek/mL | Szczyty naprężeń ścinających |
| Fala (kołysanie) | Poziome kołysanie | Bardzo niskie | Wysokie | Ograniczony transfer tlenu |
| Airlift | Gazowanie przez sparging | Niskie (jednolite) | Wysokie | Wymaga precyzyjnej kontroli gazu |
"W mieszalnikach zbiornikowych... lokalne mieszanie przez mieszadło generuje duże gradienty ścinania, które powodują, że komórki doświadczają stresu mechanicznego." – Cellexus [7]
W miarę jak bioreaktory są skalowane, kompromisy między efektywnością mieszania a ochroną komórek stają się bardziej widoczne.Systemy z mieszadłem są bardzo skuteczne w rozprowadzaniu składników odżywczych, ale wymagają starannej regulacji prędkości, aby uniknąć uszkodzenia komórek w strefach o wysokim ścinaniu. Z drugiej strony, bioreaktory falowe i z podnośnikiem powietrznym zapewniają łagodniejsze mieszanie, zmniejszając ryzyko stresu ścinającego, choć mogą mieć trudności z dostarczaniem tlenu w gęstych kulturach. Te porównania podkreślają delikatną równowagę wymaganą do optymalizacji procesów biotechnologicznych na dużą skalę przy jednoczesnej ochronie integralności komórek.
sbb-itb-ffee270
Redukcja stresu ścinającego i poprawa wzrostu komórek
Nowe projekty bioreaktorów i dodatki ochronne
Minimalizacja stresu ścinającego jest kluczowa dla promowania wzrostu komórek w produkcji mięsa hodowlanego. Innowacje w projektowaniu bioreaktorów i stosowanie dodatków ochronnych znacznie poprawiły żywotność komórek i efektywność mieszania.Jednym z obiecujących podejść są orbitalnie wstrząsane bioreaktory, które polegają na ruchu naczynia i napowietrzaniu powierzchniowym, aby uniknąć szkodliwych sił ścinających spowodowanych mieszaniem napędzanym przez wirnik i pękaniem bąbelków. Systemy te wykazały imponujące wyniki, osiągając 83 × 10⁶ komórek/mL, w porównaniu do 71.6 × 10⁶ komórek/mL w tradycyjnych systemach z mieszadłem [4].
W systemach z mieszadłem, geometria wirnika również ma znaczenie. Promieniowe wirniki Rushtona tworzą wzorce przepływu, które pozwalają komórkom na regenerację w strefach "spokojnych", zmniejszając wpływ wysokich sił ścinających. Jak zaobserwowali badacze z TTP:
Komórki w reaktorach z promieniowymi wirnikami Rushtona regenerują się podczas faz spokojnych, w przeciwieństwie do tych w systemach z podwójnymi osiowymi wirnikami [5].
Dla optymalnych wyników w produkcji mięsa hodowlanego, utrzymanie prędkości końcówki wirnika w zakresie 0.6–1.8 m/s jest zalecane do ochrony wzrostu komórek [9].
Ochronne dodatki, takie jak Poloksamer 188 (Pluronic F-68), odgrywają kluczową rolę poprzez redukcję napięcia powierzchniowego na granicy faz gaz-ciecz, chroniąc komórki przed uszkodzeniami podczas tworzenia i pękania pęcherzyków. Idealne stężenie dla Poloksameru 188 to 1 g/L, ponieważ wyższe ilości przynoszą niewielkie dodatkowe korzyści [9]. Dla komórek adherentnych hodowanych na mikronośnikach, przerywany reżim mieszania może dodatkowo poprawić wyniki. Na przykład, stosowanie wzoru 30 minut WYŁĄCZONE i 5 minut WŁĄCZONE podczas fazy zasiewu sprzyja transferowi z koralika na koralik, jednocześnie minimalizując stres hydrodynamiczny. To podejście umożliwiło osiągnięcie przez komórki satelitarne bydła gęstości 3 × 10⁶ komórek/mL [3].
Oprócz tych strategii projektowych i dodatków, poprawa dostarczania tlenu może dodatkowo zmniejszyć naprężenia ścinające.
Używanie tlenowania bez pęcherzyków
Tlenowanie bez pęcherzyków oferuje inny skuteczny sposób ochrony komórek przed uszkodzeniami ścinającymi. Pęknięcie pęcherzyków na granicy faz gaz-ciecz może generować szybkości rozpraszania energii sięgające 10⁶ do 10⁸ W/m³, znacznie przekraczając podprogowy poziom 10⁴ W/m³, który większość komórek ssaków może tolerować [9] . Eliminując pęcherzyki, ta metoda pomaga chronić kultury o wysokiej gęstości.
Napowietrzanie powierzchniowe, powszechnie stosowane w bioreaktorach z orbitalnym mieszaniem i kołysaniem, jest szczególnie skuteczne w redukcji sił ścinających.Jak podkreślono w niedawnym badaniu:
OSB wykorzystują ruch ciała naczynia i napowietrzanie powierzchniowe do skutecznego łagodzenia uszkodzeń ścinających spowodowanych przez tradycyjne łopatki wirnika oraz powstawanie lub pękanie pęcherzyków [4].
Kołyszące bioreaktory również wykazują potencjał w produkcji mięsa hodowlanego. Oferują zalety takie jak jednorazowość, niskie koszty operacyjne i łagodne środowisko hydrodynamiczne [8].
Jednak napowietrzanie powierzchniowe napotyka wyzwania przy bardzo wysokich gęstościach komórek. Na przykład, orbitujący bioreaktor osiągnął współczynnik przenoszenia masy tlenu (kLa) wynoszący 20.12 h⁻¹ przy 100 obr./min, teoretycznie wspierając gęstości komórek do 118 × 10⁶ komórek/mL .W praktyce jednak, gdy gęstość komórek przekracza 80 × 10⁶ komórek/mL, lepkość zawiesiny wzrasta, prowadząc do nienewtonowskiego, ścinającego się zachowania, które zmniejsza efektywność transferu tlenu. To podkreśla potrzebę starannej optymalizacji w miarę wzrostu gęstości komórek.
Kontrola mieszania dla produkcji na dużą skalę
Dostosowywanie prędkości mieszania i systemów monitorowania
W systemach na dużą skalę, utrzymanie precyzyjnej kontroli nad mieszaniem jest kluczowe. Przez pierwsze 24 godziny zaleca się utrzymywanie prędkości mieszania w zakresie 30–50 obr./min, aby zoptymalizować przyczepność komórek do mikronośników [6] . Badanie z East China University of Science and Technology z czerwca 2022 roku podkreśla znaczenie tego podejścia: przy 45 obr./min, mezenchymalne komórki macierzyste pochodzące z ludzkiej pępowiny osiągnęły 98.68% wskaźnik przylegania w Dniu 1, podczas gdy zwiększenie prędkości do 55 obr./min spowodowało spadek wskaźników przylegania do 51,32% [6] .
Po fazie przyłączania, mieszanie powinno nieznacznie przekraczać prędkość zawieszenia (N₍JS₎), aby zapobiec zlepianiu się komórek. Badania pokazują, że utrzymanie intensywności mieszania w pobliżu 1,3 × N₍JS₎ wspiera wzrost komórek, podczas gdy przekroczenie tej wartości do 2 × N₍JS₎ hamuje wzrost z powodu zmniejszonej efektywności przyłączania [10] .
Ciągłe monitorowanie jest kluczowe, biorąc pod uwagę wąskie marginesy operacyjne. Systemy takie jak bioreaktor BioStar 1.5c wykorzystują zaawansowane oprogramowanie do dostosowywania mieszania i przepływu gazu na podstawie informacji zwrotnych w czasie rzeczywistym z sond tlenu rozpuszczonego (DO) i pH [6].Czujniki optyczne DO odgrywają tutaj kluczową rolę, oferując precyzję potrzebną do dostosowania mieszania tylko wtedy, gdy poziomy DO spadają poniżej ustalonego progu - zazwyczaj około 40% - minimalizując tym samym naprężenia ścinające [7] [6]. Zespół z Chin Wschodnich zastosował tę metodę, używając sond Mettler Toledo, utrzymując DO na poziomie 40% i pH na poziomie 7,2. Takie podejście zaowocowało maksymalną gęstością komórek wynoszącą 27,3 × 10⁵ komórek/mL , co stanowi 2,9-krotną poprawę w porównaniu do standardowych technik hodowli wsadowej [6].
Podczas skalowania, modele dynamiki płynów obliczeniowych (CFD) są nieocenione w określaniu optymalnej prędkości mieszadła do zawieszania mikronośników bez przekraczania limitów ścinania [10][6]. Zamiast po prostu dopasowywać obroty na minutę między naczyniami, analiza CFD sugeruje wyrównanie średniego objętościowo wskaźnika odkształcenia ścinającego między reaktorami.To zapewnia, że środowisko hydrodynamiczne w większym bioreaktorze - takie jak skalowanie z kolby mieszalnikowej 200 mL do bioreaktora 1,5 L - pozostaje sprzyjające wzrostowi komórek [6].
Te strategie podkreślają znaczenie precyzyjnej kontroli i monitorowania podczas przechodzenia do zaawansowanych systemów bioreaktorów.
Znajdowanie specjalistycznego sprzętu przez Cellbase
Znajdowanie odpowiedniego sprzętu do produkcji mięsa hodowlanego może być trudne. Standardowe platformy zaopatrzenia laboratoryjnego często nie spełniają specyficznych potrzeb tej dziedziny, takich jak mieszadła o niskim ścinaniu czy optyczne czujniki tlenu rozpuszczonego dostosowane do hodowli komórek ssaków o wysokiej gęstości. W tym miejscu
Jako pierwsza dedykowana platforma B2B dla przemysłu mięsa hodowlanego,
Niezależnie od tego, czy modernizujesz swoje systemy monitorujące, czy pozyskujesz specjalistyczne komponenty, platformy takie jak
Wniosek
Utrzymanie równowagi między dostarczaniem tlenu a składników odżywczych, jednocześnie unikając szkodliwego naprężenia ścinającego, jest kluczowe dla optymalizacji mieszania w bioreaktorach do hodowli mięsa. Badania pokazują, że można to osiągnąć poprzez wybór odpowiednich projektów bioreaktorów, dostosowanie prędkości mieszania i stosowanie strategii ochronnych.
Techniki takie jak przerywane mieszanie, promieniowe mieszadła Rushtona i dostosowania w czasie rzeczywistym monitorowane za pomocą CFD (Obliczeniowa Dynamika Płynów) odgrywają dużą rolę w zapewnieniu dobrego odzyskiwania komórek i ich stałego wzrostu. W miarę jak produkcja przechodzi od kolb laboratoryjnych do przemysłowych objętości, zrozumienie zachowania płynów nienewtonowskich i utrzymanie spójnych skal długości Kolmogorowa staje się kluczowe, aby uniknąć uszkodzeń mechanicznych. Te postępy ułatwiają ochronę komórek i upraszczają wysiłki związane ze skalowaniem.
Platformy takie jak
Najczęściej zadawane pytania
Jakie problemy może powodować nadmierne mieszanie w bioreaktorach do produkcji mięsa hodowlanego?
Nadmierne mieszanie w bioreaktorach może stanowić poważny problem dla produkcji mięsa hodowlanego, ponieważ może negatywnie wpływać na wzrost i przeżywalność komórek. Intensywne mieszanie powoduje wysokie naprężenia ścinające, które mogą uszkadzać delikatne komórki zwierzęce. Tego rodzaju stres mechaniczny może prowadzić do uszkodzenia błony komórkowej, zmniejszenia żywotności, a nawet utrudnienia rozwoju tkanek.
Aby zapobiec tym wyzwaniom, kluczowe jest precyzyjne dostosowanie parametrów mieszania.Celem jest znalezienie równowagi między efektywnym transferem składników odżywczych i tlenu a minimalizowaniem stresu mechanicznego. Kluczowe czynniki, takie jak konstrukcja mieszadła, prędkość mieszania i geometria bioreaktora, muszą być starannie dostosowane, aby utrzymać zdrowe, produktywne komórki przez cały proces hodowli.
Jak wybór bioreaktora wpływa na wzrost i żywotność komórek w produkcji mięsa hodowlanego?
Wybór bioreaktora w produkcji mięsa hodowlanego jest kluczowy, ponieważ bezpośrednio wpływa na wzrost i zdrowie komórek, oddziałując na takie czynniki jak efektywność mieszania, transfer tlenu i naprężenia ścinające.
Bioreaktory z mieszadłem mechanicznym są popularną opcją do produkcji na dużą skalę, ponieważ oferują precyzyjną kontrolę nad tymi warunkami. Jednak mogą również generować siły ścinające, które mogą zaszkodzić delikatnym komórkom, co sprawia, że niezbędne jest precyzyjne dostosowanie konstrukcji mieszadeł i parametrów operacyjnych w celu zminimalizowania uszkodzeń.
Inne projekty, takie jak bioreaktory z podnoszeniem powietrznym , są prostsze i zużywają mniej energii. Jednak mogą nie zapewniać tego samego poziomu kontroli nad mieszaniem, co może wpływać na wzrost komórek. Z drugiej strony, bioreaktory z włóknami pustymi naśladują naczynia krwionośne, aby wspierać wysokie gęstości komórek, chociaż ich skalowanie może stanowić wyzwanie.
Wybór odpowiedniego bioreaktora sprowadza się do znalezienia odpowiedniej równowagi między takimi czynnikami jak skalowalność, koszt i specyficzne potrzeby komórek, aby zapewnić ich skuteczny wzrost i rozwój w produkcji mięsa hodowlanego.
Jak można zmniejszyć naprężenie ścinające podczas produkcji mięsa hodowlanego na dużą skalę?
Minimalizacja naprężenia ścinającego w produkcji mięsa hodowlanego na dużą skalę wymaga starannych dostosowań projektu i działania bioreaktora. Czynniki takie jak typ mieszadła, kształt reaktora i ustawienia mieszania odgrywają kluczową rolę.Na przykład, zmniejszenie prędkości końcówek wirnika lub wybór określonych projektów wirników może obniżyć siły ścinające, jednocześnie utrzymując odpowiednie mieszanie i dostarczanie tlenu, co jest kluczowe dla wzrostu komórek.
Innym przydatnym narzędziem w tym procesie jest obliczeniowa dynamika płynów (CFD). Symulacje CFD umożliwiają inżynierom szczegółowe badanie wzorców przepływu i rozkładu sił ścinających, pomagając im w dokonywaniu świadomych zmian projektowych. Dodatkowo, bioreaktory kołyszące się lub mieszane falowo oferują delikatniejszą alternatywę dla tradycyjnych systemów z mieszadłem, ponieważ naturalnie wytwarzają niższe siły ścinające. Włączenie monitorowania w czasie rzeczywistym z zaawansowanymi czujnikami i algorytmami sterowania predykcyjnego może dodatkowo pomóc w utrzymaniu naprężeń ścinających w bezpiecznych granicach, zapewniając płynniejszy proces produkcji.











