Certyfikacja pomieszczeń czystych jest kluczowa dla produkcji mięsa hodowlanego, zapewniając bezpieczeństwo i zgodność z przepisami brytyjskimi, takimi jak Rozporządzenie (WE) 853/2004. Bez certyfikacji, obiekty ryzykują zanieczyszczenie, niezgodność i problemy z jakością produktu. Oto krótki przegląd procesu:
- Dlaczego certyfikacja jest ważna: Zapobiega zanieczyszczeniu mikrobiologicznemu, jest zgodna z zasadami HACCP i zapewnia spójną produkcję.
- Kluczowe standardy: ISO 14644-1 (czystość powietrza), EU GMP Aneks 1 (produkcja sterylna) i EN 17141 (kontrola mikrobiologiczna).
-
Kroki do certyfikacji:
- Projektowanie i budowa: Instalacja filtrów HEPA, systemów przepływu powietrza i utrzymanie odpowiednich różnic ciśnień.
- Kwalifikacja instalacyjna (IQ): Weryfikacja, czy pomieszczenie czyste odpowiada specyfikacjom projektowym.
- Kwalifikacja operacyjna (OQ): Testowanie wydajności w kontrolowanych warunkach.
- Kwalifikacja Wydajności (PQ): Walidacja funkcjonalności podczas rzeczywistych operacji.
- Ciągłe Monitorowanie: Regularne kontrole cząstek, ciśnienia, temperatury i wilgotności.
- Stała Zgodność: Rekwalifikacja co 6–12 miesięcy lub po większych zmianach.
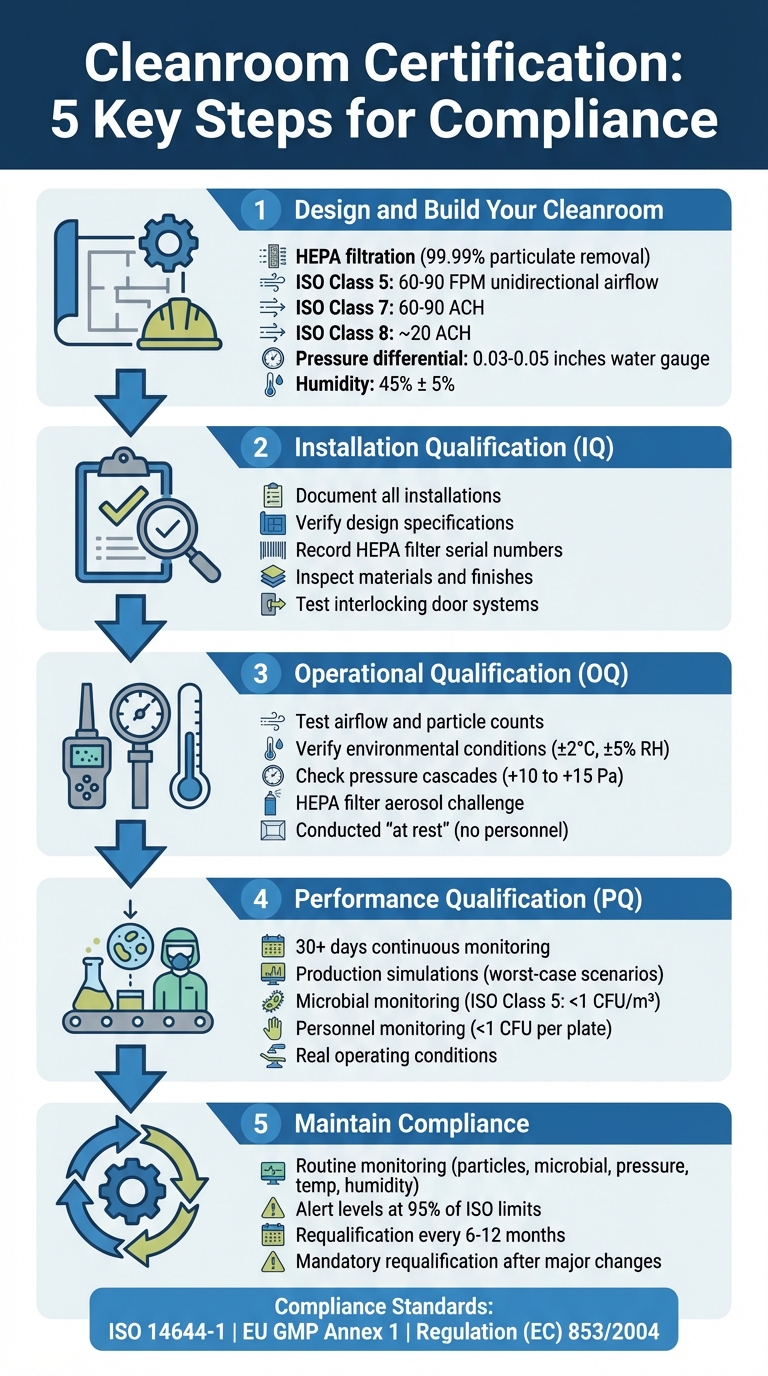
5-stopniowy Proces Certyfikacji Cleanroom dla Obiektów Produkcji Mięsa Hodowlanego
Projektowanie i Certyfikacja Cleanroom
Krok 1: Zaprojektuj i Zbuduj Swój Cleanroom
Budowa cleanroomu do produkcji mięsa hodowlanego wymaga starannego planowania wokół trzech głównych systemów: filtracji HEPA, kontroli środowiskowych i separacji przepływu pracy. Te elementy zapewniają sterylne warunki i pomagają uniknąć kosztownych modyfikacji w przyszłości.Gdy te systemy są już zainstalowane, skup się na optymalizacji ich wydajności podczas instalacji.
Wymagania dotyczące filtracji HEPA i przepływu powietrza
System obsługi powietrza jest kręgosłupem twojego pomieszczenia czystego i decyduje o tym, czy spełnia ono wymaganą klasyfikację ISO. Filtry HEPA usuwają 99,99% cząsteczek[5], ale ich skuteczność zależy od dostarczania powietrza w określonych ilościach i wzorcach dostosowanych do każdej strefy produkcyjnej.
W obszarach klasy ISO 5 - gdzie odbywają się procesy aseptyczne, takie jak zbieranie mięsa - potrzebny będzie jednokierunkowy (laminarny) przepływ powietrza z prędkością 60 do 90 stóp na minutę (FPM) [5]. Obejmuje to jednostki filtrujące z wentylatorami montowane na suficie, kierujące przepływ powietrza przez nisko umieszczone otwory wentylacyjne z wąskim kątem wylotowym.
W strefach klasy ISO 7 i 8 stosuje się mieszany projekt przepływu powietrza. Tutaj świeże powietrze zasilające miesza się z powietrzem wewnętrznym, co wymaga mniejszej liczby wymian powietrza na godzinę (ACH).Strefy klasy ISO 7 wymagają 60–90 ACH, podczas gdy strefy klasy ISO 8 potrzebują około 20 ACH[1][6]. Aby obliczyć ACH, podziel objętość dostarczanego powietrza (na godzinę) przez objętość pomieszczenia. Pamiętaj, że wyższe sufity zwiększają zarówno wymagania dotyczące przepływu powietrza, jak i koszty[3].
Różnice ciśnień są kluczowe dla utrzymania zanieczyszczeń na zewnątrz. Utrzymuj dodatnią różnicę ciśnień na poziomie 0,03–0,05 cala słupa wody między pomieszczeniami czystymi a sąsiednimi obszarami [7]. Jednak nie przekraczaj 0,1 cala słupa wody przez drzwi, ponieważ może to utrudniać ich otwieranie - wymagając do 11 funtów siły na standardowe drzwi o wymiarach 3×7 stóp[7].
Po instalacji przetestuj system filtracji pod kątem integralności, używając testów wyzwań aerozolowych, takich jak testy DOP lub PAO, aby potwierdzić brak wycieków lub słabych uszczelnień w obudowach filtrów HEPA[1]. Badania wizualizacji dymu mogą również pomóc w weryfikacji laminarnych przepływów powietrza i zapewnieniu braku turbulencji lub przepływu zwrotnego w strefach wrażliwych.
Po zainstalowaniu filtracji, kolejnym krokiem jest zapewnienie spójnych warunków środowiskowych.
Kontrola Środowiskowa dla Produkcji
Utrzymanie stabilnej temperatury, wilgotności i ciśnienia jest kluczowe dla minimalizacji ryzyka mikrobiologicznego[9]. Twój system HVAC musi nieustannie utrzymywać te parametry, jednocześnie wspierając wysokie wskaźniki wymiany powietrza wymagane dla klasyfikacji ISO twojego pomieszczenia czystego.
Kontrola temperatury jest szczególnie ważna. System musi przeciwdziałać ciepłu pochodzącemu z bioreaktorów, oświetlenia i personelu, nie zakłócając wzorców przepływu powietrza. Wilgotność względna powinna pozostać na poziomie 45% ± 5%, co pomaga zapobiegać ładunkom elektrostatycznym przyciągającym cząstki i unikać problemów z kondensacją. Ten zakres zapewnia również komfortowe środowisko pracy dla personelu w fartuchach[7].
Monitorowanie w czasie rzeczywistym parametrów środowiskowych, takich jak pH i rozpuszczony tlen, może pomóc w wykrywaniu wczesnych oznak wzrostu drobnoustrojów[9]. Ciągłe monitorowanie powietrza, powierzchni i wody to kolejna istotna praktyka, aby wykryć zanieczyszczenie, zanim się rozprzestrzeni. Dodatkowo, zaprojektuj swój system HVAC z krótkim czasem odzyskiwania - to zapewnia, że pomieszczenie czyste szybko wraca do określonego poziomu czystości po zdarzeniu zanieczyszczenia, zmniejszając przestoje[1].
Gdy kontrola środowiskowa jest już wdrożona, skup się na zarządzaniu przepływem materiałów i ludzi przez przestrzeń, aby zminimalizować ryzyko zanieczyszczenia.
Zarządzanie przepływem materiałów i personelu
"Pracownicy cleanroom są największym źródłem zanieczyszczeń w cleanroomie i wszystkie krytyczne procesy powinny być izolowane od drzwi dostępu i ścieżek personelu." - Vincent A. Sakraida, Inżynier[7]
Personel stanowi największe ryzyko zanieczyszczenia w cleanroomach, zrzucając cząstki skóry, włosy i inne zanieczyszczenia[7][6]. Aby temu zaradzić, układ cleanroomu powinien fizycznie oddzielać krytyczne procesy od obszarów o dużym natężeniu ruchu i punktów dostępu.
Materiały powinny poruszać się w jednym kierunku - z obszarów niższej klasy do obszarów wyższej klasy - z wykorzystaniem zwalidowanych procesów dezynfekcji lub sterylizacji po drodze[8].Sterylizatory dwustronne, takie jak autoklawy z podwójnymi drzwiami lub tunele depirogenacyjne, są idealne do przenoszenia przedmiotów do obszarów przetwarzania aseptycznego bez kompromisów w jakości powietrza[8].
Śluzy powietrzne działają jako bufory między obszarami o różnych poziomach czystości. Strefy ISO Klasy 7 lub czystsze powinny zawierać przedsionek do ubierania się, co zapobiega przedostawaniu się zanieczyszczeń z zewnątrz do obszarów produkcyjnych[6]. Dla stref Klasy A i B systemy drzwi z blokadą zapewniają, że tylko jedne drzwi mogą być otwarte w danym czasie[8]. Jeśli oddzielne śluzy powietrzne dla personelu i materiałów nie są możliwe, proceduralne rozdzielenie czasowe może pomóc uniknąć jednoczesnego przemieszczania się między strefami[8].
Ogranicz dostęp do krytycznych przestrzeni do jednego punktu dostępu, aby zmniejszyć ryzyko zanieczyszczenia krzyżowego[7].Okna obserwacyjne lub zdalne kamery mogą pozwolić przełożonym monitorować działania bez wchodzenia do pomieszczenia czystego, co zmniejsza niepotrzebny dostęp[8].
Każde z tych działań odgrywa kluczową rolę w uzyskaniu certyfikacji pomieszczenia czystego i zapewnieniu, że Twoje obiekty spełniają surowe normy wymagane do bezpiecznej i zgodnej produkcji mięsa hodowlanego.
Krok 2: Ukończenie Kwalifikacji Instalacji (IQ)
Po zakończeniu budowy następnym krokiem jest Kwalifikacja Instalacji (IQ). Ten proces zapewnia, że każdy element pomieszczenia czystego został prawidłowo zainstalowany przed przejściem do testów operacyjnych. W zasadzie IQ działa jako most między zakończeniem fizycznej budowy a rozpoczęciem równoważenia HVAC, potwierdzając, że wszystko jest gotowe do następnej fazy.
"Kontrole Kwalifikacji Instalacji (IQ) zapewniają, że sprzęt, komponenty i konfiguracja czystego pomieszczenia są zgodne ze specyfikacjami producenta i że wszystko zostało zainstalowane poprawnie." - Kjeld Lund, Specjalista ds. Czystych Pomieszczeń [11]
IQ koncentruje się na stanie "jak zbudowano" - kiedy struktura czystego pomieszczenia jest ukończona, ale sprzęt produkcyjny nie jest jeszcze na miejscu. Głównym celem jest zapewnienie, że to, co zostało zbudowane, odpowiada oryginalnemu projektowi, a wszelkie odstępstwa są odpowiednio udokumentowane i rozwiązane.
Dokumentuj Wszystkie Kroki Instalacji
Szczegółowa dokumentacja jest kluczowa na tym etapie. Potrzebne będą szczegółowe zapisy "jak zbudowano", które obejmują zaktualizowane rysunki architektoniczne, listy sprzętu HVAC, sekwencje sterowania i schematy okablowania elektrycznego. Te zapisy powinny odzwierciedlać, jak czyste pomieszczenie zostało faktycznie zbudowane, a nie tylko jak było planowane.
Dla każdego filtra HEPA lub ULPA zanotuj numer seryjny, dokładną lokalizację i datę instalacji. Ważne jest, aby natychmiast po instalacji sprawdzić filtry pod kątem uszkodzeń transportowych - nawet drobne nieszczelności mogą zagrozić integralności pomieszczenia czystego. Oznacz każdy element wyposażenia i czujnik unikalnym identyfikatorem, który odpowiada liście sprzętu, co ułatwi przyszłe audyty i konserwację.
Certyfikaty kalibracji dla wszystkich instrumentów monitorujących muszą być również zarchiwizowane. Obejmuje to liczniki cząstek, czujniki różnicy ciśnień, sondy temperatury i wilgotności oraz urządzenia przepływu powietrza. Jak wyjaśnia Toni Horsfield z ISO Cleanroom, "Certyfikat kalibracji [dla liczników cząstek] jest zawarty w raporcie walidacyjnym pomieszczenia czystego." [10]
Inspekcje materiałów i wykończeń są równie ważne. Zweryfikuj, czy panele ścienne, podłogi, drzwi, przejścia i uszczelniacze spełniają standardy GMP.Powierzchnie powinny być niepylące, o niskiej zawartości lotnych związków organicznych (VOC) i odpowiednio uszczelnione. Drzwi i okna muszą być równo z ścianami, aby utrzymać integralność ciśnieniową.
Prowadź dziennik odchyleń dla wszelkich odchyleń projektowych, notując oceny i podjęte działania korygujące. Ten dziennik stanie się później częścią końcowego raportu walidacyjnego, konsolidując wszystkie ustalenia z fazy instalacji.
Zweryfikuj Specyfikacje Projektowe
Po ukończeniu zapisów instalacyjnych, kolejnym krokiem jest upewnienie się, że każdy system jest zgodny z zatwierdzonym projektem. Porównaj Specyfikację Wymagań Użytkownika (URS) z fizycznymi instalacjami, aby potwierdzić, że nic nie zostało pominięte podczas wysyłki lub montażu.
Dla systemów HVAC i filtracji sprawdź, czy jednostki obsługi powietrza, połączenia przewodów i pozycje dyfuzorów odpowiadają rysunkom projektowym.Potwierdź, że filtry HEPA są prawidłowo osadzone w swoich obudowach i że wszystkie testy ciśnienia przewodów zostały pomyślnie zakończone. Zarejestruj specyfikacje i karty danych dla każdej jednostki filtracyjnej wentylatora.
Weryfikacja strukturalna obejmuje inspekcję blokad, śluz powietrznych i przejść, aby upewnić się, że działają zgodnie z przeznaczeniem. Przetestuj systemy drzwi blokujących, aby upewnić się, że obie drzwi nie mogą otworzyć się jednocześnie. Sprawdź, czy wszystkie uszczelki są nienaruszone i czy pomieszczenie czyste może utrzymać wymagane różnice ciśnień.
Uruchom system HVAC, aby osiągnąć warunki stanu ustalonego przed przejściem do następnego etapu testowania.
Przeprowadzanie IQ z precyzją jest kluczowe, ponieważ stanowi podstawę dla wszystkich kolejnych etapów kwalifikacji. Pomijanie kroków lub pośpiech w dokumentacji może prowadzić do komplikacji podczas testów operacyjnych i audytów regulacyjnych. Dokonując tych kontroli dokładnie, zapewniasz płynne przejście do kwalifikacji operacyjnej.
Krok 3: Przeprowadź Kwalifikację Operacyjną (OQ)
Gdy Kwalifikacja Instalacyjna potwierdzi, że wszystko jest zainstalowane poprawnie, następnym krokiem jest Kwalifikacja Operacyjna (OQ). Ta faza zapewnia, że pomieszczenie czyste działa zgodnie z zamierzeniami w określonych warunkach. Zazwyczaj testy te są przeprowadzane "w spoczynku", co oznacza, że system HVAC działa, ale nie ma obecności personelu ani aktywności produkcyjnych.
"Walidacja dostarcza obiektywnych dowodów na to, że pomieszczenie czyste spełnia swoje przeznaczenie: utrzymuje stabilną, wolną od zanieczyszczeń atmosferę zarówno w warunkach statycznych (w spoczynku), jak i operacyjnych." - Standard Tech [12]
Testy OQ są kluczowe dla wykazania zgodności z normami ISO 14644-1 i GMP. Dla zakładów produkujących mięso hodowlane ten krok jest szczególnie ważny, ponieważ procesy biologiczne opierają się na ścisłej kontroli cząsteczek i mikroorganizmów.Aby zapewnić dokładne wyniki, ustabilizuj pomieszczenie czyste przez co najmniej 30 minut przed rozpoczęciem testów, aby uniknąć zafałszowanych wyników liczenia cząstek [12]. Te kontrole opierają się na fazie instalacji, tworząc podstawy do dostrojenia kontroli środowiskowych.
Testowanie przepływu powietrza i liczenia cząstek
Liczenie cząstek unoszących się w powietrzu jest podstawą klasyfikacji ISO. Używając skalibrowanego licznika cząstek laserowych, zmierz stężenie cząstek w powietrzu, aby potwierdzić zgodność z wymaganą klasą ISO. Dla klasy ISO 5 odnieś się do limitów cząstek określonych w tabeli standardów.
Liczba miejsc pobierania próbek zależy od wielkości pomieszczenia czystego. ISO 14644-1 dostarcza jasnych wytycznych: większe pomieszczenia wymagają większej liczby punktów pobierania próbek, rozmieszczonych w układzie siatki [16]. Jeśli testujesz od dwóch do dziewięciu lokalizacji, musisz obliczyć 95% górną granicę ufności (UCL), aby określić zgodność.Dla dziesięciu lub więcej punktów pomiarowych, to obliczenie jest niepotrzebne [15].
Pomiary prędkości i objętości przepływu powietrza zapewniają, że wskaźnik wymiany powietrza spełnia specyfikacje projektowe. Użyj anemometru do pomiaru prędkości w różnych punktach, zwłaszcza w pobliżu krytycznych obszarów procesowych, i potwierdź, że te wartości odpowiadają celom projektowym.
Badania dymowe oferują wizualny sposób sprawdzenia kierunku przepływu powietrza, zapewniając, że porusza się ono z czystszych do mniej czystych stref. Generuj dym w pobliżu drzwi, przejść i innych wrażliwych obszarów, aby wykryć nieszczelności lub turbulencje, które mogą zakłócać przepływ powietrza [12]. Chociaż liczniki cząstek są precyzyjne, badania dymowe mogą ujawnić problemy, takie jak strefy stagnacji, które w przeciwnym razie mogłyby pozostać niezauważone.
Filtry HEPA i ULPA muszą być również ponownie zweryfikowane podczas OQ. Użyj testu aerozolowego, aby sprawdzić nieszczelności w filtrach lub ich uszczelnieniach.Nawet drobne błędy instalacyjne mogą obniżyć wydajność, dlatego zawsze należy ponownie przetestować po każdej konserwacji lub wymianie filtra [12].
Po potwierdzeniu wydajności przepływu powietrza, uwaga skupia się na warunkach środowiskowych, które wpływają zarówno na jakość produktu, jak i komfort operatora.
Zweryfikuj warunki środowiskowe
Temperatura i wilgotność odgrywają znaczącą rolę w utrzymaniu jakości produktu i zapewnieniu komfortowego środowiska pracy. Dla zakładów produkujących mięso hodowlane, cele walidacyjne to zazwyczaj ±2°C dla temperatury i ±5% dla wilgotności względnej [12]. Zaleca się ciągłe monitorowanie przez co najmniej 24 godziny, ponieważ kontrole punktowe mogą nie wykryć wahań, które mogą wpłynąć na walidację [12].
Pomieszczenia czyste dla mięsa hodowlanego zazwyczaj utrzymują zakres temperatur od 18–22°C i wilgotność względną między 30–60% [14].Te warunki wspierają procesy hodowli komórek, jednocześnie zapobiegając kondensacji, która mogłaby sprzyjać wzrostowi drobnoustrojów. Używaj skalibrowanych czujników termicznych i sond RH rozmieszczonych w całym pomieszczeniu czystym, aby zidentyfikować wszelkie zmiany warunków.
Kaskady ciśnienia to kolejny kluczowy czynnik. Zapewniają one przepływ powietrza z czystszych do mniej czystych obszarów, zmniejszając ryzyko zanieczyszczenia. Zweryfikuj różnice ciśnień - zazwyczaj +10 do +15 Pa między sąsiednimi pomieszczeniami klasyfikowanymi - używając skalibrowanych manometrów. Dokonaj pomiarów przy drzwiach i przejściach w warunkach stanu ustalonego, aby potwierdzić prawidłowe relacje ciśnienia [12].
Testowanie czasu odzyskiwania mierzy, jak szybko pomieszczenie czyste wraca do zgodności po zdarzeniu zanieczyszczenia. Wprowadź kontrolowane źródło cząstek, a następnie monitoruj, jak długo trwa powrót liczby cząstek do poziomu bazowego.Szybsze czasy regeneracji wskazują na lepszy projekt przepływu powietrza i bardziej skuteczną kontrolę zanieczyszczeń [1].
Aby uniknąć opóźnień lub kosztownych ponownych testów, skalibruj wszystkie instrumenty bezpośrednio przed testowaniem OQ. Zapisz wszystkie istotne szczegóły, w tym datę, godzinę, lokalizację, identyfikator instrumentu i warunki środowiskowe dla każdego testu. Ta dokumentacja jest niezbędna do raportu walidacyjnego i będzie wymagana podczas audytów regulacyjnych [12].
sbb-itb-ffee270
Krok 4: Przeprowadź Kwalifikację Wydajności (PQ)
Kwalifikacja Wydajności (PQ) ocenia wydajność twojego pomieszczenia czystego w rzeczywistych warunkach produkcyjnych, z działającym sprzętem i aktywnie pracującym personelem [1][12].Budując na kwalifikacjach instalacyjnych i operacyjnych, PQ zapewnia potwierdzenie, że czysta sala działa konsekwentnie i niezawodnie podczas rzeczywistych operacji.
"PQ weryfikuje wydajność czystej sali w rzeczywistych warunkach operacyjnych, w tym działanie sprzętu i aktywność personelu." - G-CON [1]
Aby zapewnić dokładne testowanie, faza PQ powinna obejmować co najmniej 30 dni ciągłego monitorowania. Ten wydłużony okres pomaga zidentyfikować zmiany, takie jak wahania temperatury podczas cykli produkcyjnych lub zmiany w zanieczyszczeniu mikrobiologicznym spowodowane ruchem personelu, które krótsze testy mogą przeoczyć. Dla zakładów produkujących mięso hodowlane, gdzie ścisła kontrola zanieczyszczeń jest kluczowa, PQ oferuje udokumentowany dowód, że czysta sala pozostaje zgodna podczas rutynowych operacji.
Przeprowadź symulacje produkcji
Symulacje produkcji powinny odtwarzać najgorsze scenariusze.Mogą one obejmować maksymalne obłożenie, jednoczesne działanie wszystkich urządzeń oraz tymczasowe ryzyko zanieczyszczenia, takie jak częste otwieranie drzwi lub intensywny ruch [1][13]. Podejście oparte na ryzyku, takie jak analiza trybu i skutków awarii (FMEA), może pomóc w identyfikacji miejsc pobierania próbek na podstawie ryzyka zanieczyszczenia, przepływu materiałów i obszarów o dużym natężeniu ruchu [16].
Monitorowanie mikrobiologiczne podczas tych symulacji jest kluczowe. Jednostki tworzące kolonie (CFU) powinny być śledzone zarówno za pomocą metod aktywnych, jak i pasywnych [14][17]. Dla czystych pomieszczeń klasy ISO 5, limit działania dla zanieczyszczenia mikrobiologicznego wynosi zazwyczaj 1 CFU/m³ [14].
Ponieważ ludzie są największym źródłem cząstek w czystych pomieszczeniach, monitorowanie personelu jest równie ważne.Pobieranie próbek z opuszka palca w rękawiczce może potwierdzić prawidłowe techniki aseptyczne, z dopuszczalnym limitem poniżej 1 CFU na płytkę [17]. Operatorzy powinni być wcześniej poinformowani o protokołach ubierania się i poruszania, aby zapobiec sztucznym skokom poziomów zanieczyszczenia [12].
Dodatkowo, przetestuj, jak szybko czyste pomieszczenie odzyskuje stan po kontrolowanym wyzwaniu cząsteczkowym. Wprowadź źródło cząsteczek i zmierz czas potrzebny na powrót warunków do stanu wyjściowego. Ten proces ocenia przepływ powietrza i skuteczność systemów kontroli zanieczyszczeń [1][12].
Ustaw Monitorowanie Środowiskowe
Po testach symulacyjnych, ciągłe monitorowanie środowiskowe zapewnia spójne działanie.Te systemy dostarczają danych w czasie rzeczywistym na temat kluczowych parametrów, takich jak cząstki unoszące się w powietrzu, zanieczyszczenia mikrobiologiczne, temperatura, wilgotność i różnice ciśnień. Jest to niezbędne do wykrywania zmian wydajności, zanim doprowadzą one do problemów z zgodnością [1]. W produkcji mięsa hodowlanego ciągłe monitorowanie jest nieodzowne.
Podczas fazy kwalifikacji przeprowadzaj pobieranie próbek powietrza pod kątem mikrobiologicznym co 1–2 godziny w strefach krytycznych, aby potwierdzić skuteczną kontrolę zanieczyszczeń [14]. Używaj agaru sojowego tryptozowego (TSA) do wykrywania bakterii, inkubując próbki w temperaturze 30–35°C przez minimum trzy dni, oraz agaru Sabourauda (SAB) do wykrywania grzybów i pleśni, inkubując w temperaturze 20–25°C przez co najmniej siedem dni [17]. Unikaj używania aerozoli lub środków dezynfekujących w pobliżu próbnika powietrza podczas testowania.Jeśli zastosowano rotacyjne środki dezynfekujące lub 70% alkohol izopropylowy, odczekaj co najmniej pięć minut przed rozpoczęciem pobierania próbek powietrza [17].
Ustal jasne limity ostrzegawcze i działania dla wszystkich monitorowanych parametrów. Poziomy ostrzegawcze sygnalizują potrzebę przeprowadzenia dochodzenia, gdy wartości zaczynają odbiegać od normy, podczas gdy limity działania wymagają natychmiastowego podjęcia działań korygujących, jeśli parametry przekraczają dopuszczalne zakresy [14]. Prowadź szczegółową dokumentację każdego pomiaru, w tym datę, czas, lokalizację, szczegóły dotyczące instrumentu i warunki środowiskowe. To zapewnia, że zawsze jesteś przygotowany na audyty i możesz wykazać zgodność z normami ISO 14644 i GMP.
Krok 5: Utrzymuj zgodność poprzez monitorowanie
Po zakończeniu kwalifikacji wydajności praca się nie kończy. Utrzymanie zgodności wymaga ciągłego monitorowania i okresowej rekwalifikacji.Certyfikacja pomieszczeń czystych nie jest jednorazowym osiągnięciem - wymaga stałego wysiłku, aby utrzymać obiekt w "stanie kontroli". Dla obiektów produkujących mięso hodowlane, ten ciągły proces zapewnia spełnienie zarówno standardów regulacyjnych, jak i operacyjnych, rozszerzając skrupulatne praktyki faz kwalifikacyjnych na codzienne operacje.
Wdrażanie rutynowego monitoringu
Aby zapewnić, że Twoje pomieszczenie czyste pozostaje zgodne ze standardami ISO 14644 i GMP, musisz regularnie monitorować zanieczyszczenia mikrobiologiczne i cząsteczkowe. Kluczowe parametry, na które należy zwracać uwagę, to:
- Liczba cząsteczek
- Poziomy mikrobiologiczne
- Ciśnienie
- Temperatura
- Wilgotność
- Przepływ powietrza
Częstotliwość monitorowania powinna być zgodna z klasyfikacją pomieszczenia czystego i dokładną oceną ryzyka.Na przykład, strefy klasy ISO 5 często wymagają ciągłego lub godzinowego monitorowania cząstek podczas produkcji, podczas gdy mniej krytyczne obszary mogą wymagać jedynie codziennych lub cotygodniowych kontroli.
Ustaw poziomy alarmowe na 95% limitów ISO, aby wcześnie wykrywać potencjalne problemy. Te poziomy działają jako ostrzeżenie, gdy parametry zaczynają się zmieniać, co skłania do przeprowadzenia dochodzenia, zanim sytuacja się pogorszy. Z drugiej strony, limity działania wymagają natychmiastowego podjęcia działań korygujących, jeśli parametry przekroczą dopuszczalne zakresy [14] .
Innym istotnym elementem monitorowania jest pobieranie próbek z opuszka palca w rękawiczce (GFS). Ta metoda zapewnia, że personel utrzymuje właściwe techniki aseptyczne. Standardowe kryterium to zazwyczaj mniej niż 1 CFU na płytkę [17]. Wykonywanie GFS po krytycznych zadaniach aseptycznych lub na koniec każdej zmiany pomaga wcześnie zidentyfikować i rozwiązać problemy z techniką.
Podczas gdy rutynowe monitorowanie pomaga utrzymać codzienną kontrolę, rekwalifikacja zapewnia, że systemy czystych pomieszczeń pozostają skuteczne w dłuższej perspektywie.
Zaplanować Rekwalifikację
Rekwalifikacja powinna być przeprowadzana co 6 do 12 miesięcy. Jednakże, pewne wydarzenia sprawiają, że rekwalifikacja jest obowiązkowa, takie jak remonty strukturalne, instalacje nowego sprzętu, wymiany filtrów HEPA lub znaczące zmiany w systemie HVAC [1][14].
Podczas rekwalifikacji wiele testów z fazy Kwalifikacji Operacyjnej będzie musiało zostać powtórzonych. Należą do nich:
- Zliczanie cząstek w powietrzu
- Testowanie integralności filtrów HEPA (udowadniając 99,99% skuteczności dla cząstek ≥0.3 mikrony)
- Pomiary prędkości przepływu powietrza
- Kontrole różnicy ciśnień
Jednym z szczególnie krytycznych testów jest test czasu odzyskiwania, który mierzy, jak szybko pomieszczenie czyste wraca do docelowego poziomu czystości po zdarzeniu zanieczyszczenia. Ten test weryfikuje zdolność systemu HVAC do skutecznego radzenia sobie ze stresem [1].
Utrzymuj Plan Główny Walidacji (VMP), aby dokumentować wszystkie etapy kwalifikacji (IQ, OQ, PQ) oraz harmonogram ponownej kwalifikacji. Upewnij się, że wszystkie instrumenty używane do testowania - takie jak liczniki cząstek i anemometry - są skalibrowane i posiadają certyfikaty śledzone do standardów krajowych [1] [14]. To zapewnia dokładność i niezawodność w twoich działaniach zgodności.
Źródła sprzętu do pomieszczeń czystych dla zgodności
Znajdź zweryfikowanych dostawców na Cellbase
Gdy standardy operacyjne i wydajnościowe Twojego pomieszczenia czystego są ustalone i zweryfikowane, kolejnym krokiem jest pozyskanie odpowiedniego sprzętu do utrzymania zgodności. W przypadku produkcji mięsa hodowlanego oznacza to współpracę z dostawcami, którzy rozumieją unikalne wymagania branży.
Zapewnij zgodność z GMP podczas zakupu
Po weryfikacji sprzętu, proces zakupu musi również spełniać rygorystyczne standardy GMP.
Dodatkowo, platforma priorytetowo traktuje materiały spełniające wymagania GMP. Na przykład, materiały konstrukcyjne takie jak stal nierdzewna 316L z polerowanymi, niepylącymi powierzchniami są wyróżniane. Te materiały są odporne na wielokrotną dezynfekcję chemiczną i wspierają zweryfikowane protokoły Cleaning-in-Place (CIP) i Sterilisation-in-Place (SIP) [4]. Weryfikując zgodność materiałów na początku, można uniknąć kosztownych przeróbek lub cykli ponownej kwalifikacji w późniejszym czasie. To proaktywne podejście pomaga utrzymać zgodność, oszczędzając jednocześnie czas i zasoby.
Podsumowanie
Kluczowe wnioski
Uzyskanie certyfikacji cleanroom jest kluczowe dla utrzymania jakości produktu i spełnienia standardów regulacyjnych. Zaczyna się od zaprojektowania cleanroomu wyposażonego w filtrację HEPA, kontrolowany przepływ powietrza i efektywny przepływ materiałów. Proces kontynuuje się poprzez trzystopniowe podejście do kwalifikacji: Kwalifikacja Instalacyjna (IQ), Kwalifikacja Operacyjna (OQ) i Kwalifikacja Wydajnościowa (PQ). Te etapy zapewniają, że wszystkie systemy działają skutecznie w rzeczywistych warunkach pracy.
Certyfikacja na tym się nie kończy. Ciągłe monitorowanie czynników takich jak temperatura, wilgotność, ciśnienie i liczba cząstek jest niezbędne do identyfikacji wszelkich problemów z wydajnością. Regularna rewalidacja zapewnia zgodność z ISO 14644-1 i standardami GMP, tworząc solidne ramy dla przyszłych usprawnień.
Kolejne kroki dla Twojego obiektu
Aby dostosować swój obiekt do tych standardów, rozważ opracowanie Planu Głównego Walidacji (VMP). Plan ten integruje procesy kwalifikacyjne z codziennymi potrzebami operacyjnymi, pomagając wyprzedzać wymagania regulacyjne [1]. Dodatkowo, wdrożenie systemu zarządzania bezpieczeństwem żywności opartego na HACCP jest kluczowe. Przynajmniej jeden członek zespołu powinien być przeszkolony na poziomie 4 w zasadach HACCP, aby zapewnić zgodność [2].
W przypadku potrzeb sprzętowych, zwróć się do
FAQ
Jakie są korzyści z certyfikacji pomieszczeń czystych dla produkcji mięsa hodowlanego?
Certyfikacja pomieszczeń czystych odgrywa kluczową rolę w produkcji mięsa hodowlanego, zapewniając zgodność z rygorystycznymi normami bezpieczeństwa i środowiskowymi. Certyfikowane pomieszczenia czyste są zaprojektowane w celu minimalizacji ryzyka zanieczyszczenia przez mikroby i cząstki, utrzymując sterylne warunki niezbędne do hodowli komórek. Chroni to nie tylko jakość i bezpieczeństwo końcowego produktu, ale także zapewnia zgodność z międzynarodowo uznawanymi standardami, takimi jak klasyfikacje ISO i klasy GMP - kluczowe wymagania dla zatwierdzenia regulacyjnego i akceptacji rynkowej.
Poza zgodnością, certyfikacja zwiększa niezawodność operacyjną poprzez walidację krytycznych systemów, takich jak przepływ powietrza, filtracja i monitorowanie środowiska. Systemy te współpracują w celu zmniejszenia ryzyka zanieczyszczenia, umożliwiając spójną produkcję i poprawiając ogólną wydajność procesu.Certyfikowany cleanroom również buduje zaufanie wśród interesariuszy, upraszcza inspekcje regulacyjne i wspiera działania związane ze skalowaniem, prezentując zgodność z najlepszymi praktykami w zarządzaniu kontrolowanymi środowiskami.
Jak często należy przeprowadzać rekwalifikację cleanroomów, aby zapewnić zgodność?
Cleanroomy muszą być regularnie rekwalifikowane, aby zapewnić, że spełniają standardy branżowe. Częstotliwość tego procesu zależy od kilku czynników, w tym klasyfikacji cleanroomu, jego użytkowania oraz wyników ocen ryzyka lub planów monitorowania środowiskowego.
Zazwyczaj rekwalifikacja odbywa się raz w roku. Jednak w środowiskach wysokiego ryzyka lub w sytuacjach związanych z istotnymi zmianami - takimi jak modernizacje sprzętu czy zmiany układu - mogą być wymagane częstsze kontrole. Ciągłe monitorowanie wydajności jest również kluczowe, aby zweryfikować, czy przepływ powietrza, filtracja i kontrola środowiskowa nadal spełniają wymagane standardy.
Jakie czynniki środowiskowe należy monitorować w pomieszczeniu czystym do produkcji mięsa hodowlanego?
Aby zapewnić zgodność i zmniejszyć ryzyko zanieczyszczenia w zakładach produkujących mięso hodowlane, kluczowe jest ścisłe monitorowanie kilku czynników środowiskowych. Należą do nich liczba cząstek, zanieczyszczenie mikrobiologiczne, wzorce przepływu powietrza, różnice ciśnienia powietrza, temperatura i poziomy wilgotności. Regularne monitorowanie tych elementów pomaga utrzymać standardy GMP i tworzy kontrolowane środowisko niezbędne do produkcji.
Poprzez staranne zarządzanie tymi warunkami, zakłady mogą chronić jakość produktu, jednocześnie spełniając surowe kryteria wymagane do certyfikacji pomieszczeń czystych.











