La technologie analytique des procédés (PAT) intègre la surveillance de la qualité en temps réel dans les processus de fabrication, améliorant ainsi la cohérence et réduisant les déchets. Elle est particulièrement utile dans la production de viande cultivée, où le contrôle précis de facteurs tels que le pH, l'oxygène et les nutriments est crucial. La PAT combine des capteurs en ligne, la chimiométrie et des systèmes automatisés pour garantir la qualité du produit tout en respectant les normes réglementaires.
Étapes clés pour mettre en œuvre la PAT :
- Identifier les paramètres critiques du procédé (CPP) : Concentrez-vous sur des facteurs tels que la température, l'oxygène dissous, le pH et le glucose.
- Choisir les outils de surveillance : Utilisez des capteurs en ligne (e.g., spectroscopie Raman) pour des données en temps réel.
- Intégrer les systèmes PAT : Connectez les capteurs aux bioréacteurs pour un contrôle automatisé en boucle fermée.
- Développer des modèles prédictifs : Utilisez l'analyse de données pour optimiser les processus.
- Assurer la conformité : Suivre les directives réglementaires GMP, ISO 17025 et autres.
Des plateformes comme
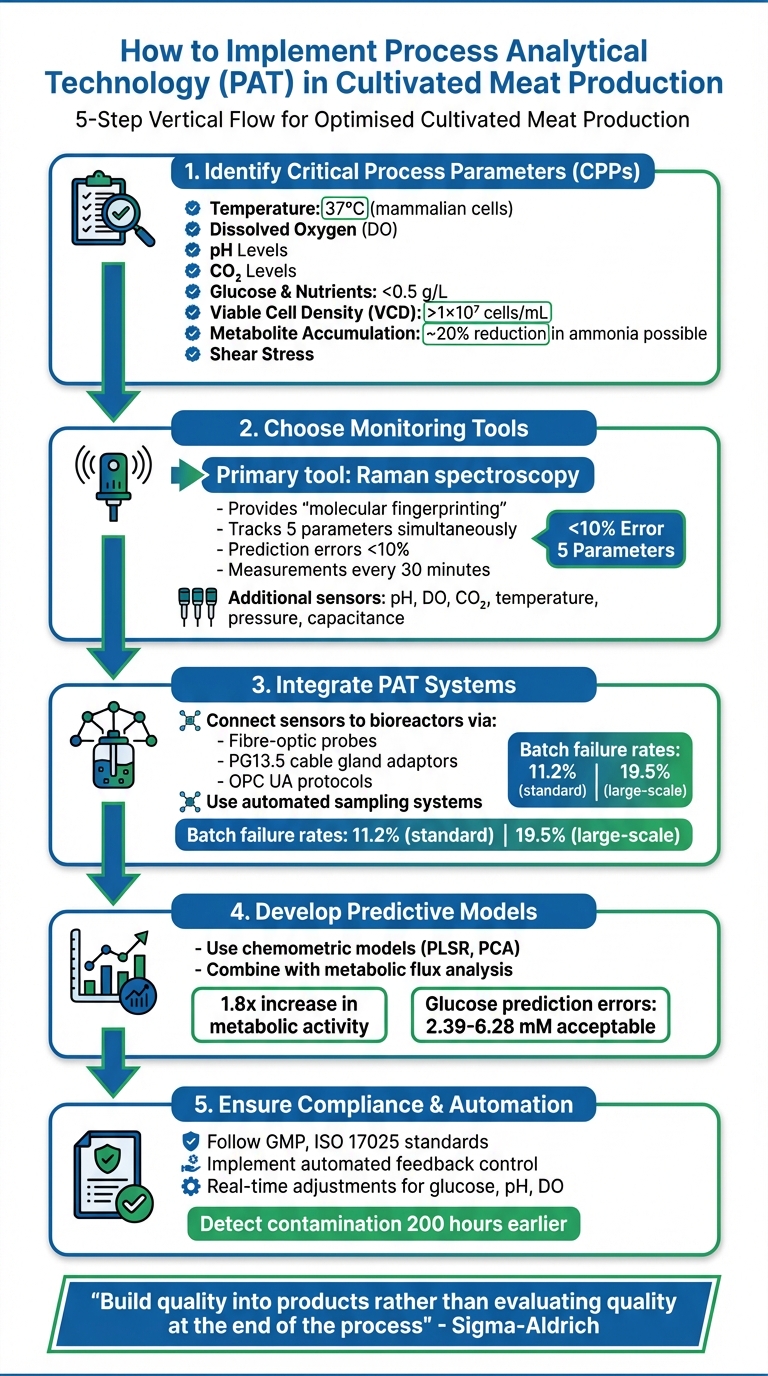
Processus en 5 étapes pour la mise en œuvre du PAT dans la production de viande cultivée
Discussion d'experts en biotraitement I - Mise en œuvre du PAT
Identification des paramètres critiques du processus (CPP)
Pour assurer le succès de la production de viande cultivée, il est essentiel d'identifier les paramètres critiques du processus (CPP) qui influencent la viabilité cellulaire, le rendement en biomasse et la qualité du produit. Une mauvaise gestion de ceux-ci peut compromettre l'ensemble des productions.
Paramètres Clés à Surveiller
La Température est un facteur clé. Les cellules de mammifères prospèrent à environ 37°C, tandis que les cellules de poissons et d'insectes nécessitent des environnements beaucoup plus frais pour maintenir une activité métabolique optimale [2].
L'Oxygène Dissous (OD) est un autre élément critique pour le métabolisme aérobie. À mesure que la production augmente, assurer un transfert d'oxygène suffisant devient plus difficile [2]. Sans assez d'oxygène, les cellules peuvent passer à un métabolisme anaérobie, entraînant une accumulation d'acide lactique, ce qui peut entraver la croissance.
Les Niveaux de pH sont une fenêtre sur l'état métabolique de la culture. Toute fluctuation peut perturber l'activité enzymatique, nuire à la santé des cellules et affecter les caractéristiques du produit, telles que la texture et la capacité de rétention d'eau [2][3].
Les niveaux de dioxyde de carbone (CO₂) doivent être soigneusement gérés, surtout dans les opérations à grande échelle. Les cellules animales sont particulièrement sensibles aux niveaux élevés de CO₂, ce qui rend la surveillance constante essentielle [2].
Le glucose et les nutriments sont les principales sources d'énergie pour les cellules. Si les niveaux de glucose chutent trop bas, les cellules peuvent mourir de faim, entraînant la mort ou une différenciation prématurée [2]. Maintenir des concentrations de glucose faibles (e.g., en dessous de 0,5 g/L) peut prévenir un métabolisme inefficace et réduire l'accumulation de lactate [4].
La densité cellulaire viable (VCD) aide à suivre les phases de croissance de la culture - latence, exponentielle et stationnaire - permettant de déterminer le meilleur moment pour la récolte [2]. Pour la viande cultivée, des densités cellulaires élevées sont souvent considérées comme étant supérieures à 1×10⁷ cellules/mL [2].
Accumulation de Métabolites - tels que l'ammoniac et l'acide lactique - peut entraver la croissance et réduire la viabilité cellulaire. Surveiller et contrôler ces sous-produits toxiques est crucial. Par exemple, une méthode a permis de réduire de 20 % les niveaux d'ammoniac toxique [2].
Stress de Cisaillement causé par les agitateurs ou les bulles de gaz pose un défi unique. Contrairement aux cellules microbiennes, les cellules animales n'ont pas de paroi cellulaire protectrice, ce qui les rend plus vulnérables aux dommages. Les niveaux de stress tolérables varient selon les espèces et doivent être ajustés pour chaque lignée cellulaire [2].
Ces paramètres fournissent la base pour optimiser la production de viande cultivée.
Paramètres Spécifiques à la Viande Cultivée
Bien que les facteurs ci-dessus s'appliquent largement, la production de viande cultivée introduit des défis uniques qui nécessitent une attention particulière.
Sensibilité au CO₂ est particulièrement importante.Les cellules animales utilisées dans la production alimentaire sont plus sensibles à l'inhibition par le CO₂ par rapport aux cellules microbiennes, ce qui en fait un paramètre critique à gérer [2].
La montée en échelle de la production apporte de nouvelles priorités. Dans la biopharmacie, les bioréacteurs atteignent généralement un maximum de 20 000 L pour les produits de haute valeur. Cependant, la viande cultivée nécessitera des volumes nettement plus importants pour rester économiquement viable. Pour mettre cela en perspective, le plus grand bioréacteur microbien jamais construit contient 1 500 000 L - une échelle que la production de viande cultivée pourrait un jour devoir atteindre [2].
La gestion thermique varie selon les espèces. Les cellules non mammifères nécessitent des systèmes de chauffage et de refroidissement entièrement différents, rendant le contrôle de la température très spécifique à chaque espèce [2]. Cette variabilité exige des systèmes de technologie analytique de procédé (PAT) flexibles.
Enfin, trouver le bon équipement de surveillance pour ces paramètres peut être délicat. Des plateformes comme
Maîtriser ces CPP est une étape nécessaire avant de mettre en œuvre des systèmes de contrôle en temps réel via des outils PAT.
Sélection et Intégration des Outils PAT
Une fois que vous avez identifié les paramètres critiques du processus, l'étape suivante consiste à sélectionner des capteurs qui correspondent à vos besoins - en particulier en termes de localisation des mesures et de rapidité de réponse. La surveillance en ligne se distingue ici. Étant donné que les capteurs restent dans le flux de processus, ils fournissent les informations en temps réel les plus rapides et les plus dynamiques par rapport aux méthodes en ligne ou hors ligne [6]. Pour des paramètres comme le pH ou l'oxygène dissous, qui nécessitent un retour immédiat, les capteurs en ligne éliminent les retards causés par l'échantillonnage.
Choisir des capteurs et des technologies
Un outil remarquable dans ce domaine est la spectroscopie Raman, un choix privilégié pour la production de viande cultivée. Sa capacité à fournir un "empreinte moléculaire" le rend particulièrement efficace pour identifier des molécules organiques comme le glucose et le lactate, tout en étant insensible à l'eau [6][7]. Une étude menée par Merck/Sigma-Aldrich en janvier 2026 a mis en évidence l'efficacité de l'analyseur Raman ProCellics™ et du logiciel Bio4C® PAT Raman. Ce système a surveillé une culture de cellules CHO dans un bioréacteur à double enveloppe de 3L, prenant des mesures toutes les 30 minutes. Notamment, il a suivi cinq paramètres simultanément et a distingué avec précision entre les densités cellulaires totales et viables lors d'un événement de dilution cellulaire le sixième jour, avec une marge d'erreur inférieure à 10% [11].
"La spectroscopie Raman est devenue un choix privilégié pour le PAT dans la surveillance et le contrôle des bioprocédés en amont car elle facilite le contrôle avancé des procédés et permet une qualité de procédé constante." - Karen A Esmonde-White, Endress+Hauser [8]
La spectroscopie Raman n'est pas seulement précise ; elle prédit les niveaux de métabolites clés avec des erreurs inférieures à 10% [7][11]. Mais Raman seul ne suffit pas. Vous aurez également besoin de capteurs standard de bioréacteur pour le pH, l'oxygène dissous, le CO₂, la température, la pression et la capacitance [10][6]. Pour rationaliser les opérations et réduire les risques de contamination - surtout puisque les taux d'échec des lots dans la production de viande cultivée tournent autour de 11,2%, atteignant 19,5% dans les installations à plus grande échelle - les systèmes d'échantillonnage automatisés sont indispensables [5].
Lors de la sélection des capteurs, assurez-vous qu'ils sont compatibles avec l'Analyse de Données Multivariées (MVDA) et le Plan d'Expériences (DOE) logiciel [1]. Cette compatibilité garantit que les outils peuvent évoluer des petits bioréacteurs de R&D à la production commerciale à grande échelle [1].
Intégration des Outils PAT dans les Systèmes de Bioréacteurs
Les systèmes de bioréacteurs modernes simplifient l'intégration des outils PAT. Les mesures non destructives et en ligne sont rendues possibles grâce à l'utilisation de sondes à fibre optique, qui sont montées via des adaptateurs de presse-étoupe standard PG13.5. Ces sondes se connectent parfaitement aux systèmes de bioréacteurs via les protocoles OPC UA [8][9][11][1].
Du côté des données, des plateformes comme Bio4C® PAT Raman Software ou BioPAT® MFCS transforment les données des capteurs en informations exploitables pour un contrôle en temps réel [10][11]. Ces systèmes utilisent des outils avancés comme l'Analyse en Composantes Principales (PCA) et les Moindres Carrés Partiels (PLS) pour convertir des données spectrales complexes en paramètres de processus significatifs [9].
"L'application de la technologie Raman... permet une compréhension et un contrôle complets des processus dans la fabrication biopharmaceutique, permettant aux utilisateurs de prendre les bonnes décisions en toute confiance." - Merck/Sigma-Aldrich [11]
Lors de la construction de modèles Raman, des techniques telles que l'ajout d'analytes - où des concentrations connues d'analytes sont ajoutées - aident à rompre les corrélations entre les composés, garantissant que le modèle ne repose pas sur des tendances indirectes [1]. L'incorporation d'une large gamme de conditions de processus en utilisant le DOE garantit que les modèles sont suffisamment robustes pour gérer les variations à l'échelle commerciale [1].
Une fois les défis d'intégration relevés, la prochaine tâche consiste à trouver le bon équipement PAT.
Approvisionnement en Équipement PAT pour la Viande Cultivée
Trouver les bons outils pour la surveillance en temps réel dans la production de viande cultivée peut être délicat. Heureusement, des plateformes comme
Étant donné que les milieux de culture représentent souvent plus de 50 % des coûts de production [5], se procurer un équipement de surveillance efficace pour optimiser l'utilisation des nutriments n'est pas seulement pratique mais économiquement judicieux.
sbb-itb-ffee270
Construction de modèles prédictifs pour l'optimisation des processus
Une fois que vous avez déployé les outils PAT, l'étape suivante consiste à utiliser des modèles prédictifs pour estimer des variables difficiles à mesurer directement, telles que la viabilité cellulaire et les niveaux de métabolites [12]. En analysant les données spectrales, vous pouvez obtenir un contrôle de processus plus rapide et plus intelligent. Le défi réside dans la transformation de ces données en modèles prédictifs fiables.
Développement de modèles chimiométriques
La régression des moindres carrés partiels (PLSR) est un excellent point de départ pour traiter les signaux superposés et bruyants souvent rencontrés dans la production de viande cultivée [7][13]. Pour affiner les spectres Raman, qui peuvent inclure 1 000 à 3 000 variables par mesure [7], prétraitez les données en utilisant des calculs de dérivées. Cela aide à réduire le bruit tout en préservant les pics critiques. Cependant, faites attention à ne pas trop lisser les données, car cela pourrait effacer les signaux mêmes dont votre modèle dépend.
La sélection des variables est tout aussi importante. L'analyse en composantes principales (ACP) peut aider à identifier quelles régions spectrales sont le plus fortement liées à votre paramètre cible. Par exemple, une étude de 2018 a révélé que la huitième composante principale (PC8) était fortement corrélée avec la concentration de glucose. Les chercheurs ont utilisé cette information pour affiner leur modèle PLSR [7]. Cette approche ciblée réduit le risque de surapprentissage et garantit que le modèle se concentre sur des données significatives.
Pour la production de viande cultivée, combiner des modèles basés sur les données avec des modèles mécanistes, comme l'analyse de bilan de flux (FBA), peut être particulièrement efficace. En 2023, Oxford Biomedica a utilisé un système PAT basé sur la réfractométrie (le système Ranger) pour surveiller les cultures de cellules HEK293T.En intégrant des données en temps réel avec l'analyse des flux métaboliques, ils ont découvert comment le pH influençait directement les niveaux d'oxygène intracellulaire et l'activité métabolique. Cette stratégie hybride a conduit au développement d'un plan d'exploitation du pH qui a augmenté l'activité métabolique de 1,8 fois par rapport aux processus non optimisés [12][14].
Une fois votre modèle construit, l'étape suivante consiste à s'assurer qu'il fonctionne avec précision et fiabilité dans des conditions d'exploitation réelles.
Validation des modèles pour une utilisation en production
Le véritable test d'un modèle réside dans sa validation. Commencez par l'évaluer par rapport à un jeu de données indépendant - des données qui ne faisaient pas partie de la phase d'entraînement. Utilisez des métriques comme l'erreur quadratique moyenne de prédiction (RMSEP) pour évaluer sa précision. Pour la surveillance du glucose dans les processus de viande cultivée, les erreurs de prédiction allant de 2,39 mM à 6.28 mM sont généralement acceptables pour le contrôle automatisé en temps réel [7].
La scalabilité est un autre facteur clé. Votre modèle doit fournir des résultats cohérents, qu'il soit appliqué dans un petit bioréacteur de R&D ou dans un grand système commercial. Une étude de 2018 a montré qu'un modèle PLSR a maintenu sa précision prédictive lorsqu'il a été étendu d'un système de 10 L à un système de 100 L [7].
Enfin, testez le modèle dans des conditions dynamiques en utilisant le "parameter probing". Cela implique de modifier des variables comme le pH ou l'oxygène dissous pour vérifier si le modèle suit les changements avec précision [14]. Oxford Biomedica a utilisé cette méthode pour valider un système de contrôle autonome du pH [12]. Après cela, effectuez des tests en boucle fermée pour confirmer que le système PAT peut maintenir les paramètres dans la plage souhaitée [14].
Mise en œuvre du contrôle de processus en temps réel
Le contrôle de processus en temps réel va au-delà des modèles prédictifs en utilisant des données continues pour maintenir des performances optimales. En convertissant les données des capteurs en direct en ajustements automatisés, ces systèmes garantissent que des conditions clés telles que les niveaux de nutriments, le pH et l'oxygène dissous sont constamment régulées - sans nécessiter d'intervention manuelle. Cela réduit non seulement les coûts de main-d'œuvre et les erreurs humaines, mais garantit également une qualité de produit plus constante. Pour la production de viande cultivée, une telle automatisation est révolutionnaire pour atteindre l'optimisation des processus en temps réel.
Pour que cela fonctionne, il est crucial de mesurer directement les paramètres critiques du processus (CPP) et d'alimenter ces signaux dans votre système de contrôle.Dan Kopec, un expert PAT chez Sartorius Stedim Biotech, souligne l'importance de cette approche :
La meilleure façon de contrôler un paramètre de procédé critique (CPP) est de mesurer ce paramètre spécifique, d'intégrer le signal en direct dans votre système de contrôle et d'appliquer un algorithme de rétroaction intelligent pour une boucle de contrôle automatisée.[4]
Ces boucles de rétroaction comparent les lectures des capteurs en temps réel aux points de consigne prédéfinis. En utilisant des algorithmes PID, elles ajustent automatiquement des paramètres critiques comme l'alimentation en nutriments, le pH et l'oxygène dissous pour que tout fonctionne sans accroc.
Par exemple, dans la production de viande cultivée, les capteurs in situ fournissent des mesures quasi-instantanées. Les capteurs de capacité, par exemple, peuvent suivre le volume cellulaire viable en traitant les cellules comme des microcondensateurs dans un champ de radiofréquence. Ces données peuvent ensuite déclencher des contrôles automatisés de saignement cellulaire dans les processus de perfusion continue, aidant à maintenir une densité cellulaire stable.[4]
Configuration des systèmes de contrôle en boucle fermée
Dans la production de viande cultivée, des paramètres tels que le glucose, le pH et l'oxygène dissous influencent directement la croissance cellulaire et l'efficacité métabolique. Maintenir des niveaux de glucose bas (environ 0,1–0,5 g/L) est particulièrement important pour éviter l'accumulation de lactate.[4] Pour y remédier, Sartorius Stedim Biotech a développé le système BioPAT Trace. Cette technologie utilise des biocapteurs enzymatiques et une sonde de dialyse avec une membrane de 10 kDa pour fournir des mesures de glucose aussi fréquemment qu'une fois par minute - sans perte de volume. Cela garantit une haute densité cellulaire dans les bioréacteurs de perfusion.[4]
L'automatisation du contrôle du pH peut également conduire à des améliorations significatives.Dans une étude, des chercheurs d'Oxford Biomedica et de WattBE Innovations ont utilisé le système PAT Ranger Refractive Index (RI) pour surveiller les cultures cellulaires HEK293T. En développant un 'Indice de Taux Métabolique' (MRI) et en ajustant les points de consigne de pH, ils ont obtenu une augmentation de 1,8 fois de l'activité métabolique. Cette technique, souvent appelée "sondage de paramètres", implique de modifier des variables pour observer les réponses du système et affiner les conditions opérationnelles.[12]
Pour améliorer encore la fiabilité, des capteurs virtuels peuvent servir de secours aux capteurs matériels. Par exemple, un capteur virtuel basé sur des lectures de capacitance pourrait vérifier les données de glucose d'une sonde Raman. Cette redondance aide à détecter la dérive ou la défaillance des capteurs avant qu'elle ne perturbe le processus - une protection particulièrement utile face à une grande variabilité des processus.
Exemples d'automatisation en temps réel dans la viande cultivée
Les stratégies de contrôle en temps réel ont déjà donné des résultats impressionnants dans diverses applications. Par exemple, Sartorius Stedim Biotech a collaboré avec le Centre de Recherche Médicale de GSK pour utiliser la plateforme BioPAT pour l'alimentation automatisée en boucle fermée dans les cultures de cellules CHO. Cela a éliminé l'échantillonnage manuel et assuré un approvisionnement constant en nutriments.[4]
Dans un autre exemple, Oxford Biomedica a intégré le système Ranger RI avec l'analyse du flux métabolique pour créer une stratégie autonome de contrôle du pH. Ce système s'est adapté à l'état métabolique des cellules et a détecté la contamination microbienne jusqu'à 200 heures plus tôt que les méthodes traditionnelles, démontrant le potentiel de la surveillance en temps réel pour prévenir les échecs de lots coûteux.[12]
Les plateformes comme
Comme le résume bien Kopec :
L'automatisation et la surveillance en temps réel devraient améliorer les processus avec des gains de qualité et de rendement ainsi que des réductions des coûts de main-d'œuvre, des risques et des déchets. [4]
Pour commencer, concentrez-vous sur les paramètres les plus critiques - généralement le glucose, le pH et l'oxygène dissous - et élargissez progressivement l'automatisation à mesure que vous acquérez une compréhension plus approfondie de votre processus. Cette approche étape par étape est essentielle pour optimiser la production de viande cultivée grâce au contrôle en temps réel.
Conclusion : Étapes pour la mise en œuvre du PAT
Intégrer la technologie analytique des procédés (PAT) dans la production de viande cultivée nécessite une approche claire et méthodique.Commencez par identifier vos Paramètres Critiques de Procédé (CPPs) - ceux-ci peuvent inclure les niveaux de glucose, le pH et l'oxygène dissous, qui ont tous une influence directe sur la qualité du produit. Une fois ceux-ci définis, choisissez des outils PAT comme la spectroscopie Raman ou les capteurs de capacitance pour permettre une surveillance en temps réel.
L'étape suivante consiste à intégrer ces capteurs dans vos systèmes de bioréacteurs et à créer des modèles prédictifs pour interpréter les données collectées. Priorisez la surveillance en ligne chaque fois que possible, car cela élimine les retards et réduit le risque de contamination pendant le processus.
Les systèmes de rétroaction automatisés jouent un rôle crucial ici, en convertissant les données brutes en ajustements immédiats et exploitables. Comme le dit si bien Sigma-Aldrich:
Un objectif clé du PAT est d'intégrer la qualité dans les produits plutôt que d'évaluer la qualité à la fin du processus.[6]
Cette approche proactive réduit non seulement les coûts de main-d'œuvre, mais garantit également une qualité de produit constante tout en réduisant le gaspillage.
Une fois que les systèmes de rétroaction automatisés sont opérationnels, l'accent devrait être mis sur l'approvisionnement en équipements PAT appropriés. Un équipement fiable est essentiel pour le succès, et des plateformes comme
Au fur et à mesure que votre compréhension du processus s'approfondit, étendez progressivement l'automatisation pour atteindre une production évolutive et cohérente tout en respectant les normes réglementaires.En suivant ces étapes, la mise en œuvre de PAT peut devenir l'épine dorsale d'un processus de production de viande cultivée plus efficace et fiable.
FAQ
Quels sont les avantages de l'utilisation de la Technologie Analytique de Procédé (PAT) dans la production de viande cultivée ?
La Technologie Analytique de Procédé (PAT) joue un rôle clé dans l'amélioration du contrôle des processus et de la cohérence des produits dans la production de viande cultivée. Avec la surveillance en temps réel de facteurs cruciaux comme la température, les niveaux de pH et l'oxygène dissous, PAT assure des conditions de croissance optimales pour les cellules tout en minimisant les risques de problèmes de processus inattendus. Le résultat ? Des rendements plus élevés, une qualité constante et des coûts de production réduits.
Un autre avantage de PAT est son soutien à un cadre Qualité par la Conception (QbD).En connectant directement les données analytiques aux caractéristiques de qualité spécifiques du produit, cela réduit la dépendance aux méthodes traditionnelles de test de point final. Cette approche accélère non seulement les processus de validation mais permet également des décisions basées sur les données qui améliorent la reproductibilité et permettent des stratégies de contrôle prédictif.
Pour les entreprises dans le domaine de la viande cultivée, des plateformes telles que
Comment la spectroscopie Raman améliore-t-elle la surveillance en temps réel dans les systèmes PAT pour la production de viande cultivée ?
La spectroscopie Raman joue un rôle crucial dans la surveillance en temps réel au sein des systèmes PAT (Technologie Analytique de Procédé) en fournissant des mesures rapides, non invasives et en ligne des paramètres clés du processus.Cela aide à maintenir un contrôle de processus plus strict et garantit une qualité de produit constante tout au long.
Une de ses caractéristiques remarquables est la capacité à détecter plusieurs molécules simultanément. Par exemple, il peut surveiller les niveaux de glucose, de lactate et d'ammonium tout en évaluant la viabilité cellulaire et les caractéristiques du produit - le tout en une seule mesure. Les sondes Raman modernes sont conçues pour être installées directement dans les flux de bioréacteurs, permettant une collecte continue de données sans avoir besoin d'extraire des échantillons.
Un autre avantage est son support pour le contrôle automatisé en boucle fermée. En fournissant des données en temps réel, la spectroscopie Raman permet des ajustements précis des apports nutritifs, garantissant des conditions de production optimales. Sa flexibilité dans le dimensionnement et le transfert de modèles à travers différentes tailles de réacteurs améliore encore son utilité dans la production de viande cultivée, augmentant l'efficacité et minimisant le risque d'erreurs.
Quels sont les principaux défis de l'extension de la Technologie Analytique de Procédé (PAT) pour la production de viande cultivée ?
L'extension de la PAT (Technologie Analytique de Procédé) pour la production de viande cultivée à grande échelle comporte son lot de défis, nécessitant une planification et une exécution minutieuses. Un problème clé réside dans la gestion et l'intégration des volumes énormes de données générés par les instruments PAT. À mesure que la production s'intensifie, maintenir l'exactitude des données tout en assurant une intégration fluide dans les systèmes de contrôle devient une tâche plus complexe.
Un autre obstacle important est la performance des capteurs dans les bioréacteurs à l'échelle industrielle. Les capteurs qui fonctionnent bien dans des installations plus petites rencontrent souvent des défis dans des systèmes plus grands, où des facteurs comme les forces de cisaillement et les variations de température peuvent compromettre la précision des mesures en temps réel.
Il y a aussi la question de l'acquisition d'équipements spécialisés adaptés aux exigences uniques de la production de viande cultivée. Des plateformes telles que
Aborder ces défis tôt - en sélectionnant des capteurs fiables, en construisant des systèmes de données évolutifs et en planifiant l'approvisionnement de manière stratégique - peut aider les entreprises à naviguer plus efficacement vers une production à l'échelle commerciale.











