Maintenir des niveaux de pH précis est crucial pour la production de viande cultivée. Les cellules de mammifères prospèrent dans une plage de pH étroite (7,1–7,4), mais l'acidification métabolique, l'accumulation de CO₂ et les défis de mélange rendent le contrôle du pH complexe, surtout dans les bioréacteurs à grande échelle. Les stratégies efficaces incluent :
- Barbotage de gaz: Élimine l'excès de CO₂ sans augmenter l'osmolalité ou provoquer des pics de pH localisés.
- Capteurs avancés: Les capteurs potentiométriques offrent une grande précision pour les systèmes en acier inoxydable, tandis que les capteurs optiques fonctionnent bien avec les bioréacteurs à usage unique.
- Optimisation des tampons: L'ajout de tampons comme HEPES améliore la stabilité mais nécessite un équilibre soigneux pour éviter une production excessive de lactate.
- Systèmes automatisés: Les ajustements en temps réel utilisant des boucles de rétroaction assurent des niveaux de pH constants.
Ces approches aident à surmonter des défis tels que l'accumulation d'acide lactique et le stress de cisaillement, améliorant ainsi la santé cellulaire et les rendements de production.
Comprendre les mesures de pH dans le bioprocédé
Principaux défis de la gestion du pH
Cette section explore les principaux facteurs qui contribuent à l'instabilité du pH, en s'appuyant sur les défis précédemment discutés.
Acidification métabolique et accumulation d'acide lactique
L'acide lactique est un obstacle majeur dans le bioprocédé de viande cultivée. Lorsque les cellules métabolisent le glucose par glycolyse, elles produisent du lactate et des ions hydrogène dans un rapport de 1:1. Ce processus crée une charge acide significative, faisant du lactate le principal moteur de l'acidification du milieu [1].
La capacité tampon des milieux de culture standard - généralement entre 1,1 et 1,6 mM par unité de pH [1] - est souvent insuffisante pendant les périodes de croissance cellulaire rapide.Alors que les cellules se multiplient, leur production de déchets métaboliques augmente, submergeant la capacité du milieu à maintenir un pH stable. La chute brutale du pH pendant cette phase peut être directement attribuée à la production d'acide lactique glycolytique [1], soulignant le rôle crucial du lactate dans la déstabilisation du pH du milieu.
Les complications ne s'arrêtent pas là. L'accumulation de CO2 ajoute une autre couche de complexité.
Accumulation de CO2 et dérive du pH
La respiration cellulaire introduit du CO2 dans le milieu, où il se dissout pour former de l'acide carbonique. Le problème clé est la pression partielle du CO2 dissous (pCO2), qui influence la capacité du CO2 à s'échapper des cellules. Lorsque les niveaux de pCO2 dans le milieu augmentent trop, le CO2 devient piégé à l'intérieur des cellules, provoquant une chute dangereuse du pH intracellulaire et conduisant finalement à la mort cellulaire [2].
"Si la pCO2 est trop élevée, le CO2 ne peut pas quitter les cellules, donc le pH intracellulaire va chuter et les cellules mourront." - Alicat Scientific [2]
Ce problème devient plus prononcé dans les bioréacteurs à grande échelle. Ces systèmes ont un rapport surface/volume plus faible, ce qui réduit l'efficacité du dégazage du CO2 par rapport aux petits récipients [3]. Même les opérations de routine, comme le transfert de milieu dans un incubateur à CO2, peuvent provoquer des fluctuations de pH. Par exemple, de petits volumes de milieu commencent à s'alcaliniser presque immédiatement, avec une constante de temps de 2 à 3 heures [1].
En plus des défis chimiques, les processus physiques jouent également un rôle important dans l'instabilité du pH.
Impacts du mélange et du stress de cisaillement sur la stabilité du pH
Ajuster le pH en ajoutant une base introduit ses propres risques.Lorsque le bicarbonate de sodium ou des bases similaires sont pompés dans des bioréacteurs, un mauvais mélange peut créer des zones localisées de pH élevé qui nuisent aux cellules voisines [2] [3]. D'autre part, l'agitation vigoureuse nécessaire pour distribuer uniformément la base peut entraîner un stress de cisaillement et la formation de mousse, qui sont tous deux nuisibles aux cellules de mammifères fragiles [2] [3].
Dans des expériences contrôlées, l'ajout de base pour stabiliser le pH a souvent réduit la viabilité cellulaire en raison de l'augmentation de l'osmolalité [3]. Cela crée un équilibre difficile à atteindre : un mélange insuffisant entraîne des points chauds de pH, tandis qu'un mélange excessif empêche les points chauds mais augmente le stress mécanique. Le problème devient encore plus complexe lors de l'augmentation d'échelle, où des temps de mélange plus longs rendent plus difficile le maintien d'un contrôle efficace du pH sans compromettre la santé des cellules.
Technologies pour la Surveillance et le Contrôle du pH
Maintenir le pH dans la plage étroite de 7,1 à 7,4 est crucial pour les cultures de cellules de mammifères, nécessitant des outils de surveillance précis et fiables [2]. Les capteurs potentiométriques, qui agissent comme des électrodes pour mesurer les ions hydrogène libres, sont la norme pour la surveillance continue du pH dans les bioréacteurs [1]. Ces capteurs fournissent des données en temps réel, permettant aux systèmes automatisés de faire des ajustements immédiats pour maintenir les niveaux de pH requis. Leur haute précision les rend essentiels pour les opérations à grande échelle. Parallèlement, les indicateurs optiques offrent un autre moyen efficace de mesurer le pH.
Les indicateurs optiques reposent sur l'analyse spectroscopique pour fournir des mesures quantitatives du pH.Bien que le rouge de phénol soit souvent utilisé comme indicateur visuel, des lectures plus précises sont obtenues grâce à l'analyse ratiométrique de l'absorbance à deux longueurs d'onde spécifiques - 560 nm et 430 nm [1] . Cette méthode compense des facteurs tels que le volume du milieu ou la concentration de colorant, garantissant des résultats cohérents et précis.
"La concentration des ions H+ libres n'est pas intuitive à prédire, mais heureusement simple à mesurer (e.g. avec des électrodes ou des colorants indicateurs)." - Johanna Michl et al., Université d'Oxford [1]
Les systèmes modernes de contrôle du pH vont au-delà de la surveillance en intégrant ces mesures dans des boucles de rétroaction automatisées qui régulent dynamiquement les niveaux de pH.
Les systèmes de rétroaction automatisés exploitent les données des capteurs pour effectuer des ajustements en temps réel, éliminant ainsi le besoin d'intervention manuelle. Ces systèmes peuvent ajuster le pH en ajoutant une base ou en utilisant des techniques de barbotage de gaz [2].Pour les bioréacteurs à grande échelle, le barbotage de gaz est particulièrement efficace. En utilisant des régulateurs de débit massique, les niveaux de CO2 peuvent être ajustés rapidement et uniformément, assurant une régulation uniforme du pH [2]. En revanche, le pompage de base, bien qu'efficace pour les systèmes plus petits, peut créer des déséquilibres de pH localisés et augmenter l'osmolalité, le rendant moins pratique pour les récipients plus grands [2]. Cependant, le barbotage de gaz nécessite une attention particulière à la conception des barbotteurs pour éviter le stress de cisaillement qui pourrait nuire aux cellules [2]. Pour ceux dans la production de viande cultivée, investir dans des systèmes de contrôle avancés des gaz peut conduire à une meilleure santé cellulaire et à des rendements plus élevés, en faisant une dépense qui en vaut la peine.
sbb-itb-ffee270
Stratégies pour la gestion du pH à grande échelle
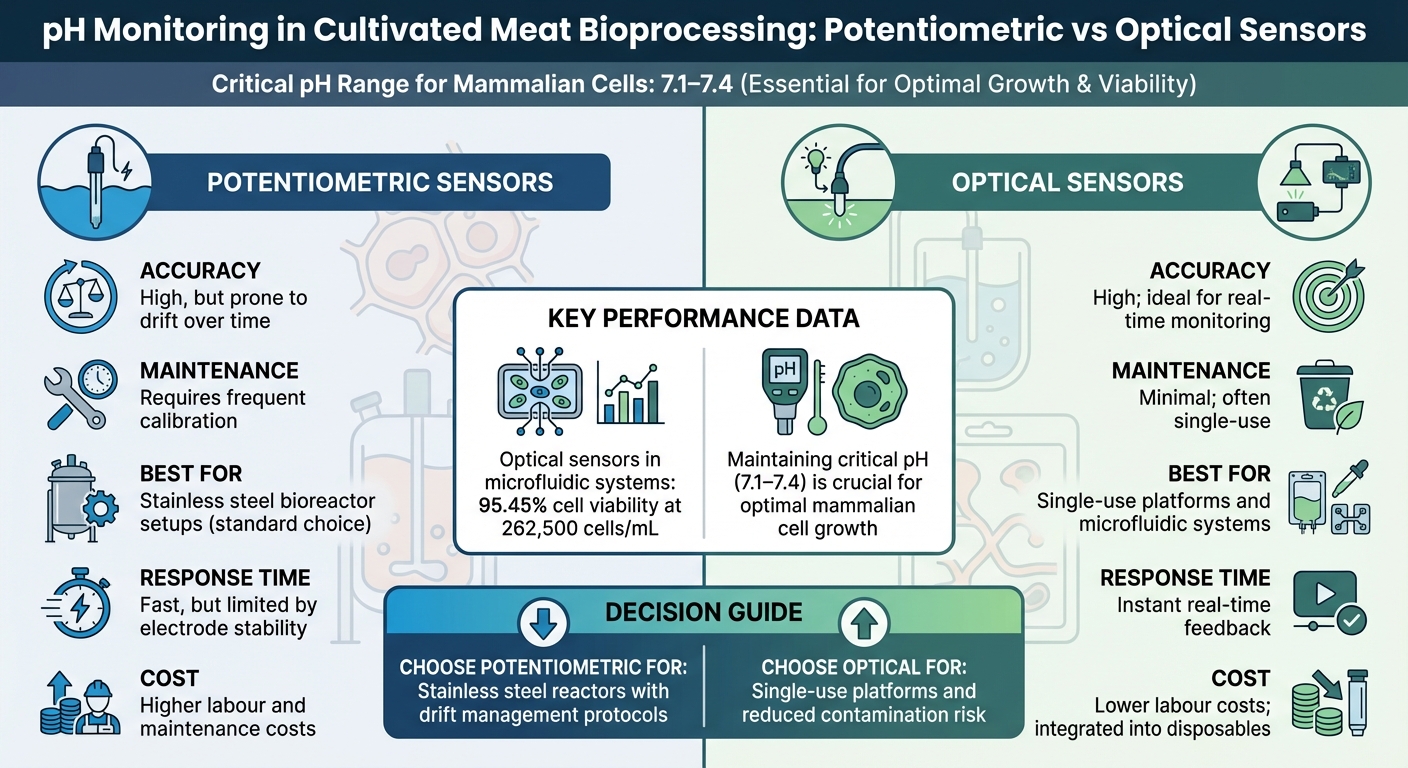
Capteurs de pH potentiométriques vs optiques pour les bioréacteurs de viande cultivée
Capteurs potentiométriques vs optiques : une comparaison
Choisir la bonne technologie de capteur devient de plus en plus important à mesure que la production de viande cultivée s'intensifie. Les capteurs potentiométriques sont le choix privilégié pour les bioréacteurs en acier inoxydable en raison de leur précision et de leur réponse rapide. Cependant, ils présentent des défis tels que la nécessité d'un étalonnage régulier et une susceptibilité à la dérive lors de processus prolongés. Jacob Crowe, Responsable du support technique des applications chez
"Au fil du temps, les mesures de pH peuvent dériver, ce qui affectera la stabilité et la performance du processus.Il est essentiel de surveiller et d'atténuer la dérive du pH pour prévenir les effets néfastes sur le métabolisme et le processus global [8].
D'autre part, les capteurs optiques apparaissent comme une option pratique, en particulier pour les systèmes de bioréacteurs à usage unique. Ces capteurs peuvent être préinstallés dans des sacs jetables, réduisant ainsi les risques de contamination et éliminant le besoin de stérilisation entre les cycles [7]. Dans les systèmes microfluidiques, les capteurs optiques ont montré d'excellents résultats, atteignant des viabilités cellulaires de 95,45 % à des densités de 262 500 cellules/mL [9].
| Caractéristique | Capteurs Potentiométriques | Capteurs Optiques |
|---|---|---|
| Précision | Élevée, mais sujette à la dérive | Élevée; idéale pour la surveillance en temps réel |
| Entretien | Nécessite un étalonnage fréquent | Minime; souvent à usage unique |
| Évolutivité | Standard pour les installations en acier inoxydable | Idéal pour l'usage unique et la microfluidique |
| Temps de Réponse | Rapide, limité par la stabilité de l'électrode | Retour d'information instantané en temps réel |
| Implications de Coût | Coûts de main-d'œuvre et d'entretien plus élevés | Main-d'œuvre réduite; intégré dans les produits jetables |
Le choix du capteur dépend en grande partie du type de réacteur.Les bioréacteurs en acier inoxydable peuvent bénéficier de capteurs potentiométriques avec des mesures pour gérer la dérive, tandis que les plateformes à usage unique peuvent tirer parti de la facilité des capteurs optiques intégrés [7] [8]. Ces décisions affectent directement la manière dont la stabilité du pH est maintenue lors de l'optimisation du milieu.
Optimisation du Milieu et Améliorations des Tampons
Une fois les capteurs appropriés en place, stabiliser le système tampon du milieu de culture devient essentiel pour maintenir le contrôle du pH lors de la montée en échelle. Les cellules de mammifères dépendent du système tampon CO₂/HCO₃⁻ (pKa 6,15 à 37°C), mais sa capacité tampon est souvent insuffisante. Par exemple, le DMEM standard avec 10% de FBS fournit généralement seulement 1,1 à 1,6 mM de capacité tampon [1].
Pour remédier à cela, l'ajout de tampons non volatils (NVB) comme le HEPES (pKa 7.3 à 37°C) peuvent renforcer considérablement le tamponnement sans provoquer de décalages osmolaires problématiques [1]. La méthode recommandée consiste à titrer d'abord le milieu jusqu'au pH cible, puis à ajouter du NaHCO₃ à une concentration alignée avec le pCO₂ de l'incubateur. Cette approche réduit la dérive initiale du pH lorsque le milieu frais est exposé au CO₂, un processus qui peut prendre jusqu'à deux heures avec les NVB [1].
Cependant, des systèmes de tamponnement plus forts peuvent déclencher une glycolyse accrue, entraînant une production plus élevée de lactate. Dans certaines lignées cellulaires, jusqu'à 90 % du glucose est directement converti en lactate [1], et une amélioration du tamponnement peut parfois amplifier cet effet, entraînant une accumulation accrue d'acide lactique [10].
Techniques de Barbotage et d'Agitation
Le barbotage de gaz offre un moyen pratique de gérer le pH dans la production de viande cultivée à grande échelle.Alicat Scientific notes:
"Les bulles de gaz des spargers peuvent être mélangées et distribuées plus rapidement que la base, et avec beaucoup moins d'agitation" [2].
En distribuant uniformément les bulles de gaz, le sparging offre une approche plus cohérente que les ajouts de base chimique. Par exemple, une étude de 2018 a montré que le maintien de taux de sparging constants tout en augmentant l'aération de l'espace libre permettait aux titres de rester stables lors du passage de 30 L à 250 L [2].
Les macro spargers, qui produisent des bulles de 1 à 4 mm de diamètre, sont particulièrement efficaces pour éliminer l'excès de CO₂ de la culture. Cela augmente naturellement le pH, évitant ainsi le besoin de bases chimiques qui pourraient élever l'osmolalité [2] [5]. Une nouvelle stratégie de contrôle du pH "uniquement par gaz" utilise des boucles de rétroaction automatisées de sparging d'air.Lorsque le pH diminue, le flux d'air augmente pour éliminer davantage de CO₂. Cette méthode a été mise à l'échelle avec succès des bioréacteurs ambr®250 à des cuves de 200 L, maintenant des niveaux de pH précis tout au long des cultures en fed-batch [6] .
Équilibrer un transfert de gaz efficace avec un stress de cisaillement minimal reste un défi critique lors de la mise à l'échelle. Les bioréacteurs à circulation par airlift, qui utilisent une circulation entraînée par le gaz, offrent une option de mélange plus douce avec un stress de cisaillement réduit. Les simulations de dynamique des fluides computationnelle (CFD) peuvent également aider à identifier les zones de cisaillement élevé près des pales de l'agitateur, permettant d'optimiser les conceptions de bioréacteurs avant la mise à l'échelle [4]. Combiner ces approches avec des outils avancés de
Approvisionnement en équipements de contrôle du pH via Cellbase
Pourquoi choisir Cellbase pour l'approvisionnement ?
Un contrôle précis du pH est essentiel dans le biotraitement de la viande cultivée, ce qui rend crucial l'approvisionnement en équipements adéquats. Les plateformes générales de fournitures de laboratoire manquent souvent des connaissances spécialisées requises pour les plages de pH étroites dans ce domaine.
En utilisant
Recherche de technologies de contrôle du pH grâce à Cellbase
Pour le passage à l'échelle, la plateforme offre un accès à des contrôleurs de débit massique et à des spargeurs spécialisés, qui sont essentiels pour une gestion efficace du pH à base de gaz. Comme le souligne Alicat Scientific :
"Maintenir le pH à des niveaux biologiques sains est potentiellement l'outil le plus puissant dans le traitement en amont pour augmenter les titres de produit" [2].
De plus,
Les spécialistes des achats peuvent également se procurer des équipements pour le dépouillement du CO₂, y compris des capteurs de CO₂ autoclavables et des sondes de pH à usage unique. Ces outils soutiennent des stratégies évolutives pour maintenir un contrôle précis du pH, facilitant l'intégration de la gestion avancée du pH dans la production à grande échelle [11]. En offrant des solutions ciblées,
Conclusion : Meilleures pratiques pour le contrôle du pH dans le biotraitement de la viande cultivée
Maintenir une plage de pH de 7,1 à 7,4 est crucial pour la survie des cellules mammifères dans la production de viande cultivée [2] . Garder le pH dans cette plage joue un rôle clé dans l'amélioration des rendements de production lors du biotraitement en amont.
Pour relever les défis du contrôle du pH, plusieurs pratiques efficaces ont émergé. Une méthode remarquable est l'utilisation de l'insufflation de gaz au lieu de l'ajout de base lors de la montée en échelle. L'insufflation de gaz élimine efficacement l'excès de CO₂ en le distribuant uniformément avec une agitation minimale, ce qui aide à éviter des problèmes tels que les incohérences de pH et les fluctuations d'osmolalité [2]. Une étude de 2021 par Aryogen Pharmed a démontré le succès de cette méthode à une échelle de 250 litres, réalisant une augmentation de 51 % du rendement final du produit [3].
Une autre pratique importante est la surveillance directe du pH , qui offre une compréhension plus complète de la santé de la culture par rapport à la simple mesure du pCO₂.Ceci est particulièrement vital car les niveaux de CO₂ dissous ne tiennent pas compte de l'accumulation d'acide lactique, qui peut représenter jusqu'à 90 % du métabolisme du glucose dans certaines lignées cellulaires [1]. La surveillance directe du pH devient encore plus cruciale pendant la phase de croissance exponentielle lorsque l'activité métabolique atteint son apogée.
Pour les tampons non volatils comme le HEPES, il est essentiel de considérer l'équilibre du tampon. Les tampons HEPES peuvent prendre jusqu'à deux heures pour se stabiliser et doivent être soigneusement titrés avec du bicarbonate et du CO₂ [1]. Cependant, augmenter la capacité tampon peut involontairement augmenter la production de lactate, ce qui peut contrecarrer l'effet stabilisateur souhaité [1]. Lorsqu'elles sont combinées avec des techniques de surveillance basées sur des capteurs et de barbotage de gaz, ces considérations de tampon aident à maintenir des conditions de processus stables et optimales.
FAQs
Comment le barbotage de gaz soutient-il le contrôle du pH dans la production de viande cultivée ?
Le barbotage de gaz joue un rôle important dans le maintien de l'équilibre des niveaux de pH pendant la production de viande cultivée. À mesure que les cellules se développent, elles libèrent du dioxyde de carbone (CO₂) comme sous-produit de la respiration. Ce CO₂ peut abaisser le pH du milieu de culture, ce qui peut nuire à la santé des cellules. En introduisant des gaz tels que l'air, l'oxygène ou des gaz inertes dans le bioréacteur, le barbotage aide à éliminer l'excès de CO₂. Cela empêche le milieu de devenir trop acide et maintient le pH stable.
Maintenir le milieu de culture dans la plage de pH idéale d'environ 7,1 à 7,4 est crucial pour une croissance cellulaire saine et une productivité optimale. Lorsqu'il est associé à des systèmes tampons et à une surveillance en temps réel à l'aide de capteurs de pH, le barbotage de gaz améliore non seulement l'efficacité du processus, mais augmente également la viabilité des cellules. C'est un élément essentiel pour assurer le succès du biotraitement de la viande cultivée.
Qu'est-ce qui rend les capteurs potentiométriques un meilleur choix que les capteurs optiques pour la surveillance du pH dans la production de viande cultivée ?
Les capteurs potentiométriques jouent un rôle important dans la production de viande cultivée grâce à leur capacité à fournir des mesures de pH en temps réel avec une grande précision. Maintenir des niveaux de pH appropriés est essentiel pour créer l'environnement adéquat pour la croissance cellulaire, et ces capteurs excellent dans la fourniture des données nécessaires pour y parvenir. De plus, ils sont relativement abordables et s'intègrent parfaitement dans les bioréacteurs à grande échelle, ce qui les rend idéaux pour une surveillance continue dans les environnements industriels.
De plus, ces capteurs sont conçus pour faire face aux défis des milieux de culture complexes, offrant des performances fiables même dans des conditions exigeantes. Cependant, ils nécessitent un étalonnage périodique pour maintenir leur précision.Avec leur mélange de précision, fiabilité et rentabilité, les capteurs potentiométriques sont devenus un choix privilégié pour un contrôle efficace du pH dans le biotraitement de la viande cultivée.
Pourquoi l'accumulation d'acide lactique rend-elle difficile le maintien de niveaux de pH stables ?
L'accumulation d'acide lactique complique le contrôle du pH en augmentant l'acidité de l'environnement de culture, provoquant une baisse du pH. Cela peut nuire à la viabilité et à la productivité des cellules, car la plupart des cellules ont besoin d'une plage de pH soigneusement contrôlée pour croître et fonctionner correctement.
Gérer les niveaux d'acide lactique est crucial dans le biotraitement de la viande cultivée pour soutenir une croissance cellulaire saine et maintenir la qualité du produit. Des approches telles que la surveillance en temps réel du pH, l'utilisation de tampons de pH, ou l'ajustement des protocoles d'alimentation peuvent aider à stabiliser l'environnement et éviter les variations de pH dommageables.











