L'agitation est cruciale dans la production de viande cultivée, garantissant que les cellules reçoivent de l'oxygène et des nutriments tout en évitant l'accumulation de déchets. Cependant, une agitation excessive provoque des problèmes tels que le détachement des cellules, des dommages aux membranes et une croissance réduite. Trouver le bon équilibre est essentiel, en particulier dans les bioréacteurs à grande échelle, où même des ajustements mineurs peuvent avoir un impact sur la production.
Points Clés:
- Agitation Optimale: Des études montrent que 60 tr/min dans les réacteurs à cuve agitée est idéal pour équilibrer l'apport en nutriments et le stress de cisaillement.
-
Types de Bioréacteurs:
- Cuve Agitée: Mélange efficace mais risque de stress de cisaillement élevé.
- Bioréacteurs à Vagues: Mélange doux, limité par le transfert d'oxygène.
- Systèmes à Airlift: Mélange uniforme avec faible stress mais nécessitent un contrôle précis.
- Mesures de Protection : Des additifs comme Poloxamer 188 et une oxygénation sans bulles réduisent les dommages cellulaires.
- Défis de Mise à l'Échelle : Les systèmes plus grands augmentent les risques de cisaillement, nécessitant une surveillance précise et une modélisation CFD.
Maintenir un contrôle précis de l'agitation est crucial pour l'échelle de production de viande cultivée tout en protégeant l'intégrité cellulaire.
Comment l'Agitation Affecte la Croissance et la Survie Cellulaire
Ce que Montrent les Études Récentes
Des recherches récentes ont identifié des seuils d'agitation spécifiques qui impactent la croissance et la survie des cellules. Par exemple, une étude ABM-CFD utilisant des cellules FS-4 sur des microporteurs dans un bioréacteur à cuve agitée de 100 mL a révélé que 60 rpm est la vitesse de mélange optimale. À cette vitesse, les nutriments et l'oxygène sont distribués uniformément, avec un stress de cisaillement restant entre 0–80 mPa. Cependant, dépasser 60 rpm entraîne des dommages et un détachement des cellules en raison des forces accrues.À 220 tr/min, le nombre de Reynolds de l'impulseur monte en flèche de 1 444 à 5 294,7, signifiant un passage à un écoulement turbulent. Cette turbulence génère des tourbillons plus petits que les microporteurs, ce qui peut endommager les cellules et leurs membranes [2].
Une autre étude portant sur les cellules souches mésenchymateuses dérivées du cordon ombilical humain a mis en évidence comment même de légères augmentations de l'intensité de l'agitation réduisent significativement les taux d'adhésion. Cela démontre la haute sensibilité des cellules adhérentes au stress mécanique [6].
Ces résultats soulignent l'importance de calibrer précisément les vitesses de mélange, ce qui reste un domaine clé d'amélioration continue.
Trouver la bonne intensité de mélange
Le principal défi est de trouver un équilibre entre la vitesse minimale d'agitation nécessaire pour suspendre les microporteurs (N<sub>js</sub>) sans dépasser les limites de contrainte de cisaillement.Pour les cellules de viande, les conditions idéales impliquent un taux de dissipation d'énergie d'environ 1 mW·kg⁻¹ et un temps de mélange inférieur à 10 secondes [1].
"Maintenir un micro et macro-environnement favorable pour les cellules sans les soumettre à un stress mécanique excessif dû à l'agitation nécessitera de l'innovation et de l'optimisation dans la conception et les processus des bioréacteurs" [2].
Une agitation excessive peut avoir deux effets néfastes : la mort cellulaire immédiate lorsque le stress dépasse un seuil critique, et un stress cumulatif menant à la quiescence. Les deux résultats entravent la productivité. Cela rend le contrôle précis de l'intensité de l'agitation un facteur critique pour le succès commercial, surtout dans la production à grande échelle. Dans des systèmes avec des volumes aussi grands que 20 m³, même une agitation minimale peut provoquer le détachement des cellules, soulignant la complexité de l'augmentation d'échelle tout en maintenant la viabilité cellulaire.
Introduction aux bioréacteurs : Mélange, agitation & cisaillement
Méthodes de mélange des bioréacteurs et leurs effets
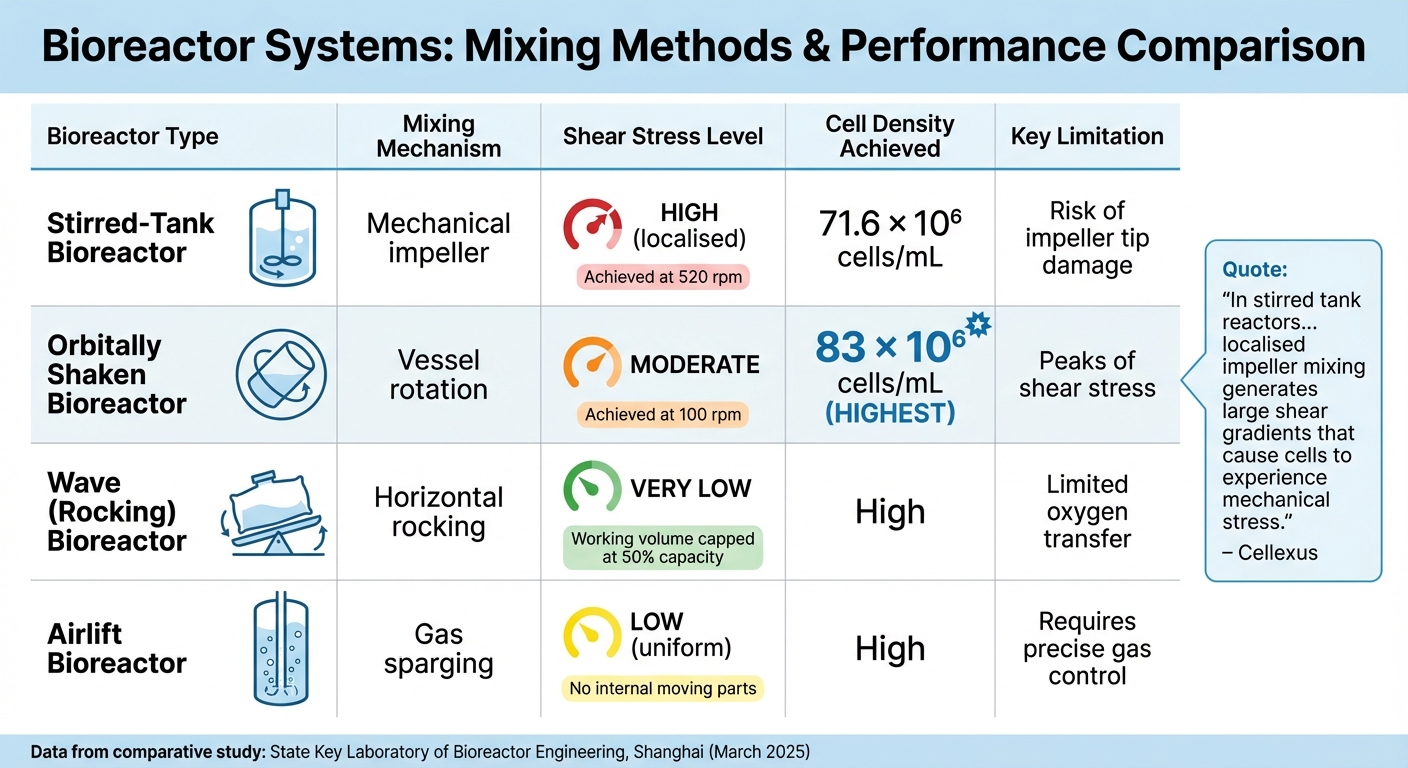
Comparaison des types de bioréacteurs pour la production de viande cultivée
Comparaison des différents systèmes de bioréacteurs
La conception d'un bioréacteur joue un rôle crucial dans l'équilibre de la distribution des nutriments et la gestion du stress mécanique. Chaque type de bioréacteur crée des conditions de mélange distinctes, qui affectent directement la survie et la productivité des cellules. Choisir le bon système signifie trouver un équilibre entre une distribution efficace des nutriments et la minimisation des forces mécaniques qui pourraient nuire aux cellules.
Les bioréacteurs à cuve agitée s'appuient sur des turbines mécaniques pour mélanger la culture. Les turbines Rushton produisent des flux radiaux, entraînant des zones de cisaillement localisées, surtout près des extrémités des turbines.En revanche, les turbines à pales inclinées et les hélices marines créent des flux plus doux, mieux adaptés aux cellules mammaliennes délicates. Une étude menée en mars 2025 par le State Key Laboratory of Bioreactor Engineering à Shanghai a comparé la performance des cellules CHO-K1 dans des bioréacteurs à cuve agitée et à agitation orbitale. Le système à cuve agitée a atteint 71,6 × 10⁶ cellules/mL à 520 tr/min, tandis que le système à agitation orbitale a atteint 83 × 10⁶ cellules/mL à seulement 100 tr/min [4].
Les bioréacteurs à vagues (balancement) éliminent complètement les turbines, utilisant un sac jetable qui se balance sur un plateau pour créer des vagues douces pour le mélange. Cet environnement à faible cisaillement est idéal pour les lignées cellulaires fragiles. Cependant, ces systèmes dépendent de l'aération de surface, ce qui peut limiter le transfert d'oxygène dans les cultures à haute densité. Pour maintenir une formation de vagues efficace, le volume de travail est limité à 50 % de la capacité totale du sac [7].
Les bioréacteurs à circulation d'air utilisent un mélange pneumatique, où le barbotage de gaz fait circuler le liquide entre un tube ascendant et un tube descendant. Sans pièces mobiles internes, les systèmes à circulation d'air offrent une dissipation d'énergie uniforme et des forces de cisaillement plus faibles par rapport aux cuves agitées. Contrairement aux bioréacteurs à onde, les conceptions à circulation d'air offrent un meilleur transfert d'oxygène grâce à leur circulation efficace [7] .
| Type de bioréacteur | Mécanisme de mélange | Contrainte de cisaillement | Densité cellulaire atteinte | Limitation principale |
|---|---|---|---|---|
| Cuve agitée | Hélice mécanique | Élevée (localisée) | 71.6 × 10⁶ cellules/mL | Risque de dommages à l'extrémité de l'agitateur |
| Agité orbitalement | Rotation du récipient | Modéré | 83 × 10⁶ cellules/mL | Pics de contrainte de cisaillement |
| Vague (Balancement) | Balancement horizontal | Très faible | Élevé | Transfert d'oxygène limité |
| Airlift | Barbotage de gaz | Faible (uniforme) | Élevé | Nécessite un contrôle précis des gaz |
"Dans les réacteurs à cuve agitée... le mélange localisé par l'agitateur génère de grands gradients de cisaillement qui provoquent un stress mécanique sur les cellules." – Cellexus [7]
À mesure que les bioréacteurs augmentent en échelle, les compromis entre l'efficacité du mélange et la protection des cellules deviennent plus apparents.Les systèmes à cuve agitée sont très efficaces pour distribuer les nutriments, mais nécessitent des ajustements de vitesse minutieux pour éviter d'endommager les cellules dans les zones de cisaillement élevé. D'autre part, les bioréacteurs à vagues et à circulation d'air offrent un mélange plus doux, réduisant le risque de stress de cisaillement, bien qu'ils puissent avoir des difficultés avec l'apport d'oxygène dans les cultures denses. Ces comparaisons soulignent l'équilibre délicat nécessaire pour optimiser le biotraitement à grande échelle tout en protégeant l'intégrité cellulaire.
sbb-itb-ffee270
Réduction du stress de cisaillement et amélioration de la croissance cellulaire
Nouveaux designs de bioréacteurs et additifs protecteurs
Minimiser le stress de cisaillement est essentiel pour favoriser la croissance cellulaire dans la production de viande cultivée. Les innovations dans la conception des bioréacteurs et l'utilisation d'additifs protecteurs ont considérablement amélioré la viabilité cellulaire et l'efficacité du mélange.Une approche prometteuse implique des bioréacteurs secoués orbitalement, qui reposent sur le mouvement du récipient et l'aération de surface pour éviter les forces de cisaillement dommageables causées par le mélange entraîné par l'hélice et la rupture des bulles. Ces systèmes ont démontré des résultats impressionnants, produisant 83 × 10⁶ cellules/mL, comparé à 71.6 × 10⁶ cellules/mL dans les systèmes traditionnels à cuve agitée [4] .
Dans les systèmes à cuve agitée, la géométrie de l'hélice fait également une différence. Les hélices radiales de type Rushton créent des schémas d'écoulement qui permettent aux cellules de se rétablir dans des zones "calmes", réduisant l'impact des forces de cisaillement élevées. Comme l'ont observé les chercheurs de TTP :
Les cellules dans les réacteurs à hélice radiale de type Rushton se rétablissent pendant les phases calmes, contrairement à celles dans les systèmes à double hélice axiale [5].
Pour des résultats optimaux dans la production de viande cultivée, il est important de maintenir la vitesse de pointe de l'hélice entre 0.6–1.8 m/s est recommandé pour protéger la croissance cellulaire [9] .
Les additifs protecteurs comme le Poloxamer 188 (Pluronic F-68) jouent un rôle clé en réduisant la tension de surface à l'interface gaz-liquide, protégeant les cellules des dommages lors de la formation et de la rupture des bulles. La concentration idéale pour le Poloxamer 188 est de 1 g/L, car des quantités plus élevées offrent peu d'avantages supplémentaires [9]. Pour les cellules adhérentes cultivées sur des microporteurs, un régime d'agitation intermittent peut encore améliorer les résultats. Par exemple, utiliser un schéma de 30 minutes OFF et 5 minutes ON pendant la phase de semis favorise le transfert de perle à perle tout en minimisant le stress hydrodynamique. Cette approche a permis aux cellules satellites bovines d'atteindre des densités de 3 × 10⁶ cellules/mL [3] .
En plus de ces stratégies de conception et d'additifs, améliorer la livraison d'oxygène peut encore réduire le stress de cisaillement.
Utilisation de l'oxygénation sans bulles
L'oxygénation sans bulles offre un autre moyen efficace de protéger les cellules des dommages de cisaillement. La rupture de bulles à l'interface gaz-liquide peut générer des taux de dissipation d'énergie aussi élevés que 10⁶ à 10⁸ W/m³, dépassant largement le seuil sublétal de 10⁴ W/m³ que la plupart des cellules mammifères peuvent tolérer [9] . En éliminant les bulles, cette méthode aide à protéger les cultures à haute densité.
L'aération de surface, couramment utilisée dans les bioréacteurs à agitation orbitale et à bascule, est particulièrement efficace pour réduire les forces de cisaillement.Comme le souligne une étude récente:
Les OSB utilisent le mouvement du corps du vaisseau et l'aération de surface pour atténuer efficacement les dommages de cisaillement causés par les pales d'hélice traditionnelles et la formation ou la rupture de bulles [4].
Les bioréacteurs à bascule montrent également un potentiel pour la production de viande cultivée. Ils offrent des avantages tels que la jetabilité, des coûts d'exploitation faibles et un environnement hydrodynamique doux [8].
Cependant, l'aération de surface rencontre des défis à des densités cellulaires très élevées. Par exemple, un bioréacteur secoué orbitalement a atteint un coefficient de transfert de masse d'oxygène (kLa) de 20,12 h⁻¹ à 100 rpm, soutenant théoriquement des densités cellulaires allant jusqu'à 118 × 10⁶ cellules/mL.En pratique, cependant, lorsque la densité cellulaire dépasse 80 × 10⁶ cellules/mL, la viscosité de la suspension augmente, entraînant un comportement non newtonien et rhéofluidifiant qui réduit l'efficacité du transfert d'oxygène. Cela souligne la nécessité d'une optimisation minutieuse à mesure que les densités cellulaires augmentent.
Contrôle de l'agitation pour la production à grande échelle
Ajustement des vitesses de mélange et systèmes de surveillance
Dans les systèmes à grande échelle, maintenir un contrôle précis de l'agitation est crucial. Pour les premières 24 heures, il est recommandé de maintenir les vitesses de mélange entre 30–50 tr/min pour optimiser l'attachement des cellules aux microporteurs [6] . Une étude de l'Université des Sciences et Technologies de Chine Orientale en juin 2022 souligne l'importance de cette approche : à 45 tr/min, les cellules souches mésenchymateuses dérivées du cordon ombilical humain ont atteint un 98.Taux d'adhérence de 68% le jour 1, tandis que l'augmentation de la vitesse à 55 tr/min a fait chuter les taux d'adhérence à 51,32% [6] .
Après la phase d'attachement, l'agitation doit légèrement dépasser la vitesse juste suspendue (N₍JS₎) pour éviter l'agglomération des cellules. Les recherches montrent que le maintien d'une intensité d'agitation proche de 1,3 × N₍JS₎ favorise la croissance cellulaire, tandis que la dépasser jusqu'à 2 × N₍JS₎ entrave la croissance en raison d'une efficacité d'attachement réduite [10] .
Une surveillance continue est essentielle, compte tenu des marges opérationnelles étroites. Des systèmes comme le bioréacteur BioStar 1.5c utilisent des logiciels avancés pour ajuster l'agitation et le flux de gaz en fonction des retours en temps réel des sondes d'oxygène dissous (DO) et de pH [6]. Les capteurs DO optiques jouent un rôle clé ici, offrant la précision nécessaire pour ajuster l'agitation uniquement lorsque les niveaux de DO tombent en dessous d'un seuil défini - généralement autour de 40% - minimisant ainsi le stress de cisaillement [7] [6]. L'équipe de Chine de l'Est a employé cette méthode en utilisant des sondes Mettler Toledo, maintenant le DO à 40% et le pH à 7,2. Cette approche a abouti à une densité cellulaire maximale de 27,3 × 10⁵ cellules/mL, une amélioration de 2,9 fois par rapport aux techniques de culture en batch standard [6].
Lors de la mise à l'échelle, les modèles de dynamique des fluides computationnelle (CFD) sont inestimables pour déterminer la vitesse optimale de l'agitateur afin de suspendre les microporteurs sans dépasser les limites de cisaillement [10][6]. Au lieu de simplement faire correspondre les tours par minute entre les cuves, l'analyse CFD suggère d'aligner le taux de déformation de cisaillement moyen en volume entre les réacteurs. Cela garantit que l'environnement hydrodynamique dans un bioréacteur plus grand - tel que le passage d'un flacon agitateur de 200 mL à un bioréacteur de 1,5 L - reste propice à la croissance cellulaire [6].
Ces stratégies soulignent l'importance d'un contrôle et d'une surveillance précis lors de la transition vers des systèmes de bioréacteurs avancés.
Recherche d'Équipements Spécialisés Grâce à Cellbase
Se procurer le bon équipement pour la production de viande cultivée peut être délicat. Les plateformes d'approvisionnement de laboratoire standard ne répondent souvent pas aux besoins spécifiques de ce domaine, tels que les turbines à faible cisaillement ou les capteurs optiques d'oxygène dissous adaptés aux cultures cellulaires de mammifères à haute densité. C'est là que
En tant que premier marché B2B dédié à l'industrie de la viande cultivée,
Que vous mettiez à niveau vos systèmes de surveillance ou que vous vous procuriez des composants spécialisés, des plateformes comme
Conclusion
Obtenir le bon équilibre entre l'apport en oxygène et en nutriments tout en évitant le stress de cisaillement nocif est essentiel pour optimiser l'agitation dans les bioréacteurs de viande cultivée. La recherche montre que cela peut être réalisé en choisissant les bons designs de bioréacteurs, en ajustant finement les vitesses de mélange et en utilisant des stratégies de protection.
Des techniques comme l'agitation intermittente, les turbines radiales de Rushton et les ajustements en temps réel surveillés par CFD (dynamique des fluides computationnelle) jouent un rôle important pour garantir que les cellules se rétablissent bien et croissent régulièrement. À mesure que la production passe des flacons de laboratoire à des volumes industriels, comprendre le comportement des fluides non newtoniens et maintenir des échelles de longueur de Kolmogorov cohérentes devient crucial pour éviter les dommages mécaniques. Ces avancées facilitent la protection des cellules et simplifient les efforts de mise à l'échelle.
Des plateformes telles que
FAQ
Quels problèmes une agitation excessive peut-elle causer dans les bioréacteurs pour la viande cultivée ?
Une agitation excessive dans les bioréacteurs peut être un problème sérieux pour la production de viande cultivée, car elle peut avoir un impact négatif sur la croissance et la survie des cellules. Un mélange vigoureux crée un stress de cisaillement élevé, ce qui peut nuire aux cellules animales délicates. Ce type de stress mécanique peut entraîner des dommages à la membrane cellulaire, une viabilité réduite et même entraver le développement des tissus.
Pour prévenir ces défis, il est crucial de peaufiner les paramètres d'agitation.L'objectif est de trouver un équilibre entre un transfert efficace de nutriments et d'oxygène tout en minimisant le stress mécanique. Des facteurs clés tels que la conception de l'agitateur, la vitesse de mélange et la géométrie du bioréacteur doivent être soigneusement ajustés pour maintenir des cellules saines et productives tout au long du processus de culture.
Comment le choix du bioréacteur affecte-t-il la croissance et la viabilité des cellules dans la production de viande cultivée?
Le choix du bioréacteur dans la production de viande cultivée est crucial, car il impacte directement la croissance et la santé des cellules en influençant des facteurs tels que l'efficacité du mélange, le transfert d'oxygène et le stress de cisaillement.
Les bioréacteurs à cuve agitée sont une option populaire pour la production à grande échelle car ils offrent un contrôle précis de ces conditions. Cependant, ils peuvent également produire des forces de cisaillement qui pourraient nuire aux cellules fragiles, rendant essentiel le réglage précis des conceptions d'agitateurs et des paramètres de fonctionnement pour minimiser les dommages.
D'autres conceptions, telles que les bioréacteurs à circulation d'air, sont plus simples et consomment moins d'énergie. Mais elles peuvent ne pas offrir le même niveau de contrôle sur le mélange, ce qui peut affecter la croissance des cellules. D'autre part, les bioréacteurs à fibres creuses imitent les vaisseaux sanguins pour soutenir des densités cellulaires élevées, bien que leur mise à l'échelle puisse être un défi.
Le choix du bon bioréacteur revient à trouver le bon équilibre entre des facteurs tels que l'évolutivité, le coût et les besoins spécifiques des cellules pour garantir qu'elles se développent et prospèrent efficacement pour la production de viande cultivée.
Comment le stress de cisaillement peut-il être réduit lors de la production de viande cultivée à grande échelle ?
Minimiser le stress de cisaillement dans la production de viande cultivée à grande échelle nécessite des ajustements minutieux de la conception et du fonctionnement du bioréacteur. Des facteurs tels que le type d'hélice, la forme du réacteur et les paramètres de mélange jouent un rôle clé.Par exemple, réduire les vitesses de pointe des turbines ou opter pour des conceptions spécifiques de turbines peut diminuer les forces de cisaillement tout en maintenant un mélange et une distribution d'oxygène appropriés, ce qui est crucial pour la croissance cellulaire.
Un autre outil utile dans ce processus est la dynamique des fluides numérique (CFD). Les simulations CFD permettent aux ingénieurs d'étudier en détail les schémas d'écoulement et la distribution des cisaillements, les aidant à apporter des ajustements de conception éclairés. De plus, les bioréacteurs à bascule ou à mélange par vagues offrent une alternative plus douce aux systèmes traditionnels à cuve agitée, car ils produisent naturellement des forces de cisaillement plus faibles. L'incorporation de la surveillance en temps réel avec des capteurs avancés et des algorithmes de contrôle prédictif peut également aider à maintenir le stress de cisaillement dans des limites sûres, assurant un processus de production plus fluide.











