La stabilité génétique est cruciale pour la production de viande cultivée. Sans elle, les lignées cellulaires peuvent muter, entraînant une qualité incohérente, des risques pour la sécurité et des échecs de production. Passer de milliers à des trillions de cellules amplifie ces risques, rendant les systèmes de contrôle de qualité robustes essentiels. Les régulateurs comme la FDA et l' EMA exigent une preuve de stabilité avant d'approuver les produits, car même de légers changements génétiques peuvent déclencher des résultats allergènes ou nocifs.
Les principaux défis incluent la dérive génétique, l'accumulation de mutations et l'activation d'oncogènes. Ces problèmes surviennent lors de passages cellulaires prolongés, de pressions sélectives et de stress environnementaux pendant la production. Des méthodes de test avancées, telles que le caryotypage, les puces SNP et le séquençage de nouvelle génération (NGS), aident à détecter et à résoudre ces risques. Des stratégies préventives comme la banque de cellules structurée et l'ingénierie génétique ciblée protègent davantage contre l'instabilité.
Les producteurs doivent intégrer le contrôle de la qualité à chaque étape de la production - de la banque de cellules aux bioréacteurs à grande échelle. Des outils comme le profilage STR, les tests de contamination et les essais fonctionnels garantissent la cohérence et la sécurité. Des plateformes comme
Accélérer le développement de lignées cellulaires de l'ADN à la banque de cellules maîtresses - AGC Biologics
Défis courants dans le maintien de la stabilité génétique
Assurer la stabilité génétique tout au long du cycle de production de la viande cultivée n'est pas une mince affaire. L'ampleur même de la production offre de nombreuses opportunités pour que des changements génétiques se développent et se propagent. Reconnaître ces défis est essentiel pour mettre en place des systèmes de contrôle de la qualité efficaces.
Dérive génétique et accumulation de mutations
Le passage cellulaire prolongé est une source majeure d'instabilité génomique dans la production de viande cultivée. Les lignées cellulaires immortalisées, par leur nature, sont sujettes à des changements génomiques, ce qui peut entraîner des mutations spontanées lors de la culture à long terme [6][5]. À mesure que les cellules subissent de multiples dédoublements de population, des erreurs dans la réplication de l'ADN s'accumulent, entraînant des populations cellulaires diverses et, potentiellement, une perte de fonction. Christopher Frye et Luhong He de BioPharm International soulignent ce problème :
Les lignées cellulaires CHO dérivées de manière clonale ont souvent été observées pour diverger, devenant une population hétérogène sur de longues périodes de sous-culture [6].
Dans les environnements industriels, environ 20 % des lignées cellulaires de production présentent une hétérogénéité transgénique considérable au fil des générations successives [6]. Ces mutations peuvent survenir tôt, lors de la réplication de l'ADN après la transfection, ou en raison d'erreurs lors de l'intégration de gènes étrangers dans le génome hôte [5].
Les pressions sélectives ajoutent une autre couche de complexité. Des agents comme les antibiotiques et les marqueurs métaboliques (e.g. , MTX) utilisés pour stabiliser les lignées cellulaires peuvent en fait augmenter les taux de mutation [6][5]. Dans certains cas, plus la concentration de ces agents est élevée, plus le taux de mutation est élevé [6]. Les facteurs de stress environnementaux - tels que les pénuries de nutriments, les conditions de culture sous-optimales lors de la montée en échelle, et le stress physique dû à l'expansion - peuvent encore déstabiliser l'intégrité génétique [6][5].
Shuai Wang, Directeur du Développement de Lignées Cellulaires chez WuXi Biologics, note :
Les niveaux de mutation sont susceptibles de changer au cours du passage cellulaire en raison de la plasticité génomique des cellules d'ovaire de hamster chinois (CHO) [5].
Les changements épigénétiques jouent également un rôle. Les transgènes peuvent être partiellement ou complètement perdus ou réduits au silence pendant le processus de culture, affectant la stabilité à long terme. Ces mutations accumulées nuisent non seulement à la fonction cellulaire mais augmentent également le risque d'activation des oncogènes.
Risques d'Activation des Oncogènes
L'activation des oncogènes représente une préoccupation critique en matière de sécurité pour les producteurs de viande cultivée, car elle peut compromettre des lots de production entiers. L'instabilité génétique peut conduire à l'activation des oncogènes par des mécanismes tels que l'hyperméthylation, ce qui peut entraîner des profils similaires à ceux des tumeurs [3][1]. L'expansion rapide requise dans la production augmente encore la probabilité d'accumuler ces mutations nocives [5][6].
C'est un défi bien reconnu. Selon le Consortium International pour l'Innovation & Qualité dans le Développement Pharmaceutique (IQ), 67% des répondants estiment que les mutations génétiques posent une menace plus grande que l'incorporation erronée d'acides aminés pendant la production [5] . Un cas de mai 2024 illustre la gravité de ce problème : WuXi Biologics a découvert que 43% des clones d'un programme de développement de lignées cellulaires portaient la même mutation ponctuelle génétique. La cause principale ? Un niveau de variante de 2,1% à 2,2% dans l'ADN plasmidique utilisé lors de la transfection, qui n'a pas été détecté par le séquençage traditionnel de Sanger. Pour y remédier, l'entreprise a intégré le séquençage de nouvelle génération (NGS) dans ses processus de contrôle qualité pour détecter ces variantes tôt [5].
La détection précoce des anomalies génétiques est cruciale, car les changements oncogéniques peuvent compromettre des lots entiers. Le caryotypage standard en bandes G peut identifier des sous-populations anormales avec seulement 14 % de mosaïcisme dans vingt métaphases cellulaires [1]. Des techniques plus avancées comme le NGS peuvent détecter des mutations génétiques dans des cellules clonales avec une sensibilité de 0,5 % [5].
L'analyse de la méthylation de l'ADN est un autre outil précieux pour évaluer le potentiel tumorigène :
Parce que les niveaux de méthylation de l'ADN et l'hyperméthylation de certains gènes se produisent lors de l'initiation et de la progression du cancer, l'analyse des profils de méthylation de l'ADN pourrait fournir des informations complémentaires sur le potentiel tumorigène des cellules [3].
Le véritable défi réside dans la mise en œuvre de systèmes de surveillance robustes capables d'identifier ces changements avant qu'ils ne compromettent la sécurité.Pour les producteurs de viande cultivée, maintenir la stabilité génétique pendant l'expansion rapide des cellules exige des mesures de contrôle de qualité avancées. Des plateformes spécialisées comme
Méthodes de Test de Contrôle de Qualité
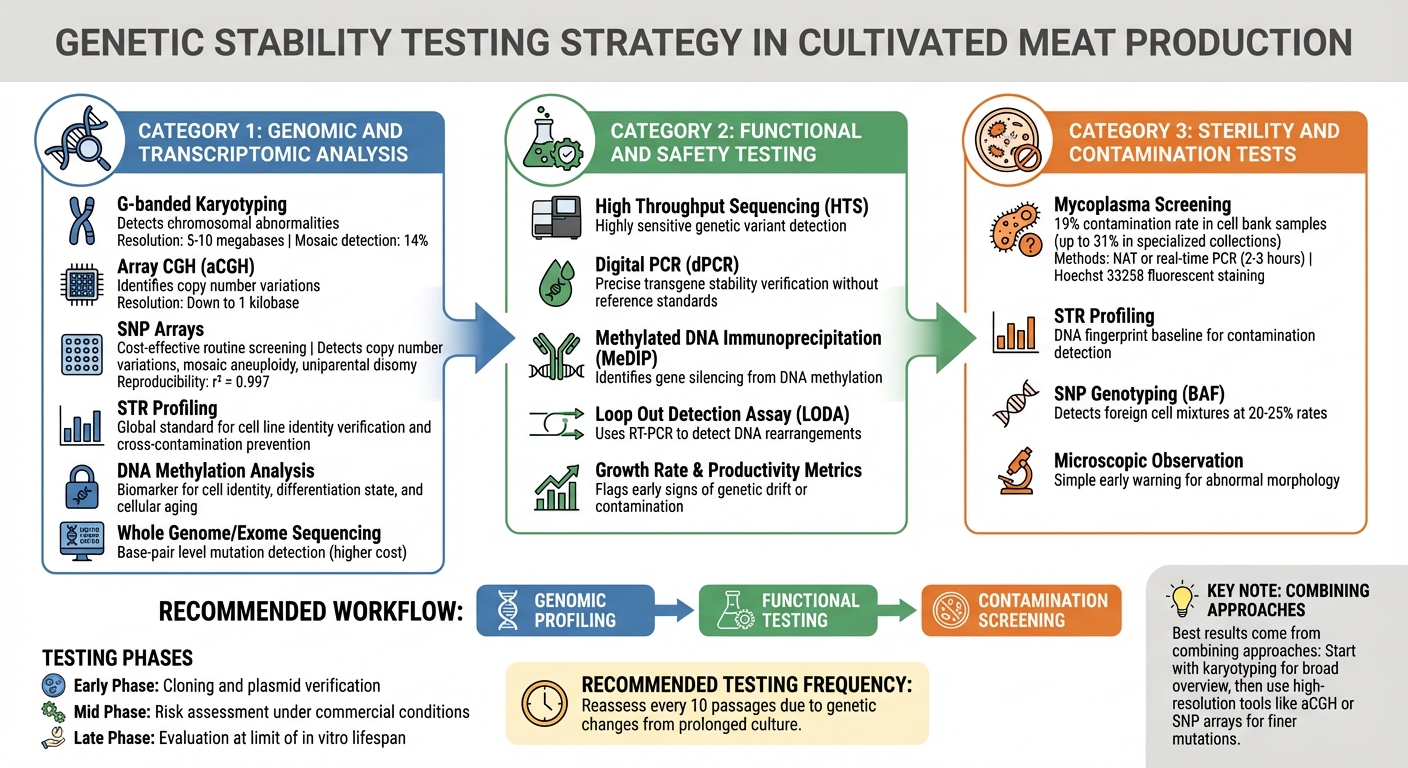
Méthodes de Test de Contrôle de Qualité pour la Stabilité Génétique dans les Lignes Cellulaires de Viande Cultivée
Identifier l'instabilité génétique avant qu'elle n'affecte la production nécessite une stratégie de test à plusieurs niveaux. Les producteurs de viande cultivée s'appuient sur des méthodes qui détectent tout, des grands changements chromosomiques aux mutations d'une seule base. Le choix des techniques dépend des risques présents à chaque étape de la production. Ces outils génomiques agissent comme le premier point de contrôle, suivi par des évaluations fonctionnelles et de contamination détaillées.
Analyse Génomique et Transcriptomique
Le caryotypage en bandes G est un outil clé pour identifier les principaux problèmes chromosomiques tels que les anomalies numériques et les grandes réarrangements structurels, comme les translocations. Bien qu'il puisse détecter des niveaux de mosaïque d'environ 14 %, sa résolution est limitée aux changements de 5 à 10 mégabases, ce qui signifie que les altérations plus petites peuvent passer inaperçues [1].
L'hybridation génomique comparative sur puce (aCGH) offre une résolution plus élevée, identifiant les variations du nombre de copies jusqu'à 1 kilobase. De même, les puces de polymorphisme nucléotidique simple (SNP) fournissent une option rentable pour le dépistage de routine, détectant les variations du nombre de copies, l'aneuploïdie en mosaïque et la disomie uniparentale. Les études de validation ont montré que les puces SNP sont hautement reproductibles, avec des mesures de la fréquence des allèles B (BAF) atteignant un impressionnant r² = 0.997 [8] [1].
Rocio Aguilar-Quesada du Biobanque du Système de Santé Publique Andalou souligne la valeur de la combinaison des méthodes :
Le caryotypage reste un test polyvalent, surtout lorsqu'il est complété par des tests à haute résolution [1].
Le profilage par répétition en tandem courte (STR) est la norme mondiale pour vérifier l'identité des lignées cellulaires et prévenir la contamination croisée [1] [9]. Par ailleurs, l'analyse de la méthylation de l'ADN sert de biomarqueur pour l'identité cellulaire, l'état de différenciation et le vieillissement cellulaire [1]. Pour la détection des mutations au niveau des paires de bases, le séquençage du génome entier ou de l'exome est une option, bien qu'il soit plus coûteux par rapport aux méthodes basées sur des puces [1].
Les meilleurs résultats proviennent de la combinaison de ces approches. Commencez par le caryotypage pour une vue d'ensemble, puis utilisez des outils à haute résolution comme l'aCGH ou les puces SNP pour capturer des mutations plus fines. Une réévaluation régulière - idéalement tous les 10 passages - est cruciale, car une culture prolongée peut entraîner des changements génétiques [10]. Ces informations génomiques sont ensuite complétées par des essais fonctionnels pour garantir un comportement cellulaire cohérent tout au long de la production.
Tests Fonctionnels et de Sécurité
Le profilage génomique seul ne suffit pas. Les tests fonctionnels confirment que les cellules conservent leurs caractéristiques prévues pendant l'expansion. Des indicateurs comme les taux de croissance et la productivité peuvent signaler des signes précoces de dérive génétique ou de contamination [9].
Le séquençage à haut débit (HTS) est très sensible pour détecter les variantes génétiques, tandis que la PCR numérique (dPCR) vérifie précisément la stabilité des transgènes sans avoir besoin de standards de référence [11] . Christopher Frye et Luhong He de BioPharm International soulignent l'importance de cette étape :
La lignée cellulaire de production est la base de tout bioprocédé, et donc, une caractérisation génétique appropriée de la lignée cellulaire de production est absolument cruciale pour le succès du développement du procédé [6].
La stabilité épigénétique est également critique. L'immunoprécipitation de l'ADN méthylé (MeDIP) aide à identifier la répression génique causée par la méthylation de l'ADN, une raison courante de la baisse de productivité [7]. Des outils comme le Loop Out Detection Assay (LODA) utilisent la RT-PCR pour détecter les réarrangements de l'ADN, par exemple lorsqu'un gène d'intérêt est supprimé tandis que le marqueur sélectable reste [7].
Les tests doivent s'aligner avec la phase de production : les tests de phase précoce se concentrent sur le clonage et la vérification des plasmides, les tests de phase intermédiaire évaluent les risques dans des conditions commerciales, et les tests de phase tardive évaluent les cellules à la limite de leur durée de vie in vitro [6]. Commencer les expériences avec des cellules fraîches et à faible passage provenant d'une banque de cellules maîtresses réduit le risque de dérive génétique [9].
Tests de Stérilité et de Contamination
Les tests de contamination sont essentiels pour éviter les facteurs qui pourraient déstabiliser la génétique. Mycoplasma est particulièrement préoccupant, car il altère le métabolisme et le comportement des cellules sans provoquer de changements visibles dans la culture [1]. Des études révèlent une contamination par mycoplasmes dans 19 % des échantillons de banques cellulaires, certaines collections spécialisées montrant des taux aussi élevés que 31 % [1].
Le dépistage régulier des mycoplasmes à l'aide de techniques sensibles d'amplification des acides nucléiques (NAT) ou de PCR en temps réel peut fournir des résultats semi-quantitatifs en 2 à 3 heures [1]. La coloration fluorescente Hoechst 33258 est une autre méthode, révélant des motifs de fluorescence extracellulaire caractéristiques [9].
Le profilage STR établit une empreinte ADN pour les lignées cellulaires, servant de référence pour détecter la contamination croisée [9]. De plus, le génotypage SNP utilisant les distributions de fréquence des allèles B (BAF) peut identifier la contamination par d'autres lignées cellulaires, détectant des mélanges de cellules étrangères à des taux de 20 à 25 % [8].
L'observation microscopique est un outil d'alerte précoce simple mais efficace, car une morphologie cellulaire anormale signale souvent des problèmes de culture [9]. La mise en œuvre d'un système de gestion de la qualité, tel que ISO 9001:2015, ainsi que les Bonnes Pratiques des Méthodes In Vitro (GIVIMP), aide à maintenir des conditions de culture standardisées et reproductibles, réduisant le risque d'instabilité génomique [10].
Pour les producteurs de viande cultivée ayant besoin d'accéder à des équipements et matériaux de test spécialisés, des plateformes comme
sbb-itb-ffee270
Stratégies de Prévention pour l'Instabilité Génétique
Détecter l'instabilité génétique est une chose ; la prévenir est un autre défi entièrement.Pour maintenir la stabilité génétique intacte, les producteurs de viande cultivée ont besoin de systèmes bien conçus qui empêchent les lignées cellulaires de dériver avant que des problèmes ne surviennent. Deux stratégies clés mènent la voie ici : banque de cellules structurée et ingénierie génétique ciblée. Ensemble, ces approches s'attaquent directement aux risques de dérive génétique et d'activation des oncogènes.
Banque de Cellules et Cryopréservation
L'accumulation de mutations est une préoccupation réelle, donc un système de banque de cellules fiable est indispensable. La norme de l'industrie implique un système à deux niveaux : une Banque de Cellules Maîtresse (BCM) et une Banque de Cellules de Travail (BCT). Cette configuration assure un point de départ cohérent pour la production. Limiter le nombre de passages est crucial, car chaque passage augmente le risque de mutations. En stockant les cellules dans l'azote liquide, l'activité biologique est effectivement mise en pause, réduisant le risque de changements génétiques pendant le stockage.
Au lieu de suivre le temps, l'âge cellulaire est mesuré par les doublages de population. Par exemple, un bioréacteur de production typique de 5 000 litres implique environ 30 doublages de population[6]. Pour maintenir la cohérence génétique, la fabrication commerciale limite ce nombre entre 45 et 60 doublages[6].
Des méthodes de dépistage comme RT-PCR et qPCR à cellule unique peuvent détecter les problèmes tôt, tels que l'épissage inhabituel de l'ARNm ou la variabilité des transgènes. Les lignées cellulaires montrant une grande variabilité dans le nombre de copies doivent être éliminées pour éviter des problèmes futurs.
Le contrôle de la qualité est non négociable. De manière alarmante, des études ont révélé que jusqu'à 31 % des lignées cellulaires dans certaines banques étaient contaminées par des mycoplasmes [3] . Pour éviter cela, le profilage STR est utilisé pour confirmer l'authenticité des lignées cellulaires tout au long du processus de bancarisation.Comme souligné par la Recherche et Preuves de la FSA:
Parce que les cellules bancarisées sont le matériau de départ pour le produit final, des normes élevées pourraient être exigées par les régulateurs à l'avenir pour garantir un produit carné sûr et de haute qualité[2].
Génie Génétique pour la Stabilité
Le génie génétique offre une autre couche de défense en améliorant directement la stabilité des lignées cellulaires. Des techniques comme l'intégration ciblée (TI), en particulier l'Échange de Cassette Médié par Recombinase (RMCE), permettent l'insertion précise de transgènes dans des emplacements génomiques spécifiques. Cette approche évite l'imprévisibilité de l'intégration aléatoire, où les effets de position et l'instabilité du nombre de copies peuvent causer des ravages. Bien que le RMCE dans les cellules CHO ait des taux d'efficacité inférieurs à 0,1%[12], les clones résultants sont plus prévisibles et stables.
Le choix du système d'expression est également important. Par exemple, le système Glutamine Synthetase (GS) aboutit généralement à environ cinq copies de transgène par cellule, tandis que le système Dihydrofolate Reductase (DHFR) peut amplifier le nombre de copies jusqu'à 1 000[6]. Bien que des nombres de copies plus élevés puissent sembler attrayants, ils augmentent la probabilité d'altérations de l'ADN, ce qui rend les systèmes basés sur GS un choix plus judicieux pour une stabilité à long terme.
Pour minimiser davantage les risques, la mutagenèse site-spécifique et le dépistage NGS pré-transfection sont cruciaux. Étant donné que le séquençage Sanger a une limite de détection plus élevée, le NGS peut détecter des mutations plasmidiques en dessous de 0,5 %, améliorant ainsi le succès du dépistage des clones à plus de 90 %[5].
Shuai Wang et ses collègues de WuXi Biologics soulignent l'importance de cette vigilance :
Étant donné que l'optimisation des processus ne peut pas rectifier les mutations au niveau des gènes, surveillez rigoureusement les niveaux de mutation dans les clones stables[5].
Pour les producteurs ayant besoin d'outils spécialisés - que ce soit pour la cryopréservation, l'ingénierie génétique ou la caractérisation des lignées cellulaires -
Intégration du contrôle qualité dans la production
Intégrer le contrôle qualité à chaque phase de production est crucial. Sans un système structuré, même les lignées cellulaires bien entretenues peuvent subir des changements lors de l'expansion et de la montée en échelle. Le contrôle qualité ne doit pas être une réflexion après coup - il doit être une partie centrale de la production. Cela commence à l'étape de l'augmentation, où des systèmes de gestion stricts et des environnements contrôlés jouent un rôle clé.
Contrôle de la qualité lors de l'expansion et de l'augmentation
Comme discuté précédemment, les tests génomiques et de contamination sont essentiels, surtout lors de l'augmentation. Passer de petits volumes à des milliers de litres introduit de nouveaux risques, chaque passage cellulaire augmentant la probabilité de mutations. Un Système de Gestion de la Qualité (SGQ) aide à gérer ces risques efficacement. Par exemple, entre 2017 et 2022, Josep M. Canals et son équipe à l'Université de Barcelone ont mis en œuvre le SGQ ISO 9001:2015 pour standardiser les cultures de cellules souches pluripotentes humaines. Leur analyse rétrospective des données de G-banding et aCGH a révélé une réduction significative des aberrations chromosomiques par rapport aux conditions pré-adaptation[10] [13] . Les canaux ont souligné l'importance de la surveillance continue:
L'instabilité génétique montrée par les hPSCs en culture rend la réévaluation fréquente de l'intégrité génomique une exigence essentielle lors de la planification de leur utilisation pour des expériences[10].
Le dépistage génomique de routine est indispensable. Des techniques comme le caryotypage par bandes G et l'aCGH détectent les changements structurels, tandis que le séquençage de nouvelle génération (NGS) identifie les mutations à des niveaux inférieurs à 0,5%[5]. L'analyse de la courbe de croissance peut également signaler des problèmes précoces, tels que la contamination ou la dérive génétique[9] . La surveillance environnementale ajoute une couche de sécurité supplémentaire, avec des pratiques comme le test de plaque de sédimentation et les contrôles semestriels des filtres HEPA garantissant que l'environnement de production reste stable et sans stress pour les lignées cellulaires[4].
La cohérence dans les milieux et les réactifs est tout aussi importante. L'utilisation de milieux définis sans sérum comme mTeSR1, ainsi que de réactifs avec un certificat d'analyse, aide à réduire la variation d'un lot à l'autre et limite le risque de contamination virale[10][4]. Des vérifications régulières de la morphologie - simples observations microscopiques à différentes densités de culture - peuvent détecter les premiers signes de différenciation ou de stress[9]. Pour l'approvisionnement en équipements ou réactifs spécialisés, des plateformes comme
Essais fonctionnels pour la cohérence des produits
Alors que la surveillance génomique protège le processus, les essais fonctionnels garantissent que les cellules fonctionnent comme prévu.La stabilité génétique seule ne suffit pas ; les cellules doivent également maintenir leur capacité à fonctionner correctement à travers les lots de production. Dans la viande cultivée, cela signifie confirmer que les cellules souches, telles que les cellules satellites musculaires, peuvent encore se différencier en tissu musculaire ou adipeux mature après expansion[2] . Les essais de différenciation sont essentiels pour vérifier cela.
Les essais métaboliques comme MTT, LDH et Resazurin fournissent un aperçu de la santé et de la viabilité des cellules[4][9]. Ceux-ci, combinés avec le profilage des répétitions courtes en tandem (STR), aident à confirmer que les lignées cellulaires restent authentiques et exemptes de contamination croisée tout au long du processus de production[1][9].
L'analyse transcriptionnelle est une autre étape critique.Xiaoyue Chen et Sam Zhang recommandent:
Le séquençage de l'ADNc plutôt que de l'ADN génomique est recommandé pour la détection des mutations afin d'évaluer les risques au niveau de la transcription[5].
Cette méthode offre une image plus précise du produit final, car elle reflète comment les gènes sont exprimés plutôt que simplement leurs emplacements génomiques. En associant le dépistage génomique à des essais fonctionnels, les producteurs peuvent s'assurer que chaque lot répond à des normes strictes de sécurité, de qualité et de performance à chaque étape de la production.
Conclusion
Maintenir la stabilité génétique est crucial pour produire de la viande cultivée de manière sûre et cohérente. Francisco J. Molina-Ruiz et ses collègues du Laboratoire de cellules souches et de médecine régénérative soulignent les risques:
Les changements génétiques dans les hPSCs pourraient compromettre non seulement la sécurité des produits cellulaires à base de hPSC... mais aussi conduire à une propension de différenciation hétérogène du matériau de départ, des profils d'expression génique altérés et une inefficacité du produit cellulaire final [10].
Les enjeux sont importants - plus de 531 lignées cellulaires mal identifiées ont été enregistrées par le Comité International d'Authentification des Lignées Cellulaires [1].
Aborder ces problèmes nécessite un cadre de contrôle qualité robuste. Cela implique de combiner des méthodes telles que le profilage STR, le caryotypage par bandes G, l'aCGH et le NGS avancé [5], ainsi que des systèmes tels que l'ISO 9001:2015 pour standardiser les processus et minimiser les anomalies chromosomiques [13].
Les facteurs économiques motivent également la nécessité de ces mesures.La dérive génétique peut entraîner des cellules mutées à obtenir un avantage de croissance, potentiellement gâchant des lots de production entiers [10][11]. Avec l'accent croissant sur les cellules souches pluripotentes humaines, la demande pour des lignées cellulaires stables n'a jamais été aussi grande. Comme l'explique le professeur David L. Kaplan de l'Université Tufts:
Les lignées cellulaires immortalisées sont généralement considérées comme une exigence pour la génération de grandes quantités de tissus comestibles à partir d'un bioprocédé stable et robuste [14] .
Pour les producteurs de viande cultivée, le contrôle de la qualité doit être intégré à chaque étape - du dépistage des plasmides à la surveillance de la production à grande échelle. En combinant des tests approfondis avec des stratégies préventives, les producteurs peuvent garantir des résultats cohérents et fiables.
FAQ
À quelle fréquence les tests de stabilité génétique doivent-ils être effectués lors de la montée en échelle ?
Les tests de stabilité génétique sont une étape cruciale lors de la montée en échelle et doivent être effectués régulièrement. La fréquence de ces tests dépend en grande partie de la lignée cellulaire spécifique et du processus en question. Pour réduire les risques de mutations et maintenir la pluripotence des cellules, il est judicieux d'établir une limite de passage informée par une analyse génétique.
Quels tests détectent le mieux les petites mutations et les grands changements chromosomiques ?
Des tests tels que l'analyse de l'array SNP et le génotypage SNP à l'échelle du génome sont e
Quelle est la manière la plus simple de prévenir la dérive génétique entre les lots de production ?
Pour minimiser la dérive génétique, il est crucial de réaliser régulièrement des analyses génétiques et fonctionnelles des lignées cellulaires et de limiter le nombre de passages qu'elles subissent. Mettez en œuvre des pratiques telles que l'établissement de banques de cellules maîtresses et la vérification régulière de la stabilité génétique, comme recommandé dans les protocoles de contrôle qualité. Ces mesures sont essentielles pour maintenir la cohérence et garantir des résultats fiables entre les différents lots de production.











