Les échafaudages en hydrogel sont essentiels pour la production de viande cultivée, fournissant un cadre 3D pour la croissance cellulaire et la formation de tissus. Cependant, garantir leur sécurité et leur efficacité nécessite des tests approfondis de biocompatibilité. Les principaux défis incluent :
- Résidus chimiques : Les sous-produits toxiques de la polymérisation et des agents de réticulation peuvent nuire aux cellules.
- Problèmes de chimie de surface : Les hydrogels synthétiques manquent souvent de la bioactivité nécessaire pour l'adhésion cellulaire.
- Réponses immunitaires et dégradation : Certains échafaudages provoquent une inflammation ou se dégradent de manière à nuire aux tissus environnants.
Les solutions à ces défis incluent des méthodes de purification, des modifications de surface (e.g. , peptides RGD), et des conceptions d'échafaudages hybrides qui combinent des matériaux synthétiques et naturels.Les méthodes de test comme les essais de cytotoxicité, les évaluations des propriétés mécaniques et les études de dégradation garantissent que les échafaudages répondent aux exigences de sécurité et fonctionnelles. Les plateformes comme
Échafaudages Hydrogel 3D Pour la Culture de Chondrocytes Articulaires & Génération de Cartilage l Aperçu du Protocole
Défis Courants dans les Tests de Biocompatibilité
Les tests de biocompatibilité pour les échafaudages hydrogel présentent leur lot de défis, notamment en ce qui concerne la viabilité cellulaire et la formation efficace de tissus. Les principaux coupables ? Les résidus chimiques, les propriétés de surface et le comportement de dégradation. Ces facteurs peuvent avoir un impact significatif sur l'adhésion, la croissance et la survie des cellules. Examinons de plus près ces défis.
Toxicité résiduelle des composants chimiques
La sécurité est une priorité absolue dans la production de viande cultivée, et le contrôle des produits chimiques toxiques résiduels est une partie critique du processus. Les monomères non réagis issus de la polymérisation radicalaire, tels que le HEMA et les acrylates, peuvent sérieusement compromettre la survie des cellules. Les acrylates sont particulièrement problématiques, étant plus toxiques que les méthacrylates, qui eux-mêmes sont plus nocifs que les acrylamides [2].
Les agents de réticulation comme le diméthacrylate d'éthylène peuvent laisser des résidus toxiques qui ne se dégradent pas facilement [2]. De plus, les déclencheurs de polymérisation - tels que les initiateurs et les agents inducteurs de radicaux - posent des risques s'ils ne sont pas complètement réagis ou correctement éliminés [2].
Pour résoudre ce problème, la purification par dialyse est souvent employée pour éliminer ces monomères résiduels et agents de réticulation avant que les échafaudages ne soient ensemencés avec des cellules [2]. Obtenir des taux de conversion élevés pendant la polymérisation est également essentiel, en particulier pour les méthodes de gélification in situ où les risques de lixiviation sont accrus [2]. Une approche d'évaluation systématique, conforme aux normes ISO 10993, peut aider à identifier la source de la cytotoxicité - qu'il s'agisse de résidus de stérilisation, de changements de pH ou d'absorption de milieu - plutôt que de se fier à des hypothèses issues de la littérature existante [4].
Problèmes de chimie de surface affectant l'adhésion cellulaire
Les hydrogels synthétiques comme PEG, PHEMA et PVA sont naturellement hydrophiles et bioinertes.Bien que cela réduise le risque de déclencher une réponse de corps étranger, cela rend également plus difficile l'attachement des protéines sériques [2]. Christopher D. Spicer de l'Université de York souligne le problème :
"La forte hydrophilicité du PHEMA le rend bioinert, résistant à l'adhésion des cellules et des protéines" [2].
Contrairement à la matrice extracellulaire native, qui fournit les signaux chimiques nécessaires à la liaison cellulaire, ces matériaux synthétiques manquent de tels indices. En conséquence, les cellules ont tendance à adopter une forme arrondie, indiquant une mauvaise interaction avec le matériau de l'échafaudage [2]. De plus, l'absence de charge de surface suffisante signifie que ces échafaudages ne parviennent pas à exploiter les interactions électrostatiques essentielles pour l'adhésion cellulaire initiale [2].
Fait intéressant, les chercheurs ont découvert que l'ajout de motifs topographiques à l'échelle micrométrique aux surfaces de PHEMA peut aider les cellules souches mésenchymateuses humaines à se propager et à s'allonger, surmontant certaines des limitations du matériau [2]. Spicer note :
"Contrairement à la morphologie arrondie adoptée sur des surfaces planes, indicative de mauvaises interactions avec le matériau sous-jacent, les cellules ont pu se propager et s'allonger en réponse aux signaux topographiques fournis" [2].
Réponse immunitaire et sous-produits de dégradation
Les échafaudages peuvent provoquer des réponses immunitaires, entraînant une encapsulation fibreuse qui isole le matériau [2]. Ce problème est particulièrement prononcé avec les agents de réticulation chimique comme le glutaraldéhyde, connus pour déclencher de fortes réactions inflammatoires. Par exemple, dans les études d'implantation sous-cutanée chez le rat, les éponges réticulées au glutaraldéhyde ont développé des couches tissulaires épaisses (0,85 ± 0,34 mm), tandis que les éponges réticulées avec de la transglutaminase microbienne ont montré des couches beaucoup plus fines (0,19 ± 0,16 mm) [5].
Le moment et les sous-produits de la dégradation de l'échafaudage ajoutent une autre couche de complexité. Les échafaudages à base de polyester, tels que PLA ou PGA, libèrent des monomères acides lorsqu'ils se décomposent, ce qui peut entraîner une augmentation locale du pH et des dommages tissulaires. Comme l'explique Spicer :
"L'accumulation de monomères d'acide glycolique et lactique suite à la dégradation des échafaudages à base de poly(ester) a été montrée pour entraîner une augmentation locale du pH et des dommages tissulaires résultants" [2].
Les échafaudages qui se dégradent trop rapidement perdent leur intégrité structurelle, ce qui est crucial pour l'adhésion cellulaire et le développement tissulaire [5]. Par exemple, après un mois d'implantation, les éponges de gélatine réticulées par EDC n'ont retenu que 2,7 % ± 1,7 % de leur volume, tandis que les éponges réticulées par glutaraldéhyde ont maintenu 69,1 % ± 4,3 % [5]. Même les matériaux considérés comme bioinertes, comme le PEG, peuvent parfois provoquer des réactions immunitaires, telles que le développement d'anticorps anti-PEG chez certains patients, compliquant leur utilisation in vivo [2].
Méthodes de test standard pour la biocompatibilité
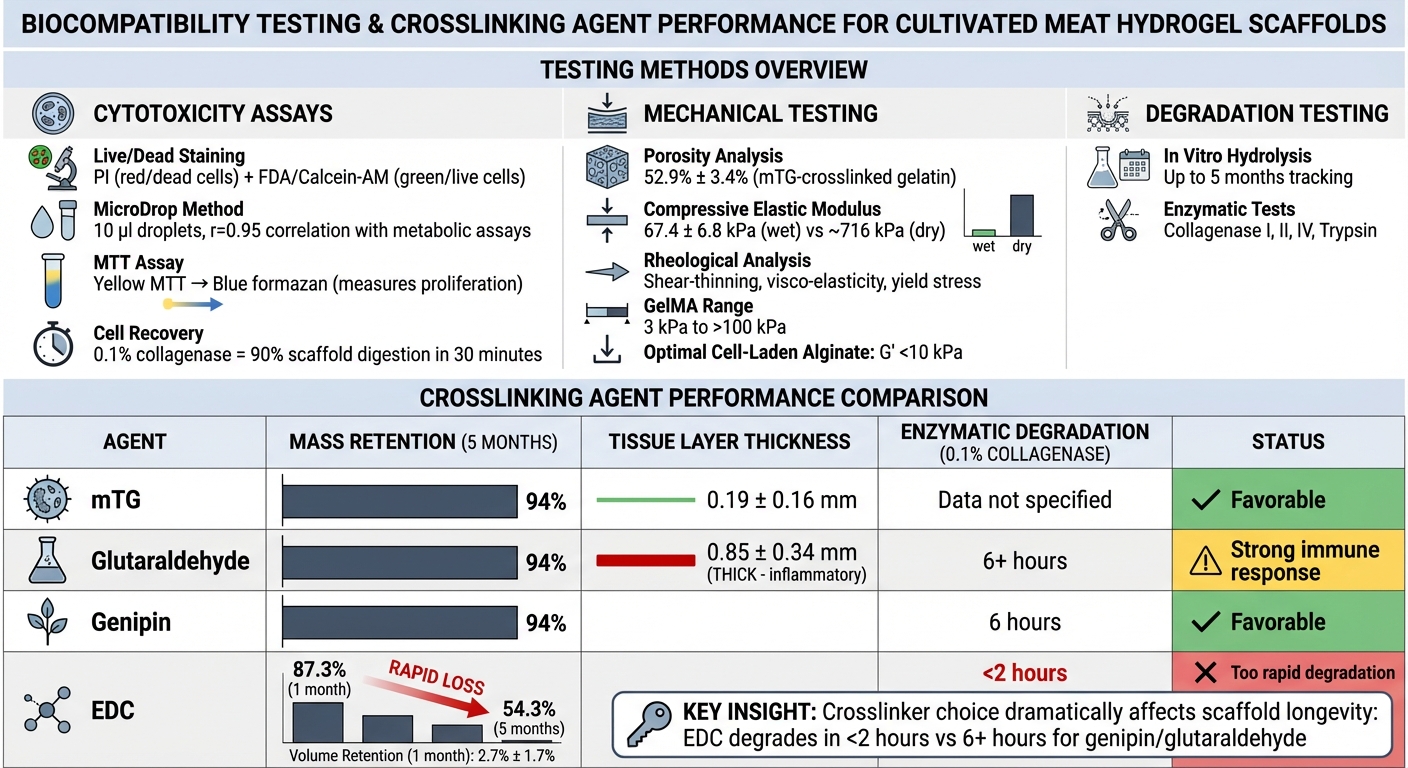
Méthodes de test de biocompatibilité et comparaison des performances de réticulation pour les échafaudages en hydrogel
L'évaluation de la biocompatibilité implique une combinaison de tests de cytotoxicité, d'évaluations des propriétés mécaniques et d'études de dégradation. Ces méthodes rigoureuses garantissent que les échafaudages en hydrogel non seulement soutiennent la croissance cellulaire, mais répondent également aux normes de sécurité et de texture nécessaires pour la viande cultivée.
Essais de cytotoxicité et de viabilité cellulaire
La coloration Live/Dead est une méthode éprouvée pour évaluer la viabilité cellulaire au sein de structures tridimensionnelles d'hydrogel. Ce processus utilise l'iodure de propidium (PI) pour colorer en rouge les noyaux des cellules mortes, tandis que l'acétate de fluorescéine (FDA) ou Calcein-AM met en évidence les cellules vivantes en vert. Cette approche de double coloration offre une visualisation claire de la distribution des cellules à travers la matrice du scaffold [6] [7]. La méthode MicroDrop, qui utilise des gouttelettes de 10 µl, a montré une forte corrélation (r=0,95) avec les essais métaboliques, ce qui en fait une alternative fiable [6].
L'essai MTT est un autre outil précieux, mesurant la prolifération cellulaire et l'activité métabolique.Il fonctionne en convertissant le MTT jaune clair en formazan bleu foncé, offrant un moyen efficace de comparer la croissance cellulaire à long terme à travers divers types d'échafaudages [7] . Cependant, dans les hydrogels visqueux, le test CCK8 peut produire des résultats faussement positifs en raison d'interactions non spécifiques [6] . Pour récupérer les cellules des échafaudages 3D, une solution de collagénase à 0,1% est très efficace, digérant jusqu'à 90% de l'échafaudage en 30 minutes tout en minimisant les dommages cellulaires [7].
Une fois la viabilité cellulaire confirmée, l'étape suivante consiste à évaluer les propriétés structurelles et mécaniques de l'échafaudage.
Test des Propriétés Mécaniques et Structurelles
Les tests mécaniques garantissent que les échafaudages peuvent physiquement soutenir la croissance cellulaire tout en permettant une diffusion adéquate des nutriments. L'analyse de la porosité est essentielle pour maintenir la viabilité cellulaire, car elle assure un mouvement adéquat des nutriments, de l'oxygène et des déchets dans les cultures 3D [1] . Le module élastique en compression à l'état hydraté est utilisé pour mesurer à quel point l'échafaudage imite la texture de la viande conventionnelle. Par exemple, des éponges de gélatine réticulées avec de la transglutaminase microbienne (mTG) ont démontré une porosité de 52,9 % ± 3,4 % et un module élastique en compression de 67,4 ± 6,8 kPa lorsqu'elles sont humides [7] .
Pour les échafaudages bi-imprimés, l'analyse rhéologique joue un rôle clé dans l'évaluation des propriétés telles que le comportement de fluidification par cisaillement, la visco-élasticité et la contrainte de seuil. Ces paramètres garantissent une extrusion fluide pendant l'impression et l'intégrité structurelle après dépôt [3] . Les hydrogels GelMA, par exemple, peuvent être adaptés pour atteindre une rigidité allant d'environ 3 kPa à plus de 100 kPa, selon les exigences tissulaires. Cependant, pour l'alginate chargé de cellules, l'imprimabilité optimale et la viabilité cellulaire sont généralement liées à des valeurs de module de stockage (G') inférieures à 10 kPa [3]. Comme l'ont noté Rency Geevarghese et ses collègues :
"L'imprimabilité, la stabilité et la biocompatibilité ne sont pas indépendantes et doivent être ajustées soigneusement pour se contrebalancer" [3].
Au-delà des propriétés mécaniques immédiates, la stabilité à long terme des échafaudages est tout aussi importante.
Tests de biodégradation et de stabilité à long terme
Pour garantir que les échafaudages restent fonctionnels pendant le développement cellulaire, les tests de dégradation évaluent leur longévité.Les tests d'hydrolyse in vitro suivent la perte de masse sur de longues périodes - jusqu'à cinq mois dans des environnements aqueux - pour évaluer la stabilité [7] . Les tests de dégradation enzymatique, utilisant des protéases comme la Collagénase I, II, IV, et la Trypsine, fournissent des informations supplémentaires sur le comportement des échafaudages dans des conditions biologiques [7].
Le type d'agent de réticulation a un impact significatif sur les taux de dégradation. Par exemple, dans les tests d'hydrolyse, les éponges de gélatine réticulées avec mTG, glutaraldéhyde ou génipine ont conservé 94% de leur masse initiale après cinq mois. En revanche, les éponges réticulées avec EDC ont montré une forte diminution de la stabilité, avec une masse tombant à 87,3% après un mois et seulement 54,3% restant après cinq mois [7]. Lors de la dégradation enzymatique avec 0.1% de collagénase, les éponges EDC se sont presque complètement dissoutes en deux heures, tandis que les éponges réticulées au génipin ont mis six heures à se dégrader complètement [7].
La stabilité mécanique diminue également de manière significative après absorption d'eau. Par exemple, le module élastique en compression des éponges mTG sèches, qui est d'environ 716 kPa, chute à environ 67 kPa lorsqu'elles sont humides [7]. Tester les propriétés mécaniques dans un état hydraté est donc essentiel pour une évaluation précise.
sbb-itb-ffee270
Solutions pour Améliorer la Biocompatibilité des Hydrogels
Lorsque la biocompatibilité des hydrogels est insuffisante, il existe des méthodes éprouvées pour améliorer les performances des échafaudages. Ces approches répondent à des défis tels que la toxicité chimique, la faible adhésion cellulaire et la dégradation rapide, garantissant de meilleures performances des échafaudages dans la production de viande cultivée.L'accent est mis sur l'amélioration de l'attachement cellulaire, l'ajustement des propriétés mécaniques et la gestion des taux de dégradation.
Modifications de surface pour un meilleur attachement cellulaire
Les hydrogels synthétiques, tels que PEG, PVA et PHEMA, sont naturellement bio-inertes, rendant l'attachement cellulaire difficile sans signaux supplémentaires. Une solution courante consiste à incorporer des peptides RGD, qui fournissent les sites de liaison nécessaires aux cellules. La gélatine et son dérivé, GelMA, contiennent naturellement ces peptides, ce qui les rend largement utilisés dans les échafaudages de viande cultivée. Les chercheurs de l'Université de Technologie de Silésie ont souligné ceci :
"La gélatine a été identifiée comme un composant prometteur de bioencre favorisant la croissance cellulaire en raison de la présence de motifs peptidiques d'attachement cellulaire comme RGD (arginine-glycine-acide aspartique)" [3].
D'autres techniques incluent le modelage topographique à l'échelle micrométrique, qui introduit des indices physiques pour encourager la propagation des cellules sur des surfaces autrement plates [2]. Ajuster la charge de surface peut également améliorer les interactions électrostatiques avec les cellules [2]. De plus, les polymères synthétiques peuvent être modifiés avec des motifs bioactifs, tels que RGDS ou IKVAV, pour soutenir plus efficacement la liaison cellulaire [2].
Composition des matériaux et conceptions de structures hybrides
Les structures hybrides combinent la résistance des polymères synthétiques avec la bioactivité des matériaux naturels, répondant aux limitations des conceptions à composant unique.Les polymères synthétiques comme le PEG et le PCL offrent une chimie prévisible et de fortes propriétés mécaniques, tandis que les polymères naturels tels que le collagène, la chitosane et l'alginate fournissent des environnements qui imitent la matrice extracellulaire (ECM), favorisant l'adhésion et la croissance des cellules [9][2].
Par exemple, une étude de 2023 publiée dans Scientific Reports a démontré un échafaudage hybride réalisé en combinant un hydrogel de PEG-gélatine avec un maillage de PCL. Ce design a soutenu la formation d'une couche cellulaire épithéliale serrée en utilisant des cellules MDCK sur neuf jours, le maillage de PCL fournissant un support mécanique pour la membrane d'hydrogel de 100 µm d'épaisseur [8] . De même, une étude de 2012 a montré que l'immobilisation de la gélatine sur des surfaces de films hydrophobes en PCL améliorait l'attachement et la croissance des cellules endothéliales de la veine ombilicale humaine (HUVEC), avec de meilleurs résultats liés à des quantités plus élevées de gélatine immobilisée [10].
L'ajout de carboxyméthylcellulose (CMC) aux encres à base d'alginate peut améliorer à la fois les propriétés mécaniques et la capacité de gonflement grâce à des interactions électrostatiques [3]. Les hydrogels mécaniquement robustes contiennent généralement 0,1 à 10 % de polymère en poids, mais les gels avec des pores plus petits que 10 µm peuvent entraver le mouvement et l'infiltration des cellules [2].
Ces stratégies améliorent non seulement la compatibilité cellulaire, mais permettent également un contrôle précis de la longévité des échafaudages, qui est étroitement liée aux taux de dégradation.
Dégradation contrôlée par ajustements de réticulation
La densité de réticulation joue un rôle clé à la fois dans les taux de dégradation et la rigidité mécanique. Les méthodes de double réticulation, telles que la combinaison de la réticulation ionique (e.g. , utilisant CaCl₂ pour l'alginate) avec la photo-réticulation (e.g. , durcissement UV pour GelMA), offrent un meilleur contrôle sur la stabilité de l'échafaudage. Les liaisons ioniques fournissent un support temporaire, tandis que les liaisons covalentes assurent une structure à long terme [3].
Les hydrogels GelMA peuvent atteindre une large gamme de modules de stockage (G') - de environ 3 kPa à plus de 100 kPa - selon la concentration en polymère et l'exposition aux UV [3]. Pour l'alginate chargé de cellules, des valeurs de G' inférieures à 10 kPa sont souvent optimales pour maintenir l'imprimabilité et la viabilité cellulaire [3]. Inclure des liaisons dégradables, telles que des liaisons disulfure ou des séquences de polyester, permet aux échafaudages de se décomposer en macromères résorbables que les cellules peuvent remplacer par la MEC native [2]. Cependant, les réticulations à base de polyester comme le PLA ou le PGA nécessitent une surveillance attentive du pH, car la libération d'acide glycolique ou lactique peut entraîner des dommages tissulaires dus à l'acidité [2].
L'utilisation de phenyl-2,4,6-triméthylbenzoylphosphinate de lithium (LAP) comme photo-initiateur pour la polymérisation UV est une autre façon d'améliorer la cytocompatibilité par rapport aux méthodes plus anciennes [3][8]. Maintenir un contrôle strict de la température à 37°C et respecter des protocoles de mélange précis assure une réticulation uniforme et une dégradation prévisible [3].
Utilisation de Cellbase pour l'approvisionnement en échafaudages
Trouver les bons échafaudages en hydrogel biocompatibles pour la production de viande cultivée peut être compliqué, surtout lorsqu'on s'appuie sur des fournisseurs de laboratoire généraux qui peuvent manquer d'expertise en matériaux de qualité alimentaire et en conformité réglementaire.
Fournisseurs Vérifiés pour la Viande Cultivée
"L'alginate est idéal car il imite très bien la texture de la viande et est déjà approuvé comme ingrédient alimentaire" [11].
Les fournisseurs répertoriés sur
Processus d'approvisionnement simplifiés
Au-delà des normes vérifiées,
Conclusion
Les tests de biocompatibilité pour les échafaudages en hydrogel dans la production de viande cultivée sont un exercice d'équilibre impliquant plusieurs facteurs interconnectés.Le trilemme "biocompatibilité-imprimabilité-stabilité" souligne comment l'amélioration d'une propriété peut parfois en compromettre une autre. Par exemple, l'utilisation de concentrations élevées de polymères peut améliorer la stabilité structurelle mais peut également augmenter le stress de cisaillement lors de l'extrusion, ce qui pourrait nuire aux cellules [3]. De même, les sous-produits de dégradation de matériaux comme le PLA peuvent affecter négativement les cellules environnantes [2][1].
Les méthodes de test doivent aborder ces interactions complexes pour garantir que les échafaudages répondent aux normes rigoureuses de la production de viande cultivée. Des techniques telles que les essais de cytotoxicité, les évaluations des propriétés mécaniques et les études de dégradation à long terme aident collectivement à garantir que les échafaudages maintiennent la viabilité cellulaire tout au long de leur cycle de vie.Comme l'explique Małgorzata Katarzyna Włodarczyk-Biegun:
"L'imprimabilité, la stabilité et la biocompatibilité ne sont pas indépendantes et doivent être ajustées soigneusement pour se contrebalancer" [3].
Des approches innovantes comme la double réticulation - qui combine des méthodes ioniques et covalentes - peuvent atteindre un module de stockage allant de ~3 kPa à plus de 100 kPa tout en soutenant la viabilité cellulaire [3]. D'autres avancées, telles que les modifications de surface avec des peptides bioactifs comme RGD et les échafaudages hybrides qui mélangent des polymères naturels et synthétiques, améliorent la biocompatibilité. La dégradation contrôlée par une réticulation précise affine encore la performance des échafaudages. Cependant, des défis subsistent, tels que la variabilité d'un lot à l'autre des polymères naturels, qui peut affecter la cohérence dans la production à grande échelle [1]. Ces ajustements techniques sont essentiels pour l'approvisionnement en matériaux répondant aux exigences spécifiques de la production de viande cultivée. En fin de compte, atteindre le bon équilibre des propriétés chimiques, mécaniques et biologiques est la clé du succès des échafaudages en hydrogel.
FAQs
Comment puis-je identifier les résidus toxiques dans un échafaudage en hydrogel ?
Pour repérer les résidus toxiques dans un échafaudage en hydrogel, les tests de biocompatibilité sont essentiels. Ce processus se concentre sur la détection des réponses cytotoxiques, qui indiquent des effets nocifs sur les cellules. Une approche largement utilisée est les essais de cytotoxicité, tels que l'échantillonnage direct des cellules, qui évalue la viabilité et le comportement des cellules.
Les signes à surveiller incluent les dommages à la membrane cellulaire, l'apoptose (mort cellulaire programmée), ou la mort cellulaire. En combinant ces méthodes, vous pouvez détecter et évaluer de manière approfondie tout résidu nocif pouvant entraver la croissance cellulaire.
Quels tests prédisent le mieux l'adhésion cellulaire dans les hydrogels 3D ?
Les essais d'adhésion cellulaire sont un moyen fiable d'évaluer la capacité des cellules à adhérer aux hydrogels 3D. Ces tests mesurent des aspects clés tels que l'attachement et la croissance des cellules sur les échafaudages d'hydrogel, offrant des informations importantes sur la compatibilité du matériau avec les systèmes biologiques.
Comment puis-je ajuster la dégradation de l'échafaudage sans nuire aux cellules ?
Pour ajuster finement la dégradation de l'échafaudage sans compromettre la santé cellulaire, vous pouvez modifier la composition chimique de l'hydrogel. Par exemple, ajuster la densité de réticulation ou incorporer des liaisons biodégradables peut aider à trouver un équilibre entre stabilité et dégradation. L'utilisation de polymères particuliers, comme les hydrogels à base de collagène, offre une autre approche, permettant une dégradation contrôlée pour favoriser la croissance et la différenciation cellulaires. Des ajustements réfléchis garantissent que l'échafaudage se dégrade à un rythme qui soutient les processus cellulaires tout en maintenant les cellules viables.











