La surveillance de la densité cellulaire en temps réel est essentielle pour améliorer la production de viande cultivée. Les méthodes traditionnelles, comme les tests au bleu trypan, sont lentes, sujettes à la contamination et manquent souvent les changements rapides de croissance cellulaire. La mesure en temps réel fournit des données continues, permettant des ajustements précis des nutriments, une détection précoce des problèmes et une qualité de produit constante.
Différentes méthodes analytiques pour la surveillance des cellules vivantes incluent:
- Capteurs de Biocapacitance: Mesurent les cellules viables en détectant les membranes intactes. Les systèmes de fréquence de balayage réduisent les erreurs à 5,5–11%.
- Capteurs de Turbidité Optique: Suivent la densité cellulaire totale par diffusion de la lumière mais ne peuvent pas distinguer les cellules vivantes des cellules mortes.
- Surveillance de l'Impédance RF: Idéal pour les systèmes à haute densité, se concentrant sur les cellules vivantes dans des configurations à micro-porteurs ou immobilisées.
- Spectroscopie Raman: Offre un profilage chimique détaillé, identifiant les cellules viables et les métabolites.
- Spectroscopie NIR: Suit rapidement plusieurs paramètres mais a du mal avec les signaux qui se chevauchent.
Chaque méthode a ses forces et ses limites, rendant l'étalonnage et la validation essentiels pour la précision. Des plateformes comme
Incyte Arc : Surveillance en temps réel de la densité cellulaire viable pour un contrôle de bioprocédé plus intelligent
sbb-itb-ffee270
Technologies pour la mesure en temps réel de la densité cellulaire
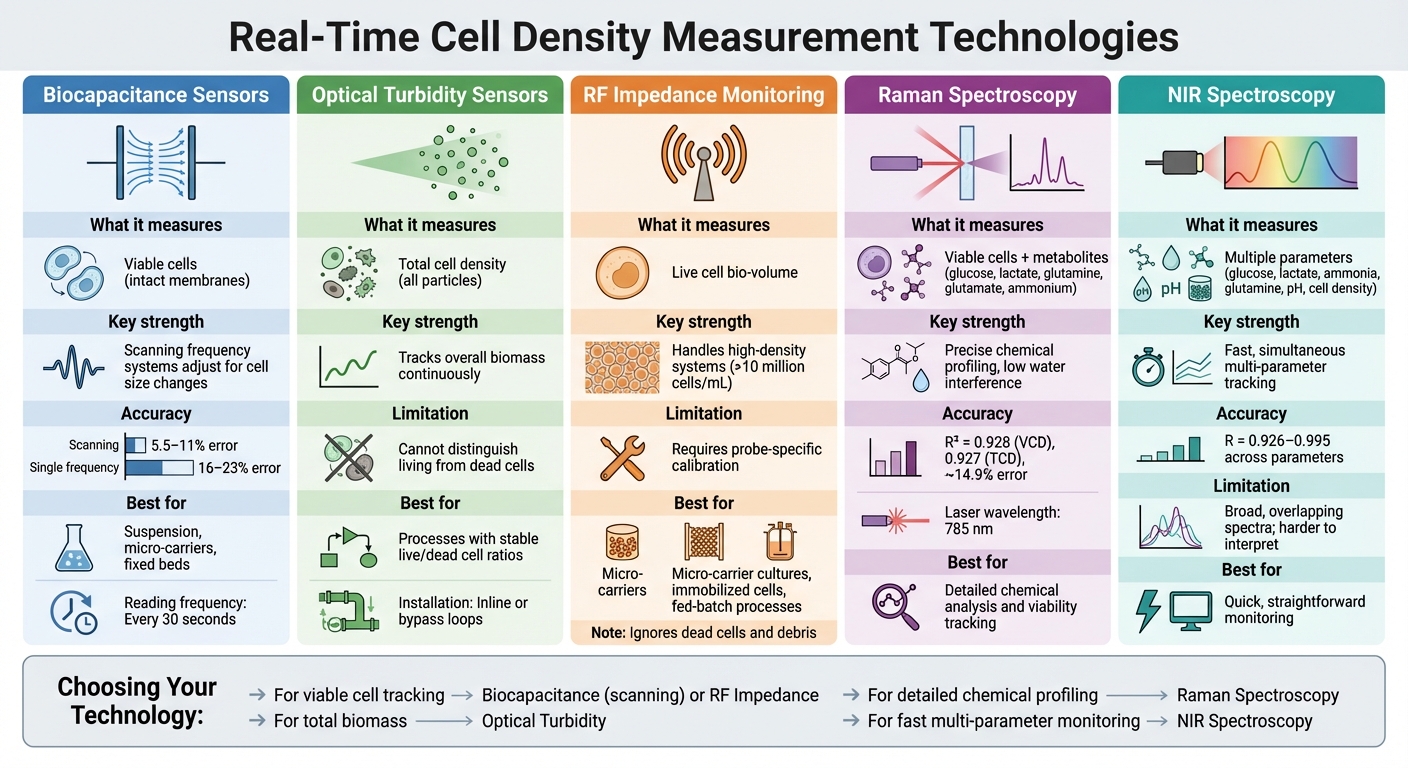
Comparaison des technologies de mesure de la densité cellulaire en temps réel pour la viande cultivée
Pour répondre à la demande de retour d'information continu sur le processus, divers capteurs pour bioréacteurs de viande cultivée permettent désormais une mesure précise en temps réel de la densité cellulaire. Chaque méthode offre une approche unique, répondant soit aux cellules viables, soit à la biomasse totale, selon les besoins spécifiques du processus.
Capteurs basés sur la biocapacitance
Les capteurs de biocapacitance fonctionnent en appliquant un champ électrique à une suspension cellulaire. Les cellules vivantes, avec des membranes intactes, agissent comme de minuscules condensateurs. Leurs membranes empêchent les ions dans le cytoplasme de passer, provoquant une polarisation et créant une charge mesurable.Les cellules mortes, cependant, manquent de membranes intactes et ne contribuent pas au signal[1].
Cette technique repose sur la β-dispersion, où les cellules se polarisent complètement à des fréquences inférieures à 100 kHz, entraînant une permittivité élevée. En balayant une gamme de fréquences (50–20,000 kHz) et en appliquant une analyse multivariée, ces capteurs peuvent corriger les changements de taille des cellules. Cet ajustement réduit les erreurs de mesure de 16–23% à une plage beaucoup plus basse de 5,5–11%[1].
Pour garantir l'exactitude, la sonde doit d'abord être mise à zéro dans un milieu stérile avant l'inoculation, suivie d'une calibration en utilisant la concentration connue de cellules au départ. Des appareils comme l'Aber FUTURA pico s'intègrent parfaitement dans les bioréacteurs, fournissant des lectures fraîches toutes les 30 secondes.Ces capteurs sont très efficaces pour les cellules en suspension, attachées à des micro-porteurs ou immobilisées dans des lits fixes - des scénarios où les méthodes de comptage traditionnelles échouent souvent[1][2].
Pour mesurer la biomasse totale, les méthodes optiques offrent une autre option viable.
Capteurs de Turbidité Optique
Les capteurs de turbidité optique déterminent la densité cellulaire totale en mesurant la lumière diffusée par toutes les particules dans la culture, y compris les cellules vivantes, les cellules mortes et les débris. Bien que ces capteurs ne puissent pas différencier la biomasse viable de la non-viable, ils sont particulièrement utiles lorsque le ratio de cellules vivantes à mortes reste stable tout au long du processus. L'étalonnage implique de corréler les lectures de turbidité avec des comptages cellulaires hors ligne à divers stades de la culture. Ces capteurs peuvent être installés en ligne ou dans des boucles de dérivation, fournissant une surveillance continue pour aider à déterminer le moment optimal de la récolte.
Surveillance d'impédance radiofréquence
La surveillance d'impédance radiofréquence (RF) partage certains principes avec les capteurs de biocapacitance, se concentrant sur la détection des cellules avec des membranes intactes tout en ignorant les cellules mortes et les débris[1][2]. Cette méthode est particulièrement adaptée aux systèmes impliquant des cellules immobilisées ou cultures sur microporteurs, où l'échantillonnage hors ligne peut être difficile. L'impédance RF peut gérer des concentrations de cellules viables dépassant 10 millions de cellules/mL dans les processus en fed-batch, ce qui en fait un choix e
| Technologie | Mesures | Force clé | Limitation |
|---|---|---|---|
| Biocapacitance (Fréquence unique) | Volume de cellules viables | Mise en œuvre simple | Sensible aux changements de diamètre (erreur de 16 à 23%)[1] |
| Biocapacitance (Balayage) | Concentration de cellules viables | S'adapte aux changements de taille (5.5–11% d'erreur)[1] | Nécessite une analyse multivariée |
| Turbidité optique | Densité cellulaire totale | Détecte la biomasse totale | Ne peut pas distinguer les cellules viables des cellules mortes[2] |
| Impédance RF | Bio-volume des cellules vivantes | Fonctionne bien avec les micro-supports et les lits fixes | Nécessite une calibration spécifique à la sonde |
Méthodes spectroscopiques pour l'analyse multi-paramètres
Les méthodes spectroscopiques portent la surveillance des processus à un niveau supérieur en allant au-delà des mesures à paramètre unique comme celles fournies par les capteurs de capacité et de turbidité.Ces techniques analysent comment la lumière interagit avec les molécules dans la culture, offrant des informations en temps réel non seulement sur le nombre de cellules, mais aussi sur les niveaux de nutriments, les concentrations de métabolites et d'autres variables de processus essentielles. En créant des profils chimiques détaillés, elles complètent les capteurs de capacitance et de turbidité, fournissant des données plus riches pour une meilleure prise de décision.
Spectroscopie Raman
La spectroscopie Raman fonctionne en mesurant la diffusion inélastique de la lumière. Lorsqu'un laser (généralement à 785 nm) frappe un échantillon, la lumière diffusée change de longueur d'onde en fonction des liaisons chimiques des molécules qu'elle rencontre. Le profilage chimique précis de cette méthode permet de différencier les cellules viables des cellules mortes et d'identifier des métabolites individuels tels que le glucose, le lactate, la glutamine, le glutamate et l'ammonium - le tout sans perturber le système[3] [5].
Un des principaux avantages de la spectroscopie Raman est sa faible sensibilité à l'eau, une interférence courante dans les méthodes infrarouges. Cela la rend particulièrement bien adaptée aux environnements riches en nutriments que l'on trouve dans la production de viande cultivée[3][5]. La technologie peut être mise en œuvre à l'aide de sondes d'immersion à fibre optique ou en mesurant à travers les hublots des bioréacteurs, garantissant que la stérilité est maintenue tout au long du processus[4][5].
Entre 2010 et 2011, des chercheurs de Bristol-Myers Squibb ont démontré le potentiel de la spectroscopie Raman en ligne dans des bioréacteurs de 500 L. En utilisant un instrument Kaiser Optical Systems RamanRXN3, ils ont développé des modèles de calibration avec des coefficients de détermination (R²) de 0,928 pour la densité cellulaire viable (VCD) et de 0,927 pour la densité cellulaire totale (TCD). L'erreur moyenne était d'environ 14.9 %, comparable à la marge d'erreur de 10 % de la méthode de référence elle-même[3] .
"La spectroscopie Raman... semble être la méthode spectroscopique la plus prometteuse pour l'analyse en ligne de systèmes de culture cellulaire complexes." - Nicholas R. Abu-Absi, Process Sciences, Bristol-Myers Squibb[3]
Pour garantir des résultats précis, le système doit être calibré en utilisant des données hors ligne avec la régression PLS. L'application de la première dérivée et des corrections SNV peut aider à réduire les décalages de base et les interférences de fluorescence[3][4]. À mesure que de nouvelles données deviennent disponibles, les modèles de calibration doivent être mis à jour pour tenir compte des variations entre les séries[3][4]. Pour les applications de viande cultivée, des plateformes comme
Spectroscopie dans le proche infrarouge (NIR)
Alors que la spectroscopie Raman est e
Les systèmes NIR capturent principalement les signaux de densité cellulaire à travers les effets de base causés par la diffusion de la lumière[6]. Dans des études avec des cultures cellulaires HEK293, la NIR a suivi avec succès les populations de cellules viables à des densités de 8,5–9,0 × 10⁶ cellules/mL, avec des coefficients de corrélation allant de 0,926 à 0.995 à travers divers paramètres[6].
Cependant, les spectres NIR sont larges et se chevauchent, ce qui les rend plus difficiles à interpréter par rapport au Raman. Bien que le NIR excelle en vitesse et simplicité, il ne peut égaler la capacité du Raman à différencier la densité cellulaire viable de la densité totale basée sur les différences biochimiques[3]. En fin de compte, le choix entre ces méthodes dépend de vos besoins spécifiques : le NIR est idéal pour une surveillance rapide et simple, tandis que le Raman est meilleur pour une analyse chimique détaillée et le suivi de la viabilité.
Validation et Corrélation des Données en Temps Réel
Corrélation avec les Données Analytiques Hors Ligne
Les capteurs en temps réel nécessitent une calibration précise à l'aide de méthodes de référence hors ligne pour garantir des données fiables. Par exemple, les mesures à fréquence unique sont efficaces pour suivre le volume cellulaire viable, grâce à leur sensibilité aux changements de diamètre cellulaire.
Le balayage de fréquence, qui mesure la permittivité sur une large gamme de fréquences (généralement de 50 à 20 000 kHz), offre une approche plus nuancée. Ces données alimentent l'analyse de données multivariées (MVDA), permettant de différencier les changements de taille et de nombre de cellules. Un étalonnage précis est essentiel pour maintenir la qualité de la production, surtout lors des ajustements de processus en temps réel. Un exemple notable vient d'octobre 2019, lorsque des chercheurs de Sartorius Stedim Biotech ont validé une sonde de capacité en ligne dans des bioréacteurs de 250 mL utilisant des cellules CHO. Ils ont développé un modèle de moindres carrés partiels orthogonaux (OPLS) basé sur des données de cinq cultures standard en fed-batch, en balayant la permittivité à 25 fréquences distinctes. Cette approche a permis au modèle de prédire des concentrations cellulaires viables (VCC) dépassant 10 millions de cellules/mL, le balayage de fréquence réduisant significativement les erreurs par rapport aux données à fréquence unique [7] .
"Le modèle a fourni une prédiction des VCC avec des erreurs relatives de 5,5 à 11 %, ce qui est en bon accord avec le critère d'acceptation basé sur la précision de la méthode de référence hors ligne (environ 10 % d'erreur relative) et fortement amélioré par rapport aux résultats à fréquence unique (16 à 23 % d'erreur relative)." – Springer Nature [7]
Pour affiner davantage la précision, l'application d'un filtre de Savitzky-Golay (deuxième ordre) aide à minimiser le bruit du signal avant la comparaison. De plus, effectuer un étalonnage en un point au stade de l'inoculation améliore la précision du capteur [7]. Ces étapes posent collectivement les bases d'une validation fiable dans divers scénarios opérationnels.
Protocoles de Validation
Une fois l'étalonnage traité, une validation rigoureuse garantit que le processus reste fiable. Une méthode efficace est la validation Leave-One-Batch-Out (LOB). Cela implique de créer plusieurs modèles en excluant systématiquement un lot du jeu de données d'entraînement et en l'utilisant comme ensemble de test pour évaluer la performance prédictive.
Les essais de robustesse sont une autre étape critique. Dans l'étude de 2019, les chercheurs ont introduit des déviations de processus délibérées, telles qu'une étape de dilution de 30 % et des stratégies d'alimentation modifiées, pour tester la fiabilité du modèle MVDA dans des conditions non standard. Même avec ces variations, le modèle a fourni des prédictions précises, avec des erreurs relatives comprises entre 6,7 % et 13,2 %. Ce niveau de fiabilité est particulièrement crucial pour la production de viande cultivée, où la variabilité du processus est courante lors de la montée en échelle.
Enfin, définissez des critères d'acceptation réalistes qui s'alignent avec la marge d'erreur inhérente de 10 % des méthodes hors ligne comme les essais au bleu trypan. L'utilisation d'entrées standardisées de viande cultivée peut également aider à stabiliser ces bases.En établissant un seuil d'erreur relative de 10 % pour les capteurs en temps réel, vous assurez une validation par rapport à une norme pratique plutôt que de poursuivre des niveaux de précision inatteignables [7].
Intégration de la surveillance en temps réel dans le contrôle des processus
Développement de modèles de capteurs logiciels
Une fois l'étalonnage effectué, l'étape cruciale suivante consiste à intégrer les sorties des capteurs dans le contrôle des processus. Après avoir validé les capteurs en temps réel, l'accent est mis sur le développement de modèles de capteurs logiciels. Ces modèles transforment les données brutes des capteurs en informations exploitables, souvent à l'aide d'algorithmes tels que les moindres carrés partiels (PLS) ou les moindres carrés partiels orthogonaux (OPLS). Ces méthodes aident à relier des signaux en ligne complexes, tels que le balayage de capacité multi-fréquence, à des indicateurs critiques du processus comme la concentration cellulaire viable (VCC).
Pour construire ces modèles, vous aurez besoin de données en ligne et hors ligne appariées.Les étapes de prétraitement - comme la centration moyenne et la mise à l'échelle - sont essentielles avant d'entraîner le modèle avec des données de culture standard. Un exemple notable provient de Sartorius Stedim Cellca GmbH, où les chercheurs ont utilisé une sonde pico FUTURA d'Aber Instruments avec des cultures de cellules CHO. Leurs modèles prédictifs ont atteint des erreurs relatives comprises entre 5,5 % et 11 %, une nette amélioration par rapport aux mesures à fréquence unique, qui montrent généralement des erreurs allant de 16 % à 23 % [7].
Le déploiement de ces modèles permet des ajustements de processus automatisés. Par exemple, dans la production de viande cultivée utilisant des micro-supports ou des lits fixes, les capteurs d'impédance à radiofréquence offrent un avantage unique. Ils soutiennent l'alimentation dynamique en nutriments et l'élimination des déchets, basées sur le volume cellulaire viable. Comme John P. Carvell et Jason E.Dowd a souligné :
"L'impédance RF est utilisée pour surveiller la concentration de cellules vivantes immobilisées sur des micro-porteurs ou des lits fixes dans des processus cGMP où les méthodes traditionnelles de comptage de cellules vivantes hors ligne sont inexactes ou impossibles à réaliser" [2].
Ce niveau d'intégration non seulement améliore le contrôle des processus, mais prépare également le terrain pour répondre aux cadres réglementaires, qui sont explorés ensuite.
Alignement avec les cadres PAT
Dans la production de viande cultivée, la combinaison de la surveillance en temps réel avec la Technologie Analytique de Procédé (PAT) et les principes de Qualité par la Conception (QbD) assure à la fois la conformité réglementaire et l'efficacité opérationnelle. Le processus commence par l'identification des Attributs Critiques de Qualité (CQA) et des Paramètres Critiques de Procédé (CPP). Cela nécessite une collaboration interfonctionnelle entre les équipes de R&D, d'assurance qualité et de réglementation [8]. Une approche par étapes fonctionne le mieux : définir des objectifs clairs, sélectionner les outils appropriés, réaliser des analyses des modes de défaillance, intégrer avec les systèmes SCADA/MES, former le personnel, et passer à l'échelle avec validation [8].
Par exemple, en janvier 2026, une entreprise biopharmaceutique mondiale a appliqué avec succès cette stratégie intégrée PAT lors d'un transfert de technologie à travers les continents. Les résultats ? Taux de déviation des lots à l'échelle commerciale inférieurs à 2 % et une réduction de 30 % des délais de disposition des lots par rapport aux campagnes précédentes [8].
Le passage à la Vérification Continue des Processus (CPV) déplace l'accent des tests rétrospectifs vers un contrôle proactif et en temps réel. Les capteurs de biocapacitance, par exemple, surveillent la densité cellulaire viable et la cinétique de croissance tout en gérant les apports en nutriments. Cette approche non seulement répond aux normes CPV mais approfondit également la compréhension des processus [8]. L'ingénieur en chimie et bioprocédés Akanksha Prasad l'a bien résumé:
"PAT n'est plus quelque chose de simplement agréable à avoir. Il est devenu la base pour fabriquer des médicaments de nouvelle génération de manière sûre, efficace et à grande échelle" [8].
Ce même principe s'applique à la production de viande cultivée. Une croissance cellulaire constante et une qualité de produit exigent une approche rigoureuse du contrôle des processus et de la conformité.
Pour ceux du secteur de la viande cultivée, des plateformes comme
Considérations Pratiques pour la Mise en Œuvre
Choisir la Bonne Technologie
Le choix du bon système de surveillance dépend de vos objectifs de mesure spécifiques.Par exemple, les capteurs de capacité à fréquence unique sont souvent liés au Volume Cellulaire Viable (VCV) plutôt qu'à la Concentration Cellulaire Viable (VCC). Cela est dû au fait que leur signal reflète à la fois le nombre de cellules et les changements de taille des cellules, ce qui peut parfois entraîner des lectures gonflées - en particulier lorsque les cellules sont stressées ou vieillissantes.
En revanche, les systèmes de balayage de fréquence mesurent la capacité sur une gamme de fréquences (généralement de 50 à 20 000 kHz). Ces systèmes s'appuient sur des modèles multivariés pour séparer les changements de taille des cellules de la densité cellulaire réelle, réduisant ainsi considérablement les erreurs de prédiction par rapport aux systèmes à fréquence unique.
L'impédance radiofréquence reste un choix populaire en raison de son coût abordable et de sa sensibilité aux cellules viables. Les cellules mortes et les impuretés ne se polarisent pas, ce qui signifie qu'elles n'interfèrent pas avec le signal.Lors du choix d'un système, réfléchissez à la facilité avec laquelle il s'intègre dans des environnements de bioréacteurs stériles et s'il fonctionne avec bioréacteurs à usage unique vs réutilisables. Les technologies avancées, comme la spectroscopie Raman ou la capacité de balayage en fréquence, nécessitent des approches de modélisation multivariée (e.g. , OPLS ou PLS) pour interpréter leurs ensembles de données complexes [7].
Pour les producteurs de viande cultivée, des plateformes telles que
Une fois que vous avez choisi un système, un étalonnage précis et un dépannage efficace sont essentiels pour maintenir des mesures fiables.
Étalonnage et Dépannage
Pour garantir des lectures précises, commencez par mettre à zéro la sonde de capacité dans un milieu stérile avant l'inoculation.Cette étape garantit que seuls les changements liés à la croissance sont détectés. Ensuite, effectuez un étalonnage en un point en alignant le décalage de trajectoire en ligne avec votre concentration cellulaire d'inoculation connue. Pour des prédictions fiables, entraînez des modèles multivariés en utilisant des données provenant d'au moins cinq cultures standard pour tenir compte des variations telles que les différents lots de milieu. L'application d'un filtre de Savitzky–Golay (deuxième ordre polynomial) peut aider à réduire le bruit du signal et à lisser les fluctuations. Bien que les systèmes en ligne soient puissants, les mesures hors ligne quotidiennes restent essentielles. Si les résultats hors ligne dévient au-delà d'un seuil défini (e.g. , 0,05 unités pour le pH), réétalonnez votre système en ligne [7].
La dérive du signal est un autre défi, souvent causé par des changements de diamètre cellulaire dus à des limitations nutritionnelles, au stress ou au vieillissement. Les systèmes de balayage multifréquence peuvent y remédier en utilisant une analyse multivariée pour tenir compte de ces variations.
Les méthodes de référence hors ligne, telles que les essais au bleu trypan, ont généralement une erreur de mesure d'environ 10 %. Plutôt que d'attendre une déviation nulle, validez la précision de votre système en ligne par rapport à cette marge. De plus, la mise en œuvre de modèles d'évolution par lots (BEM) peut aider à établir des trajectoires de "lot d'or". Ces modèles agissent comme des alarmes automatisées, signalant les déviations de processus en temps réel [7].
Conclusion
La surveillance en temps réel de la densité cellulaire est devenue un élément essentiel de la production de viande cultivée. Le suivi continu des concentrations cellulaires viables offre des avantages clairs : réduction des coûts de milieu grâce à l'alimentation automatisée, identification rapide des déviations de processus et minimisation des risques de contamination. Comme l'a souligné une équipe de recherche, "VCC est fortement lié aux titres de produit et est également considéré comme un attribut de processus.La surveillance du VCC permet l'optimisation et le contrôle des processus qui conduisent à des titres plus élevés et à des processus efficaces" [1].
Le paysage technologique d'aujourd'hui offre plusieurs solutions fiables. Parmi elles, les systèmes de balayage de fréquence combinés à des modèles multivariés se distinguent par une précision comparable aux méthodes hors ligne.
Pour mettre en œuvre ces systèmes efficacement, une planification minutieuse est essentielle. Le succès dépend d'une calibration robuste à travers plusieurs séries d'entraînement et d'une vérification hors ligne cohérente.
Pour les producteurs de viande cultivée recherchant des outils de surveillance spécifiques à la lignée cellulaire,
À mesure que les opérations se développent, la valeur des données en temps réel augmente. Les modèles d'évolution par lots vous permettent de définir des trajectoires de "lot d'or", identifiant automatiquement les écarts avant qu'ils ne puissent affecter la qualité du produit [1] . Ce changement transforme la surveillance de la densité cellulaire en un atout stratégique pour améliorer les processus et réduire les risques.
FAQs
Quel capteur devrais-je utiliser pour la densité cellulaire viable par rapport à la biomasse totale?
Les capteurs de capacitance sont une excellente option pour mesurer la densité cellulaire viable car ils détectent la capacitance générée par les membranes cellulaires polarisées.Cela les lie directement à la présence de cellules vivantes, permettant une surveillance en temps réel efficace.
Cela dit, ces capteurs ne sont pas les mieux adaptés pour mesurer la biomasse totale. Puisqu'ils se concentrent principalement sur les cellules vivantes, ils ne prennent pas en compte les cellules mortes ou la biomasse globale. Pour la densité cellulaire viable, cependant, les capteurs de capacité restent la solution de choix.
Comment calibrer et valider une sonde de capacité en ligne ?
Pour calibrer une sonde de capacité en ligne, commencez par utiliser des concentrations cellulaires connues obtenues à partir de méthodes hors ligne comme le comptage cellulaire. Cela vous permet de faire correspondre les lectures de capacité avec les nombres réels de cellules. La validation implique de tester la sonde sous différentes densités cellulaires et conditions de milieu pour confirmer son exactitude et sa cohérence. Il est également crucial d'effectuer des vérifications régulières de la calibration par rapport aux mesures hors ligne, en particulier lors de l'augmentation de la production ou de la modification des conditions de milieu.Cela garantit que la sonde continue de fournir des mesures fiables de la densité cellulaire viable.
Comment transformer les signaux en ligne en capteurs logiciels pour le contrôle de l'alimentation ?
Pour transformer les signaux en ligne en capteurs logiciels pour le contrôle de l'alimentation dans la production de viande cultivée, vous pouvez vous appuyer sur des données de capteurs en temps réel, telles que le balayage de fréquence de la capacitance. En traitant ces signaux à travers des modèles multivariés, vous pouvez estimer des paramètres critiques comme la densité cellulaire viable.
Les capteurs basés sur la capacitance jouent un rôle clé ici. Ils mesurent la capacitance de la membrane cellulaire, qui reflète directement la santé cellulaire. Lorsque ces sorties de capteurs sont intégrées dans des algorithmes de contrôle, il devient possible d'automatiser les ajustements de nutriments, maintenant des conditions de croissance idéales tout au long du processus.











