La production de viande cultivée est limitée par la croissance lente des cellules et la sénescence précoce dans les lignées cellulaires primaires par rapport aux lignées immortalisées. L'édition génétique CRISPR offre des solutions ciblées pour surmonter ces défis.
Voici les cinq principales cibles CRISPR et leurs rôles dans l'amélioration de la prolifération cellulaire, de la différenciation et de l'évolutivité pour la viande cultivée :
- Myostatine (MSTN) : Stimule la croissance des cellules musculaires en supprimant les limites naturelles de croissance.
- P53 (TP53) : Prolonge la durée de vie des cellules et augmente les taux de prolifération, bien qu'il puisse réduire la différenciation.
- HIF1A : Aide les cellules à survivre dans des environnements pauvres en oxygène, essentiel pour les cultures denses en bioréacteurs.
- Facteurs Régulateurs Myogéniques (MYOD1, MYOG) : Favorise la formation et l'alignement des cellules musculaires.
- CDKN2A : Contourne la sénescence, permettant une prolifération cellulaire à long terme.
Ces cibles abordent des problèmes clés tels que la sénescence réplicative, les faibles rendements et la dépendance au sérum. Cependant, équilibrer la prolifération avec la différenciation et garantir la sécurité sont essentiels pour réussir.
Comparaison rapide :
| Cible CRISPR | Avantage clé | Défis |
|---|---|---|
| Myostatine (MSTN) | Favorise la croissance musculaire | Risque d'effets hors cible ; problèmes de viabilité |
| P53 (TP53) | Prolonge la durée de vie, stimule la prolifération | Réduction de la différenciation ; préoccupations de sécurité |
| HIF1A | Soutient la survie en faible oxygène | Nécessite une édition précise pour éviter les perturbations |
| MYOD1, MYOG | Améliore la formation musculaire | Équilibrer la prolifération et la différenciation |
| CDKN2A | Permet la prolifération à long terme | Risques hors cible ; nécessite un milieu sans sérum |
La technologie CRISPR redéfinit la production de viande cultivée, visant des rendements plus élevés et des coûts de production réduits tout en répondant aux préoccupations éthiques.
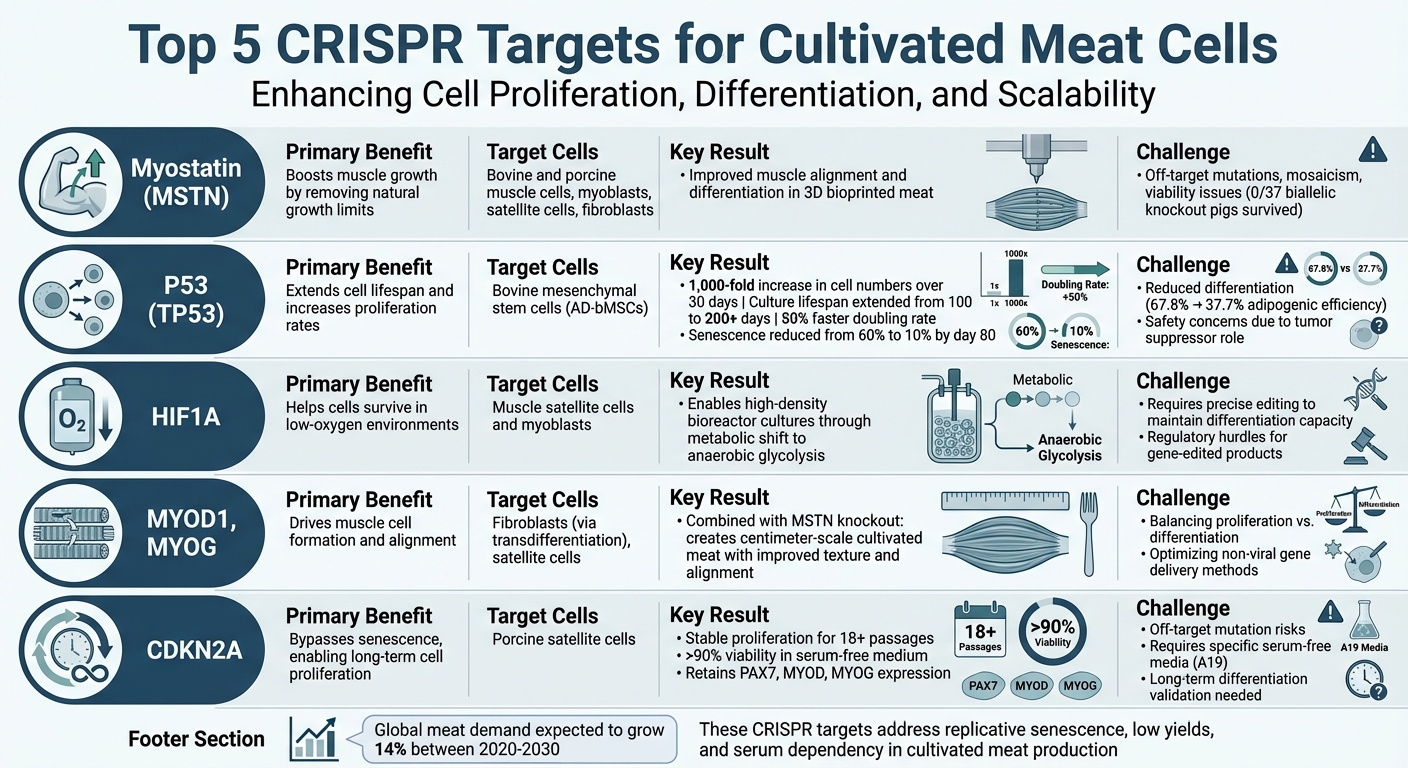
Les 5 principales cibles CRISPR pour la viande cultivée : comparaison des avantages et des défis
1. Gène de la myostatine (MSTN)
Supprimer le frein naturel à la croissance musculaire est possible en éliminant le gène MSTN. Ce processus favorise la prolifération et la différenciation accrues des cellules musculaires à la fois par hyperplasie et hypertrophie [5] [6].
Avantage principal
En mars 2025, des chercheurs de l'Université nationale de Séoul ont fait des progrès significatifs en combinant des cellules bovines avec knockout MSTN avec l'impression 3D par traitement numérique de la lumière. Cette approche a amélioré l'alignement et la différenciation des muscles, aboutissant à de la viande cultivée avec des caractéristiques similaires à celles du steak traditionnel [5] .
Plus tôt, en mai 2022, des scientifiques de l'Université Northwest A&F en Chine ont utilisé un système de livraison CRISPR/Cas9 optimisé (100 ng/μL d'ARNm Cas9 et 200 ng/μL de sgRNAs) pour créer des moutons knockout homozygotes MSTN. Sur 16 agneaux nés, quatre ont été confirmés comme knockouts homozygotes. Ces agneaux ont montré des poids corporels significativement plus élevés à 30, 60 et 90 jours par rapport à leurs homologues non modifiés, tout en maintenant des paramètres de qualité de la viande tels que le pH, la graisse intramusculaire et les niveaux de protéines brutes [6] .
Applicabilité du type de cellule
L'édition du gène MSTN améliore le potentiel myogénique de divers types de cellules, y compris les myoblastes primaires, les cellules satellites, les fibroblastes (par trans-différenciation dirigée par MYOD1) et les cellules souches mésenchymateuses. Cela est réalisé en surmontant les limites naturelles de la prolifération cellulaire [5][1].
Défis potentiels
Malgré ses avantages, MSTN knockout n'est pas sans complications. Il a été lié à des problèmes de viabilité chez les animaux vivants et à des obstacles techniques tels que des mutations hors cible et le mosaïcisme. Par exemple, une étude de juin 2022 a rapporté que bien que les porcs édités MSTN aient montré une croissance musculaire accrue, aucun des 37 porcs knockout bialléliques n'a survécu [7][8][6].
"Le knockout de MSTN améliore la production de viande cultivée de type steak médiée par MYOD1." [5]
Ensuite, nous explorerons le gène suppresseur de tumeur P53 et son importance pour assurer une prolifération cellulaire soutenue.
sbb-itb-ffee270
2. Gène Suppresseur de Tumeur P53
Désactiver le gène TP53 supprime les points de contrôle critiques du cycle cellulaire, ce qui accélère considérablement la prolifération cellulaire.P53 joue un rôle central en tant que suppresseur de tumeur, initiant l'arrêt du cycle cellulaire et la sénescence en réponse au stress cellulaire. Sans ce point de contrôle, les cellules peuvent accumuler de la biomasse beaucoup plus rapidement et maintenir des périodes de culture plus longues [1].
Avantage Principal
Début 2025, Communications Biology a publié une étude mettant en lumière les effets transformateurs de l'édition de TP53 sur les cellules souches mésenchymateuses bovines. Les résultats étaient frappants : une augmentation de 1 000 fois du nombre de cellules sur 30 jours et une durée de culture prolongée de 100 à plus de 200 jours. Les cellules modifiées ont montré un taux de doublement cellulaire 50 % plus rapide et, au jour 80, les niveaux de sénescence ont chuté de manière significative - d'environ 60 % dans les cellules non modifiées à seulement 10 % dans les cellules modifiées.De plus, ces cellules ont conservé un profil d'expression génique "plus jeune", marqué par une réplication de l'ADN améliorée et une synthèse protéique soutenue, reflétant les cellules de passage précoce [1].
Applicabilité du type de cellule
Les cellules souches mésenchymateuses dérivées du tissu adipeux bovin (AD‑bMSCs) sont particulièrement bien adaptées aux modifications TP53. Ces cellules rencontrent naturellement la sénescence réplicative, ce qui limite leur potentiel d'expansion. Étant donné que les cellules souches mésenchymateuses représentent environ 25 % des sources cellulaires utilisées dans la production de viande cultivée, l'édition TP53 offre une solution pratique, équilibrant leur capacité à rester multipotentes avec une évolutivité industrielle [1].
Défis potentiels
Cependant, cette approche n'est pas sans défis. Un inconvénient majeur est la capacité de différenciation réduite.L'étude Communications Biology a rapporté une diminution de l'efficacité de la différenciation adipogénique, passant de 67,8 % dans les cellules non éditées à 37,7 % dans les clones knockout TP53. L'analyse transcriptomique a révélé une augmentation de l'activité des gènes du cycle cellulaire mais une diminution des gènes liés à la différenciation musculaire et à l'adhésion. De plus, puisque TP53 est un suppresseur de tumeur crucial et que son inactivation est une caractéristique du cancer, cette stratégie soulève des préoccupations en matière de sécurité et de réglementation. Bien que ces cellules soient destinées à la consommation plutôt qu'à un usage médical, de telles questions méritent une attention particulière [1].
"Parmi tous les candidats, le knockout TP53 a produit l'effet le plus prononcé, avec une augmentation de plus de 1 000 fois en abondance d'ici le jour 30."
- Communications Biology [1]
Ensuite, explorons une autre cible CRISPR importante.
3.Hypoxia-Inducible Factor 1-Alpha (HIF1A)
HIF1A joue un rôle crucial en aidant les cellules de viande cultivée à s'adapter à des environnements pauvres en oxygène souvent rencontrés dans des bioréacteurs avec capteurs intégrés. Ce régulateur devient particulièrement important lorsque la pénétration de l'oxygène est limitée. En utilisant CRISPR pour stabiliser HIF1A, les cellules peuvent maintenir la production d'énergie et rester viables, même sous des niveaux d'oxygène réduits.
Avantage Principal
L'édition de HIF1A reprogramme le métabolisme cellulaire, le faisant passer de la respiration dépendante de l'oxygène à la glycolyse anaérobie. Ce changement garantit que les cellules continuent à produire de l'énergie dans des conditions hypoxiques. Le résultat ? La capacité de cultiver des cellules à des densités plus élevées sans risque de privation d'oxygène. C'est un changement radical pour l'augmentation de la production de viande cultivée, surtout lors de la création de constructions tissulaires plus épaisses.
Applicabilité du type de cellule
Les cellules satellites musculaires et les myoblastes bénéficient le plus des modifications HIF1A. Ce sont les acteurs clés du développement des fibres musculaires, et leur survie dans des bioréacteurs densément peuplés est cruciale pour atteindre des rendements élevés. La stabilisation de HIF1A permet à ces cellules de changer efficacement de voies métaboliques, garantissant leur viabilité même pendant de longues périodes de culture.
Défis potentiels
Un défi majeur est de s'assurer que les cellules modifiées conservent leur capacité à se différencier en fibres musculaires fonctionnelles après plusieurs passages. Cela nécessite un ajustement technique pour éviter toute perte de capacité de différenciation. Au-delà du laboratoire, les obstacles réglementaires et la perception du public ajoutent de la complexité. Les produits carnés modifiés génétiquement doivent passer des évaluations de sécurité approfondies pour la consommation humaine et l'impact environnemental avant de pouvoir être commercialisés.En attendant, l'acceptation des consommateurs de tels produits varie considérablement selon les régions [3]. Ces défis soulignent la nécessité de perfectionner les techniques d'édition génétique avant de s'étendre à de nouvelles cibles. Ensuite, nous explorerons les gènes qui améliorent davantage la différenciation myogénique.
4. Facteurs Régulateurs Myogéniques (MRFs : MYOD1, MYOG)
MYOD1 joue un rôle critique dans l'engagement des cellules dans la lignée myogénique, tandis que MYOG facilite la fusion des myoblastes en myotubes matures. Fait intéressant, la surexpression de MYOD1 peut reprogrammer les fibroblastes en cellules myogéniques, contournant efficacement les limites de sénescence naturelle observées dans les cellules satellites primaires [5].
Bénéfice Principal
Lorsque la surexpression de MYOD1 est combinée avec le knockout de MSTN dans les fibroblastes bovins, et intégrée avec l'impression 3D DLP sur hydrogels à motifs de rainures de 100 µm, les résultats sont impressionnants.Cette approche améliore l'alignement et la différenciation musculaires, permettant la création de structures de viande cultivée à l'échelle du centimètre. Une étude publiée en mars 2025 dans le Journal of Animal Science and Biotechnology a mis en avant cette méthode, utilisant la livraison non virale de MYOD1 en parallèle avec l'inactivation de MSTN médiée par CRISPR pour concevoir des fibroblastes bovins [5]. En éliminant les signaux inhibiteurs sur la différenciation musculaire, cette stratégie oriente les cellules vers une identité myogénique plus forte, résultant en une viande cultivée avec une meilleure texture. Cette approche duale souligne l'importance de l'équilibre précis entre les voies de prolifération et de différenciation.
Applicabilité selon le type de cellule
Les fibroblastes sont un e
Défis Potentiels
L'un des principaux obstacles est de trouver le bon équilibre entre la prolifération et la différenciation des cellules. Par exemple, les modifications génétiques visant à augmenter l'expansion cellulaire - comme l'inactivation de TP53 - peuvent involontairement supprimer des facteurs clés de différenciation musculaire, ce qui pourrait entraver la capacité des cellules à mûrir en tissu musculaire fonctionnel [1]. De plus, bien que des méthodes non virales telles que le système de transposon Piggybac soient préférées pour des raisons de sécurité alimentaire, elles nécessitent une optimisation minutieuse pour assurer une livraison efficace des gènes. Les facteurs externes, comme les micro-rainures imprimées en 3D, restent essentiels pour obtenir un alignement correct des fibres musculaires [5] .
5. Régulateurs du cycle cellulaire (e.g. , CDKN2A)
CDKN2A joue un rôle clé dans le déclenchement de la sénescence, arrêtant efficacement la division cellulaire. En utilisant CRISPR/Cas9 pour éliminer CDKN2A, les chercheurs peuvent contourner la limite de Hayflick. Cela permet aux cellules souches musculaires de continuer à se diviser bien au-delà de leur durée de vie habituelle tout en conservant leur capacité à se différencier en tissu musculaire fonctionnel. Cette avancée relève l'un des plus grands défis de la production de viande cultivée : produire les quantités massives de cellules viables et fonctionnelles nécessaires à la fabrication à l'échelle industrielle.
Avantage Principal
Cibler CDKN2A aborde directement le problème de la prolifération cellulaire limitée dans la production de viande cultivée.
L'édition de CDKN2A améliore l'évolutivité et réduit les coûts. Par exemple, en juin 2025, une équipe de recherche de l'Université Agricole de Nanjing, dirigée par Shijie Ding, Chunbao Li, et Guanghong Zhou, a publié leurs résultats dans Food Materials Research. Ils ont réussi à développer des lignées de cellules satellites porcines éditées par CRISPR avec un knockout de CDKN2A. Ces cellules ont démontré une prolifération stable pendant plus de 18 passages dans un milieu sans sérum A19, avec des taux de viabilité dépassant 90%. De manière importante, les cellules ont conservé l'expression des régulateurs myogéniques clés (PAX7, MYOD, et MYOG) et se sont différenciées en myotubes matures, positifs pour MyHC.Lorsqu'elles sont ensemencées sur des échafaudages 3D à base de plantes, ces cellules modifiées ont formé des structures semblables à de la viande avec une amélioration de la mastication et de la gommeux [2].
"Les cellules knockout CDKN2A basées sur CRISPR fournissent une source renouvelable de progéniteurs musculaires, réduisant la dépendance aux biopsies animales répétées." – Food Materials Research [2]
Applicabilité du type de cellule
Cellules satellites porcines, qui sont cruciales pour la régénération musculaire, répondent particulièrement bien à l'édition CDKN2A. Cette approche présente également un potentiel pour d'autres espèces de bétail. Un avantage clé des cellules éditées CDKN2A est leur compatibilité avec des formulations de milieux sans sérum. Cela élimine le besoin de sérum de veau fœtal coûteux et éthiquement controversé, réduisant la variabilité entre les lots et minimisant les risques de contamination [2].
Défis Potentiels
Bien que l'étude de Nanjing ait mis en évidence des avantages significatifs, il existe des défis pour des applications plus larges de CRISPR dans la viande cultivée. Les mutations hors cible restent une préoccupation et doivent être soigneusement surveillées. De plus, les normes de sécurité réglementaires pour les produits alimentaires génétiquement modifiés doivent être rigoureusement respectées. Les chercheurs doivent également garantir une différenciation à long terme pour s'assurer que le produit final ressemble étroitement au tissu musculaire naturel. Cela rend le raffinement des protocoles et la validation approfondie des échafaudages 3D essentiels [2].
Ces résultats, ainsi que d'autres cibles CRISPR, sont résumés dans le tableau de comparaison suivant.
Tableau de Comparaison
Tableau : Ce qui suit résume les cinq cibles CRISPR qui améliorent la prolifération cellulaire, la différenciation et l'adaptation métabolique pour une production évolutive de viande cultivée.
| Cible CRISPR | Bénéfice Principal | Types de Cellules Cibles | Défis | |
|---|---|---|---|---|
| Myostatine (MSTN) | Augmente la croissance musculaire | Cellules musculaires bovines et porcines | Nécessite une compréhension génomique détaillée ; risque de changements phénotypiques non intentionnels si non géré avec soin [4] | |
| P53 (TP53) | Augmente considérablement la prolifération ; retarde le vieillissement réplicatif (augmentation de plus de 1 000 fois de l'abondance cellulaire au jour 30) [1] | Cellules souches mésenchymateuses bovines (bMSCs) | Capacité de différenciation réduite ; la différenciation adipogénique passe de 67,8% à 37. | 7 % ; régulation négative des gènes liés aux muscles [1] |
| HIF1A | Améliore l'adaptation métabolique | Cellules bovines et porcines | Nécessite une édition minutieuse pour éviter les perturbations métaboliques [4] | |
| MRFs (MYOD1, MYOG) | Essentiel pour la formation et la régénération des fibres musculaires | Cellules satellites porcines (cellules souches musculaires) [2] | Difficile de maintenir des niveaux d'expression élevés pendant une expansion rapide pour une mise à l'échelle industrielle [2] | |
| CDKN2A | Soutient une prolifération stable sur plus de 18 passages avec >90 % de viabilité ; contourne le vieillissement [2] | Cellules satellites porcines (cellules souches musculaires) [2] | Nécessite un milieu sans sérum spécifique (e.g. , A19) pour préserver la pluripotence et la différenciation sur une culture à long terme [2] |
Choisir les bonnes cibles implique de trouver un équilibre entre la prolifération cellulaire et la capacité à se différencier efficacement. Cela souligne l'importance de peaufiner ces processus dans l'ingénierie cellulaire de la viande cultivée.
Conclusion
La technologie CRISPR offre un potentiel immense pour relever les défis critiques de la production de viande cultivée, y compris la prolifération cellulaire limitée, la sénescence et les coûts de production élevés. Par exemple, l'inactivation de TP53 a montré qu'elle augmentait l'abondance cellulaire de plus de 1 000 fois en seulement 30 jours [1]. De même, les modifications de CDKN2A permettent aux cellules de proliférer de manière stable sur 15 à 18 passages avec plus de 90 % de viabilité dans des conditions sans sérum [2] . Cela réduit la dépendance au sérum animal coûteux et minimise le besoin de biopsies animales répétées.
Cependant, trouver le bon équilibre entre la prolifération cellulaire rapide et la capacité à se différencier en tissu musculaire reste un défi majeur. Bien que l'élimination de TP53 augmente considérablement le nombre de cellules, elle peut entraver la différenciation. Par conséquent, maintenir le rôle de régulateurs comme MYOD1 et MYOG est crucial pour générer un tissu musculaire mature adapté à la viande cultivée.
Pour les équipes de recherche visant à appliquer ces stratégies génétiques,
Avec une demande mondiale de viande qui devrait croître de 14 % entre 2020 et 2030 [1] , ces cibles CRISPR ouvrent la voie à des solutions évolutives et rentables dans la production de viande cultivée.
FAQs
Quelle cible CRISPR stimule le plus la croissance sans affecter la différenciation ?
La meilleure cible CRISPR pour améliorer la croissance tout en maintenant la différenciation est le système de cellules satellites génétiquement modifiées sans sérum. Cette méthode soutient une croissance cellulaire cohérente et une différenciation efficace, ce qui en fait un choix solide pour la production de viande cultivée à grande échelle.
Comment les modifications TP53 ou CDKN2A peuvent-elles être sécurisées pour la viande cultivée ?
Pour s'assurer que les modifications TP53 ou CDKN2A sont sûres pour la viande cultivée, plusieurs étapes importantes sont suivies. Celles-ci incluent des tests approfondis de stabilité génétique, l'établissement de systèmes de banque cellulaire structurés, et l'utilisation d'outils avancés tels que le séquençage de nouvelle génération pour détecter toute mutation. En plus de cela, le respect strict des lignes directrices de conformité réglementaire garantit à la fois la sécurité et la cohérence tout au long du processus de production.
Quelles modifications aident les cellules à prospérer dans des bioréacteurs à faible teneur en oxygène et à haute densité ?
Développer des milieux sans sérum adaptés avec le bon mélange de nutriments, de facteurs de croissance, de lipides, d'acides aminés non essentiels et d'antioxydants joue un rôle clé dans la stimulation de la prolifération et de la différenciation cellulaires. Ces ajustements non seulement soutiennent une meilleure viabilité cellulaire mais améliorent également la fonctionnalité, surtout dans des conditions difficiles comme les environnements à faible teneur en oxygène et à haute densité.











