- Objectif: Assure que les bioréacteurs répondent aux normes réglementaires et de production, en maintenant la stérilité, un contrôle environnemental précis, et la sécurité alimentaire.
- Caractéristiques principales: Les bioréacteurs à cuve agitée ont été choisis pour leur adéquation aux cellules musculaires bovines, offrant des forces de cisaillement contrôlées et une évolutivité.
- Défis: La mise à l'échelle des bioréacteurs pour des densités cellulaires élevées et la réduction des coûts ont nécessité de repenser les matériaux, les méthodes de stérilisation et la conception des processus.
- Solutions: Le passage à des matériaux de qualité alimentaire, l'utilisation de méthodes de stérilisation rentables et l'intégration de logiciels de contrôle bioprocédés pour l'optimisation des processus ont permis de réduire considérablement les coûts.
- Résultats: Les coûts de production ont chuté de manière spectaculaire, avec une augmentation de la productivité par 15 et jusqu'à 92% de réduction des émissions de gaz à effet de serre lorsqu'ils sont alimentés par des énergies renouvelables.
Cette étude décrit comment les protocoles de validation et les choix de conception intelligents rapprochent la viande cultivée de la parité de prix avec la viande conventionnelle.
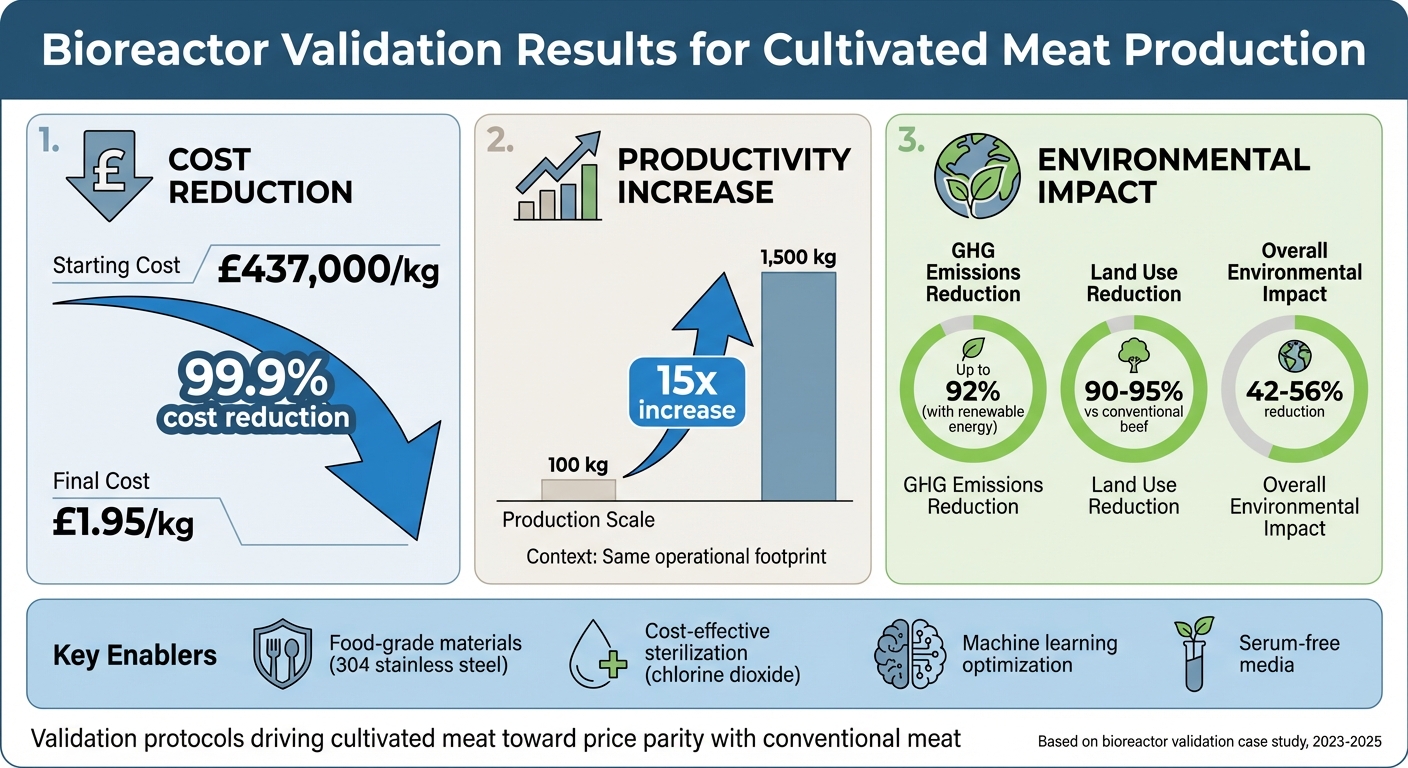
Impact de la Validation des Bioréacteurs : Réduction des Coûts et Avantages Environnementaux dans la Production de Viande Cultivée
Exigences Réglementaires pour la Validation des Bioréacteurs
Normes Réglementaires Applicables
Dans l'industrie de la viande cultivée, respecter des normes réglementaires strictes est une partie essentielle du processus de validation des bioréacteurs. Au Royaume-Uni, la Food Standards Agency (FSA) et Food Standards Scotland (FSS) classent la viande cultivée sous "produits d'origine animale" (POAO). Cette classification garantit que les réglementations en matière de sécurité alimentaire et d'hygiène s'appliquent à toutes les étapes de production, y compris les opérations des bioréacteurs.Cependant, selon les directives britanniques (décembre 2025), bien que ces produits relèvent de la catégorie POAO, ils ne se qualifient pas légalement comme "viande". Cette distinction signifie que certaines exigences conventionnelles en matière de bien-être animal et de microbiologie sont exclues, façonnant les protocoles de validation spécifiques nécessaires au Royaume-Uni.
À l'échelle mondiale, les évaluations de sécurité varient en durée. Singapour et les États-Unis terminent généralement les examens en 12 mois, tandis que l'Union européenne prend en moyenne environ 18 mois. Le Royaume-Uni a tracé sa propre voie avec le CCP Sandbox Programme, financé jusqu'en février 2027. Cette initiative permet aux régulateurs de collaborer directement avec des entreprises telles que Gourmey, Hoxton Farms, et Mosa Meat, en rationalisant les exigences en matière de données et en accélérant les évaluations de sécurité.
"Le programme sandbox nous permet d'accélérer les connaissances réglementaires pour réduire les obstacles aux technologies alimentaires émergentes sans compromettre les normes de sécurité."
– Dr. Thomas Vincent, Directeur adjoint de l'Innovation, FSA [3]
Indépendamment de la juridiction, les entreprises doivent soumettre des dossiers de sécurité détaillés avant d'entrer sur le marché. Ces dossiers décrivent les processus de production, la composition des produits et les données de sécurité. Ils doivent également confirmer que la viande cultivée est nutritionnellement comparable à la viande conventionnelle, y compris des analyses des macro- et micronutriments, ainsi que des profils d'acides aminés et d'acides gras.
Exigences du protocole de validation
Les normes réglementaires exigent des protocoles de validation de bioréacteur rigoureux pour garantir des opérations sûres et contrôlées. Un élément clé est la mise en œuvre d'un plan d'Analyse des Dangers et Points Critiques pour leur Maîtrise (HACCP).Ce cadre identifie et atténue les risques à chaque étape de la production, depuis la biopsie cellulaire initiale jusqu'à la récolte finale de la masse cellulaire. Étant donné la nouveauté de la production de viande cultivée, les évaluations de sécurité doivent aborder les dangers potentiels tout au long du processus.
Les protocoles de validation doivent prouver que les systèmes de bioréacteurs maintiennent des conditions stériles pendant les cycles de production, empêchant efficacement la contamination microbienne. De plus, ces protocoles doivent évaluer si les protéines de la viande cultivée pourraient déclencher des réactions allergiques chez les consommateurs.
"Notre nouvelle orientation apporte de la clarté aux entreprises, les aidant à comprendre et à démontrer correctement aux régulateurs alimentaires britanniques comment leurs produits sont sûrs. Plus précisément, cette orientation garantit que les entreprises ont évalué les risques allergéniques potentiels et qu'ils sont nutritionnellement appropriés avant de pouvoir être autorisés à la vente."
– Dr. Thomas Vincent, Directeur adjoint de l'Innovation, FSA [2]
Au Royaume-Uni, la validation se concentre sur la fourniture de données suffisantes pour une évaluation scientifique des risques plutôt que sur l'octroi d'une autorisation de mise sur le marché. Nicolas Morin-Forest, Co-fondateur & PDG de GOURMEY, a souligné cette distinction :
"La validation de la Grande-Bretagne marque une étape critique dans notre parcours réglementaire des nouveaux aliments et confirme que nous progressons maintenant vers une évaluation complète des risques, nous rapprochant ainsi de la mise à disposition de nos produits aux consommateurs." [4]
sbb-itb-ffee270
Sélection du bioréacteur et spécifications du système
Technologie de bioréacteur sélectionnée
L'installation a opté pour un bioréacteur à cuve agitée, un choix motivé par sa performance fiable avec des cellules progénitrices de muscle bovin. Les facteurs clés influençant cette décision comprenaient les besoins spécifiques des cellules, l'échelle de production souhaitée et les considérations de coût globales.
Les cellules musculaires bovines, étant dépendantes de l'ancrage, nécessitent de faibles forces de cisaillement - inférieures à 0,1 N/m² - pour éviter les dommages pendant la culture. Le design du réacteur agité répondait à cette exigence tout en se révélant adaptable à la fois pour les expériences à l'échelle pilote et la production commerciale. Le coût était un autre facteur majeur, les unités à l'échelle pilote étant positionnées comme plus accessibles pour les budgets typiques du secteur de la viande cultivée que dans l'industrie pharmaceutique[5][7].
L'échelle de production visait des volumes entre 100 et 1 000 litres pour assurer la faisabilité commerciale. Les systèmes modulaires à réacteur agité ont été choisis par rapport aux alternatives à lit fixe en raison de leur capacité à augmenter l'échelle par un facteur de 10 sans dépasser les limites de transfert de masse, maintenant des valeurs de kLa supérieures à 50 h⁻¹.Ces systèmes visent à produire 1–10 kg de viande cultivée par lot tout en équilibrant l'investissement en capital pour une capacité évolutive [7][8].
Caractéristiques de Conception du Système
Une fois le bioréacteur à cuve agitée sélectionné, sa conception a intégré des fonctionnalités avancées pour favoriser une croissance cellulaire optimale. Le système d'échange de gaz utilise la technologie de micro-diffuseur, délivrant des bulles entre 20–100 µm. Cette configuration atteint des valeurs de kLa de 100–200 h⁻¹ à 37°C, maintenant les niveaux d'oxygène dissous à 30–50% de saturation. Pour gérer le dépouillement du CO₂, l'aération de l'espace de tête est combinée avec des contacteurs à membrane et des capteurs anti-mousse[5][6].
Pour un mélange efficace, le bioréacteur utilise des double turbines Rushton, fonctionnant à des vitesses de 50–150 tr/min.Cela garantit un mélange uniforme avec des taux de cisaillement inférieurs à 5 000 s⁻¹, protégeant les cellules des dommages tout en maintenant les gradients de nutriments sous 10 %. L'agitation est contrôlée par PID, avec un retour d'information en temps réel sur les niveaux de pH et d'oxygène dissous, soutenant des taux de perfusion de 1 à 5 volumes de réacteur par jour[5][7].
La scalabilité était un point clé de la conception. Le bioréacteur maintient une similarité géométrique à différentes échelles, respectant un rapport hauteur-diamètre de 2:1. Les turbines optimisées par CFD assurent une montée en échelle linéaire, et les tests pilotes ont montré une rétention de 95 % de la viabilité cellulaire lors du passage de 10 litres à 200 litres. La conception modulaire permet une intégration dans des systèmes de production plus grands tout en respectant les normes de conformité GxP [7][8].
La technologie analytique de procédé est également intégrée, avec la spectroscopie Raman pour la surveillance en temps réel de paramètres critiques tels que le pH (6,8–7,2) et le lactate (maintenu en dessous de 2 g/L). Des modèles prédictifs, adaptés de la production d'anticorps monoclonaux, suivent les niveaux de glucose avec des valeurs de R² supérieures à 0,95, garantissant un contrôle précis du processus[5] [6][7].
Ces fonctionnalités améliorent non seulement la culture cellulaire mais répondent également aux normes de validation rigoureuses requises par les organismes de réglementation du Royaume-Uni.
Exécution du Protocole de Validation
Procédures de Validation Principales
Pour garantir l'intégrité opérationnelle, un protocole de validation approfondi a été réalisé, incorporant des caractéristiques de conception avancées. La surveillance en temps réel a joué un rôle clé, avec des capteurs de technologie analytique de procédé (PAT) suivant en continu des paramètres critiques tels que l'oxygène dissous, le pH et les niveaux de CO₂ pendant chaque cycle de culture[6] . Le processus a commencé avec des cellules ensemencées à une densité de 1×10⁵ cellules/mL, cultivées pendant une semaine dans un milieu contenant 3 g/L de glucose. La spectroscopie Raman a été utilisée pour surveiller les niveaux de lactate et de glucose tout au long[5].
L'analyse du stress de cisaillement a confirmé que les forces d'agitation restaient en dessous de 0,1 Pa, qui est la limite critique pour les cellules musculaires bovines. Les tests post-stress ont démontré que la viabilité cellulaire restait au-dessus de 90%[6].
Les tests de stérilité ont été étendus à toutes les matières premières, avec une attention particulière aux milieux de culture. Les fournisseurs devaient fournir des certificats d'analyse, vérifiés par des tests tiers, conformément aux normes des installations britanniques.Le protocole comprenait des immunoessais ELISA pour détecter les endotoxines des bactéries gram-négatives, ainsi que la cytométrie en flux pour identifier les contaminants en fonction de la taille, de la forme et des propriétés de fluorescence des cellules[9] .
Méthodes d'optimisation des processus
Une fois la stabilité du système confirmée, les efforts se sont concentrés sur le raffinement du processus en utilisant des analyses avancées. Les algorithmes d'apprentissage automatique ajustaient dynamiquement les débits de milieu et les vitesses d'agitation en fonction des données PAT continues. Ces modèles, entraînés sur des ensembles de données de plans d'expériences (DoE), ont identifié des stratégies d'alimentation rentables en corrélant les mesures de permittivité avec la qualité de la biomasse[6] . Cette approche était particulièrement efficace pendant la phase de prolifération, où des taux de croissance constants sont cruciaux pour la production commerciale.
La spectroscopie Raman, initialement développée pour la production d'anticorps monoclonaux, a été adaptée avec succès pour les applications de viande cultivée. Sa spécificité d'analyte a permis à l'installation d'adopter des protocoles de validation établis tout en maintenant la précision nécessaire pour la surveillance en temps réel tout au long du cycle de culture[5].
Défis techniques et solutions
Problèmes de mise à l'échelle et de productivité
Passer des bioréacteurs des laboratoires à la production commerciale n'a pas été une mince affaire. L'installation visait à produire 10–100 kg de viande cultivée, nécessitant un nombre énorme de 10¹²–10¹³ cellules pour atteindre cet objectif [11]. Cependant, atteindre des densités cellulaires élevées s'est avéré être un obstacle significatif.Bien que les bioréacteurs à fibres creuses puissent théoriquement atteindre des densités de 10⁸ à 10⁹ cellules/mL [13], les conceptions de bioréacteurs conventionnels n'ont pas répondu aux attentes pour la production de viande cultivée.
Matt McNulty, un chercheur associé du GFI, a expliqué la racine du problème : "Les bioréacteurs utilisés dans la viande cultivée sont encore largement adaptés des conceptions alimentaires et pharmaceutiques conventionnelles. Ces conceptions ne sont pas spécifiquement adaptées aux besoins de production de viande cultivée et entraînent donc des coûts plus élevés en raison des inefficacités de cette inadéquation" [12]. Cette inadéquation entre la conception et l'objectif a nécessité une révision complète de l'équipement et des processus.
Solutions mises en œuvre et données de performance
Pour relever ces défis, l'installation a retravaillé son équipement et ses protocoles pour s'aligner plus étroitement sur les exigences spécifiques de la production de viande cultivée.L'une des principales modifications a consisté à passer des normes de qualité pharmaceutique aux normes de qualité alimentaire. Par exemple, l'équipe a remplacé les cuves en acier inoxydable 316 par des alternatives en acier inoxydable 304, qui répondaient aux exigences de sécurité alimentaire tout en réduisant considérablement les coûts d'investissement [12]. De plus, le processus traditionnel de stérilisation sur place à la vapeur a été remplacé par un traitement au dioxyde de chlore gazeux. Cet ajustement a permis l'utilisation de cuves à parois plus fines fabriquées à partir de matériaux alternatifs, réduisant ainsi davantage les coûts [12].
Une autre mesure d'économie a consisté à passer de l'eau de qualité pharmaceutique à de l'eau de qualité alimentaire classée comme "Généralement reconnue comme sûre" (GRAS) pour la préparation des milieux [12]. L'équipe a également introduit des microporteurs et des échafaudages comestibles, qui non seulement ont résolu les problèmes de détachement cellulaire mais ont également respecté les réglementations de sécurité alimentaire [11].
Pour optimiser davantage les opérations, l'installation a mis en œuvre des systèmes de capteurs multiplexés. Ces capteurs ont fourni des données de performance en temps réel, qui pouvaient être utilisées dans des applications d'apprentissage automatique pour affiner les processus [12]. Collectivement, ces changements ont eu un impact spectaculaire sur les coûts de production, les réduisant considérablement [10]. Cette réduction remarquable des coûts souligne comment l'alignement des protocoles de production avec les normes réglementaires peut atteindre une échelle commerciale sans sacrifier la sécurité ou la qualité.
Résultats de Validation et Impact sur l'Industrie
Résultats de Performance Mesurés
Grâce à des tests rigoureux, le système a démontré un saut impressionnant en productivité. En utilisant la technologie de bioréacteur continu sans bulles, la productivité de la croissance cellulaire a augmenté de 15 fois, augmentant la production de 100 kg à 1 500 kg - le tout dans le même espace opérationnel[16]. Lors de l'étape de différenciation, des ajustements pour optimiser la biomasse cellulaire ont conduit à une augmentation de 128%, ce qui a considérablement réduit l'impact environnemental global de 42–56%. La transition du métabolisme des cellules C2C12 à CHO a également joué un rôle important dans la réduction des impacts environnementaux, atteignant des réductions allant jusqu'à 67% lorsqu'elle est alimentée par des sources d'énergie renouvelables[14]. Encore plus frappant, l'utilisation d'énergie renouvelable a réduit les émissions de gaz à effet de serre jusqu'à 92% et réduit l'utilisation des terres de 90–95% par rapport aux méthodes traditionnelles de production de bœuf [15] [16]. Ces résultats ouvrent la voie à une adoption plus large dans l'industrie.
Contributions aux pratiques de l'industrie
Les résultats de validation ont redéfini les normes pour la conception de bioréacteurs et la conformité réglementaire dans la production de viande cultivée. En montrant que les normes de qualité alimentaire peuvent remplacer efficacement celles de qualité pharmaceutique sans compromettre la sécurité, le processus a introduit une feuille de route économique pour l'industrie. Par exemple, passer de l'acier inoxydable 316 à 304, combiné à la stérilisation au dioxyde de chlore et à l'utilisation d'eau classée GRAS, a considérablement réduit les coûts d'investissement tout en maintenant la conformité.
Au-delà de la faisabilité technique prouvée, ces avancées modifient les références de l'industrie. Les modèles économiques suggèrent que le traitement continu par rapport au traitement en lots pourrait offrir 55% d'économies sur les coûts d'investissement et d'exploitation sur une décennie [1]. Pour les équipes d'approvisionnement, des plateformes comme
Conclusion
Principales Conclusions
Cette analyse met en évidence comment la production de viande cultivée peut progresser vers le succès commercial en faisant des choix d'équipement judicieux et en affinant les protocoles opérationnels. Opter pour des matériaux de qualité alimentaire comme l'acier inoxydable 304 au lieu de l'acier inoxydable 316 plus coûteux garantit la sécurité et la conformité tout en réduisant les coûts. Le passage à des milieux sans sérum, tel que validé par l'Agence Alimentaire de Singapour avec l'approbation des formulations de GOOD Meat au début de 2023, élimine les défis éthiques et financiers liés aux intrants d'origine animale[15].
Le passage à la production avec des réacteurs à levage pneumatique, en particulier à 260 000 L, a montré un fort potentiel pour réduire les coûts par rapport aux réacteurs à cuve agitée de 42 000 L[17]. Cependant, atteindre des densités cellulaires élevées - jusqu'à 2 × 10⁸ cellules/mL - nécessite des systèmes de perfusion avancés pour gérer les déchets métaboliques comme l'ammoniac et le lactate. L'optimisation des processus s'est avérée essentielle pour relever ces défis[11]. Pour les équipes d'approvisionnement, des plateformes telles que
Développements futurs
Avec l'efficacité des coûts et le contrôle des processus validés, l'accent est désormais mis sur les bioréacteurs à méga-échelle, qui promettent de redéfinir l'économie de la production.L'annonce de GOOD Meat en mai 2022 d'une installation comprenant dix bioréacteurs de 250 000 L - capables de produire 13 700 tonnes métriques de poulet et de bœuf cultivés par an - marque un passage significatif des projets pilotes à la production à l'échelle industrielle[11][15]. Cela s'aligne avec le critère économique établi par Patrick G. Negulescu et al. de l'Université de Californie, Davis:
"Pour être directement compétitifs avec le bœuf, les produits CM, ou du moins le coût de production, doivent baisser à un niveau commercialement compétitif"[17]
Les projections indiquent que cet objectif est à portée de main, surtout que les coûts des médias continuent de diminuer davantage.
Des innovations telles que les microporteurs comestibles et les systèmes hybrides, qui combinent l'expansion et la différenciation des cellules dans un seul récipient, devraient simplifier les processus de validation et réduire les risques de contamination. Les protocoles décrits dans cette étude de cas offrent un modèle reproductible pour les entreprises qui augmentent leurs opérations, prouvant que des tests rigoureux peuvent coexister avec une réduction des coûts. À mesure que davantage d'installations adoptent ces méthodes validées, l'industrie de la viande cultivée se rapproche de la parité des prix avec la viande traditionnelle. Parallèlement, le secteur offre des avantages environnementaux notables, notamment jusqu'à 92 % de réduction des émissions de gaz à effet de serre lorsqu'il est alimenté par des sources d'énergie renouvelables[15].
Récapitulatif des bioréacteurs : capteurs, modélisation, mise à l'échelle et conception alternative de réacteurs
FAQs
Quelles preuves les régulateurs attendent-ils dans un dossier de validation de bioréacteur pour la viande cultivée ?
Les organismes de réglementation exigent des dossiers de validation de bioréacteur pour confirmer que les systèmes fonctionnent dans des paramètres définis. Cela implique d'assurer une performance de processus cohérente et une surveillance en temps réel des facteurs clés tels que les niveaux de pH, l'oxygène dissous, et la température. De plus, les tests de stérilité jouent un rôle crucial dans la prévention de la contamination. Le respect de normes telles que ISO 14644-1 et EU GMP Annexe 1 est obligatoire pour maintenir le contrôle microbien et respecter les pratiques de fabrication stériles.
Comment un bioréacteur à cuve agitée peut-il être mis à l'échelle sans nuire aux cellules musculaires bovines?
La mise à l'échelle d'un bioréacteur à cuve agitée pour la production de viande cultivée implique la gestion du stress de cisaillement , qui peut nuire aux cellules musculaires bovines. Pour y remédier, des outils comme la dynamique des fluides computationnelle (CFD) et les modèles de réduction d'échelle sont utilisés pour prédire les schémas d'écoulement. Ces informations guident les ajustements de la conception de l'agitateur et des vitesses d'agitation, aidant à réduire les dommages cellulaires.
Il est tout aussi important d'assurer une distribution uniforme des nutriments et de l'oxygène. Des systèmes de surveillance avancés, combinés à des techniques de mélange efficaces, sont essentiels pour créer des conditions cohérentes. Cette approche aide à minimiser le stress localisé et soutient la santé cellulaire tout au long de la production à grande échelle.
Quels changements de validation de réduction des coûts ont le plus grand impact sur l'économie unitaire ?
L'adoption de bioréacteurs à usage unique a un effet notable sur la réduction des coûts mesurés en £/kg. Bien que ces systèmes réduisent les investissements initiaux en capital et les dépenses de main-d'œuvre, ils entraînent des coûts de consommables plus élevés. De plus, l'introduction de la surveillance en temps réel et des technologies de recyclage des milieux améliore l'efficacité opérationnelle. Ces avancées non seulement rationalisent les processus mais conduisent également à des économies de coûts à long terme.











