Le criblage CRISPR à haut débit transforme le secteur de la viande cultivée en permettant des modifications génétiques précises pour améliorer la performance des lignées cellulaires. Voici ce que vous devez savoir:
- Défi clé: La production de viande cultivée nécessite des lignées cellulaires qui croissent efficacement, résistent au vieillissement et se différencient en tissus musculaires et adipeux.
- Rôle de CRISPR: En ciblant des milliers de gènes simultanément, ces plateformes identifient les modifications génétiques qui améliorent la croissance, retardent la sénescence et soutiennent la différenciation.
- Résultats notables: Des études ont montré que l'inactivation de gènes comme TP53 et PTEN dans les cellules souches mésenchymateuses bovines peut augmenter la prolifération jusqu'à 1 000 fois en 30 jours et prolonger leur durée de vie de 100 à 200 jours.
- Applications: Les outils CRISPR tels que les criblages par knockout, CRISPRi et CRISPRa sont utilisés pour optimiser la croissance cellulaire, réguler l'expression génique et équilibrer la prolifération avec la différenciation.
- Outils de l'industrie: Des techniques avancées comme RMCE, RNA-seq et les plateformes unicellulaires intègrent les résultats CRISPR avec des données multi-omiques, garantissant des améliorations précises et évolutives.
Pour les ingénieurs en bioprocédés et les professionnels de la R&D, ces innovations répondent aux goulets d'étranglement critiques dans la mise à l'échelle des processus de viande cultivée tout en maintenant la qualité et la fonctionnalité des cellules. L'intégration de CRISPR avec des systèmes automatisés et des ressources adaptées comme
Principes fondamentaux de CRISPR-Cas9 pour les criblages de knockout à l'échelle du génome
Comment fonctionne CRISPR-Cas9 dans l'édition de gènes à grande échelle
Le système CRISPR-Cas9 repose sur une nucléase Cas9 associée à un ARN guide simple (sgRNA) pour cibler des séquences d'ADN spécifiques. Une fois que le sgRNA dirige Cas9 vers l'emplacement génomique souhaité, l'enzyme crée une cassure double brin dans l'ADN. Cette cassure est principalement réparée par jonction d'extrémités non homologues (NHEJ), un processus sujet aux erreurs qui introduit souvent de petites insertions ou délétions (indels). Ces indels peuvent provoquer des mutations de décalage de cadre, perturbant ainsi efficacement la fonction du gène ciblé [1]. Ce mécanisme précis est la base pour réaliser des criblages de knockout à l'échelle du génome, qui sont essentiels pour identifier les régulateurs critiques du comportement cellulaire.
Pour le dépistage à grande échelle, les chercheurs utilisent une bibliothèque diversifiée de sgRNAs, généralement introduite dans une population cellulaire mixte par transduction lentivirale. Pour s'assurer que chaque cellule ne reçoit qu'une seule altération génétique, une faible multiplicité d'infection (MOI d'environ 0,3) est maintenue [1]. Au fil du temps, les cellules avec des mutations avantageuses ont tendance à proliférer plus efficacement que les autres, un phénomène observé dans une variété de types cellulaires et de conditions expérimentales.
Des méthodes de livraison alternatives, telles que l'échange de cassette médié par recombinase (RMCE), offrent une précision supplémentaire en ciblant des "zones d'atterrissage" génomiques spécifiques pour réduire la variabilité des sites d'intégration. Par exemple, une étude utilisant des cellules CHO-K1 a employé une méthode RMCE sans virus pour cribler 111 651 gRNAs uniques à travers 21 585 gènes. Cette approche a identifié des gènes essentiels pour la condition physique des cellules sur des périodes de 16 et 37 jours [7].
Avantages du dépistage à l'échelle du génome
Les criblages par inactivation à l'échelle du génome tirent parti de la précision de CRISPR-Cas9 pour étudier systématiquement des milliers de gènes. Cela permet aux chercheurs de découvrir des gènes qui influencent la survie cellulaire, la croissance et les réponses au stress. Au-delà des facteurs génétiques, l'optimisation de la fonctionnalisation de surface est essentielle pour améliorer l'attachement et la croissance des cellules dans ces systèmes. Une telle exploration impartiale est particulièrement pertinente pour la production de viande cultivée, où les cellules souches mésenchymateuses (qui représentent environ 25 % des sources cellulaires) rencontrent souvent des défis tels qu'une prolifération limitée et une sénescence précoce [1].
sbb-itb-ffee270
Méthodes de criblage de bibliothèques CRISPR groupées
Construction de bibliothèques CRISPR groupées
Les bibliothèques CRISPR groupées commencent par une collection soigneusement sélectionnée d'ARN guides simples (sgRNAs).Dans le contexte de la recherche sur la viande cultivée, les bibliothèques ciblées sont souvent conçues pour se concentrer sur des familles de gènes spécifiques, telles que les facteurs de transcription ou les régulateurs de la prolifération cellulaire. Cette approche aide à équilibrer le coût avec l'évolutivité tout en gardant l'accent sur les traits pertinents pour le phénotype souhaité [1].
Le processus commence par la synthèse d'oligonucléotides sous forme de pool, leur amplification via PCR, et leur clonage dans un vecteur de livraison. Par exemple, une bibliothèque spécifique aux bovins construite au début de 2025 comprenait 3 000 sgRNA ciblant 603 gènes pour identifier les facteurs influençant l'expansion des cellules souches [1]. À plus grande échelle, les criblages à l'échelle du génome peuvent atteindre une complexité beaucoup plus élevée. Un exemple est un criblage de cellules d'ovaire de hamster chinois (CHO), qui a utilisé 111 651 gRNA uniques pour cibler 21 585 gènes [7].
La transduction lentivirale est couramment utilisée pour délivrer ces bibliothèques à une faible multiplicité d'infection (environ 0,3), garantissant que chaque cellule subit une seule modification génétique [1]. Alternativement, des méthodes sans virus comme l'échange de cassette médié par recombinase (RMCE) intègrent la bibliothèque de gRNA dans des "zones d'atterrissage" génomiques prédéterminées au sein d'une lignée cellulaire maîtresse. Cette technique atteint une couverture de gRNA de 99,9% avec un biais minimal [7].
Pour maintenir une fiabilité statistique, les chercheurs assurent une couverture élevée - typiquement 500 à 600 cellules par sgRNA [1] [7] . Certaines plateformes utilisent des systèmes Cas9 inductibles (iCas9), permettant un contrôle précis du moment où l'édition génétique se produit. Par exemple, l'édition peut être déclenchée après que les cellules atteignent un état spécifique, tel qu'une haute densité ou le début de la sénescence. Ce contrôle temporel est particulièrement utile pour étudier les phases non prolifératives, qui sont cruciales pour surmonter les barrières de sénescence en choisissant entre lignes cellulaires primaires vs immortalisées pour l'extension de la production de viande cultivée [4] .
Une fois la bibliothèque construite, les chercheurs passent à des essais de criblage ciblés pour évaluer la fonction des gènes.
Approches de Criblage pour les Lignes Cellulaires de Viande Cultivée
Après avoir construit la bibliothèque, les chercheurs évaluent la performance cellulaire en utilisant des essais de compétition et des techniques de tri fonctionnel. Une méthode largement utilisée est l'essai de prolifération basé sur la compétition, qui identifie les changements génétiques conférant une résistance à la croissance ou à la sénescence - des traits clés pour optimiser les lignes cellulaires pour la viande cultivée.
Les criblages à court terme (durant environ 30 jours) identifient les gènes qui influencent immédiatement le cycle cellulaire, tandis que les criblages à long terme (jusqu'à 200 jours) se concentrent sur les gènes qui aident les cellules à surmonter la sénescence réplicative. C'est un défi crucial dans l'augmentation de la production de viande cultivée [1]. Pour des traits plus complexes, tels que la sécrétion de protéines améliorée ou l'expression de marqueurs spécifiques, le tri cellulaire activé par fluorescence (FACS) est utilisé. Un exemple est le "test de sécrétion par capture à froid", qui isole les populations cellulaires productives en capturant les protéines sécrétées à la surface cellulaire avant le tri [7] [5].
La validation est une étape cruciale pour confirmer les résultats du criblage. Le test de Fitness Cellulaire (CelFi), par exemple, suit le ratio des mutations hors cadre par rapport aux mutations dans le cadre au fil du temps.Si les cellules avec des mutations hors cadre disparaissent de la population, cela suggère que le gène ciblé est essentiel pour la condition physique cellulaire [2].
En juin 2025, des chercheurs dirigés par Shijie Ding à l'Université Agricole de Nanjing ont utilisé CRISPR/Cas9 pour créer CDKN2A–/– lignes de cellules satellites porcines . Ces cellules modifiées ont maintenu une prolifération stable pendant au moins 15 passages dans des conditions sans sérum tout en conservant des marqueurs de pluripotence. Lorsqu'elles sont ensemencées sur un échafaudage comestible 3D à base de plantes, elles ont formé des constructions semblables à de la viande avec une texture améliorée, y compris une mastication et une gomme améliorées [8].
"Ces résultats démontrent l'utilité du criblage CRISPR pour optimiser les traits des cellules souches bovines et offrent une voie vers une production de viande cultivée plus évolutive à l'avenir." – Communications Biology [1]
Écrans génétiques CRISPR groupés dans les cellules de mammifères | Aperçu du protocole
CRISPRi et CRISPRa pour les écrans de régulation génique réversible
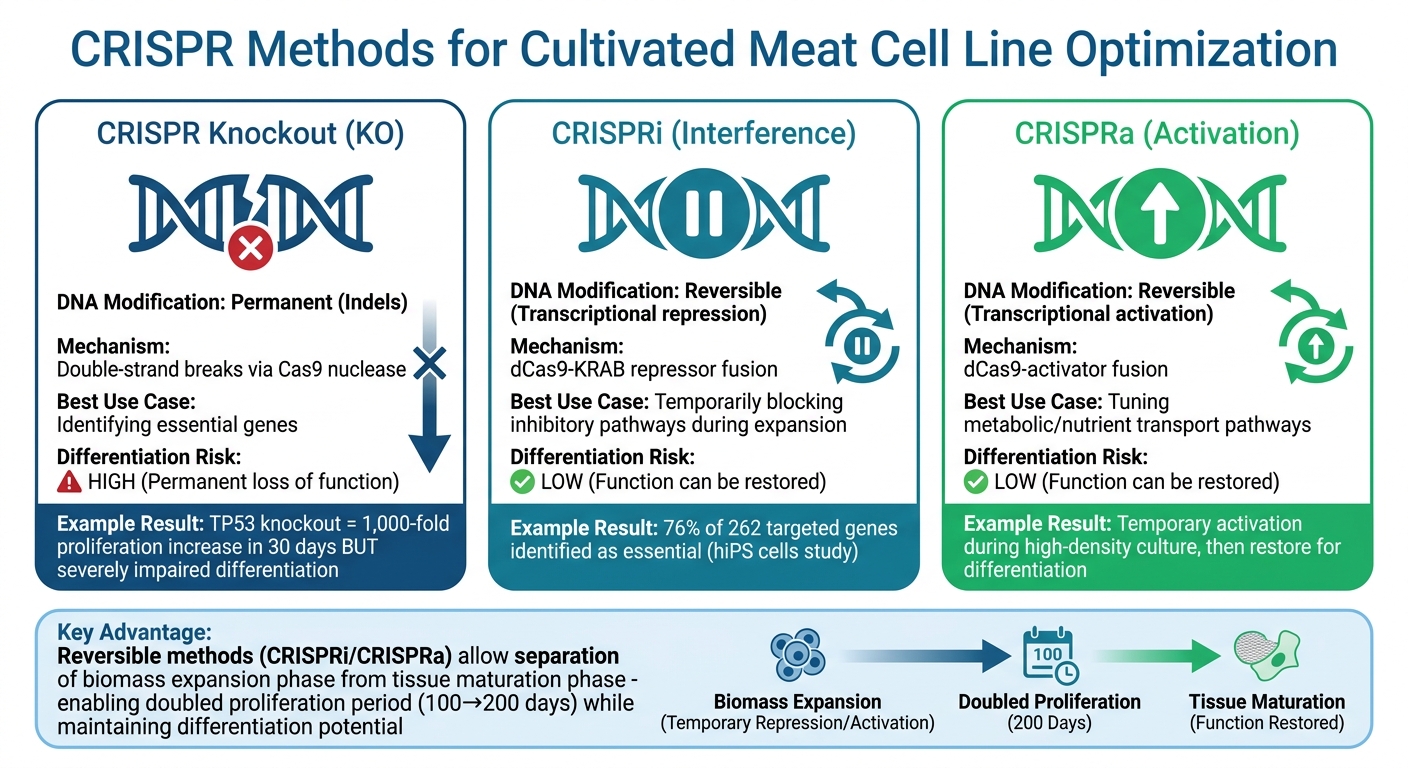
Méthodes d'édition génique CRISPR pour la viande cultivée : comparaison Knockout vs CRISPRi/CRISPRa
Utilisation de CRISPRi et CRISPRa en génomique fonctionnelle
En ce qui concerne l'amélioration de la production de viande cultivée, l'interférence CRISPR (CRISPRi) et l'activation CRISPR (CRISPRa) offrent des outils puissants. Ces techniques utilisent une protéine Cas9 inactive associée à des répresseurs ou des activateurs, permettant aux chercheurs d'ajuster temporairement l'expression génique sans apporter de modifications permanentes à l'ADN [10].
Cette réversibilité est particulièrement importante pour relever un défi majeur : les gènes qui favorisent la croissance rapide des cellules interfèrent souvent avec les étapes ultérieures de la différenciation en tissu musculaire ou adipeux. Par exemple, l'élimination permanente du gène TP53 dans les cellules souches mésenchymateuses bovines peut augmenter la prolifération de plus de 1 000 fois en seulement 30 jours, mais compromet gravement leur capacité à se différencier [1]. CRISPRi offre une solution plus flexible en bloquant temporairement les voies qui inhibent la différenciation pendant l'expansion de la biomasse dans les bioréacteurs pour viande cultivée. Une fois que les cellules sont prêtes pour la maturation des tissus, la fonction normale des gènes peut être rétablie.
En octobre 2025, des chercheurs comme Gabriele Casagrande Raffi et Roderick L. Beijersbergen de l'Institut du Cancer des Pays-Bas ont développé un système CRISPR inductible.Cette approche retarde l'édition génétique jusqu'à ce que les cellules atteignent des états spécifiques - tels qu'une haute densité ou une phase non proliférative - aidant à préserver la viabilité cellulaire [4].
CRISPRi se distingue également par sa précision par rapport à l'interférence ARN traditionnelle (ARNi). L'ARNi conduit souvent à des résultats incohérents et à des effets hors cible, tandis que CRISPRi offre une répression génique plus fiable et spécifique [2]. Un autre avantage est que CRISPRi évite de déclencher une toxicité liée à p53, souvent causée par des réponses aux dommages de l'ADN. Dans une étude de 2025 dirigée par Liqin Wang à Sun Yat-sen University Cancer Centre, les chercheurs ont utilisé un système KRAB–dCas9 inductible par la doxycycline pour cribler 262 gènes dans des cellules souches pluripotentes induites humaines (cellules hiPS). Ils ont découvert que 76 % des gènes ciblés liés à la traduction (200 sur 262) étaient essentiels à la croissance, démontrant l'efficacité du système [10].
Cette capacité à affiner l'expression génique rend CRISPRi et CRISPRa des outils précieux pour équilibrer la prolifération et la différenciation cellulaires dans la recherche en génomique fonctionnelle.
Adapter les écrans réversibles pour les applications de viande cultivée
La régulation génique réversible offre des solutions aux défis clés de la production de viande cultivée. Par exemple, CRISPRa peut activer temporairement des gènes impliqués dans le transport des nutriments ou les voies métaboliques pendant la culture à haute densité. Une fois que les cellules atteignent la densité souhaitée, le système peut ramener l'expression génique à des niveaux normaux, soutenant une différenciation appropriée en tissu musculaire ou adipeux.
Les systèmes inductibles permettent également de séparer la phase d'expansion de la biomasse de la maturation des tissus. CRISPRi peut supprimer les gènes associés à la sénescence pendant le processus de mise à l'échelle, doublant efficacement la période de prolifération des cellules bovines d'environ 100 jours à plus de 200 jours [1]. Après avoir atteint une biomasse suffisante, les chercheurs peuvent rétablir l'expression génique normale pour permettre la différenciation. Cette approche est particulièrement utile pour les cellules souches mésenchymateuses, qui ont tendance à entrer en sénescence tôt en culture [1].
"L'édition génétique ciblée de ces deux processus pourrait optimiser l'efficacité de l'expansion des CSM tout en maintenant leur multipotence essentielle et leur potentiel de différenciation, faisant ainsi progresser les systèmes de viande cultivée à grande échelle." – Communications Biology [1]
Le tableau ci-dessous met en évidence les différences entre les méthodes de régulation génique réversibles et permanentes :
| Caractéristique | CRISPR Knockout (KO) | CRISPRi / CRISPRa |
|---|---|---|
| Modification de l'ADN | Permanent (Indels) | Réversible (Transcriptionnelle) |
| Mécanisme | Cassures double brin | Fusion dCas9-effecteur |
| Meilleur cas d'utilisation | Identifier les gènes essentiels | Ajuster les voies métaboliques/de croissance |
| Risque de différenciation | Élevé (Perte de fonction permanente) | Faible (La fonction peut être restaurée) |
Cette comparaison illustre comment les méthodes de régulation génique réversible peuvent être adaptées pour répondre aux défis spécifiques du développement de lignées cellulaires pour la production de viande cultivée.
Combinaison des écrans CRISPR avec les technologies de panel cellulaire et de génotypage
Lier les écrans CRISPR avec l'analyse multi-omique
L'intégration de l'analyse multi-omique et du génotypage automatisé dans les écrans CRISPR affine leur utilité, en particulier pour faire progresser le développement de lignées cellulaires de viande cultivée.
Combiner les écrans CRISPR avec l'analyse multi-omique, telle que le séquençage de l'ARN, permet aux chercheurs de cartographier les effets des éliminations spécifiques de gènes sur les voies cellulaires. Cela est particulièrement pertinent pour la viande cultivée, où comprendre comment les cellules équilibrent la prolifération et la différenciation est crucial.
Par exemple, un écran CRISPR knockout groupé ciblant 600 gènes dans les cellules souches mésenchymateuses dérivées du tissu adipeux bovin, associé à l'ARN-seq, a révélé que l'élimination de TP53 et PTEN retardait la sénescence.Ces cellules ont maintenu un profil d'expression génique jeune, avec des gènes du cycle cellulaire régulés à la hausse, entraînant une augmentation de 50 % des taux de doublement d'ici le jour 50 après transduction [1].
Les plateformes monocellulaires comme CROP-seq vont plus loin en détectant simultanément à la fois les changements de sgRNA et transcriptomiques dans les cellules individuelles [6]. Ce niveau de précision est inestimable pour identifier les modifications génétiques qui améliorent la différenciation musculaire ou la synthèse des protéines - des facteurs critiques pour atteindre la texture et les propriétés nutritionnelles souhaitées dans la viande cultivée.
Une autre approche prometteuse implique le dépistage de panneaux cellulaires, où les perturbations CRISPR sont testées sur diverses lignées cellulaires provenant de différents donneurs, sites anatomiques et espèces. Par exemple, les chercheurs ont validé la bibliothèque MyoCRISPR-KOLib sur des lignées de myoblastes humains provenant de sept donneurs. En utilisant un système de sélection à toxine divisée, ils ont identifié 250 gènes essentiels à la fusion des myoblastes. Parmi ceux-ci, 41 gènes ont été confirmés par des bases de données médicales comme jouant un rôle dans la morphologie du muscle squelettique [6]. Cette validation multi-lignes garantit que les cibles génétiques restent robustes à travers les variations biologiques, une considération clé pour l'extension de la production de viande cultivée.
Ces découvertes ouvrent la voie à des plateformes automatisées et évolutives qui combinent des criblages génétiques avec un génotypage détaillé pour des applications industrielles.
Automatisation et évolutivité dans les plateformes intégrées
L'automatisation est essentielle pour gérer les vastes ensembles de données et échantillons générés par les plateformes intégrées CRISPR et de génotypage. Les systèmes RMCE, qui permettent une livraison sans virus et spécifique au site des bibliothèques de sgRNA, représentent une avancée majeure. Ces plateformes garantissent que chaque cellule reçoit une copie unique et cohérente de sgRNA, réduisant ainsi la variabilité. RMCE a déjà démontré une couverture élevée de la bibliothèque avec un biais minimal dans les cellules d'ovaire de hamster chinois (CHO) [5].
"Une plateforme de criblage génétique à haut débit et sans biais est essentielle pour le développement des usines CHO de nouvelle génération." - Équipe de recherche sur l'ovaire de hamster chinois [5]
La scalabilité est encore améliorée par des outils de validation comme le test de Fitness Cellulaire (CelFi). Ce test utilise le séquençage profond ciblé pour surveiller les profils d'indel au fil du temps, en suivant le ratio des mutations dans le cadre par rapport à celles hors cadre. En corrélant ces mutations avec des avantages ou des désavantages de croissance, les chercheurs peuvent vérifier efficacement les cibles génétiques dans les lignées cellulaires de viande cultivée [2].
| Technologie | Méthode d'Intégration | Avantage Principal pour la Viande Cultivée |
|---|---|---|
| RNA-seq / Multi-omics | Lier les résultats CRISPR aux profils transcriptomiques | Comprendre comment les gènes régulent la croissance et la différenciation [1][6] |
| Systèmes à Toxines Séparées | Lier la fusion cellulaire à la sélection de viabilité | Sélection quantitative de cellules capables de fusion ou défectueuses [6] |
| Plateformes RMCE | Intégration site-spécifique de bibliothèques gRNA | Criblage à haut débit, sans virus, avec des nombres de copies de gènes constants [5] |
| CROP-seq | CRISPR unicellulaire + RNA-seq | Détection simultanée de sgRNA et des changements transcriptomiques [6] |
| CelFi Assay | Séquençage profond ciblé des indels | Validation rapide des cibles génétiques en suivant les changements de fréquence allélique [2] |
Ces plateformes avancées simplifient le processus allant de l'identification des cibles génétiques à la validation de leur impact sur la condition physique des cellules. Cette efficacité soutient le développement de lignées cellulaires suffisamment robustes pour la production de viande cultivée à grande échelle.
Utilisation des écrans CRISPR pour améliorer la croissance et la prolifération des lignées cellulaires
Les méthodes de criblage CRISPR sont devenues un outil puissant pour améliorer les performances des lignées cellulaires, offrant des avantages directs pour la production de viande cultivée.
Exemples d'améliorations des lignées cellulaires basées sur CRISPR
Les criblages CRISPR ont amélioré avec succès les performances des lignées cellulaires dans la recherche sur la viande cultivée. Par exemple, un criblage par knockout groupé ciblant 600 gènes dans des cellules souches mésenchymateuses dérivées de tissu adipeux bovin a identifié TP53 et PTEN comme inhibiteurs clés de la croissance. L'élimination de TP53 a considérablement augmenté l'abondance cellulaire en 30 jours[1] . De plus, les cellules souches mésenchymateuses bovines modifiées ont montré un taux de doublement moyen supérieur de 12%[1] .
En ciblant les gènes suppresseurs de tumeurs, les chercheurs ont prolongé la durée de vie proliférative des cellules d'environ 100 à plus de 200 jours, contournant ainsi efficacement la limite de Hayflick. Ce retard de la sénescence permet une expansion de la biomasse sur des périodes pertinentes pour l'industrie[1].
Dans un autre exemple, des chercheurs de l'Université Agricole de Nanjing, dirigés par Shijie Ding, Chunbao Li et Guanghong Zhou, ont utilisé CRISPR/Cas9 pour développer des lignées cellulaires satellites porcines CDKN2A−/−. Ces cellules modifiées ont maintenu une prolifération stable pendant au moins 18 passages dans un milieu sans sérum personnalisé à 19 composants (A19). Elles ont également été ensemencées avec succès sur des échafaudages comestibles, créant des structures de type viande avec une amélioration de la mastication et de la gommeuse[8]. Les cellules ont maintenu une viabilité de plus de 90 % à travers plusieurs passages dans des conditions sans sérum[8].
"Les cellules knockout CDKN2A basées sur CRISPR fournissent une source renouvelable de progéniteurs musculaires, réduisant la dépendance aux biopsies animales répétées."
Ces exemples soulignent comment les cribles CRISPR peuvent identifier des modifications génétiques qui améliorent les taux de croissance, retardent le vieillissement cellulaire et permettent une culture sans sérum - trois aspects essentiels pour l'extension de la production de viande cultivée.
Défis de mise à l'échelle pour les lignées cellulaires optimisées par CRISPR
Bien que les lignées cellulaires optimisées par CRISPR présentent des avantages évidents, leur mise à l'échelle pour une utilisation industrielle présente des défis. Une prolifération accrue se fait souvent au détriment de la différenciation.Par exemple, les knockouts de TP53 dans les cellules souches mésenchymateuses bovines ont été associés à une expression réduite des gènes de différenciation musculaire, ce qui peut entraver leur capacité à mûrir en tissu comestible[1]. Pour y remédier, des stratégies supplémentaires, telles que l'ajout de suppléments de milieu ou l'activation de facteurs de transcription spécifiques, peuvent être nécessaires pour restaurer la différenciation après expansion[1].
Un autre problème critique est le maintien de la stabilité génétique. Les variations du nombre de copies de gènes (aneuploïdie) et les effets hors cible lors de l'édition CRISPR peuvent entraîner des résultats incohérents ou des faux positifs dans les études de criblage[2]. Des outils comme le test de Fitness Cellulaire (CelFi) aident à atténuer ces risques en surveillant le ratio des indels hors cadre au fil du temps, garantissant que les avantages de croissance observés sont directement liés aux modifications prévues[2].
Des obstacles économiques et techniques subsistent également. Les cellules souches mésenchymateuses, qui représentent environ 25 % des sources cellulaires dans l'industrie de la viande cultivée, font face à des défis tels que le coût élevé des facteurs de croissance, la nécessité de médias optimisés sans sérum, et le développement de bioréacteurs à grande échelle (capacités de 10 000 à 50 000 L)[1][9][11]. De plus, assurer la texture souhaitée lorsque les cellules sont ensemencées sur des échafaudages 3D reste une tâche complexe[11].
"L'état actuel de la viande cultivée fait face à des défis importants, notamment des coûts élevés, des problèmes d'évolutivité et la nécessité de progrès technologiques supplémentaires."
- Communications Biology [1]
Surmonter ces défis nécessite une approche globale qui combine l'optimisation génétique avec des avancées dans la formulation des milieux, la technologie des bioréacteurs et les protocoles de différenciation. Bien que les cribles CRISPR fournissent des informations génétiques essentielles, traduire ces découvertes en solutions évolutives exigera des systèmes intégrés et des processus de validation rigoureux. Ces efforts sont essentiels pour faire passer la production de viande cultivée du laboratoire à la viabilité commerciale.
Comment Cellbase Soutient la Recherche CRISPR dans la Viande Cultivée
Le criblage CRISPR a déjà montré son potentiel, mais le faire évoluer pour une utilisation industrielle nécessite l'accès à des outils et ressources spécialisés. C'est là que
Accéder aux ressources CRISPR via Cellbase
Contrairement aux fournisseurs pharmaceutiques à large spectre,
En novembre 2025,
"Chaque entreprise de viande cultivée à qui nous avons parlé perdait du temps sur le même casse-tête d'approvisionnement. Trouver des fournisseurs pour des composants critiques signifiait passer des pages de fournisseurs pharmaceutiques qui ne comprenaient pas les applications alimentaires."
- David Bell, Fondateur de Cultigen Group [15]
En centralisant ces ressources,
Favoriser la Collaboration dans le Développement de Viande Cultivée
La plateforme est conçue pour répondre aux exigences des projets commerciaux à grande échelle, comme ceux entrepris par Believer Meats et Aleph Farms. Ces projets nécessitent une infrastructure pour des bioréacteurs de 50 000 litres et des chaînes d'approvisionnement optimisées, que
Conclusion
Le criblage CRISPR à haut débit est passé d'un concept prometteur à un outil essentiel pour faire progresser le développement de la viande cultivée. L'impact de cette technologie sur l'optimisation des lignées cellulaires est indéniable. Par exemple, des percées récentes ont montré que les modifications génétiques peuvent doubler la durée de vie proliférative des cellules souches bovines de 100 à 200 jours, réduire les populations de cellules sénescentes de 60 % à seulement 10 %, et atteindre une augmentation stupéfiante de 1 000 fois de l'abondance cellulaire en un seul mois [1]. Ces avancées marquent un passage clair de la recherche expérimentale à des applications industrielles pratiques.
Les plateformes compactes et les bibliothèques ciblées répondent à certains des défis les plus urgents dans le domaine. Les systèmes microfluidiques numériques permettent désormais de réaliser des criblages avec seulement 3 000 cellules par condition, rendant possible le travail avec des cellules animales primaires limitées qui ne sont pas disponibles dans le commerce.Pendant ce temps, des bibliothèques ciblées comme MyoCRISPR-KOLib ciblent efficacement 90 % des transcrits pertinents tout en couvrant seulement un tiers du génome [3][6]. Ce niveau de précision et d'efficacité est crucial pour surmonter les contraintes de ressources et augmenter la production.
"Ces résultats démontrent l'utilité du criblage CRISPR pour optimiser les traits des cellules souches bovines et offrent une voie vers une production de viande cultivée plus évolutive à l'avenir." [1]
Malgré ces avancées, le succès dépend de l'accès à la bonne infrastructure. Les chercheurs ont besoin de bibliothèques d'ARN guides spécifiques à l'espèce, de milieux de culture conçus pour les applications alimentaires, de bioréacteurs compatibles et d'outils analytiques adaptés à la production de viande cultivée plutôt qu'à l'usage pharmaceutique.Répondant à ces besoins,
Pour les équipes travaillant à concevoir la prochaine vague de lignées cellulaires de viande cultivée, les outils et technologies sont prêts. Le défi réside maintenant dans le déploiement rapide et efficace de la sélection CRISPR pour réaliser tout son potentiel.
FAQs
Comment choisir entre CRISPR knockout, CRISPRi et CRISPRa pour une sélection?
Le choix entre ces systèmes dépend de votre question biologique spécifique et du résultat que vous visez:
- CRISPR knockout: Cette méthode perturbe entièrement la fonction du gène, ce qui la rend idéale pour étudier les effets de la perte ou de l'inactivation d'un gène.
- CRISPRi: En réprimant l'expression des gènes sans couper l'ADN, cette approche est bien adaptée pour étudier les gènes essentiels ou lorsque la suppression réversible est nécessaire.
- CRISPRa: Si vous avez besoin de réguler à la hausse l'expression des gènes, ce système est le choix idéal. Il est particulièrement utile pour examiner les effets de la surexpression, tels que la promotion de la prolifération ou de la différenciation cellulaire.
Lors de votre décision, prenez en compte votre modèle cellulaire, les gènes que vous ciblez et les objectifs globaux de votre expérience.
Comment pouvez-vous augmenter la prolifération sans nuire à la différenciation musculaire ou adipeuse?
Augmenter la prolifération des cellules musculaires ou adipeuses tout en maintenant leur capacité à se différencier est un défi clé dans la production de viande cultivée.Une approche prometteuse implique l'édition de gènes basée sur CRISPR, qui permet une manipulation précise des gènes pour améliorer la croissance ou prolonger la durée de vie des cellules. Par exemple, cibler la myostatine (MSTN) peut favoriser la croissance cellulaire, tandis que l'édition de CDKN2A aide les cellules à contourner la sénescence.
Cela dit, atteindre un équilibre entre prolifération et différenciation est crucial. Une mauvaise gestion de certaines cibles, telles que P53 (TP53), pourrait nuire à la différenciation, compromettant potentiellement la qualité des tissus. Pour naviguer dans ces complexités, le criblage CRISPR à haut débit est essentiel. Cette technique identifie les régulateurs de gènes les plus efficaces, ouvrant la voie à un développement de tissus évolutif et sain dans la production de viande cultivée.
Qu'est-ce qui est nécessaire pour valider les résultats d'un criblage CRISPR avant de passer à l'échelle d'une lignée cellulaire ?
La validation des résultats d'un criblage CRISPR pour la production de viande cultivée nécessite une approche méthodique. Tout d'abord, la fonction du gène doit être confirmée par des expériences indépendantes, telles que des knockouts de gènes, pour s'assurer que les effets observés sont reproductibles. Ensuite, il est crucial d'évaluer la pertinence biologique de ces gènes en examinant leur impact sur des facteurs tels que la prolifération cellulaire, la viabilité et la longévité.
Les évaluations de sécurité sont tout aussi importantes pour exclure les effets hors cible ou l'instabilité génétique qui pourraient compromettre le processus. La validation fonctionnelle dans des conditions qui imitent les environnements industriels, tels que les bioréacteurs, est une autre étape critique. Cela garantit que les modifications génétiques fonctionnent comme prévu dans les environnements de production à grande échelle. Des tests approfondis à chaque étape sont indispensables avant d'envisager une montée en échelle.











