Walidacja pożywek wzrostowych jest obowiązkowym krokiem dla firm zajmujących się mięsem hodowlanym, które starają się o zatwierdzenie na rynku brytyjskim. Proces ten zapewnia bezpieczeństwo, jakość i zgodność produktów z rygorystycznymi ramami regulacyjnymi, takimi jak brytyjskie przepisy dotyczące nowej żywności (UE 2015/2283). Oto, co musisz wiedzieć:
- Kluczowe Wymagania: Pożywki wzrostowe muszą spełniać standardy dotyczące toksykologii, kontroli zanieczyszczeń, jakości odżywczej i alergenności.
- Regulacje w Wielkiej Brytanii: Agencja Standardów Żywności (FSA) wymaga zgodności z zasadami HACCP i klasyfikacji w ramach Produktów Pochodzenia Zwierzęcego (POAO).
- Standardy Globalne: Podczas gdy Wielka Brytania i UE mają podobne ramy, USA stosują przepisy CGMP zgodnie z ustawą FD&C.
- Proces Walidacji: Obejmuje dokładne testowanie składu, czystości, funkcjonalności i zgodności dostawców, wraz z solidną dokumentacją.
- Inicjatywy Wsparcia: Brytyjski regulacyjny sandbox o wartości 1,6 miliona funtów, uruchomiony w 2025 roku, wspiera firmy w spełnianiu tych standardów.
Prawidłowa walidacja zapewnia bezpieczeństwo, buduje zaufanie i jest zgodna z wymaganiami prawnymi. Artykuł zagłębia się w proces krok po kroku, w tym metody testowania, kwalifikacje dostawców i wskazówki dotyczące składania dokumentacji regulacyjnej.
Standardy Regulacyjne dla Podłoży Wzrostowych
Standardy i Wytyczne
Podłoża wzrostowe, kluczowy element w produkcji mięsa hodowlanego, muszą spełniać rygorystyczne międzynarodowe standardy regulacyjne. Standardy te różnią się w zależności od regionu, każdy z nich ma specyficzne wymagania dotyczące składu, bezpieczeństwa i czystości.
W Zjednoczonym Królestwie, pożywki wzrostowe są regulowane zgodnie z przepisami dotyczącymi nowej żywności (przyswojone Rozporządzenie (UE) 2015/2283). Przed zatwierdzeniem na rynek wymagana jest dokładna ocena bezpieczeństwa [1]. Agencja ds. Standardów Żywności (FSA) klasyfikuje produkty hodowane komórkowo jako Produkty Pochodzenia Zwierzęcego (POAO) zgodnie z Rozporządzeniem (WE) 853/2004. Ta klasyfikacja nakłada na producentów obowiązek wdrożenia systemów zarządzania bezpieczeństwem żywności opartych na zasadach Analizy Zagrożeń i Krytycznych Punktów Kontroli (HACCP) [3]. FSA jest również w trakcie opracowywania szczegółowych wytycznych technicznych dotyczących składu pożywek wzrostowych, a dalsze aktualizacje są oczekiwane [1]. Te ramy stanowią podstawę dla bardziej szczegółowych wymagań regulacyjnych.
W Stanach Zjednoczonych, podejście jest inne.Składniki pożywek wzrostowych muszą spełniać wymagania Dobrych Praktyk Wytwarzania (CGMP) określone w Sekcji 501(a)(4)(B) Federalnej Ustawy o Żywności, Lekach i Kosmetykach (FD&C Act) [4]. FDA klasyfikuje składniki pożywek jako "materiały i odczynniki", które są regulowane przez 21 CFR części 210 i 211. Te składniki muszą przejść weryfikację jakości, aby zapobiec zanieczyszczeniom [4]. Co ciekawe, syntetyczne składniki pożywek do mięsa hodowlanego - takie jak aminokwasy, witaminy i sole - są często klasyfikowane jako urządzenia medyczne klasy I zgodnie z 21 CFR 864.2220, co zwalnia je z wymagań dotyczących zgłoszenia przed wprowadzeniem na rynek [6][7].
W Unii Europejskiej, ramy regulacyjne są zbliżone do brytyjskich, ponieważ również podążają za Rozporządzeniem (UE) 2015/2283.Europejski Urząd ds. Bezpieczeństwa Żywności (EFSA) nadzoruje proces autoryzacji [1]. Zgodnie z wytycznymi ICH Q6B, składniki pożywek wzrostowych, w tym antybiotyki, induktory i inne składniki, są traktowane jako zanieczyszczenia związane z procesem. Te zanieczyszczenia muszą być kontrolowane i redukowane do akceptowalnych poziomów [5]. Tam, gdzie to możliwe, substancje pomocnicze i odczynniki powinny spełniać standardy farmakopealne [5].
| Jurysdykcja | Podstawowe przepisy | Klasyfikacja | System bezpieczeństwa | Nadzór medialny |
|---|---|---|---|---|
| Zjednoczone Królestwo (GB) | Rozporządzenie asymilowane (UE) 2015/2283 [1] | Produkt pochodzenia zwierzęcego (POAO) [3] | HACCP (Rozp. 852/2004) [3] | Wytyczne FSA/FSS Sandbox [1] |
| Unia Europejska / NI | Rozporządzenie (UE) 2015/2283 [1] | Produkt pochodzenia zwierzęcego (POAO) [3] | HACCP (Rozp. 852/2004) [3] | Proces autoryzacji EFSA [1] |
| Stany Zjednoczone | FD&C Act Sekcja 501(a)(4)(B) [4] | Nowy lek weterynaryjny / Żywność [4] | CGMP (21 CFR 210/211) [4] | FDA CVM / USDA-FSIS [4] |
Wymagania regulacyjne dla mięsa hodowlanego
Producenci mięsa hodowlanego muszą zapewnić, że każda partia pożywki wzrostowej spełnia rygorystyczne normy bezpieczeństwa i jakości.Walidacja podłoży wzrostowych jest kluczowym aspektem szerszych ram regulacyjnych dla tych produktów. Zgodnie z zasadami HACCP (Rozporządzenie (WE) 852/2004), podłoże wzrostowe jest identyfikowane jako podstawowy wkład i potencjalne źródło zanieczyszczeń - chemicznych, mikrobiologicznych lub innych [3]. FSA podkreśla tę kwestię:
"Główne zagrożenia w produkcji produktów hodowanych komórkowo dotyczą tożsamości linii komórkowej (i jej spójności), zagrożeń wprowadzanych podczas procesu produkcji (zanieczyszczenia mikrobiologiczne, podłoże wzrostowe i pozostałe składniki w produkcie końcowym) oraz alergenów." [3]
Jeśli nastąpią zmiany w formulacji podłoża wzrostowego, wymagana jest natychmiastowa rewizja HACCP [3].W Wielkiej Brytanii, walidacja musi mieć miejsce przed wdrożeniem, aby zapewnić dokładność diagramów przepływu i skuteczność środków kontrolnych [3].
W Stanach Zjednoczonych, FDA wymaga, aby wszystkie odczynniki i składniki mediów spełniały rygorystyczne standardy jakości, aby uniknąć wprowadzenia szkodliwych czynników [4]. Dostawcy i laboratoria kontraktowe muszą przestrzegać przepisów CGMP, a każdy dostawca, który nie spełnia wymagań, powinien zostać usunięty, aby zapobiec klasyfikacji produktów jako "zafałszowane" [4]. FDA podkreśla znaczenie tego:
"Wszystkie nowe leki weterynaryjne, w tym ACTP, muszą być produkowane zgodnie z CGMP, aby zapewnić, że takie leki spełniają wymagania Federalnej Ustawy o Żywności, Lekach i Kosmetykach (FD&C Act) w zakresie bezpieczeństwa." [4]
Obecnie kilka firm uczestniczących w brytyjskim piaskownicy regulacyjnej - takich jak BlueNalu, Gourmey, Hoxton Farms, Mosa Meat, Roslin Technologies, Vital Meat, i Vow - współpracuje z FSA w celu udoskonalenia tych standardów technicznych [1]. Zgodnie z przepisami brytyjskimi, firmy mogą ubiegać się o ochronę danych do pięciu lat dla poufnych informacji przekazanych podczas procesu autoryzacji [1].
Kroki weryfikacji pożywek wzrostowych
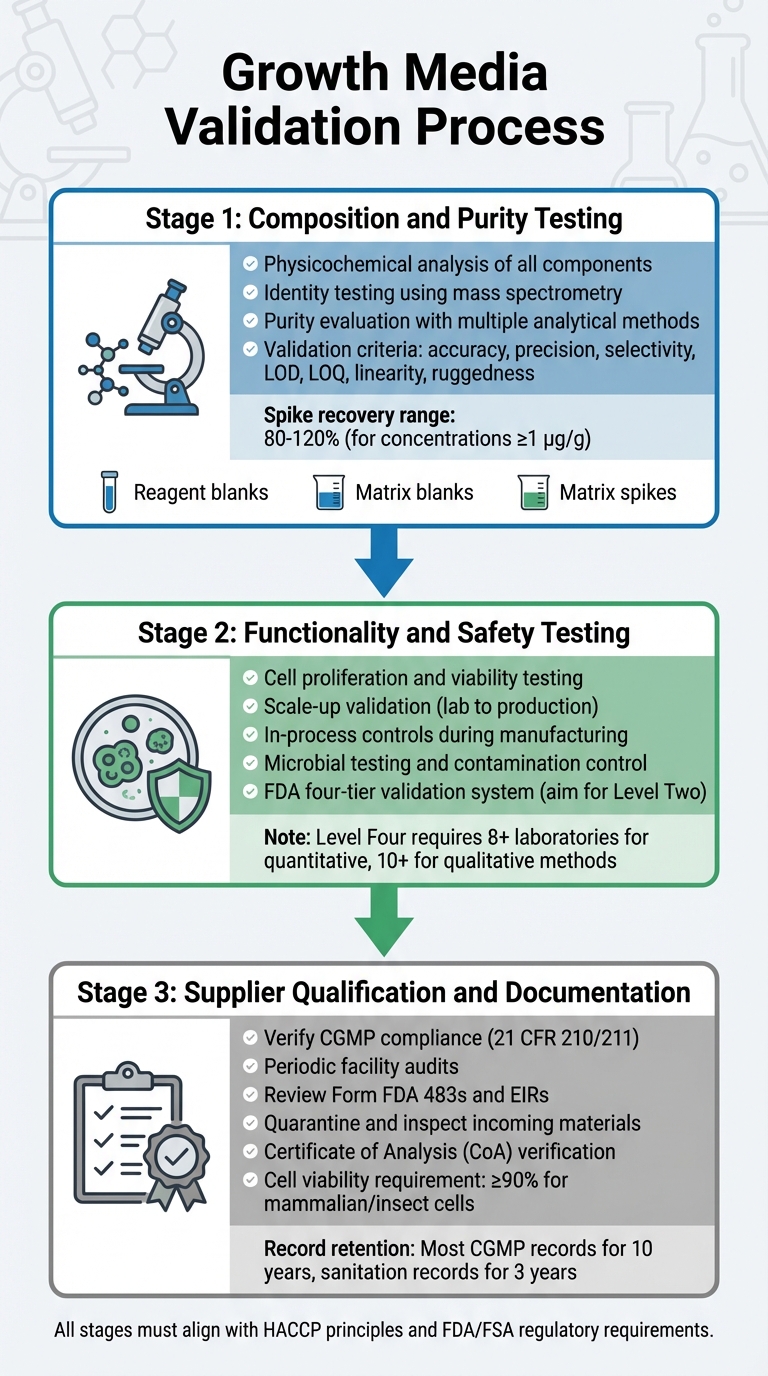
Proces weryfikacji pożywek wzrostowych dla zatwierdzenia regulacyjnego mięsa hodowlanego
Weryfikacja pożywek wzrostowych obejmuje szczegółowy proces, który bada ich skład, funkcjonalność, bezpieczeństwo i zgodność z dostawcą. Każdy krok opiera się na poprzednim, zapewniając solidny proces weryfikacji zgodny z wymaganiami regulacyjnymi. Obejmuje to testowanie składu, funkcjonalności i zgodności z dostawcą.
Testowanie składu i czystości
Pierwszy etap koncentruje się na dokładnej analizie fizykochemicznej każdego składnika. Obejmuje to identyfikację dokładnego składu, właściwości fizycznych i struktury molekularnej składników, takich jak aminokwasy, witaminy i sole nieorganiczne [5].Aby potwierdzić struktury molekularne, testy identyfikacyjne wykorzystują wysoce specyficzne metody, w tym techniki fizykochemiczne, biologiczne i immunochemiczne. Narzędzia takie jak spektrometria mas są używane do weryfikacji tożsamości molekularnych poprzez ich wzorce fragmentacji [8].
Ocena czystości wymaga wielu metod analitycznych do oddzielenia pożądanych składników od zanieczyszczeń. Testy te muszą uwzględniać zarówno zanieczyszczenia związane z procesem, jak i z produktem [5]. Techniki analityczne powinny spełniać rygorystyczne kryteria walidacji, w tym dokładność, precyzję, selektywność, granice wykrywalności (LOD), granice oznaczalności (LOQ), liniowość i wytrzymałość [8]. Protokóły walidacyjne powinny również obejmować:
- Ślepe próby odczynników w celu zapewnienia, że odczynniki są wolne od analitów.
- Puste matryce w celu potwierdzenia, że środowisko próbki nie wpływa na wynik.
- Dodatki do matrycy w celu oszacowania odzysku i dokładności.
Dla metod ilościowych przy stężeniach 1 µg/g (ppm), akceptowalne odzyski dodatków zazwyczaj mieszczą się w zakresie od 80% do 120% [8].
Aby utrzymać spójność, producenci powinni ustanowić wewnętrzne materiały odniesienia pochodzące z partii reprezentatywnych dla produkcji. Służą one jako standardy śladowe do kalibracji roboczych materiałów odniesienia [5]. Po zakończeniu testów czystości, medium musi wykazać zdolność do wspierania efektywnego wzrostu komórek i spełniać normy bezpieczeństwa.
Testowanie funkcjonalności i bezpieczeństwa
Po potwierdzeniu składu, medium musi udowodnić swoją skuteczność we wspieraniu produkcji mięsa hodowlanego. Obejmuje to wykazanie, że komórki mogą się namnażać, utrzymywać żywotność i skalować z warunków laboratoryjnych do objętości produkcyjnych. FDA wymaga kontroli w procesie produkcji, począwszy od wczesnych etapów, takich jak pasażowanie i zbieranie komórek, aby zapewnić spójność i bezpieczeństwo produktu [4].
Walidacja bezpieczeństwa obejmuje rygorystyczne testy mikrobiologiczne i kontrolę zanieczyszczeń, zgodnie z ocenami przedrynkowymi FDA [9].
FDA stosuje czteropoziomowy system walidacji metod chemicznych, od poziomu pierwszego (użycie awaryjne lub ograniczone) do poziomu czwartego (pełne badania współpracy spełniające standardy AOAC/ISO) [8].Dla rutynowych testów regulacyjnych dąż do walidacji jednolaboratoryjnej poziomu drugiego, która obejmuje kompleksową ocenę wydajności [8]. Pełne badania współpracy dla metod ilościowych wymagają udziału co najmniej ośmiu laboratoriów, podczas gdy metody jakościowe potrzebują dziesięciu [8]. Po zwalidowaniu wydajności mediów, ważne jest, aby upewnić się, że wszystkie surowce pochodzą od zgodnych dostawców.
Kwalifikacja i dokumentacja dostawców
Producenci muszą współpracować ze zweryfikowanymi dostawcami zgodnymi z CGMP. Dostawcy powinni spełniać standardy określone w 21 CFR 210/211 [4]. Weryfikacja obejmuje okresowe audyty obiektów dostawców w celu oceny zgodności z programami jakości, procedurami i ogólną zgodnością z CGMP [4].
Przed zawarciem umów należy przeanalizować historię zgodności dostawcy, w tym formularze FDA 483 i Raporty z Inspekcji Zakładów (EIR) [4]. FDA podkreśla ten obowiązek:
"Przed zawarciem jakiejkolwiek umowy, porozumienia lub innego układu z innym zakładem w celu wykonania jakiegokolwiek etapu produkcji dla Ciebie, powinieneś zweryfikować, czy zakład ten przestrzega obowiązujących przepisów CGMP." [4]
Wszystkie materiały przychodzące muszą być poddane kwarantannie i inspekcji przed zwolnieniem, aby upewnić się, że spełniają specyfikacje główne [10]. Dostawcy są zobowiązani do dostarczenia Certyfikatu Analizy (CoA) lub śledzonych wyników testów zgodnych z CGMP/GLP [10].Dla stabilnych linii komórkowych dokumentacja musi zawierać możliwą do prześledzenia historię klonowania [10]. Komórki ssacze lub owadzie zazwyczaj wymagają co najmniej 90% żywotności do akceptacji w projektach CGMP [10]. Dokumentacja powinna być przechowywana zgodnie z wytycznymi regulacyjnymi [4].
Umowy muszą jasno określać obowiązki CGMP i wymagać od dostawców powiadamiania producentów o wszelkich proponowanych zmianach w zestawach testowych lub metodach [4]. Jeśli testowanie jest zlecane na zewnątrz, należy upewnić się, że laboratoria kontraktowe używają zwalidowanych metod analitycznych i są zarejestrowane w FDA [4].
Przygotowywanie Dokumentów do Zgłoszenia Regulacyjnego
Po zwalidowaniu pożywki wzrostowej, kolejnym krokiem jest skompilowanie dossier, które wykazuje zgodność ze wszystkimi standardami bezpieczeństwa i jakości wymaganymi przez FDA i USDA-FSIS. To dossier stanowi kluczowe ogniwo między walidacją a zgodnością regulacyjną, dając władzom jasny obraz bezpieczeństwa i procesów produkcyjnych Twojej pożywki.
Wymagane Elementy Dossier Zgłoszeniowego
Twoje dossier powinno zawierać szczegółowy podział składu pożywki, wymieniając wszystkie aminokwasy, witaminy, sole nieorganiczne i czynniki wzrostu. Wytyczne FDA podkreślają, że proces przeglądu ocenia nie tylko samą pożywkę, ale cały proces produkcyjny. Obejmuje to ustanowienie linii komórkowych i banków, wdrożenie kontroli produkcji oraz weryfikację wszystkich komponentów i wkładów [11].
Dodatkowo, dossier musi zawierać szczegółową ocenę bezpieczeństwa i toksykologiczną, potwierdzającą bezpieczeństwo żywnościowe materiału hodowlanego i wszystkich jego składników. Należy dołączyć zapisy kontroli produkcji, dane walidacji procesów oraz dokumentację programu jakości, aby wykazać, że produkcja jest spójna i wolna od zanieczyszczeń.
Należy również dostarczyć zapisy weryfikacji dostaw i odczynników, pokazujące walidację wszystkich materiałów używanych w pożywce, w tym tych przygotowywanych we własnym zakresie. Dla produktów regulowanych przez USDA-FSIS, należy dołączyć plany HACCP i protokoły sanitarne. FDA zaleca przechowywanie większości zapisów CGMP przez co najmniej 10 lat, podczas gdy zapisy dotyczące czyszczenia i sanitacji obiektów powinny być przechowywane przez minimum 3 lata [4]. To jest zgodne z wysiłkami na rzecz kwalifikacji dostawców, zapewniając, że wszystkie składniki spełniają wymagania CGMP i regulacyjne.
Dokumentacja Zgodności Obiektu
Przed produkcją, przetwarzaniem lub przechowywaniem mięsa hodowlanego do spożycia przez ludzi, obiekty muszą zarejestrować się w FDA [12]. Twoja dokumentacja powinna zawierać kompleksowy plan bezpieczeństwa żywności, który uwzględnia analizę zagrożeń (biologicznych, chemicznych i fizycznych), środki zapobiegawcze (takie jak zarządzanie sanitacją, alergenami i łańcuchem dostaw) oraz procedury nadzoru [12].
Symulacje wypełniania pożywki są również kluczowym wymogiem. Obejmują one 14-dniową inkubację i testy promujące wzrost w celu potwierdzenia praktyk aseptycznych.Jak wyjaśnia FDA:
"Testy wypełnienia powinny oceniać aseptyczny montaż i działanie krytycznego (sterylnego) sprzętu, kwalifikować operatorów i oceniać ich technikę, a także wykazać, że kontrola środowiskowa jest odpowiednia" [2].
Upewnij się, że Twoje zapisy zawierają dane dotyczące kwalifikacji dostawców, takie jak testy przeprowadzone na pierwszych trzech partiach medium od dostawcy, aby potwierdzić, że odpowiadają one Certyfikatowi Analizy. Inne istotne zapisy obejmują dzienniki kontroli środowiskowej, harmonogramy kalibracji sprzętu i dane dotyczące monitorowania temperatury. Dla procesów regulowanych przez USDA przygotuj plany HACCP, pisemne standardowe procedury sanitarne (SSOP) i procedury wycofania [12][13].
sbb-itb-ffee270
Korzystanie z Cellbase do zakupu pożywek zgodnych z przepisami
Zweryfikowani dostawcy dla mięsa hodowanego
Po zatwierdzeniu formuły pożywki, kolejnym krokiem jest pozyskanie komponentów spełniających normy regulacyjne. To nie jest tak proste, jak zamawianie od ogólnych dostawców. Dla produktów hodowanych komórkowo obowiązują surowe przepisy higieniczne, a każdy składnik pożywki musi być dostarczony z odpowiednią dokumentacją do zatwierdzenia regulacyjnego [3]. W tym miejscu wkracza
Funkcje Zakupów
Platforma oferuje również przejrzyste ceny i funkcję bezpośrednich wiadomości, umożliwiając zespołom szybkie żądanie ofert, certyfikatów analizy i innych dokumentów regulacyjnych.Poprzez konsolidację tych kluczowych funkcji zaopatrzenia w jeden system dostosowany do produkcji mięsa hodowlanego,
Wniosek
Walidacja mediów wzrostowych dla zatwierdzenia regulacyjnego to nie tylko formalność - to wymóg prawny wprowadzania produktów z mięsa hodowlanego na rynek brytyjski. Obejmuje to dokładne testy składu i czystości, wdrożenie solidnego planu HACCP oraz prowadzenie szczegółowej dokumentacji na każdym etapie.
"Żywność nie może być wprowadzana na rynek, jeśli jest niebezpieczna. Oznacza to, że nie może być szkodliwa dla zdrowia ani nieodpowiednia do spożycia przez ludzi." - Agencja Norm Żywnościowych [3]
Brytyjska Agencja Norm Żywnościowych £1.6 milionów Regulatory Sandbox podkreśla swoje zaangażowanie we współpracę z graczami z branży w celu ustanowienia jasnych wytycznych technicznych dotyczących składu mediów wzrostowych [1]. Firmy, które teraz priorytetowo traktują właściwą walidację, będą w lepszej pozycji, gdy te wytyczne zostaną w pełni zdefiniowane.
Spełnianie standardów zgodności to nie tylko odhaczanie regulacyjnych wymogów - to zdobywanie zaufania konsumentów i zapewnienie bezpieczeństwa produktów. Rygorystyczne testy jakości są kluczowe zarówno dla zatwierdzenia regulacyjnego, jak i zdobycia akceptacji rynkowej. Aby usprawnić proces autoryzacji, skup się na budowaniu solidnych protokołów walidacyjnych, utrzymywaniu dokładnych zapisów i współpracy z niezawodnymi dostawcami. Te kroki nie tylko uproszczą zatwierdzenie, ale także utorują drogę do większego zaufania konsumentów.
Najczęściej zadawane pytania
Jakie są główne kroki w walidacji podłoży wzrostowych dla zatwierdzenia regulacyjnego?
Walidacja podłoży wzrostowych dla zatwierdzenia regulacyjnego polega na udowodnieniu, że formuła jest bezpieczna, niezawodna i odpowiednia do produkcji mięsa hodowlanego. Oto jak zazwyczaj wygląda ten proces:
- Ocena ryzyka: Zacznij od zdefiniowania linii komórkowej, której użyjesz, celów produktu i jego krytycznych atrybutów jakościowych (takich jak pH czy składniki odżywcze). Zidentyfikuj potencjalne zagrożenia, takie jak zanieczyszczenie mikrobiologiczne, i określ środki kontroli tych ryzyk.
- Testowanie i specyfikacje: Ustal jasne kryteria akceptacji dla czynników takich jak jałowość, czystość i moc. Używaj ustalonych metod testowania, aby zapewnić, że te standardy są konsekwentnie spełniane.
- Badania walidacyjne: Przeprowadź dokładną walidację procesu, w tym kwalifikację sprzętu i testowanie wielu partii, aby potwierdzić, że wyniki są powtarzalne i spójne.
- Testy stabilności: Sprawdź, jak medium zachowuje się w czasie, oceniając jego jakość przez cały okres przydatności do spożycia w odpowiednich warunkach przechowywania (zwykle 2–8 °C).
- Dokumentacja: Zbierz wszystko w kompleksowy dossier walidacyjny. Powinno to zawierać wszystkie wyniki testów i analizy, aby spełnić wymagania regulacyjne.
Starannie realizując każdy z tych kroków, zgromadzisz dowody potrzebne do wykazania, że medium spełnia wymagane standardy bezpieczeństwa i jakości dla produkcji mięsa hodowlanego.
Jakie są kluczowe różnice między regulacjami w Wielkiej Brytanii a USA dotyczącymi mediów wzrostowych stosowanych w mięsie hodowanym?
W Wielkiej Brytanii regulacja mediów wzrostowych dla mięsa hodowanego podlega Rozporządzeniu w sprawie nowych produktów spożywczych (Rozporządzenie UE 2015/2283), które zostało zachowane w prawie GB. Wszelkie media wzrostowe stosowane w produktach, które nie były powszechnie spożywane przed 15 maja 1997 roku, muszą przejść formalną ocenę nowej żywności przez Agencję Standardów Żywności (FSA). Proces ten wymaga złożenia szczegółowej dokumentacji, w tym informacji o składzie, pochodzeniu i czystości mediów. Dodatkowo, konieczna jest ocena ryzyka oparta na HACCP, aby wykazać, jak zanieczyszczenia są kontrolowane podczas procesu hodowli komórek.
Od grudnia 2025 roku FSA wdrożyła piaskownicę dla produktów hodowanych komórkowo. Ta inicjatywa oferuje wskazówki i wspiera szybsze zbieranie danych do aplikacji nowej żywności.Aby uzyskać ostateczną autoryzację, firmy muszą przedłożyć kompleksowy dossier, który uwzględnia bezpieczeństwo mediów, spójność i walidację produkcji. Dopiero po tej aprobacie produkt może być sprzedawany w Wielkiej Brytanii.
W przeciwieństwie do tego, Stany Zjednoczone nie mają specyficznych ram dla nowej żywności dostosowanych do mediów wzrostowych, co utrudnia bezpośrednie porównania regulacyjne. Dla firm z siedzibą w Wielkiej Brytanii, pozyskiwanie komponentów mediów, które już spełniają te surowe standardy, może uprościć proces zatwierdzania.W jaki sposób brytyjska piaskownica regulacyjna wspiera walidację mediów wzrostowych?
Brytyjska piaskownica regulacyjna dla produktów hodowlanych zapewnia dobrze zorganizowane środowisko, w którym firmy mogą testować i udoskonalać swoje formuły mediów wzrostowych. Nadzorowany przez Agencję Standardów Żywności (FSA) i Food Standards Scotland (FSS), program ten działa w sześciomiesięcznych fazach. W tym czasie firmy mogą przeprowadzać testy bezpieczeństwa, oceniać ryzyko i przeglądać dokumentację, otrzymując jednocześnie cenne informacje zwrotne od regulatorów.
To praktyczne podejście pozwala na przeprowadzanie prób praktycznych i stopniowe udoskonalenia, przyspieszając zbieranie danych dotyczących bezpieczeństwa i pomagając firmom dostosować się do wymogów regulacyjnych. Dla tych, którzy pracują nad mięsem hodowlanym, pozyskiwanie wcześniej zatwierdzonych mediów wzrostowych przez











